Россельхознадзор — Официальный сайт — Версия для печати
Ученые подведомственного Россельхознадзору Всероссийского государственного Центра качества и стандартизации лекарственных средств для животных и кормов (ФГБУ «ВГНКИ») приступили к выполнению научно-исследовательской работы, в ходе которой будет разработана новая методика определения карнитина – важной для обмена веществ аминокислоты – в лекарственных препаратах для животных, кормовых добавках и продуктах питания. Методика позволит выявлять и определять количественное содержание полезной формы карнитина (L-карнитина) в образцах продукции, и, тем самым, обеспечит поставки на российский рынок только качественных товаров. Методика будет разработана уже в конце 2019 года.
L-карнитин (левокарнитин, ЛК) – природное соединение, производное аминокислоты, которое синтезируется в организме животных и человека в печени и почках. L-карнитин играет важную роль в процессах обмена веществ: он участвует в переносе жирных кислот и в липидном обмене, оказывает антиоксидантное действие, стимулирует клеточный иммунитет, улучшает пищеварение и восстанавливает слизистую желудочно-кишечного тракта при гастритах и панкреатитах.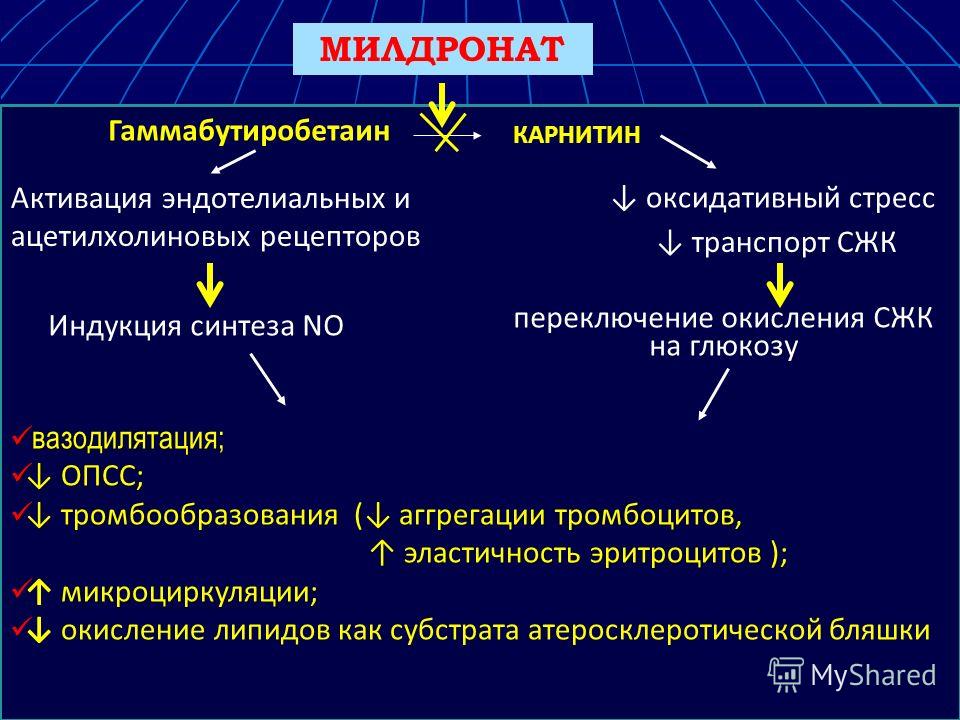
Однако молекула карнитина существует в виде двух форм (оптических изомеров): L-карнитина и D-карнитина. В отличие полезного для организма животных и человека L-карнитина, D-карнитин не обладает биологической активностью, конкурирует с L-карнитином и нарушает его синтез в организме.
Так как карнитин применяется в производстве лекарственных средств для животных, кормовых добавок и даже в продуктах питания, существует необходимость разделения полезной и вредной формы этого вещества. Тем не менее, в России нет стандартизированной методики разделения и количественного определения L- и D-карнитина. Создание такой методики – цель новой научно-исследовательской работы ФГБУ «ВГНКИ», реализуемой на базе Испытательного центра учреждения.
Новая методика ФГБУ «ВГНКИ» будет основана на высокоэффективной жидкостной хроматографии. Этот метод позволит идентифицировать оптические изомеры карнитина.
В 2019 году научные сотрудники ФГБУ «ВГНКИ» оптимизируют подготовку проб и проведут валидационные испытания методики для последующей аттестации.
Для справки:
Согласно исследованиям Первого Московского государственного медицинского университета им. И. М. Сеченова, включение L-карнитина в диету снижает уровень общего холестерина и триглицеридов и способствует устранению функциональных нарушений нервной системы.
Потребность в L-карнитине индивидуальна и возрастает при умственных, физических и эмоциональных нагрузках. В отличие от большинства известных витаминов, не существует официально утвержденной нормы его потребления.
Основным источником L-карнитина являются мясо-молочные продукты. Внутренний синтез карнитина в организме человека не всегда полностью обеспечивает потребность в нем.
СПОРТЭКСПЕРТ L-КАРНИТИН N10 САШЕ ПО 3,5Г
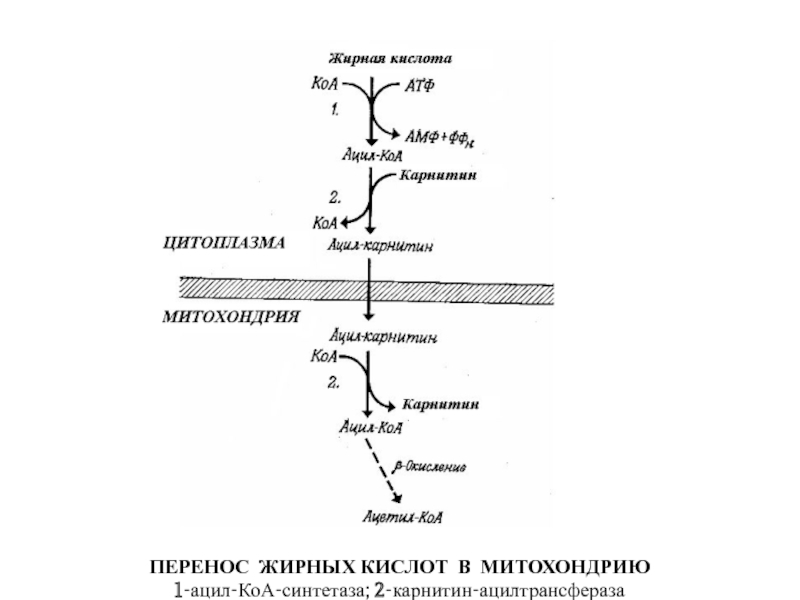 В клеточных митохондриях жирные кислоты используются непосредственно как источник энергии тела, то есть сжигаются. Таким образом, L-карнитин является мощным естественным утилизатором жира клеток тела, трансформируя этот жир в энергию.
В клеточных митохондриях жирные кислоты используются непосредственно как источник энергии тела, то есть сжигаются. Таким образом, L-карнитин является мощным естественным утилизатором жира клеток тела, трансформируя этот жир в энергию.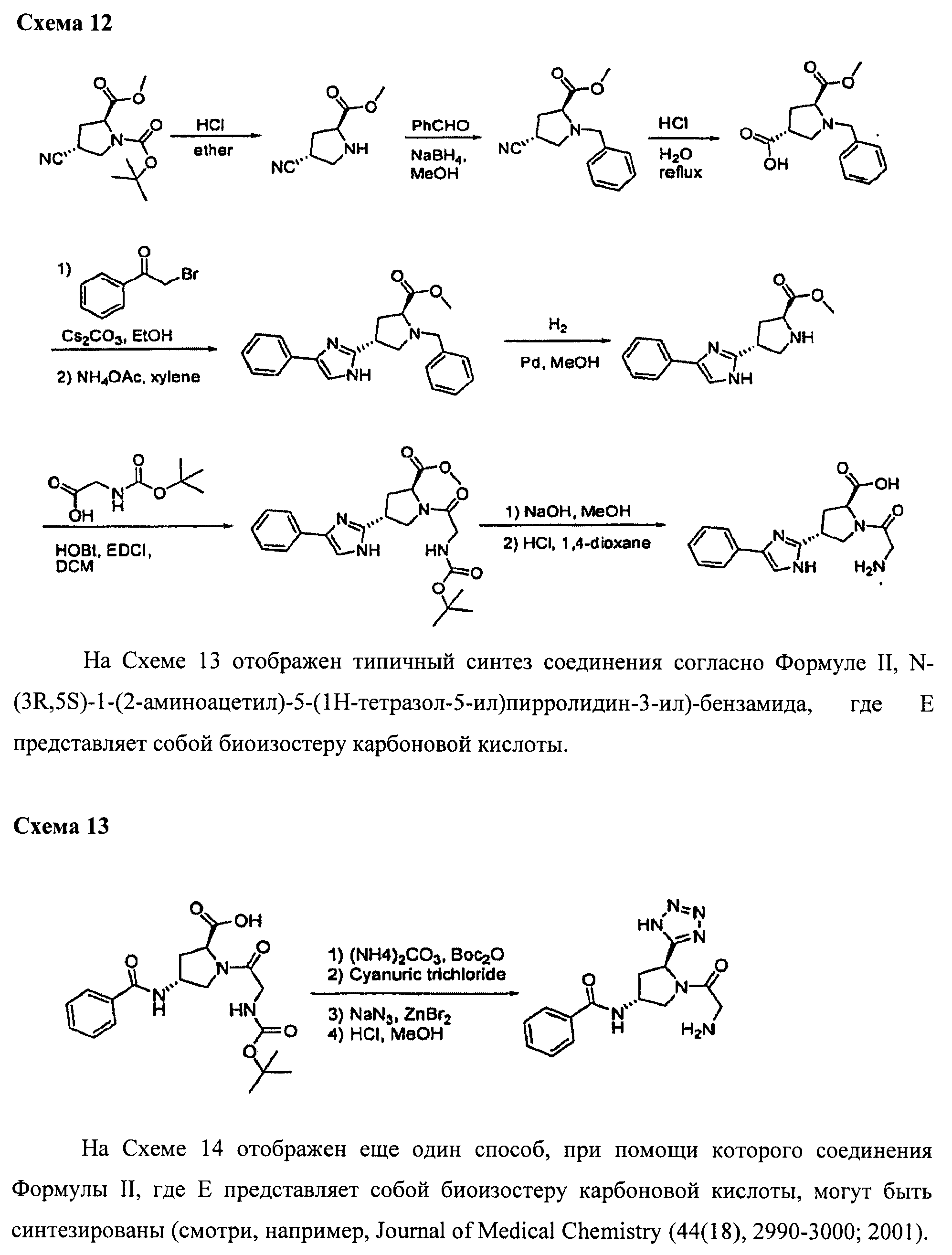
Биологически активная добавка IronMan L-Карнитин 60капсул
L-карнитин — пищевая добавка, содержащая L-карнитин в форме соли винной кислоты (тартрат L-карнитина).
L-карнитин необходим для переноса жирных кислот из цитоплазмы в клеточные энергостанции — митохондрии, где происходит их утилизация и высвобождение энергии. Благодаря этому, при приеме карнитина проявляется жиросжигающий эффект, особенно в сочетании с достаточной физической нагрузкой. Кроме того, современные данные показывают, что карнитин улучшает работу имунной системы, активизирует деятельность токсиноутилизирующих и токсиновыводящих систем, благоприятно воздействует на сердечно-сосудистую систему. Карнитин также участвует в протеиновом метаболизме и синтезе мышечной ткани.
Тартрат L-карнитина из всех солей имеет самую высокую концентрацию L-карнитина, кроме того, обладает приятным слегка кисловатым вкусом. Именно поэтому данная форма L-карнитина наиболее часто используется в производстве спортивных пищевых добавок.
Состав: желатиновая капсула(оболочка), l-карнитин тартрат, мальтодекстрин, комплексная пищевая добавка (среднецепочные триглецириды, казеинат натрия, глюкозный сироп, эмульгатор эфиры глицеридов лимонной и жирных кислот, антиокислитель смесь токоферолов), агент антислеживающий диоксид кремния.
Пищевая ценность одной порции (1 капсула)
|
|
(среднее значение)/% от рекомендуемого уровня суточного потребления: |
|
Энергетическая ценность |
5 кДж |
|
(калорийность) |
(1,2 ккал) |
|
Белки |
0,09 г |
|
Жиры |
0,01 г |
|
Углеводы |
0,016 г |
|
L-карнитин тартрат |
300 мг |
|
(в т.ч L-карнитин |
200 мг |
Рекомендации по применению: взрослым по 1 капсуле 2 раза в день во время еды. Продолжительность приема -30 дней.
Условия хранения: хранить в сухом, защищенном от света месте при температуре от 5°С + до +22°С.
Срок годности 24 месяца.
L-Карнитин — описание ингредиента, инструкция по применению, показания и противопоказания
Описание L-карнитина
L-карнитин – это соединение, родственное витаминам группы B. Оно синтезируется в почках и печени из лизина и метионина при обязательном участии железа и аскорбиновой кислоты. Часть вещества поступает в организм с мясной и молочной пищей. Наибольшая его концентрация наблюдается в мышцах.
Влияние на организм
Главная функция L-карнитина – выработка энергии. Транспортируя жирные кислоты в митохондрии, он способствует их окислению до ацетил-КоА и преобразованию в АТФ.
Карнитин оказывает антигипоксический и анаболический эффект. Стимулирует регенерацию тканей, повышает интенсивность липидного обмена, налаживает метаболизм кофермента A и, мобилизуя жировое депо, тормозит расход белков и углеводов.
Еще одно полезное свойство соединения – стимуляция ферментативной активности в ЖКТ, что повышает аппетит и нормализует пищеварение. Оно замедляет образование молочной кислоты при физических нагрузках, улучшает доставку питательных веществ к нервным волокнам и ускоряет сжигание жировых отложений между мышечными.
Оно замедляет образование молочной кислоты при физических нагрузках, улучшает доставку питательных веществ к нервным волокнам и ускоряет сжигание жировых отложений между мышечными.
Внимание! L-карнитин повышает адаптационные способности организма и улучшает работоспособность мозга, снабжая его кислородом и энергией.
Прием карнитина показан при синдроме хронической усталости, вегетососудистой дистонии, частых инфекционных или простудных заболеваниях у детей, для профилактики проблем с сердцем.
Нормы потребления L-карнитина
Взрослым людям нужно около 300 мг Л-карнитина в день. Детям до года – 10–15 мг, до 6 лет – 30–90 мг, до 18 лет – 100–300 мг соединения. В среднем, организм человека самостоятельно синтезирует 25% от требуемого суточного объема карнитина.
Дефицит (гиповитаминоз)
При недостатке карнитина наблюдается быстрая утомляемость, депрессивность, сонливость, «мышечная дрожь», пониженное артериальное давление, снижение успеваемости у школьников, сбои в работе печени и сердца.
Переизбыток (гипервитаминоз)
Переизбыток вещества также вреден. Он приводит к боли в животе, тошноте. У больных с высоким уровнем мочевины возможны миастенические расстройства.
Внимание! При возникновении симптомов избытка карнитина нужно прекратить прием препарата, сделать промывание желудка, принять адсорбент, к примеру, активированный уголь, и обратиться к врачу.
Оценка обеспеченности организма
Количество карнитина в организме определяют с помощью жидкостной хроматографии/масс-спектрометрии. Хроматография разделяет мочу на составляющие, а масс-спектрометрия идентифицирует их, выявляя концентрацию Л-карнитина.
Пищевые источники L-карнитина
Синтез L-карнитина происходит в почках и печени. Накапливается он преимущественно в мышцах. Отсюда ясно, что искать его нужно в продуктах животного происхождения. В растительной пище: фруктах, орехах, злаках – соединение присутствует в незначительных количествах.
Внимание! Чем краснее мясо, тем выше в нем концентрация Л-карнитина.
Топ-8 природных источников Л-карнитина:
- Говядина.
- Свинина.
- Ливер.
- Белое мясо.
- Куриные яйца.
- Молоко.
- Арахисовое масло.
- Злаковые.
Противопоказания и побочные эффекты
Добавки карнитина противопоказаны в период грудного вскармливания, при непереносимости белковой пищи и истощении организма. При передозировке могут проявиться побочные эффекты:
- судороги;
- диарея;
- высыпания;
- спазмы в животе;
- уремия;
- тошнота;
- бессонница.
Профилактическое и лечебное применение
Выпускается таблетированный, капсулированный и жидкий L-карнитин. Жидкий препарат принимают несколько раз в день, курсами по 3–4 недели. Суточная дозировка для взрослых – 5 мл, для детей 6–12 лет – 2–2,5 мл, для спортсменов – до 15 мл.
Жидкий препарат принимают несколько раз в день, курсами по 3–4 недели. Суточная дозировка для взрослых – 5 мл, для детей 6–12 лет – 2–2,5 мл, для спортсменов – до 15 мл.
Таблетки и капсулы пьют, не разжевывая и запивая водой. Дневная дозировка – 250–500 мг активного вещества. При активных занятиях спортом дозу можно повышать до 1500 мг. Детям препарат противопоказан.
L-Карнитин — Аминокислоты
По физическим свойствам L-карнитин — белый кристаллический порошок, гигроскопичен, хорошо растворим в воде. Существует две стереоизомерных формы: L-карнитин и D-карнитин. Биологической активностью обладает только L-форма. D-карнитин вреден для организма, так как является конкурентным антагонистом L-карнитина.
Биосинтез левокарнитина
L-карнитин синтезируется в печени и почках, из которых транспортируется в другие ткани и органы. Синтез левокарнитина протекает при участии витаминов С, В3, В6, В9, В12, железа, лизина, метионина и некоторых энзимов. При дефиците хотя бы одного из компонентов может развиваться недостаточность L-карнитина с нарушением функций организма. Это наблюдается редко, зачастую при генетическом дефекте ферментов, ответственных за синтез L-карнитина.
При дефиците хотя бы одного из компонентов может развиваться недостаточность L-карнитина с нарушением функций организма. Это наблюдается редко, зачастую при генетическом дефекте ферментов, ответственных за синтез L-карнитина.
Функции и эффекты L-карнитина
Сжигание жира. L-карнитин осуществляет транспорт жирных кислот (структурные элементы жира) в митохондриальный матрикс, где происходит их разрушение с выделением энергии. Дополнительный прием L-карнитина осуществляется в надежде интенсифицировать разрушение жиров.
Увеличение умственной и физической энергии. Как показали результаты двойного слепого плацебоконтролируемого исследования, проведенного в 2007 году в Италии, назначение L-карнитина в суточной дозе 2 г в течение 6 месяцев приводило к повышению умственной и физической активности. Испытуемые отмечали улучшение настроения, повышение выносливости и поднятие общего тонуса.
Устойчивость к стрессу. Исследованиями доказана эффективность карнитина в увеличение толерантности к стрессам и повышении адаптационных возможностей организма человека.
Исследованиями доказана эффективность карнитина в увеличение толерантности к стрессам и повышении адаптационных возможностей организма человека.
Детоксикация. L-карнитин поддерживает уровень свободного CoASH, который участвует в обезвреживании органических кислот и ксенобиотиков, необходим для функционирования некоторых ферментов и для нормальной работы цикла Кребса.
Анаболические функции. Анаболический эффект L-карнитина был установлен экспериментально, в ходе опытов с применением этой добавки ученые обратили внимание, что испытуемые не только теряли жир, но наряду с этим увеличивали сухую мышечную массу. Механизм этого действия до сих пор до конца не изучен, однако есть ряд теорий, которые объясняют анаболическое действие карнитина его участием в обмене фосфолипидов, оптимизацией баланса Ацетил-CoA/CoASH, большим использованием в качестве источника энергии жира, улучшением нейротрансмиссии.
Снижает холестерин. L-карнитин снижает уровень вредного холестерина, тем самым предотвращая сужение сосудов сердца и мозга, профилактирует инфаркты и инсульты. Кроме того, L-карнитин улучшает метаболизм миокарда, оказывает антиоксидантное действие. Клинические исследования показали, что после курса карнитина люди с заболеваниями сердца реже предъявляли жалобы, а функция миокарда улучшалась.
L-карнитин снижает уровень вредного холестерина, тем самым предотвращая сужение сосудов сердца и мозга, профилактирует инфаркты и инсульты. Кроме того, L-карнитин улучшает метаболизм миокарда, оказывает антиоксидантное действие. Клинические исследования показали, что после курса карнитина люди с заболеваниями сердца реже предъявляли жалобы, а функция миокарда улучшалась.
Другие эффекты. L-карнитин осуществляет нейропротекторное, антигипоксическое, антиоксидантное и антитиреоидное действие, предотвращает апоптоз и остеопороз, а также стимулирует регенерацию тканей.
L-карнитин в пище
Основными пищевыми источниками L-карнитина являются мясо, рыба и молочные продукты. Суточная норма этого вещества (300 мг) содержится примерно в 300-400 г сырой говядины, к тому же при термической обработке мяса значительная часть карнитина теряется, это обстоятельство диктует необходимость приема карнитина в виде дополнительных добавок.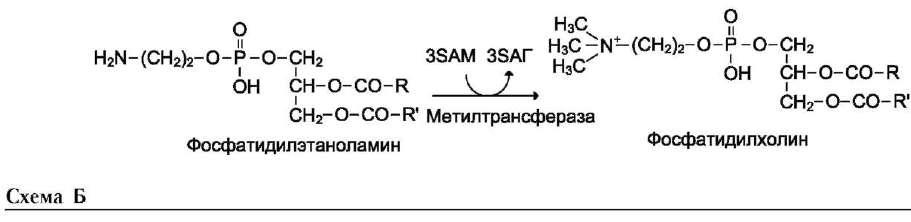
Содержание L-карнитина в пищевых продуктах в мг на 100 г продукта.
| Продукт | L-карнитин мг/100 г |
Продукт | L-карнитин мг/100 г |
| Мясной экстракт | 3686 | Грибы | 1,3-15 |
| олень, лось, северный олень | 35-193 | Птица | 4,3-13,3 |
| Овцы, козы | 16,7-190 | Морские животные | 1,7-13,2 |
| Лошадь, кенгуру | 117-166 | Сыр | 0,6-12,7 |
| Говядина | 45-143 | Молоко, молочные продукты | 2,1-9,7 |
| Заяц | 44,1-120 | Бульон | 1,1-6,1 |
| Теленок | 69,7-105 | Заменителей грудного молока | 1-4,3 |
| Кабан | 18-46 | Растительное масло, сливочное масло, маргарин | 0-1,1 |
| Мясные продукты | 1,2-38,6 | Зерновые (хлеб, макаронные изделия, рис) | 0,33-0,75 |
| Кролик | 10,2-24,4 | Орешки | 0,02-0,67 |
| Домашняя свинья | 14,4-24 | Овощи | 0,05-0,53 |
| Дичь | 3-21,1 | Фрукты | 0,01-0,35 |
L-карнитин в спорте
Карнитин важен в тех случаях, когда необходимо повысить общую и специальную выносливость в аэробных видах спорта (бег, плавание, гребля и т.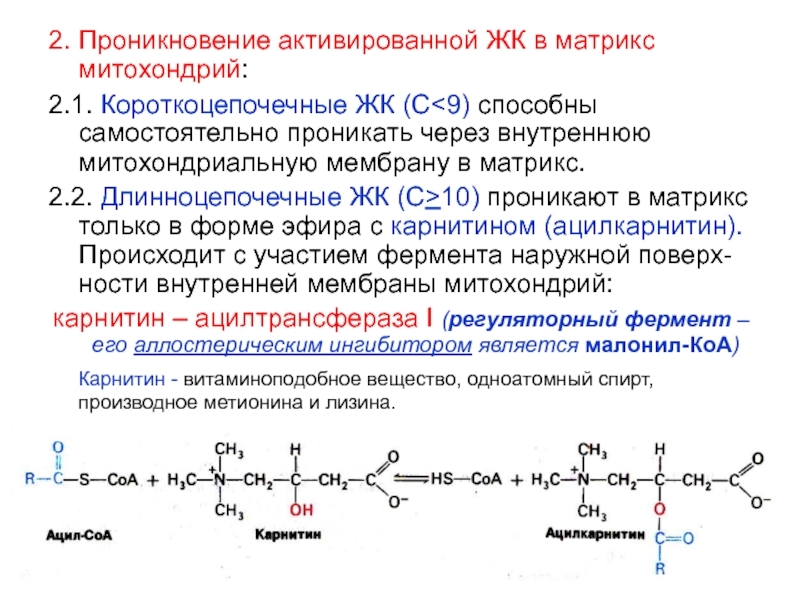 д.). Если спортсмен не озабочен снижением массы тела, максимального усиления энергетики можно достигнуть при сочетании левокарнитина с повышенным количеством жиров в рационе. Существует специальная высокожировая диета, которая назначается одновременно с большими дозами карнитина. Особенно предпочтителен такой способ усиления биоэнергетики тогда, когда нужно избежать падения массы тела в процессе тренировок.
д.). Если спортсмен не озабочен снижением массы тела, максимального усиления энергетики можно достигнуть при сочетании левокарнитина с повышенным количеством жиров в рационе. Существует специальная высокожировая диета, которая назначается одновременно с большими дозами карнитина. Особенно предпочтителен такой способ усиления биоэнергетики тогда, когда нужно избежать падения массы тела в процессе тренировок.
Левокарнитин способствует повышению выносливости как в аэробных, так и в анаэробных (пауэрлифтинг, культуризм и т.д.) видах спорта. Следует отметить, что анаболическое действие левокарнитина может быть замаскировано общим падением веса тела в результате исчезновения подкожно-жировой и внутренней жировой клетчатки. Поэтому при оценке анаболической действия карнитина следует руководствоваться критериями, отличными от таких показателей, как масса тела и объем конечностей. В данном случае это процентное соотношение массы жира и общей массы тела.
Для достижения максимального эффекта, левокарнитин должен применяться наряду с хорошо сбалансированной диетой и тренировочной программой. Левокарнитин не является допингом и может использоваться в спортивном питании без всяких ограничений.
Левокарнитин не является допингом и может использоваться в спортивном питании без всяких ограничений.
При отсутствии изначальных нарушений синтеза в организме рекомендуется применять короткими курсами, так как при длительном приеме наблюдается синдром отмены — снижается выработка собственного левокарнитина и появляется необходимость постоянно принимать экзопрепарат.
Сочетание с другими добавками
L-карнитин отлично сочетается со всеми видами препаратов ориентированных на уменьшение жировой массы, потенцирует их действие и снижает частоту побочных эффектов. L-карнитин можно принимать также и во время циклов по наборе массы, с целью предотвращения жирообразования, принимая его с протеином, гейнером и любыми другими комплексами.
Эффективным считается комбинированное применение препаратов карнитина и коэнзима Q10, поскольку их действие направлено на 2 основные точки приложения: реактивность (L-карнитин) и ресурсы психологической системы (коэнзим Q10).
Дозы L-карнитина и время приема
Оптимальными считаются дозы карнитина от 500 мг до 2 г в сутки (обычно разовая доза составляет 500 или 750 мг в 3 приема, либо 1000 мг в 2 приема). Превышать 2 г нет смысла, так как исследования не выявили никаких преимуществ более высоких доз. Принимайте L-карнитин за 30 минут перед тренировкой и утром на голодный желудок. В дни свободные от тренинга принимайте также утром и в обед между приемами пищи на голодный желудок. Именно в утренние часы и во время физических нагрузок L-карнитин обладает наибольшей активностью.
Биосинтез L-карнитина и его назначение
L-карнитин (или Л-карнитин в русской транскрипции) представляет собой соединение естественного биологического синтеза, которое по своим химическим характеристикам сходно с витаминной В-группой. Это заменимая кислота, которая формируется в печени, ее исходными компонентами выступают метионин и лизин. Другое название Л-карнитина – левокарнитин, он принимает активное участие в жировом обмене (но не в жиросжигании).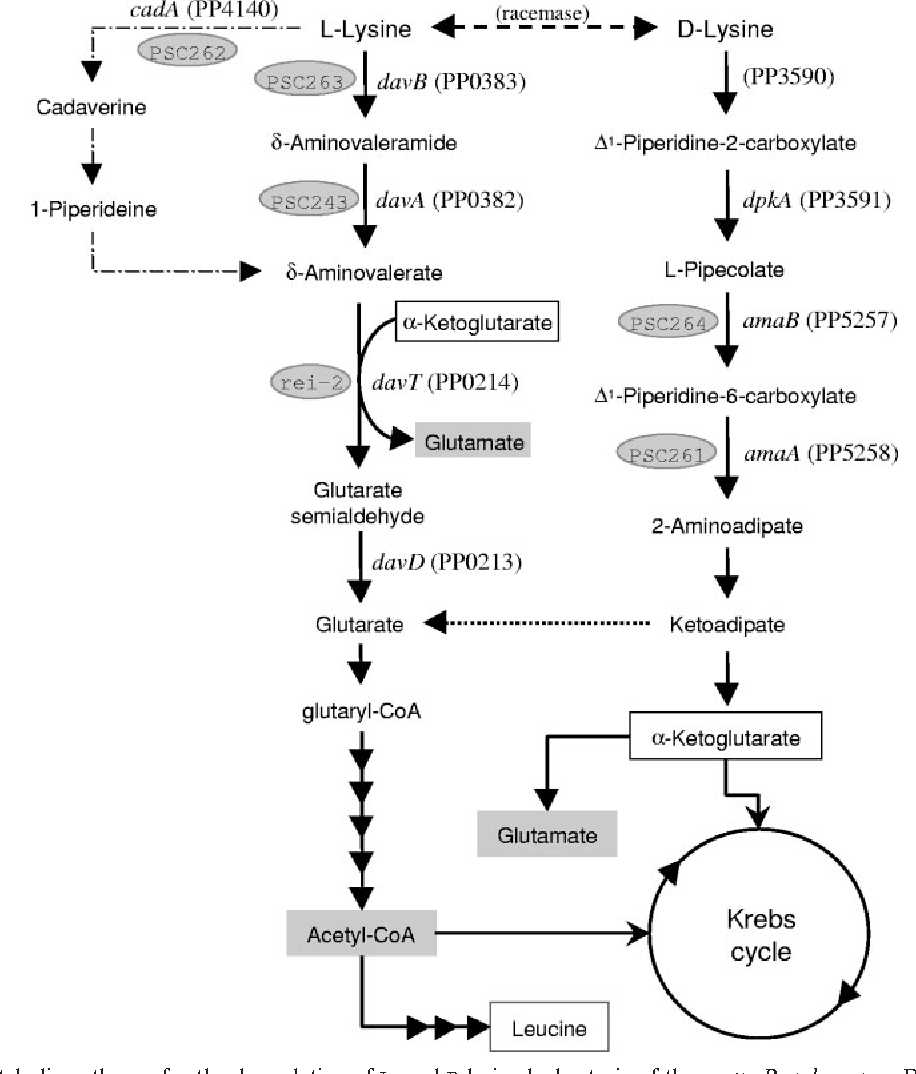
Л-карнитин не относится к разряду витаминов и вопреки распространенному заблуждению (которое многие «специализированные» сайты выдают за научные данные) его никогда не причисляли к витаминоподобным веществам и не называли витамином В11 (лишь единожды в 1905 году, ученые, впервые выделившие L-карнитин, условно назвали его «витамин Вт», причем это название почти сразу было упразднено).
Ввиду того, что Л-карнитин участвует в поддержании активности КоА (кофермент ацетилирования), в медицинской сфере он используется при хроническом дефиците левокарнитина генетического генеза, а также для лечения заболеваний почек, которые требуют проведения гемодиализа. Впервые Л-карнитин синтезировали в лабораторных условиях в 1960 году, но лишь в 1962-м, спустя более полувека после его открытия, ученые, наконец, поняли функцию L-карнитина в человеческом организме: он транспортирует жирные кислоты с длинной цепочкой сквозь внутреннюю мембрану мышечных митохондрий. Считается, что при интенсивных аэробных нагрузках, жирные кислоты в митохондриях мускулов метаболизируются в тепловую энергию, отсюда – распространенное заблуждение об эффективности L-карнитин для похудения.
На самом деле, исследование Л-карнитина и его функциональных особенностей в форме добавки продолжается до сих пор. Таких работ действительно много (об этом производители спортивного питания никогда не забывают упомянуть), однако полученные данные не носят системного и фундаментального характера, зачастую они не имеют достаточной доказательной базы и даже противоречат друг другу. Иными словами, эффективность применения Л-карнитина для похудения не является общепризнанным научным фактом (более подробно об этом – во второй части статьи).
Как уже отмечалось, L-карнитин синтезируется в печени, он вырабатывается из двух аминокислот – лизина и метионина, при активном участии витаминов группы В (3, 6, 9, 12), витамина С, железа и ряда энзимов. Недостаток любого из указанных элементов приводит к дефициту L-карнитина, что в первую очередь нарушает работу почек. Однако в подавляющем большинстве случаев подобные проблемы носят сугубо генетических характер.
Ввиду того, что биосинтез L-карнитина не обладает всесторонним научным обоснованием, некорректно говорить о его эффективности в роли спортивной добавки (в частности, это касается полезности Л-карнитина для похудения). Первое исследование, в котором утверждалось, что дополнительный прием этого вещества может способствовать повышению работоспособности и усиленному жиросжиганию, было проведено Дж. Бремером в 1983 году. Но в его работе «Карнитин – метаболизм и функционал» приводится ряд слабо аргументированных гипотез, которые не были подтверждены опытным путем.
Первое исследование, в котором утверждалось, что дополнительный прием этого вещества может способствовать повышению работоспособности и усиленному жиросжиганию, было проведено Дж. Бремером в 1983 году. Но в его работе «Карнитин – метаболизм и функционал» приводится ряд слабо аргументированных гипотез, которые не были подтверждены опытным путем.
Впоследствии исследования Л-карнитина продолжились, их пик пришелся на 2000-е годы. Из наиболее значимых справедливо выделить следующие работы: Х. Сеим «Л-карнитин и его прекурсор гамма-бетаин» (2001), В. Кузин «Карнитина хлорид (25 лет в клинической практике)» (2003), Х. Лёстер «Карнитин и сердечнососудистые заболевания» (2003), А. Штейбер «Пищевой и синтетический карнитин с точки зрения функциональности» (2004), М. Малагуарнера «Влияние Л-карнитина на здоровье людей в возрасте от 100 лет» (2007), С. Ключников «Обоснование применения L-карнитина и коэнзима Q10 у подростков» (2008), М. Декхани «Влияние превышенного употребления тартрата карнитина на показатели липидного обмена» (2015).
Ни одно их этих исследований не имеет достаточной доказательной базы, чтобы можно было признать эффективность L-карнитина для похудения. Также не доказано влияние добавок с Л-карнитином на повышение результативности тренировок. На данный момент многие «специалисты» апеллируют к исследованию М. Декхани (в вышеприведенном перечне это крайнее исследование), однако нужно понимать, что израильские ученые проводили испытания с участием всего лишь 22 добровольцев. Очевидно, что 22 участника – недостаточное количество для любого эксперимента, даже для элементарного соцопроса, не говоря уже о полноценной научной работе.
Заявления о том, что прием L-карнитина якобы повышает выносливость, защищает мышцы от разрушения и улучшает когнитивные функции атлетов, подверженных аэробным нагрузкам, были опровергнуты в 2011 году научной работой Е. Моджтаба «Отсутствие влияния добавки тартрат Л-карнитина на обмен жиров и аэробную производительность». В том же году ведущими лабораториями мира был проведен ряд экспериментов, резюмированных в научной публикации М. Алейниковой «Систематический обзор и мета-анализ исследований по изучению эффективности L-карнитина», где автор наглядно доказывает несостоятельность заявлений об эффективности этой добавки. На сегодняшний день данная работа является наиболее полной русскоязычной публикацией, адекватно отражающей уровень исследованности Л-карнитина.
Обратите внимание, что выводы о необоснованности заявлений производителей Л-карнитина основаны на экспериментах, в которых приняли участие тысячи добровольцев (все эти исследования указаны в библиографии к статье М. Алейниковой), что не идет ни в какое сравнение с двадцатью двумя участниками исследований М. Декхани. На сегодняшний день фирмы, выпускающие «жиросжигатель» L-карнитин в капсулах, порошке и жидком виде, гарантируют следующие эффекты:
Повышение интенсивности «жиросжигания». L-карнитин даже в своей естественной форме (не говоря уже о синтетических добавках) не обладает такой функцией.
Повышение умственных и физических способностей. Данный тезис базируется на экспериментальной работе, которая была проведена итальянскими учеными под руководством М. Малагуарнеры в 2007 году. Обратите внимание, что в том исследовании участвовало 66 добровольцев, возрастом (что особенно забавно!) от ста до ста шести лет.
Повышение стрессоустойчивости. Это утверждение основывается на вышеприведенном исследовании С. Ключникова, в котором принимало участие всего 48 подростков, разделенных на три функциональные группы. Очевидно, что группа из 16 человек, на которых тестировалась способность Л-карнитина к нормализации параметров вегетативной нервной системы, не может выступать в роли доказательного базиса.
Анаболический эффект. Эффективность приема Л-карнитина в контексте повышенного прироста сухой мышечной массы обосновывают работой Х. Сеима (первое исследование в вышеприведенном перечне), однако заключение этой работы основано на ряде неподтвержденных экспериментов с общим числом участников менее 50.
Снижение уровня холестерина и профилактика сердечнососудистых заболеваний.
«Американский журнал клинического питания» 1 августа 2000 года опубликовал сводную таблицу «Карнитиновые добавки и физические упражнения», в которой собраны десятки экспериментов разных лет. Эксперты журнала сделали вывод, который очевиден для любого человека, взглянувшего на данную таблицу, – влияние добавок с L-карнитином на профессиональных спортсменов попросту отсутствует.
В июне того же года в «Международном журнале спортивного питания» Р. Виллани опубликовала резюмирующую статью, где рассматриваются десятки экспериментов разных лет, посвященные эффективности Л-карнитина для похудения, а также результаты авторских исследований. Данная статья находится в свободном доступе, в том числе – на официальном сайте Национальной медицинской библиотеки США. Результат научной работы Р. Виллани подтверждает, что регулярный прием L-карнитина не способствуют снижению веса даже в сочетании с интенсивными аэробными тренировками.
Таким образом, применение L-карнитина в сфере бодибилдинга и фитнеса абсолютно необоснованно. Л-карнитин (в порошке, капсулах или в жидком виде) никак не влияет на показатели спортсмена и не является жиросжигающим препаратом. Вне зависимости от способа применения L-карнитин не дает комбинирующего эффекта с другими добавками. Любое утверждение о действенности Л-карнитина со стороны спортсмена можно рассматривать лишь как результат эффекта плацебо. Но аналогичное заявление со стороны производителя является намеренным введением в заблуждение.
Обычно Л-карнитин принимают в дозе до 2 граммов в сутки, разделенных на 2-3 приема. Интересно отметить, что исследование Р. Виллани, доказавшее неэффективность добавки в плане жиросжигания, основывалось именно на этой дозировке. Также обратите внимание, что среди вероятных побочных эффектов L-карнитина некоторые «специализированные» порталы приводят сведения о том, что регулярный прием добавки приводит к существенному повышению ТМАО (триметиламиноксида) в крови. Повышение ТМАО в перспективе вызывает атеросклеротические метаморфозы в стенках кровеносных сосудов, что в свою очередь может привести к ряду сердечнососудистых заболеваний. Однако научных работ, которыми обосновывается данное утверждение, на самом деле не существует.
В результате, прием Л-карнитина как спортивного питания не имеет ни положительных эффектов, ни побочных действий. Применение этой добавки в рамках любых тренировочных комплексов попросту бессмысленно
Тем не менее, если у вас остались какие-то вопросы, то вы можете задать их на тренировки Чемпиона и рекордсмена мира Элите России Волоскому Евгению ,обязательно вам ответит. Будьте здоровы, и не забывайте, что подтверждением эффективности той или иной добавки может служить только обоснованный экспериментальный базис!
Информация переработана и дополнена: elit-fit.ru
Автор статьи: Евгений Волоский
Карнитин | Елена Корнилова
Карнитин (он же L-карнитин, левокарнитин) — одна из самых популярных сегодня спортивных пищевых добавок. Но карнитин — не просто жиросжигатель: по своей химической структуре он схож с аминокислотой, поэтому их обычно и рассматривают вместе, но по своей физиологической роли он так же важен, как и витамины группы В.
Роль карнитина в организме
Карнитин не участвует в синтезе белков и не является нейромедиатором. Его основная функция в организме — это транспорт длинноцепочечных жирных кислот, в процессе окисления которых выделяется энергия. Также это вещество обладает способностью снижать уровень триглицеридов в крови, способствует снижению массы тела, усиливает антиоксидантное действие витаминов С и Е.
Митохондрии, маленькие энергостанции внутри наших клеток, неустанно производят АТФ — энергетическую валюту, без которой вы не сможете просуществовать и несколько секунд. «Дровишки» для синтеза АТФ — это прежде всего углеводы и жиры, соединяющиеся с кислородом через несколько биохимических реакций. Именно карнитин дает мощный толчок жирным кислотам, дабы те попали в митохондриальную топку. Без карнитина получение энергии из жиров невозможно. То есть жиры вы без него не усвоите, а клетки и ткани будут страдать от энергетического голода.
Источники карнитина
Мы способны синтезировать карнитин во взрослом возрасте, однако процесс этот непростой, для него необходимы две незаменимые аминокислоты (лизин и метионин), железо (Fe2+), витамин В6 в форме пиридоксаль-5′-фосфата, ниацин в форме никотинамидадениндинуклеотида (NAD), витамин С. Одним из ранних симптомов дефицита витамина С является усталость, которая как раз связана со снижением синтеза L-карнитина. Также для производства карнитина важная активность нескольких ферментов.
Эндогенная выработка у взрослого человека обеспечивает лишь 10% потребности организма в карнитине и при этом требует присутствия витаминов С, группы В, железа, фолиевой кислоты, аминокислот лизина, метионина и некоторых ферментов. Нехватка даже одного из необходимых кофакторов приводит к развитию дефицита карнитина.
Экзогенный карнитин поступает в организм с пищей, прежде всего с мясом (чем «краснее» мясо, тем оно насыщеннее карнитином) и другими продуктами животного происхождения, в том числе молочными. Организм «не умеет» создавать запасов карнитина на будущее, как это происходит с другими видами витаминов. Неиспользованные организмом соединения просто выводятся почками вместе с мочой.
Мужчинам из-за их большой мышечной массы требуется большее количество карнитина, чем женщинам. У вегетарианцев более вероятно возникновение дефицита этого питательного вещества, чем у «мясоедов», поскольку карнитин не встречается в белках растительного происхождения.
Запомните, карнитин хоть и содержится в пище, его там совсем немного! Например, в 100 г говяжьего стейка всего 95 мг, в 100 г трески — 5, 6 мг, в яйцах — 0,0121 мг. Восполнять сильный дефицит карнитина едой — действо, заранее обреченное на провал.
Польза карнитина для взрослых
В среднем здоровым взрослым требуется около 200−500 мг карнитина в сутки, но дозировка существенно увеличивается (в 4−20 раз) при физических, эмоциональных и умственных нагрузках. Карнитин особенно необходим при стрессе, в период беременности и кормления грудью.
Карнитин — «любимчик» спортсменов, он помогает облегчить состояние при интенсивных физических нагрузках, его принимают для снижения утомляемости, повышения работоспособности и выносливости.
Также карнитин используется в комплексной терапии при некоторых заболеваниях:
- бесплодие у мужчин
- гипоперфузия
- дисциркулярная энцефалопатия
- заболевания кожи: себорейный дерматит, псориаз
- заболевания кожи: себорейный дерматит, псориаз, очаговая склеродермия, экзема, красная волчанка
- задержка роста
- инфаркт миокарда
- ишемическая кардиопатия, инсульт
- нарушения мозгового кровообращения
- ожирение
- поражение головного мозга
- постинфарктные состояния
- стенокардия
- тиреотоксикоз (является частичным антагонистом тироксина).
Польза карнитина для детей
Карнитин для детей имеет даже более важное значение, чем для взрослых: он необходим в достаточном количестве для правильного развития и новорожденному, и растущему организму дошкольника, и школьнику при повышенных умственных и психоэмоциональных нагрузках во время учебных занятий и экзаменов.
Даю Лёве карнитин (в жидкой форме от ALLMAX Nutrition), потому что по анализам у него похрамывает окисление жирных кислот. В малышковом возрасте потребность в карнитине огромная, а синтез страдает. По исследованиям карнитин детям в дозе до 2000 мг безопасен. Я бы всем деткам вводила хотя бы аптечный «Элькар», курсом.
У детей, особенно раннего возраста, эндогенный синтез карнитина крайне ограничен: активность гамма-бутиробетаингидроксилазы у новорожденных составляет всего 12,0% от ее уровня у взрослых; а последний достигается только к 15 годам жизни. Это делает детей более уязвимыми к недостатку экзогенного поступления карнитина с пищей (особенно животного белка), которые покрывают потребности в карнитине в лучшем случае наполовину. Недостаточность эндогенного синтеза карнитина и его поступления с едой могут приводить к дефициту карнитина в организме, особенно в условиях, способствующих повышенному выведению и нарушению всасывания. В результате нередко развивается недостаточность карнитина с самыми разными ее системными проявлениями.
Это важно: карнитиновая недостаточность считается одним из основных виновников синдрома внезапной смерти младенцев.
Вот несколько выдержек из научной работы, доказывающих потребность в карнитине у детей:
Особенно быстро недостаточность карнитина формируется у детей раннего возраста. Эндогенные запасы у них крайне ограничены и быстро истощаются при различных стрессовых ситуациях (инфекционные заболевания, желудочно-кишечные расстройства, нарушения вскармливания). биосинтез карнитина у этих детей резко снижен в связи с небольшой мышечной массой и недостатком исходных белковых компонентов для синтеза, а поступление карнитина с обычными пищевыми продуктами не способно поддержать достаточный его уровень в крови и тканях. У недоношенных и детей с малой массой тела особенно выражена зависимость от дополнительного получения карнитина. Младенцы, особенно недоношенные, рождаются с низкими запасами карнитина, что может поставить их под угрозу дефицита, учитывая их быстрый темп роста.
Тяжелые заболевания различного генеза — вирусные и бактериальные инфекции (респираторные, кишечные и др.), оперативные вмешательства у детей первого года жизни значительно чаще, чем в другие возрастные периоды, ведут к выраженной карнитиновой недостаточности в связи с небольшими запасами эндогенного карнитина, низкой способностью к его биосинтезу и высоким уровнем потребления в процессе метаболизма. Именно по указанной причине у детей раннего возраста тяжело протекает период восстановления, сопровождающийся потерей аппетита, снижением прибавки массы тела, развитием гипотрофии.
Основные признаки дефицита L-карнитина являются следствием развивающихся нарушений энергетического обмена и метаболизма липидов и связанных с этим расстройств других видов обмена веществ:
- быстрая утомляемость
- мышечная слабость
- гипотония
- отставание физического и психомоторного развития
- снижение школьной успеваемости
- сонливость или раздражительность
- нарушение функции сердца, вплоть до кардиомиопатии
- увеличение размеров печени и нарушение ее функции.
Все это доказывает целесообразность использования дополнительных источников карнитина для лечения и профилактики его недостаточности в организме.
Детям на первом году жизни с вышеперечисленными заболеваниями карнитин назначается на 30−45 дней в суточной дозе 50−100 мг/кг в три равных приема перед едой.
Детям в спектре, а также с СДВГ карнитин, В2 и биотин крайне необходимы! Опыт российских педиатров показывает достоверное уменьшение аутизации при приеме карнитина: дети начинали смотреть в глаза, принимать участие в занятиях и играх. При этом их игра становилась более содержательной в соответствии с возрастными нормативами. Также у детей расширялся словарный запас, улучшалась коммуникативная функция речи. Общее соматическое состояние тоже детей становилось лучше, аппетит повышался, проблем со сном становилось меньше.
Также ученые подтвердили эффективность L-карнитина при лечении СДВГ в комплексной терапии с приемом ноотропов, препаратов метаболического ряда и атомоксетина в соответствующих возрасту дозировках (без антидепрессантов, анксиолитиков и нейролептиков!).
Диагностика дефицита карнитина
В анализах кроме общего и свободного карнитина в моче, можно посмотреть органические кислоты в моче. Повышение этилмалоновой, адипиновой и субериновой кислот — также маркер дефицита.
Кому нужно принимать карнитин?
Астеникам, людям с лишним весом, алкогольной зависимостью, женщинам, планирующим беременность и детям можно принимать карнитин курсово: 2−3 раза в год по 1,5−2 месяца. Формы: алкар, ацетил-L-карнитин, тартрат. Аптечный «Элькар» тоже подойдет (на безрыбье и рак рыба).
У карнитина, вводимого пероррально, биодоступность является низкой (≈ 10−20%), а если есть СИБР в зоне всасывания, то вообще беда. Поэтому я за восполнение высокими дозами (от 3000 до 5000 мг) жидкими или порошковыми формами. Или вводить карнитин внутримышечно/внутривенно.
Профилактические дозы: 20−30 мг на 1 кг веса, восполняющие дефицит — 50−100 мг на 1 кг веса. Пить натощак, либо за 30−60 минут до еды или через 2 часа после. При СИБР лучше вводить «Элькар» внутримышечно.
Возможные побочные явления: рыбный запах, диарея. Противопоказания: почечная недостаточность.
Карнитин «дружит» с В2, биотином, Q10, альфа-липоевой кислотой. Для повышения уровня энергии и получения ее из жиров — отличная комбинация, но для этого вы должны хорошо усваивать эти вещества из пищи, необходимы здоровые желчный и поджелудочная, если нет, то подключайте препараты желчи, ферменты с липазой.
[Биосинтез карнитина у млекопитающих] — PubMed
Окисление длинноцепочечных жирных кислот зависит от карнитина; эти жирные кислоты проникают в митохондрии для окисления только тогда, когда они связаны с карнитином в форме ацилкарнитинов. Чтобы удовлетворить потребность в карнитине, животные зависят как от экзогенных источников, так и от эндогенного синтеза. Целью данной статьи является обзор наших знаний об эндогенном синтезе карнитина.Предшественниками карнитина являются лизин и метионин, но его истинное происхождение — триметиллизин. Эта молекула либо получается с пищей, либо синтезируется в организме из L-лизина (связанного с белком), который 3 раза подряд метилируется S-аденозилметионином. Триметиллизин превращается в гидрокситриметиллизин, затем в триметиламинобутиральдегид и, наконец, в триметиламинобутрат (или гамма-бутиробетаин). Гамма-бутиробетаин гидроксилируется до карнитина.Эта цепочка реакций хорошо функционирует только при наличии трех витаминов — аскорбиновой кислоты, пиридоксина и ниацина. Исследования на крысах показали, что скелетные мышцы, сердце, кишечник, яички и особенно почки обеспечивают преобразование триметиллизина в гамма-бутиробетаин, но только яичко, и особенно печень, могут гидроксилировать гамма-бутиробетаин в карнитин. Однако у крыс относительная роль почек и печени в общем синтезе карнитина еще не определена.То же самое и с человеком, хотя было доказано, что человеческий мозг и почки, как и печень, имеют гамма-бутиробетаингидроксилазу. Известно, что скорость синтеза карнитина зависит от трех факторов — количества доступного триметиллизина, скорости переноса гамма-бутиробетаина в ткань (ткани), гидроксилирующей его, и активности гамма-бутиробетаингидроксилазы. Более того, похоже, что синтез карнитина не замедляется длительным голоданием, что он не полностью покрывает потребности организма в первые постнатальные дни и что он не снижается у двух пациентов с систематическим дефицитом карнитина.
Роль карнитина в заболевании | Питание и обмен веществ
Кендлер Б.С.: Карнитин: обзор его роли в профилактической медицине. Предыдущая Мед. 1986, 15: 373-390. 10.1016 / 0091-7435 (86)
-8.
CAS
Статья
Google ученый
De Vivo DC, Tein I: Первичные и вторичные нарушения метаболизма карнитина. Int Pediatr. 1990, 5: 8-
Google ученый
Rebouche CJ: кинетика, фармакокинетика и регуляция метаболизма L-карнитина и ацетил-L-карнитина. Ann N Y Acad Sci. 2004, 1033: 30-41. 10.1196 / Анналы.1320.003.
CAS
Статья
Google ученый
Ребуш CJ, Chenard CA: Метаболическая судьба диетического карнитина у взрослых людей: идентификация и количественная оценка метаболитов в моче и кале. J Nutr. 1991, 121: 539-546.
CAS
Google ученый
Cave MC, Hurt RT, Frazier TH, Matheson PJ, Garrison RN, McClain CJ, McClave SA: Ожирение, воспаление и потенциальное применение фармакологического питания. Nutr Clin Pract. 2008, 23: 16-34. 10.1177 / 011542650802300116.
Артикул
Google ученый
Rebouche CJ: Функция карнитина и потребности в течение жизненного цикла. Faseb J. 1992, 6: 3379-3386.
CAS
Google ученый
Ломбард К.А., Олсон А.Л., Нельсон С.Е., Ребуш К.Дж.: Карнитиновый статус лактововегетарианцев и строгих вегетарианцев для взрослых и детей. Am J Clin Nutr. 1989, 50: 301-306.
CAS
Google ученый
ВАЗ Ф.М., Вандерс Р.Дж .: Биосинтез карнитина у млекопитающих. Biochem J. 2002, 361: 417-429. 10.1042 / 0264-6021: 3610417.
CAS
Статья
Google ученый
Rebouche C: Карнитин: современное питание для здоровья и болезней.Под редакцией: Шилс М., Шике М., Росс А. и др. 2006, Филадельфия: Липпинкотт, Уильямс и Уилкинс, 537-544.
Google ученый
Анджелини С., Тревизан С., Исайя Дж., Пеголо Дж., Вергани Л.: Клинические разновидности дефицита карнитина и карнитин-пальмитоилтрансферазы. Clin Biochem. 1987, 20: 1-7. 10.1016 / S0009-9120 (87) 80090-5.
CAS
Статья
Google ученый
Bellinghieri G, Santoro D, Calvani M, Mallamace A, Savica V: Карнитин и гемодиализ. Am J Kidney Dis. 2003, 41: S116-122. 10.1053 / ajkd.2003.50099.
CAS
Статья
Google ученый
Ребуш CJ, Сейм H: метаболизм карнитина и его регуляция у микроорганизмов и млекопитающих. Annu Rev Nutr. 1998, 18: 39-61. 10.1146 / annurev.nutr.18.1.39.
CAS
Статья
Google ученый
Ахмад С: L-карнитин у диализных пациентов. Semin Dial. 2001, 14: 209-217. 10.1046 / j.1525-139X.2001.00055.x.
CAS
Статья
Google ученый
Шринивас С.Р., Прасад П.Д., Умапати Н.С., Ганапати В., Шехават П.С.: Транспорт бутирил-L-карнитина, потенциального пролекарства, через переносчик карнитина OCTN2 и переносчик аминокислот ATB (0, +). Am J Physiol Gastrointest Liver Physiol. 2007, 293: G1046-1053. 10.1152 / ajpgi.00233.2007.
CAS
Статья
Google ученый
Лопасчук Г.Д. Современные концепции исследования карнитина. Атланта. 1991
Google ученый
Breningstall GN: синдромы дефицита карнитина. Pediatr Neurol. 1990, 6: 75-81. 10.1016 / 0887-8994 (90)
-2.
CAS
Статья
Google ученый
Orngreen MC, Olsen DB, Vissing J: Толерантность к физической нагрузке при дефиците карнитин-пальмитоилтрансферазы II с внутривенным введением и пероральным приемом глюкозы. Неврология. 2002, 59: 1046-1051. 10.1001 / archneur.59.6.1046.
CAS
Статья
Google ученый
Сахлин К., Салльштедт Е.К., Бишоп Д., Тонконоги М.: Снижение окисления липидов во время тяжелых упражнений — каков механизм? J. Physiol Pharmacol. 2008, 59 (Дополнение 7): 19-30.
Google ученый
Peluso G, Barbarisi A, Savica V, Reda E, Nicolai R, Benatti P, Calvani M: Карнитин: осмолит, который играет метаболическую роль. J Cell Biochem. 2000, 80: 1-10. 10.1002 / 1097-4644 (20010101) 80: 1 <1 :: AID-JCB10> 3.0.CO; 2-W.
CAS
Статья
Google ученый
Шеннан Д.Б., Грант А., Рамзи Р.Р., Бернс С., Заммит В.А.: Характеристики транспорта L-карнитина тканью молочной железы лактирующих крыс. Biochim Biophys Acta. 1998, 1393: 49-56.
CAS
Статья
Google ученый
Burwinkel B, Kreuder J, Schweitzer S, Vorgerd M, Gempel K, Gerbitz KD, Kilimann MW: Мутации переносчика карнитина OCTN2 при системном первичном дефиците карнитина: новая мутация Arg169Gln и нетрадиционная мутация Arg282 нарушение сварки. Biochem Biophys Res Commun. 1999, 261: 484-487. 10.1006 / bbrc.1999.1060.
CAS
Статья
Google ученый
Ван И, Йе Дж, Ганапати В., Лонго Н.: Мутации в транспортере органических катионов / карнитина OCTN2 при первичном дефиците карнитина. Proc Natl Acad Sci USA. 1999, 96: 2356-2360. 10.1073 / pnas.96.5.2356.
CAS
Статья
Google ученый
Reuter SE, Faull RJ, Evans AM: Добавки L-карнитина в диализную популяцию: упускают ли австралийские пациенты? Нефрология (Карлтон). 2008, 13: 3-16.
CAS
Google ученый
Cederbaum SD, Koo-McCoy S, Tein I, Hsu BY, Ganguly A, Vilain E, Dipple K, Cvitanovic-Sojat L, Stanley C: Дефицит мембранного переносчика карнитина: долгосрочное наблюдение и мутация OCTN2 в первых задокументированных случай первичной недостаточности карнитина. Mol Genet Metab. 2002, 77: 195-201. 10.1016 / S1096-7192 (02) 00169-5.
CAS
Статья
Google ученый
Spiekerkoetter U, Huener G, Baykal T, Demirkol M, Duran M, Wanders R, Nezu J, Mayatepek E: бессимптомный и симптоматический первичный дефицит карнитина в одной семье из-за идентичных мутаций в органическом катионе / карнитине. транспортер OCTN2.J Inherit Metab Dis. 2003, 26: 613-615. 10.1023 / А: 1025968502527.
CAS
Статья
Google ученый
Wang Y, Kelly MA, Cowan TM, Longo N: миссенс-мутация в гене OCTN2, связанная с остаточной транспортной активностью карнитина. Hum Mutat. 2000, 15: 238-245. 10.1002 / (SICI) 1098-1004 (200003) 15: 3 <238 :: AID-HUMU4> 3.0.CO; 2-3.
CAS
Статья
Google ученый
Pons R, De Vivo DC: синдромы первичной и вторичной недостаточности карнитина. J Child Neurol. 1995, 10 (Дополнение 2): S8-24.
Google ученый
Коидзуми А., Нодзаки Дж., Охура Т., Кайо Т., Вада Ю., Незу Дж., Охаши Р., Тамай И., Сёдзи Ю., Такада Г., Кибира С., Мацуиси Т., Цудзи А.: Генетическая эпидемиология карнитина. ген транспортера OCTN2 в японской популяции и фенотипическая характеристика в японских родословных с первичным системным дефицитом карнитина.Hum Mol Genet. 1999, 8: 2247-2254. 10.1093 / hmg / 8.12.2247.
CAS
Статья
Google ученый
Nezu J, Tamai I, Oku A, Ohashi R, Yabuuchi H, Hashimoto N, Nikaido H, Sai Y, Koizumi A, Shoji Y, Takada G, Matsuishi T, Yoshino M, Kato H, Ohura T. , Tsujimoto G, Hayakawa J, Shimane M, Tsuji A: Первичный системный дефицит карнитина вызван мутациями в гене, кодирующем зависимый от ионов натрия переносчик карнитина. Нат Жене.1999, 21: 91-94. 10.1038 / 5030.
CAS
Статья
Google ученый
Эргувен М., Йилмаз О., Коч С., Чаки С., Айхан Ю., Донмез М., Долунай Г.: Случай раннего диагностированного дефицита карнитина с респираторными симптомами. Энн Нутр Метаб. 2007, 51: 331-334. 10.1159 / 000107675.
CAS
Статья
Google ученый
Mayatepek E, Nezu J, Tamai I, Oku A, Katsura M, Shimane M, Tsuji A: Две новые миссенс-мутации гена OCTN2 (W283R и V446F) у пациента с первичным системным дефицитом карнитина.Hum Mutat. 2000, 15: 118-10.1002 / (SICI) 1098-1004 (200001) 15: 1 <118 :: AID-HUMU28> 3.0.CO; 2-8.
CAS
Статья
Google ученый
Seth P, Wu X, Huang W., Leibach FH, Ganapathy V: Мутации в новом переносчике органических катионов (OCTN2), переносчике органических катионов / карнитина, с различными эффектами на функцию транспорта органических катионов и карнитин. транспортная функция. J Biol Chem. 1999, 274: 33388-33392. 10.1074 / jbc.274.47.33388.
CAS
Статья
Google ученый
Tang NL, Ganapathy V, Wu X, Hui J, Seth P, Yuen PM, Wanders RJ, Fok TF, Hjelm NM: Мутации OCTN2, органического переносчика катионов / карнитина, приводят к недостаточному поглощению клетками карнитина. при первичной недостаточности карнитина. Hum Mol Genet. 1999, 8: 655-660. 10,1093 / hmg / 8.4.655.
CAS
Статья
Google ученый
Sigauke E, Rakheja D, Kitson K, Bennett MJ: Дефицит карнитин-пальмитоилтрансферазы II: клинический, биохимический и молекулярный обзор. Lab Invest. 2003, 83: 1543-1554. 10.1097 / 01.LAB.0000098428.51765.83.
CAS
Статья
Google ученый
Vermeire S, Rutgeerts P: Текущее состояние генетических исследований воспалительных заболеваний кишечника. Genes Immun. 2005, 6: 637-645.
CAS
Google ученый
Ринальдо П., Матерн Д., Беннетт М.Дж .: Нарушения окисления жирных кислот. Annu Rev Physiol. 2002, 64: 477-502. 10.1146 / annurev.physiol.64.082201.154705.
CAS
Статья
Google ученый
Ринальдо П., Раймонд К., аль-Одаиб А., Беннетт М.Дж .: Клинические и биохимические особенности нарушений окисления жирных кислот. Curr Opin Pediatr. 1998, 10: 615-621. 10.1097 / 00008480-199810060-00014.
CAS
Статья
Google ученый
Scaglia F, Longo N: первичные и вторичные изменения неонатального метаболизма карнитина. Семин Перинатол. 1999, 23: 152-161. 10.1016 / S0146-0005 (99) 80047-0.
CAS
Статья
Google ученый
Winter SC: Лечение дефицита карнитина. J Inherit Metab Dis. 2003, 26: 171-180. 10.1023 / А: 1024433100257.
CAS
Статья
Google ученый
Ребуш CJ, Engel AG: метаболизм карнитина и синдромы дефицита. Mayo Clin Proc. 1983, 58: 533-540.
CAS
Google ученый
Famularo G, Matricardi F, Nucera E, Santini G, De Simone C: Дефицит карнитина: первичный и вторичный синдромы. Карнитин сегодня. Отредактировал: De Simone CFG. 1997, Остин, Техас: R.G. Компания Landes, 119-161.
Глава
Google ученый
Scholte HR, Rodrigues Pereira R, de Jonge PC, Luyt-Houwen IE, Hedwig M, Verduin M, Ross JD: первичный дефицит карнитина. J Clin Chem Clin Biochem. 1990, 28: 351-357.
CAS
Google ученый
Matera M, Bellinghieri G, Costantino G, Santoro D, Calvani M, Savica V: История L-карнитина: последствия для почечной недостаточности. J Ren Nutr. 2003, 13: 2-14. 10.1053 / jren.2003.50010.
Артикул
Google ученый
Argani H, Rahbaninoubar M, Ghorbanihagjo A, Golmohammadi Z, Rashtchizadeh N: Влияние L-карнитина на липопротеины сыворотки и подклассы HDL-C у пациентов, находящихся на гемодиализе. Nephron Clin Pract. 2005, 101: c174-179. 10.1159 / 000087411.
CAS
Статья
Google ученый
Ямазаки Н., Шинохара Ю., Шима А., Яманака Ю., Терада Х .: Выделение и характеристика кДНК и геномных клонов, кодирующих карнитин-пальмитоилтрансферазу I мышечного типа человека I.Biochim Biophys Acta. 1996, 1307: 157-161.
Артикул
Google ученый
Ямадзаки Н., Яманака Ю., Хашимото Ю., Шинохара Ю., Шима А., Терада Н: структурные особенности гена, кодирующего карнитин-пальмитоилтрансферазу мышечного типа человека I. FEBS Lett. 1997, 409: 401-406. 10.1016 / S0014-5793 (97) 00561-9.
CAS
Статья
Google ученый
Ямадзаки Н., Мацуо Т., Курата М., Сузуки М., Фудзиваки Т., Ямагути С., Терада Н., Шинохара Y: Замены трех аминокислот в карнитин-пальмитоилтрансферазе I типа сердца / мышцы человека, вызванные полиморфизмами единичных нуклеотидов.Biochem Genet. 2008, 46: 54-63. 10.1007 / s10528-007-9129-3.
CAS
Статья
Google ученый
Deschauer M, Wieser T, Zierz S: Дефицит мышечной карнитин-пальмитоилтрансферазы II: клинические и молекулярно-генетические особенности и диагностические аспекты. Arch Neurol. 2005, 62: 37-41. 10.1001 / archneur.62.1.37.
Артикул
Google ученый
Семба С., Ясудзима Х, Такано Т., Йокодзаки Х: Случай вскрытия неонатальной формы дефицита карнитин пальмитоилтрансферазы-II, вызванный новой болезненной мутацией del1737C.Pathol Int. 2008, 58: 436-441. 10.1111 / j.1440-1827.2008.02250.x.
CAS
Статья
Google ученый
Ланг Ф., Буш Г.Л., Риттер М., Фолькл Х., Вальдеггер С., Гулбинс Э., Хауссингер D: Функциональное значение механизмов регуляции объема клеток. Physiol Rev.1988, 78: 247-306.
CAS
Google ученый
Berard E, Iordache A, Barrillon D, Bayle J: L-карнитин у пациентов, находящихся на диализе: выбор режима дозирования.Int J Clin Pharmacol Res. 1995, 15: 127-133.
CAS
Google ученый
Ваннер С., Форстнер-Ваннер С., Россл С., Фурст П., Шоллмейер П., Хорл У.Х .: Метаболизм карнитина у пациентов с хронической почечной недостаточностью: влияние добавок L-карнитина. Kidney Int Suppl. 1987, 22: S132-135.
CAS
Google ученый
Wanner C, Horl WH: Карнитиновые нарушения у пациентов с почечной недостаточностью.Патофизиологические и терапевтические аспекты. Нефрон. 1988, 50: 89-102. 10.1159 / 000185137.
CAS
Статья
Google ученый
Calvani M, Benatti P, Mancinelli A, D’Iddio S, Giordano V, Koverech A, Amato A, Brass EP: Замена карнитина при терминальной стадии почечной недостаточности и гемодиализа. Ann N Y Acad Sci. 2004, 1033: 52-66. 10.1196 / Анналы.1320.005.
CAS
Статья
Google ученый
Handelman GJ: Дискуссионный форум: добавки карнитина не продемонстрировали свою эффективность у пациентов, находящихся на длительной диализной терапии. Blood Purif. 2006, 24: 140-142. 10.1159 / 000089450.
CAS
Статья
Google ученый
Бертелли А., Джованнини Л., Палла Р., Мильори М., Паничи В., Андреини Б.: Защитный эффект L-пропионилкарнитина на нефротоксичность, вызванную циклоспорином. Препараты Exp Clin Res. 1995, 21: 221-228.
CAS
Google ученый
Origlia N, Migliori M, Panichi V, Filippi C, Bertelli A, Carpi A, Giovannini L: Защитный эффект L-пропионилкарнитина при хронической нефротоксичности, вызванной циклоспорином-a. Biomed Pharmacother. 2006, 60: 77-81. 10.1016 / j.biopha.2005.06.014.
CAS
Статья
Google ученый
Shores NJ, Keeffe EB: Является ли пероральный L: -ацил-карнитин эффективной терапией печеночной энцефалопатии? Обзор литературы. Dig Dis Sci.2008
Google ученый
Malaguarnera M, Gargante MP, Cristaldi E, Vacante M, Risino C, Cammalleri L, Pennisi G, Rampello L: лечение ацетил-L: -карнитином при минимальной печеночной энцефалопатии. Dig Dis Sci. 2008
Google ученый
Терриен Дж., Роуз С., Баттерворт Дж., Баттерворт РФ: Защитный эффект L-карнитина при энцефалопатии, вызванной аммиаком, у крыс с шунтированной крысой.Гепатология. 1997, 25: 551-556. 10.1002 / hep.510250310.
CAS
Статья
Google ученый
Casas H, Murtra B, Casas M, Ibanez J, Ventura JL, Ricart A, Rodriguez F, Viscor G, Palacios L, Pages T, Rama R: Повышенный уровень аммиака в крови при гипоксии во время физических упражнений у людей. J Physiol Biochem. 2001, 57: 303-312. 10.1007 / BF03179824.
CAS
Статья
Google ученый
ДаВанзо В.Дж., Уллиан М.Э .: Введение L-карнитина обращает вспять острые изменения психического статуса у больного хроническим гемодиализом с инфекцией гепатита С. Clin Nephrol. 2002, 57: 402-405.
CAS
Google ученый
Malaguarnera M, Pistone G, Astuto M, Dell’Arte S, Finocchiaro G, Lo Giudice E, Pennisi G: L-карнитин в лечении легкой или умеренной печеночной энцефалопатии. Dig Dis. 2003, 21: 271-275. 10.1159 / 000073347.
Артикул
Google ученый
Malaguarnera M, Pistone G, Astuto M, Vecchio I, Raffaele R, Lo Giudice E, Rampello L: Влияние L-ацетилкарнитина на пациентов с циррозом печени и печеночной комой: рандомизированное двойное слепое плацебо-контролируемое исследование. Dig Dis Sci. 2006, 51: 2242-2247. 10.1007 / s10620-006-9187-0.
CAS
Статья
Google ученый
Malaguarnera M, Pistone G, Elvira R, Leotta C, Scarpello L, Liborio R: Эффекты L-карнитина у пациентов с печеночной энцефалопатией.Мир Дж. Гастроэнтерол. 2005, 11: 7197-7202.
CAS
Статья
Google ученый
Mullen KD, Gacad R: Патогенетические механизмы острой печеночной энцефалопатии. New Horiz. 1994, 2: 505-511.
CAS
Google ученый
Петегрю Дж. В., Левин Дж., МакКлюр Р. Дж.: Физико-химические, метаболические и терапевтические свойства ацетил-L-карнитина: актуальность для механизма его действия при болезни Альцгеймера и гериатрической депрессии.Мол Психиатрия. 2000, 5: 616-632. 10.1038 / sj.mp.4000805.
CAS
Статья
Google ученый
Рудман Д., Сьюэлл К. В., Ансли Дж. Д .: Дефицит карнитина у пациентов с кахектическим циррозом. J Clin Invest. 1977, 60: 716-723. 10.1172 / JCI108824.
CAS
Статья
Google ученый
ДеКарли Л.М., Либер К.С.: Жирная печень у крыс после длительного приема этанола с новой жидкой диетой с адекватным питанием.J Nutr. 1967, 91: 331-336.
CAS
Google ученый
Клацкин Г: Алкоголь и его связь с поражением печени. Гастроэнтерология. 1961, 41: 443-451.
CAS
Google ученый
Сачан Д.С., Рью Т.Х., Руарк Р.А.: Улучшение воздействия карнитина и его предшественников на жировую дистрофию печени, вызванную алкоголем. Am J Clin Nutr. 1984, 39: 738-744.
CAS
Google ученый
Rhew TH, Sachan DS: Дозозависимый липотропный эффект карнитина у крыс, страдающих хроническим алкоголизмом. J Nutr. 1986, 116: 2263-2269.
CAS
Google ученый
Израиль Й., Салазар И., Розенманн Е: Ингибирующее действие алкоголя на транспорт аминокислот в кишечнике in vivo и in vitro. J Nutr. 1968, 96: 499-504.
CAS
Google ученый
Кухайда Ф.П., Роннетт Г.В.: Модуляция карнитинпальмитоилтрансферазы-1 для лечения ожирения.Curr Opin исследует наркотики. 2007, 8: 312-317.
CAS
Google ученый
Aja S, Landree LE, Kleman AM, Medghalchi SM, Vadlamudi A, McFadden JM, Aplasca A, Hyun J, Plummer E, Daniels K, Kemm M, Townsend CA, Thupari JN, Kuhajda FP, Moran TH , Ronnett GV: Фармакологическая стимуляция мозга карнитин пальмитоил-трансфераза-1 снижает потребление пищи и массу тела. Am J Physiol Regul Integr Comp Physiol. 2008, 294: R352-361.
CAS
Статья
Google ученый
Obici S, Feng Z, Arduini A, Conti R, Rossetti L: Ингибирование гипоталамической карнитин-пальмитоилтрансферазы-1 снижает потребление пищи и производство глюкозы. Nat Med. 2003, 9: 756-761. 10,1038 / нм873.
CAS
Статья
Google ученый
Покай А., Лам Т.К., Обичи С., Гутьеррес-Хуарес Р., Муза Э.Д., Ардуини А., Россетти Л. Восстановление гипоталамического восприятия липидов нормализует энергетический и глюкозный гомеостаз у перекормленных крыс.J Clin Invest. 2006, 116: 1081-1091. 10.1172 / JCI26640.
CAS
Статья
Google ученый
Хе В., Лам Т.К., Обичи С., Россетти Л.: Молекулярное нарушение гипоталамической чувствительности к питательным веществам вызывает ожирение. Nat Neurosci. 2006, 9: 227-233. 10.1038 / нн1626.
CAS
Статья
Google ученый
Landree LE, Hanlon AL, Strong DW, Rumbaugh G, Miller IM, Thupari JN, Connolly EC, Huganir RL, Richardson C, Witters LA, Kuhajda FP, Ronnett GV: C75, ингибитор синтазы жирных кислот, модулирует АМФ-активированную протеинкиназу, чтобы изменить энергетический метаболизм нейронов.J Biol Chem. 2004, 279: 3817-3827. 10.1074 / jbc.M3109
.
CAS
Статья
Google ученый
Обичи С., Фенг З., Морган К., Стейн Д., Карканиас Дж., Россетти Л.: Центральное введение олеиновой кислоты подавляет выработку глюкозы и потребление пищи. Диабет. 2002, 51: 271-275. 10.2337 / диабет. 51.2.271.
CAS
Статья
Google ученый
Хао Дж., Шен В., Тиан С, Лю З., Рен Дж., Ло С., Лонг Дж., Шарман Э, Лю Дж .: Митохондриальные питательные вещества улучшают иммунную дисфункцию у крыс Гото-Какидзаки с диабетом 2 типа.J Cell Mol Med. 2008
Google ученый
Гудман С.И., Марки С.П., Мо П.Г., Майлз Б.С., Тенг СС: Глутаровая ацидурия; «новое» нарушение обмена аминокислот. Biochem Med. 1975, 12: 12-21. 10.1016 / 0006-2944 (75)
-5.
CAS
Статья
Google ученый
Колкер С., Келлер Д.М., Окун Дж. Г., Хоффманн Г. Ф.: Патомеханизмы нейродегенерации при дефиците глутарил-КоА дегидрогеназы.Энн Нейрол. 2004, 55: 7-12. 10.1002 / ana.10784.
Артикул
CAS
Google ученый
Baric I, Zschocke J, Christensen E, Duran M, Goodman SI, Leonard JV, Muller E, Morton DH, Superti-Furga A, Hoffmann GF: Диагностика и лечение глутаровой ацидурии типа I. J Inherit Metab Дис. 1998, 21: 326-340. 10.1023 / А: 10053
171.
CAS
Статья
Google ученый
Monavari AA, Naughten ER: Профилактика церебрального паралича при глутаровой ацидурии 1 типа с помощью диетического управления. Arch Dis Child. 2000, 82: 67-70. 10.1136 / adc.82.1.67.
CAS
Статья
Google ученый
Штраус К.А., Паффенбергер Э.Г., Робинсон Д.Л., Мортон Д.Х.: глутаровая ацидурия I типа, часть 1: естественное течение 77 пациентов. Am J Med Genet C Semin Med Genet. 2003, 121С: 38-52. 10.1002 / ajmg.c.20007.
Артикул
Google ученый
Yannicelli S, Rohr F, Warman ML: нутритивная поддержка при глутаровой ацидемии типа I. J Am Diet Assoc. 1994, 94: 183-188. 10.1016 / 0002-8223 (94)
-3.
CAS
Статья
Google ученый
Маэбаши М., Кавамура Н., Сато М., Имамура А., Йошинага К.: Выведение карнитина с мочой у пациентов с гипертиреозом и гипотиреозом: увеличение тироидным гормоном. Обмен веществ. 1977, 26: 351-356. 10.1016 / 0026-0495 (77)
-9.
CAS
Статья
Google ученый
Сима А.А.: Ацетил-L-карнитин при диабетической полинейропатии: экспериментальные и клинические данные. Препараты ЦНС. 2007, 21 (Приложение 1): 13-23. 10.2165 / 00023210-200721001-00003. обсуждение 45-16
CAS
Статья
Google ученый
Tze WJ, Sima AA, Tai J: Влияние эндокринной аллотрансплантации поджелудочной железы на дисфункцию диабетических нервов.Обмен веществ. 1985, 34: 721-725. 10.1016 / 0026-0495 (85)
-6.
CAS
Статья
Google ученый
Ward JD, Barnes CG, Fisher DJ, Jessop JD, Baker RW: Улучшение нервной проводимости после лечения у впервые диагностированных диабетиков. Ланцет. 1971, 1: 428-430. 10.1016 / S0140-6736 (71) 92415-9.
CAS
Статья
Google ученый
Sima AA: С-пептид и диабетическая невропатия.Мнение эксперта по исследованию наркотиков. 2003, 12: 1471-1488. 10.1517 / 13543784.12.9.1471.
CAS
Статья
Google ученый
Sima AA, Bril V, Nathaniel V, McEwen TA, Brown MB, Lattimer SA, Greene DA: Регенерация и восстановление миелинизированных волокон в образцах биопсии икроножного нерва от пациентов с диабетической невропатией, получавших сорбинил. N Engl J Med. 1988, 319: 548-555.
CAS
Статья
Google ученый
Biolo G, Toigo G, Ciocchi B, Situlin R, Iscra F, Gullo A, Guarnieri G: метаболический ответ на травму и сепсис: изменения в метаболизме белков. Питание. 1997, 13: 52С-57С. 10.1016 / S0899-9007 (97) 00206-2.
CAS
Статья
Google ученый
Famularo G, De Simone C, Trinchieri V, Mosca L: Карнитин и его аналоги: метаболический путь к регуляции иммунного ответа и воспаления. Ann N Y Acad Sci. 2004, 1033: 132-138.10.1196 / летопись.1320.012.
CAS
Статья
Google ученый
Famularo G, De Simone C: Новая эра карнитина ?. Иммунол сегодня. 1995, 16: 211-213. 10.1016 / 0167-5699 (95) 80159-6.
CAS
Статья
Google ученый
Penn D, Zhang L, Bobrowski PJ, Quinn M, Liu X, McDonough KH: Депривация карнитина отрицательно влияет на сердечно-сосудистую реакцию на бактериальный эндотоксин (LPS) у анестезированных новорожденных свиней.Шок. 1998, 10: 377-382. 10.1097 / 00024382-199811000-00012.
CAS
Статья
Google ученый
Penn D, Zhang L, Bobrowski PJ, Quinn M, McDonough KH: Депривация карнитина отрицательно влияет на сердечную деятельность в сердце поросят, подвергшихся стрессу из-за липополисахаридов и гипоксии / реоксигенации. Шок. 1999, 11: 120-126. 10.1097 / 00024382-199
0-00009.
CAS
Статья
Google ученый
Trumbeckaite S, Opalka JR, Neuhof C, Zierz S, Gellerich FN: Различная чувствительность сердца и скелетных мышц кролика к нарушению митохондриальной функции, вызванному эндотоксинами. Eur J Biochem. 2001, 268: 1422-1429. 10.1046 / j.1432-1327.2001.02012.x.
CAS
Статья
Google ученый
Eaton S, Fukumoto K, Stefanutti G, Spitz L, Zammit VA, Pierro A: Карнитин-пальмитоилтрансфераза I миокарда как мишень для окислительной модификации при воспалении и сепсисе.Biochem Soc Trans. 2003, 31: 1133-1136. 10.1042 / BST0311133.
CAS
Статья
Google ученый
Нанни Дж., Питтирути М., Джованнини И., Болдрини Дж., Ронкони П., Кастаньето М.: Уровни карнитина в плазме и экскреция карнитина с мочой во время сепсиса. JPEN J Parenter Enteral Nutr. 1985, 9: 483-490. 10.1177 / 014860718500
83.
CAS
Статья
Google ученый
Cederblad G, Larsson J, Nordstrom H, Schildt B: Выведение карнитна с мочой у пациентов с ожогами. Бернс. 1981, 8: 102-109. 10.1016 / 0305-4179 (81)
Артикул
Google ученый
Маккарти М.Ф., Рубин Э.Дж .: Обоснование добавления микронутриентов при диабете. Мед-гипотезы. 1984, 13: 139-151. 10.1016 / 0306-9877 (84)
-2.
CAS
Статья
Google ученый
Арслан Э., Бастерзи Ю., Аксой А., Майка С., Унал С., Сари А., Демиркан Ф .: Аддитивные эффекты карнитина и аскорбиновой кислоты на дистально обожженный спинной лоскут кожи у крыс. Med Sci Monit. 2005, 11: BR176-180.
CAS
Google ученый
Koybasi S, Taner Y: Влияние L-карнитина на заживление ран вторичным намерением на модели животных. Раны. 2005, 17: 62-66.
Google ученый
Хан Л., Бамджи М.С.: Уровни карнитина в плазме у детей с белково-калорийной недостаточностью до и после реабилитации. Clin Chim Acta. 1977, 75: 163-166. 10.1016 / 0009-8981 (77)
-7.
CAS
Статья
Google ученый
Хан Л., Бамджи МС: Дефицит тканевого карнитина из-за дефицита лизина в пище: накопление триглицеридов и сопутствующее нарушение окисления жирных кислот. J Nutr. 1979, 109: 24-31.
CAS
Google ученый
Alp H, Orbak Z, Akcay F, Tan H, Aksoy H: Уровни карнитина в плазме и моче и добавление карнитина у детей с недоеданием. J Trop Pediatr. 1999, 45: 294-296. 10.1093 / tropej / 45.5.294.
CAS
Статья
Google ученый
Веннберг А., Хилтандер А., Сьоберг А., Арфвидссон Б., Сандстром Р., Викстром И., Лундхольм К. Распространенность истощения карнитина у тяжелобольных пациентов с недостаточным питанием. Обмен веществ.1992, 41: 165-171. 10.1016 / 0026-0495 (92)
-2.
CAS
Статья
Google ученый
Winter SC, Szabo-Aczel S, Curry CJ, Hutchinson HT, Hogue R, Shug A: Дефицит карнитина в плазме. Клинические наблюдения у 51 пациента детского возраста. Am J Dis Child. 1987, 141: 660-665.
CAS
Статья
Google ученый
Люси С., Гайсслер С., Кониг Б., Кох А., Штангл Г.И., Хирче Ф., Эдер К. Агонисты PPARalpha активируют переносчики органических катионов в клетках печени крыс.Biochem Biophys Res Commun. 2006, 350: 704-708. 10.1016 / j.bbrc.2006.09.099.
CAS
Статья
Google ученый
Koch A, Konig B, Luci S, Stangl GI, Eder K: Диетический окисленный жир регулирует экспрессию переносчиков органических катионов в печени и тонком кишечнике и изменяет концентрацию карнитина в печени, мышцах и плазме крыс. Br J Nutr. 2007, 98: 882-889. 10.1017 / S000711450775691X.
CAS
Статья
Google ученый
Карлик Х, Шустер Д., Варга Ф., Клиндерт Дж., Лапин А, Хаслбергер А, Хандшур М.: Вегетарианская диета влияет на гены окислительного метаболизма и синтеза коллагена. Энн Нутр Метаб. 2008, 53: 29-32. 10.1159 / 000152871.
CAS
Статья
Google ученый
Трэйна Г., Бернарди Р., Катальдо Э, Макки М., Дуранте М., Брунелли М.: Лечение ацетил-L: -карнитином мозга крысы модулирует экспрессию генов, участвующих в нейрональном цероидном липофусцинозе.Mol Neurobiol. 2008
Google ученый
Mole SE, Williams RE, Goebel HH: Корреляции между генотипом, ультраструктурной морфологией и клиническим фенотипом в нейрональных цероидных липофускинозах. Нейрогенетика. 2005, 6: 107-126. 10.1007 / s10048-005-0218-3.
Артикул
Google ученый
Пирс Д.А., Карр С.Дж., Дас Б., Шерман Ф .: Фенотипическое изменение дефектов btn1 в дрожжах хлорохином: дрожжевая модель болезни Баттена.Proc Natl Acad Sci USA. 1999, 96: 11341-11345. 10.1073 / pnas.96.20.11341.
CAS
Статья
Google ученый
Пуэшель С.М.: Влияние приема ацетил-L-карнитина на людей с синдромом Дауна. Res Dev Disabil. 2006, 27: 599-604. 10.1016 / j.ridd.2004.07.009.
Артикул
Google ученый
Манкузо С., Бейтс Т.Э., Баттерфилд Д.А., Калафато С., Корнелиус С., Де Лоренцо А., Динкова Костова А.Т., Калабрезе В. Природные антиоксиданты при болезни Альцгеймера.Мнение эксперта по исследованию наркотиков. 2007, 16: 1921-1931. 10.1517 / 13543784.16.12.1921.
CAS
Статья
Google ученый
Ramassamy C: Новая роль полифенольных соединений в лечении нейродегенеративных заболеваний: обзор их внутриклеточных мишеней. Eur J Pharmacol. 2006, 545: 51-64. 10.1016 / j.ejphar.2006.06.025.
CAS
Статья
Google ученый
Palmieri F: Заболевания, вызванные дефектами митохондриальных носителей: обзор. Biochim Biophys Acta. 2008, 1777: 564-578. 10.1016 / j.bbabio.2008.03.008.
CAS
Статья
Google ученый
Miguel-Carrasco JL, Mate A, Monserrat MT, Arias JL, Aramburu O, Vazquez CM: Роль воспалительных маркеров в кардиозащитном эффекте L-карнитина при гипертензии, вызванной L-NAME. Am J Hypertens. 2008
Google ученый
Диаз Р., Лорита Дж., Соли М., Рамирес И.: Карнитин ухудшает как травму, так и восстановление сократительной функции после временной ишемии в перфузируемом сердце крысы. J Physiol Biochem. 2008, 64: 1-8. 10.1007 / BF03168229.
CAS
Статья
Google ученый
Арсениан М.А.: Карнитин и его производные при сердечно-сосудистых заболеваниях. Prog Cardiovasc Dis. 1997, 40: 265-286. 10.1016 / S0033-0620 (97) 80037-0.
CAS
Статья
Google ученый
Ferrari R, Merli E, Cicchitelli G, Mele D, Fucili A, Ceconi C: Терапевтические эффекты L-карнитина и пропионил-L-карнитина на сердечно-сосудистые заболевания: обзор. Ann N Y Acad Sci. 2004, 1033: 79-91. 10.1196 / Анналы.1320.007.
CAS
Статья
Google ученый
Iliceto S, Scrutinio D, Bruzzi P, D’Ambrosio G, Boni L, Di Biase M, Biasco G, Hugenholtz PG, Rizzon P: Влияние введения L-карнитина на ремоделирование левого желудочка после острого переднего миокарда инфаркт: исследование L-Carnitine Ecocardiografia Digitalizzata Infarto Miocardico (CEDIM).J Am Coll Cardiol. 1995, 26: 380-387. 10.1016 / 0735-1097 (95) 80010-Е.
CAS
Статья
Google ученый
Colonna P, Iliceto S: Инфаркт миокарда и ремоделирование левого желудочка: результаты исследования CEDIM. Карнитин Ecocardiografia Digitalizzata Infarto Miocardico. Am Heart J. 2000, 139: S124-130. 10.1067 / mhj.2000.103918.
CAS
Статья
Google ученый
Tarantini G, Scrutinio D, Bruzzi P, Boni L, Rizzon P, Iliceto S: Метаболическое лечение L-карнитином при остром инфаркте миокарда с подъемом сегмента ST. Рандомизированное контролируемое исследование. Кардиология. 2006, 106: 215-223. 10.1159 / 000093131.
CAS
Статья
Google ученый
Сингх Р.Б., Ниаз М.А., Агарвал П., Бигум Р., Растоги С.С., Сачан Д.С.: рандомизированное двойное слепое плацебо-контролируемое исследование L-карнитина при подозрении на острый инфаркт миокарда.Postgrad Med J. 1996, 72: 45-50. 10.1136 / pgmj.72.843.45.
CAS
Статья
Google ученый
Xue YZ, Wang LX, Liu HZ, Qi XW, Wang XH, Ren HZ: L-карнитин в качестве дополнительной терапии к чрескожному коронарному вмешательству при инфаркте миокарда без подъема сегмента ST. Кардиоваск наркотики Ther. 2007, 21: 445-448. 10.1007 / s10557-007-6056-9.
CAS
Статья
Google ученый
Нардин Р.А., Джонс Д.Р. Митохондриальная дисфункция и нервно-мышечные заболевания. Мышечный нерв. 2001, 24: 170-191. 10.1002 / 1097-4598 (200102) 24: 2 <170 :: AID-MUS30> 3.0.CO; 2-0.
CAS
Статья
Google ученый
Borum PR, Broquist HP, Roelops RJ: Уровни мышечного карнитина при нервно-мышечных заболеваниях. J Neurol Sci. 1977, 34: 279-286. 10.1016 / 0022-510X (77)
-2.
CAS
Статья
Google ученый
ДиМауро С., ДиМауро П.М.: Дефицит мышечной карнитин-пальмитилтрансферазы и миоглобинурия. Наука. 1973, 182: 929-931. 10.1126 / science.182.4115.929.
CAS
Статья
Google ученый
Lheureux PE, Penaloza A, Zahir S, Gris M: Научный обзор: карнитин в лечении токсичности, вызванной вальпроевой кислотой — каковы доказательства ?. Crit Care. 2005, 9: 431-440. 10.1186 / cc3742.
Артикул
Google ученый
Murphy JV, Marquardt KM, Shug AL: Нарушения метаболизма карнитина, связанные с вальпроевой кислотой. Ланцет. 1985, 1: 820-821. 10.1016 / S0140-6736 (85)
-3.
CAS
Статья
Google ученый
Spiller HA, Krenzelok EP, Klein-Schwartz W, Winter ML, Weber JA, Sollee DR, Bangh SA, Griffith JR: серия многоцентровых случаев проглатывания вальпроевой кислоты: концентрации в сыворотке и токсичность. J Toxicol Clin Toxicol. 2000, 38: 755-760.10.1081 / CLT-100102388.
CAS
Статья
Google ученый
Watson WA, Litovitz TL, Klein-Schwartz W., Rodgers GC, Youniss J, Reid N, Rouse WG, Rembert RS, Borys D: годовой отчет Американской ассоциации центров контроля за токсичными веществами за 2003 год. . Am J Emerg Med. 2004, 22: 335-404. 10.1016 / j.ajem.2004.06.001.
Артикул
Google ученый
DeVivo DC: Эффект лечения L-карнитином на гепатотоксичность, вызванную вальпроатом. Неврология. 2002, 58: 507-508.
Артикул
Google ученый
Konig SA, Siemes H, Blaker F, Boenigk E, Gross-Selbeck G, Hanefeld F, Haas N, Kohler B, Koelfen W., Korinthenberg R: тяжелая гепатотоксичность во время терапии вальпроатом: обновленная информация и отчет о восьми новые несчастные случаи. Эпилепсия. 1994, 35: 1005-1015. 10.1111 / j.1528-1157.1994.tb02546.Икс.
CAS
Статья
Google ученый
Симес Х., Нау Х., Шульце К., Виттфохт В., Дрюс Э., Пензен Дж., Зайдель У.: метаболиты вальпроата (VPA) в различных клинических условиях вероятной гепатотоксичности, связанной с VPA. Эпилепсия. 1993, 34: 332-346. 10.1111 / j.1528-1157.1993.tb02419.x.
CAS
Статья
Google ученый
Аль-Маджед А.А., Сайед-Ахмед М.М., Аль-Яхья А.А., Алиса А.М., Аль-Реджаи С.С., Аль-Шабана О.А.: Пропионил-L-карнитин предотвращает прогрессирование цисплатин-индуцированной кардиомиопатии с помощью карнитина. -деланная модель крысы.Pharmacol Res. 2006, 53: 278-286. 10.1016 / j.phrs.2005.12.005.
CAS
Статья
Google ученый
Мандавилли Б.С., Сантос Дж. Х., Ван Хаутен Б. Восстановление митохондриальной ДНК и старение. Mutat Res. 2002, 509: 127-151.
CAS
Статья
Google ученый
Costell M, O’Connor JE, Grisolia S: Возрастное снижение содержания карнитина в мышцах мышей и людей.Biochem Biophys Res Commun. 1989, 161: 1135-1143. 10.1016 / 0006-291X (89)
-0.
CAS
Статья
Google ученый
Hagen TM, Ingersoll RT, Wehr CM, Lykkesfeldt J, Vinarsky V, Bartholomew JC, Song MH, Ames BN: ацетил-L-карнитин, введенный старым крысам, частично восстанавливает митохондриальную функцию и амбулаторную активность. Proc Natl Acad Sci USA. 1998, 95: 9562-9566. 10.1073 / pnas.95.16.9562.
CAS
Статья
Google ученый
Лю Дж., Head E, Gharib AM, Yuan W, Ingersoll RT, Hagen TM, Cotman CW, Ames BN: Потеря памяти у старых крыс связана с распадом митохондрий в головном мозге и окислением РНК / ДНК: частичное восстановление путем кормления ацетил-L- карнитин и / или R-альфа-липоевая кислота. Proc Natl Acad Sci USA. 2002, 99: 2356-2361. 10.1073 / pnas.261709299.
CAS
Статья
Google ученый
Hagen TM, Liu J, Lykkesfeldt J, Wehr CM, Ingersoll RT, Vinarsky V, Bartholomew JC, Ames BN: кормление старых крыс ацетил-L-карнитином и липоевой кислотой значительно улучшает метаболические функции и снижает окислительный стресс. .Proc Natl Acad Sci USA. 2002, 99: 1870-1875. 10.1073 / pnas.261708898.
CAS
Статья
Google ученый
Sugiyama S: Ингибитор HMG CoA редуктазы ускоряет эффект старения на дыхательную функцию митохондрий диафрагмы у крыс. Biochem Mol Biol Int. 1998, 46: 923-931.
CAS
Google ученый
Сетумадхаван С., Чиннаканну П. L-карнитин и альфа-липоевая кислота улучшают возрастное снижение активности митохондриальной дыхательной цепи сердечной мышцы крысы.J Gerontol A Biol Sci Med Sci. 2006, 61: 650-659.
Артикул
Google ученый
Кумаран С., Субатра М., Балу М., Паннеерсельвам С. Прием L-карнитина улучшает митохондриальные ферменты в сердце и скелетных мышцах старых крыс. Exp Aging Res. 2005, 31: 55-67. 10.1080 / 036107305
CAS
Статья
Google ученый
Кумаран С., Паннеерселвам К.С., Шила С., Сивараджан К., Паннеерсельвам С. Возрастной дефицит митохондриального окислительного фосфорилирования в скелетных мышцах: роль карнитина и липоевой кислоты.Mol Cell Biochem. 2005, 280: 83-89. 10.1007 / s11010-005-8234-z.
CAS
Статья
Google ученый
Colucci S, Mori G, Vaira S, Brunetti G, Greco G, Mancini L, Simone GM, Sardelli F, Koverech A, Zallone A, Grano M: L-карнитин и изовалерил L-карнитин фумарат положительно влияют на пролиферация и дифференциация остеобластов человека in vitro. Calcif Tissue Int. 2005, 76: 458-465. 10.1007 / s00223-004-0147-4.
CAS
Статья
Google ученый
Maccari F, Arseni A, Chiodi P, Ramacci MT, Angelucci L: Уровни карнитинов в головном мозге и других тканях крыс разного возраста: эффект от введения ацетил-L-карнитина. Exp Gerontol. 1990, 25: 127-134. 10.1016 / 0531-5565 (90)
-2.
CAS
Статья
Google ученый
Patano N, Mancini L, Settanni MP, Strippoli M, Brunetti G, Greco G, Tamma R, Vergari R, Sardelli F, Koverech A, Colucci S, Zallone A, Grano M: L: -карнитин фумарат и изовалерил-L: -карнитин фумарат ускоряют восстановление отношения объема кости к общему объему после экспериментально индуцированного остеопороза у беременных мышей.Calcif Tissue Int. 2008, 82: 221-228. 10.1007 / s00223-008-9109-6.
CAS
Статья
Google ученый
Адамек Г., Феликс Р., Гюнтер Х.Л., Флейш Х .: Окисление жирных кислот в костной ткани и костных клетках в культуре. Характеристика и гормональные воздействия. Biochem J. 1987, 248: 129-137.
CAS
Статья
Google ученый
Hooshmand S, Balakrishnan A, Clark RM, Owen KQ, Koo SI, Arjmandi BH: Диетические добавки с l-карнитином улучшают минеральную плотность костей за счет подавления метаболизма костей у старых крыс с удаленными яичниками.Фитомедицина. 2008, 15: 595-601. 10.1016 / j.phymed.2008.02.026.
CAS
Статья
Google ученый
Corrales RM, Luo L, Chang EY, Pflugfelder SC: Влияние осмопротекторов на гиперосмолярный стресс в культивируемых эпителиальных клетках роговицы человека. Роговица. 2008, 27: 574-579. 10.1097 / ICO.0b013e318165b19e.
Артикул
Google ученый
Де Пайва С.С., Вильярреал А.Л., Корралес Р.М., Рахман Х.Т., Чанг В.Ю., Фарли В.Дж., Стерн М.Э., Нидеркорн Дж.Й., Ли Д.К., Пфлугфельдер С.К. гамма.Инвестируйте Ophthalmol Vis Sci. 2007, 48: 2553-2560. 10.1167 / iovs.07-0069.
Артикул
Google ученый
Гото Е., Яги Ю., Мацумото Ю., Цубота К.: Нарушение функциональной остроты зрения у пациентов с синдромом сухого глаза. Am J Ophthalmol. 2002, 133: 181-186. 10.1016 / S0002-9394 (01) 01365-4.
Артикул
Google ученый
Pflugfelder SC, Tseng SC, Sanabria O, Kell H, Garcia CG, Felix C, Feuer W, Reis BL: Оценка субъективных оценок и объективных диагностических тестов для диагностики нарушений слезной пленки, которые, как известно, вызывают раздражение глаз.Роговица. 1998, 17: 38-56. 10.1097 / 00003226-199801000-00007.
CAS
Статья
Google ученый
Simmons P, Chang-Lin J, Chung Q, Vehige J, Welty D: Влияние совместимых растворенных веществ на трансэпителиальное электрическое сопротивление и поглощение в модели первичных слоев эпителиальных клеток роговицы кролика. Ежегодное собрание Ассоциации исследований в области зрения и офтальмологии (ARVO). 2007, Форт-Лодердейл, Флорида, США
Google ученый
Гаррет К., Сюй С., Симмонс П.А., Вехиге Дж., Фланаган Дж. Л., Уиллкокс, доктор медицины: Экспрессия и локализация переносчика карнитина / органических катионов OCTN1 и OCTN2 в глазном эпителии. Инвестируйте Ophthalmol Vis Sci. 2008, 49: 4844-4849. 10.1167 / iovs.07-1528.
Артикул
Google ученый
Pescosolido N, Imperatrice B, Koverech A, Messano M: L-карнитин и сложный эфир с короткой цепью в слезах от пациентов с сухим глазом. Optom Vis Sci. 2009, 86: E132-138.10.1097 / OPX.0b013e318194e767.
Артикул
Google ученый
Гилбард Дж. П.: Концентрация электролитов в слезной пленке человека при лечении синдрома сухого глаза. Int Ophthalmol Clin. 1994, 34: 27-36. 10.1097 / 00004397-199403410-00005.
CAS
Статья
Google ученый
Pessotto P, Liberati R, Petrella O, Romanelli L, Calvani M, Peluso G: При экспериментальном диабете снижение уровня карнитина в хрусталике глаза является ранним важным и избирательным событием.Exp Eye Res. 1997, 64: 195-201. 10.1006 / exer.1996.0188.
CAS
Статья
Google ученый
Румец Э., Кивела Т., Тыни Т.: Карнитин пальмитоилтрансфераза I и ацил-КоА дегидрогеназа 9 в сетчатке: понимание ретинопатии при митохондриальных трехфункциональных белковых дефектах. Инвестируйте Ophthalmol Vis Sci. 2008, 49: 1660-1664. 10.1167 / iovs.07-1094.
Артикул
Google ученый
Тыни Т., Кивела Т., Лаппи М., Сумманен П., Никоскелайнен Э., Пихко Х. Офтальмологические данные о дефиците длинноцепочечной 3-гидроксиацил-КоА-дегидрогеназы, вызванном мутацией G1528C: новый тип наследственной метаболической хориоретинопатии. Офтальмология. 1998, 105: 810-824. 10.1016 / S0161-6420 (98) 95019-9.
CAS
Статья
Google ученый
Джиллингем М., Ван Калькар С., Ней Д., Вольф Дж., Хардинг С. Диетическое регулирование дефицита длинноцепочечной 3-гидроксиацил-КоА дегидрогеназы (LCHADD).Отчет о болезни и опрос. J Inherit Metab Dis. 1999, 22: 123-131. 10.1023 / А: 1005437616934.
CAS
Статья
Google ученый
Тыни Т., Пихко Х., Кивела Т.: Офтальмологическая патология при дефиците длинноцепочечной 3-гидроксиацил-КоА дегидрогеназы, вызванной мутацией G1528C. Curr Eye Res. 1998, 17: 551-559. 10.1080 / 02713689808951227.
CAS
Статья
Google ученый
Стэнли, Калифорния: Расстройства дефицита карнитина у детей. Ann N Y Acad Sci. 2004, 1033: 42-51. 10.1196 / Анналы.1320.004.
CAS
Статья
Google ученый
[31] Синтез предшественников карнитина и родственных соединений
https://doi.org/10.1016/S0076-6879(86)23033-5Получить права и содержание
Резюме издателя
В этой главе обсуждается синтез предшественников карнитина и родственные соединения. L-карнитин содержит четвертичный атом азота, который биосинтетически образуется на ранней стадии пути.Таким образом, некоторые промежуточные продукты в этом пути представляют собой четвертичные амины, которые можно легко синтезировать из коммерчески доступных исходных первичных аминов. Эти промежуточные продукты включают ɛ-N-триметил-L-лизин (из α-N-ацетил-L-лизина), γ-N-триметиламинобутиральдегид (из диэтилацеталь 4-аминобутиральдегида) и γ-бутиробетаин (из γ-аминомасляной кислоты). . Другие представляющие интерес соединения, которые синтезируются этим общим методом, включают δ- N -триметиламиновалериановую кислоту (из δ-аминовалериановой кислоты) и ɛ-N-триметиламинокапроновую кислоту (из ɛ-аминокапроновой кислоты).Другой предшественник карнитина, β -гидрокси- ɛ-N- триметил-L-лизин, получают конденсацией γ- N -триметиламинобутиральдегида с глицином в присутствии карбоната калия и сульфата меди с образованием смеси диастереомеров. . Карнитин синтезируется в виде рацемической смеси несколькими родственными методами. Например, DL-карнитин получают реакцией эпихлоргидрина с NaCN с последующей конденсацией с триметиламином и последующим гидролизом.Neurospora crassa (но, по-видимому, не у млекопитающих) ɛ- N -метил-L-лизин и ɛ- N -диметил-L-лизин являются прямыми предшественниками L-карнитина. Последнее соединение получают восстановительным метилированием α-N-ацетил-L-лизина формальдегидом и катализатором H 2 / Pd. α-Кето-ɛ- N -триметиламинокапроновая кислота, катаболический продукт ɛ-N-триметил-L-лизина, синтезируется ферментативно путем реакции ɛ- N -триметил-L-лизина с коммерческой L-аминокислотой. оксидаза.В этой главе описаны типичные методы синтеза ɛ- N — Триметил-L-лизин, ɛ- N — [метил- 14 C] ДиметилI-L-лизин, β -Гидрокси-ɛ- N — [метил- 3 H] триметил-L-лизин, γ- [1- 14 C] бутиробетаин и L- [метил- 3 H] карнитин.
Рекомендуемые статьи Цитирующие статьи (0)
Полный текст
Авторские права © 1986 Опубликовано Elsevier Inc.
Рекомендуемые статьи
Цитирование статей
Биосинтез важнейшего кофактора окисления жирных кислот карнитин стимулируется в сердце и печени после одного приступа упражнений на мышах
Мы определили, стимулирует ли один-единственный сеанс физических упражнений биосинтез карнитина и захват карнитина в печени и сердце.Свободный карнитин (FC) в плазме определяли с использованием ацетилтрансферазы и [ 14 C] ацетил-КоА на мышах Swiss Webster после 1 часа бега на беговой дорожке средней интенсивности или 4 часов и 8 часов после восстановления. Печень и сердце удаляли в тех же условиях для измерения ферментов биосинтеза карнитина (бутиробетаингидроксилаза печени, γ-BBH; триметиллизиндиоксигеназа сердца, TMLD), переносчика органических катионов-2 (OCTN2, переносчик карнитина) и рецептора, активируемого пролифератором пероксисом печени. -альфа (PPAR α , фактор транскрипции для синтеза γ -BBH и OCTN2).У тренированных мышей уровни FC в плазме снизились, в то время как экспрессия белка OCTN2 в сердце и печени увеличилась, что отражает активное поглощение FC. Во время выздоровления повышение FC до контрольных уровней было связано с повышенной экспрессией в печени γ -BBH. Экспрессия белка PPAR α стимулировалась в печени после тренировки и во время восстановления. Интересно, что белок сердца TMLD также был обнаружен после тренировки. Острые упражнения стимулируют поглощение карнитина печенью и сердцем. Быстрое возвращение уровней FC в плазме после тренировки указывает на то, что биосинтез карнитина в печени стимулируется для установления гомеостаза карнитина.Наши результаты показывают, что упражнения могут принести пользу пациентам с синдромами дефицита карнитина.
1. Введение
Карнитин является облигатным кофактором, который переносит длинноцепочечные жирные кислоты (ЖК) в митохондрии для производства энергии. Карнитин получают как из пищевых источников, так и из эндогенного биосинтеза [1]. Первая реакция биосинтеза карнитина включает гидроксилирование триметиллизина до 3-гидрокситриметиллизина триметиллизиндиоксигеназой (TMLD).Дальнейшие ферментативные реакции с участием специфической альдолазы и дегидрогеназы (4- N -триметиламинобутиральдегиддегидрогеназа, TMABA-DM) превращают 3-гидрокситриметиллизин в γ -бутиробетаин. В последней реакции γ -бутиробетаин гидроксилируется γ -бутиробетаингидроксилазой ( γ -BBH) с образованием карнитина [2]. У мышей печень является основным местом синтеза и содержит все ферменты, производящие карнитин, тогда как сердце и скелетные мышцы не имеют γ -BBH.Таким образом, γ -бутиробетаин выделяется из внепеченочных тканей в плазму и накапливается в печени, где он гидроксилируется до карнитина [3]. Захват карнитина из плазмы печеночными и внепеченочными тканями облегчается натрийзависимым переносчиком органических катионов (OCTN2) [4].
Биосинтез карнитина увеличивается в условиях, в которых скорость окисления ЖК постоянно повышается, таких как ограничение калорийности, голодание и питание с высоким содержанием жиров [5–7]. В этих условиях активация рецептора-альфа, активируемого пролифератором пероксисом (PPAR α ) неэтерифицированными ЖК (NEFA) из жировой ткани, увеличивает экспрессию γ -BBH и OCTN2 для облегчения окисления ЖК в тканях.Окисление ЖК также увеличивается в ответ на хронические тренировки, и, как и при кормлении с высоким содержанием жиров и ограничении калорий, сообщалось об увеличении экспрессии γ -BBH и OCTN2 в печени крыс [8]. Однако влияние острых физических упражнений на экспрессию γ -BBH и OCTN2 в печени еще предстоит определить, и, поскольку этот фермент широко экспрессируется в печени [2], кажется логичным, что упражнения путем активации PPAR α через NEFA. , стимулирует биосинтез карнитина.Кроме того, неясно, участвует ли сердце в начальной стадии биосинтеза карнитина или поглощение карнитина этим органом происходит при физических нагрузках. Таким образом, целью данного исследования было изучить влияние физических упражнений на биосинтез карнитина и его усвоение печенью и сердцем у мышей.
2. Методы
2.1. Протокол животных и упражнений
Комитет по уходу и использованию животных Институционального университета Среднего Запада одобрил это исследование, и за использованными животными ухаживали в соответствии с рекомендациями Руководства по уходу и использованию лабораторных животных (Институт ресурсов лабораторных животных, 1996 г.) .
Самцов мышей Swiss Webster получали в возрасте 6 недель (Charles River Laboratories, Wilmington, MA). После однонедельного периода акклиматизации мышей случайным образом распределяли в группу упражнений или контрольную группу. Мышей в группе упражнений приучали к ежедневному бегу на беговой дорожке с электрическим приводом (Exer 3/6; Columbus Instruments, Огайо, США), состоящей из 5-10-минутных сеансов бега со скоростью 8-12 м / мин в течение 5 дней. дней, как описано ранее в нашем недавнем исследовании [9].Через 48 часов после последнего сеанса упражнений на привыкание, сеанс острых упражнений выполнялся со скоростью 19 метров / мин с оценкой 8 градусов в течение 60 минут. Исходя из скорости движения полотна беговой дорожки, интенсивность упражнений соответствует ∼80% VO 2 max мышей [10]. 60-минутный период включал 10 минут разминки, постепенно увеличивая скорость до 15 метров / мин, прежде чем скорость беговой дорожки была установлена на 19 метров / мин. Мышей умерщвляли сразу после тренировки (группа острой нагрузки), через 4 часа после тренировки (4-часовая группа) или через 8 часов после тренировки (8-часовая группа).Мышей, отнесенных к контрольной группе, помещали на стационарную беговую дорожку рядом с беговой дорожкой, используемой для фактических сеансов бега, и усыпляли в те же моменты времени, что и мышей, тренирующихся. В отдельной группе мышей () плазму собирали при идентичных условиях физической нагрузки для измерения уровней NEFA. Мышей содержали по 4 в клетке и содержали в комнате с 12: 12-часовым циклом свет-темнота и кормили стандартной диетой (Teklad, 18% белковая диета, Harlan Laboratories, Мэдисон, Висконсин) и водой ad libitum.
2.2. Сбор тканей и измерение метаболитов в плазме
Мышей умерщвляли в атмосфере 100% CO 2 с немедленным проведением хирургической торакотомии и индукции пневмоторакса. Образцы крови получали сердечной пункцией, плазму отделяли центрифугированием и затем хранили при -80 ° C для последующего измерения карнитина с помощью радиоферментного анализа с использованием карнитинацетилтрансферазы и [ 14 C] ацетил-КоА [11]. Уровни NEFA в плазме измеряли калориметрическим методом на основе ацилирования кофермента А (Wako Chemicals, Ричмонд, Вирджиния, США).Печень и сердце удаляли, замораживали щипцами, охлажденными до температуры жидкости N 2 , и хранили для экспрессии генов и белков.
2.3. Количественный анализ цепной реакции полимеразы в реальном времени (ПЦР)
Выделение
РНК и методы ПЦР были описаны ранее [8]. Содержание РНК выделяли из печени с использованием РНК STAT-60 в соответствии с протоколом, предоставленным производителем (AMS Biotechnology, Abingdon, UK). КДНК первой цепи синтезировали с использованием системы синтеза первой цепи SuperScript TM (Invitrogen, Карлсбад, Калифорния, США).Количественную ПЦР в реальном времени проводили с использованием праймеров, перечисленных в таблице 1, с 18S рРНК (Sigma-Aldrich Life Science, The Woodlands, TX), использованной в качестве внутреннего контроля. Мы выбрали 18S в качестве внутреннего контроля для нормализации ввода кДНК, потому что на этот ген не влияли хронические физические упражнения [8, 12]. Однако, чтобы подтвердить, не влиял ли на 18S острые физические нагрузки, в качестве внутреннего контроля использовались β -актин и GAPDH. Никаких различий между контрольной группой и группами упражнений не наблюдалось для β -актина () или GAPDH ().Относительные уровни мРНК определяли количественно с использованием метода дельта-дельта CT.
2.4. Вестерн-блоттингАнализ содержания белка в печени и сердце проводили с использованием методов, описанных ранее [8]. Образцы (20 µ г) подвергали иммуноблот-анализу с использованием антител против OCTN2, γ -BBH, PPAR α и TMLD (Santa Cruz Biotechnology Inc., Даллас, Техас). В качестве внутреннего контроля блоты повторно зондировали антителом против актина (Sigma-Aldrich Life Science, The Woodlands, TX).Значения в контрольной группе были нормализованы к произвольным единицам для сравнения с группами упражнений. 2,5. Статистический анализГрупповые средние различия определяли с использованием одностороннего дисперсионного анализа с последующим сравнением Тьюки-Крамера для апостериорного анализа. Все значения представлены как среднее ± SEM. Значение считалось статистически значимым. 3. РезультатыНе было различий в массе тела между группами мышей в конце исследования.Масса тела в контрольной, острой, 4-часовой и 8-часовой группах составила 34,2 ± 0,2, 33,7 ± 0,8, 34,7 ± 0,8 и 35,1 ± 0,9 г соответственно. Из-за сходного веса тела, веса сердца и печени мышей из трех групп упражнений были объединены. Масса сердца в контрольной группе и группе упражнений составила 0,138 ± 0,003 и 0,148 ± 0,005 г соответственно. Вес печени составлял 1,26 ± 0,10 и 1,42 ± 0,1 г соответственно у контрольных и тренированных мышей. Влияние физических упражнений и восстановления на уровень карнитина показано на Рисунке 1.Уровни общего карнитина, измеренные как сумма свободного и этерифицированного карнитина в плазме, оставались неизменными во время упражнений и восстановления (рис. 1 (а)). Однако интенсивные упражнения привели к значительному снижению уровней свободного карнитина, за которым последовало быстрое возвращение к контрольным уровням во время восстановления (рис. 1 (b)). Уровни этерификации в плазме были немного увеличены во время упражнений, и восстановление отмечалось возвращением к контрольным уровням (рис. 1 (c)). Отношение этерифицированного карнитина к свободному карнитину увеличивалось при физических нагрузках, но снижалось до контрольных значений во время восстановления (рис. 1 (d)).Изменения свободного карнитина во время упражнений и восстановления отражают поглощение и биосинтез этого кофактора, соответственно. Чтобы подтвердить, что уменьшение свободного карнитина отражает активное поглощение, мы определили экспрессию OCTN2 в печени и сердце. Как показано на Фигуре 2, экспрессия мРНК и экспрессия белка этого транспортного белка были увеличены примерно на 40% по сравнению с контрольными уровнями после упражнений и восстановления в печени (Фигуры 2 (а) и 2 (b)). В сердце было обнаружено аналогичное увеличение экспрессии белка (рис. 2 (c)).Биосинтез карнитина является функцией множества тканей, причем последняя реакция включает гидроксилирование γ -бутиробетаина до карнитина с помощью γ -BBH, происходящего в печени. Сердце также экспрессирует ключевые ферменты пути биосинтеза, но не имеет γ -BBH [3]. Мы определили, связано ли увеличение уровней свободного карнитина в плазме, наблюдаемое во время выздоровления, с экспрессией γ -BBH в печени. Как показано на Рисунке 3, экспрессия мРНК в печени увеличивалась на ~ 45% после упражнений и в период восстановления (Рисунок 3 (а)).Это увеличение было встречено одновременным изменением экспрессии белка только при выполнении упражнений (рис. 3 (b)). Мы также обнаружили, что TMLD, который превращает триметиллизин в 3-гидрокситриметиллизин, также проявляется после острой нагрузки на сердце (рис. 3 (c)). Доказательства показывают, что условия, связанные с повышенной скоростью окисления ЖК, стимулируют экспрессию PPAR α в печени и генов, участвующих в удалении ЖК, включая γ -BBH и OCTN2 [7]. Неясно, регулируют ли острые упражнения экспрессию PPAR α в печени.Как показано на Фигуре 4, уровни белка PPAR α были увеличены в печени после упражнений и оставались повышенными в течение первых 4 часов восстановления по сравнению с контрольной группой. Чтобы подтвердить, стимулировалось ли окисление ЖК во время упражнений, в печени измеряли экспрессию мРНК карнитин пальмитоилтрансферазы 1a (CPT-1a). На рис. 5 показано, что экспрессия мРНК этого фермента увеличивалась на ~ 45% в ответ на сильную физическую нагрузку и оставалась повышенной через 8 часов после периода восстановления.Помимо увеличения экспрессии CPT-1a в печени, изменения уровней NEFA в плазме также отражают увеличение окисления ЖК, вызванное физической нагрузкой. Хотя уровни NEFA в плазме не были значимыми, снижение на ~ 17% наблюдалось после одного часа упражнений (0,32 ± 0,02 в контроле по сравнению с 0,25 ± 0,02 мэкв / л в острой группе), что указывает на усиление экстракции NEFA тканями. Однако через 8 часов после выздоровления уровни NEFA в плазме были почти на 80% выше по сравнению с контрольной группой (0.25 ± 0,02 против 0,45 ± 0,16 мэкв / л). Измерение NEFA в плазме через 24 часа после тренировки показало возврат к контрольным уровням (0,32 ± 0,02 против 0,27 ± 0,01 мэкв / л). 4. ОбсуждениеВлияние острых физических упражнений на биосинтез карнитина и гомеостаз у мышей не определено. Наши результаты показывают, что острые упражнения вызывали значительное снижение уровня свободного карнитина в плазме, в то время как выздоровление отмечалось быстрым возвратом к контрольным уровням.Эти изменения свободного карнитина в плазме крови указывают на активацию как механизмов захвата, так и биосинтеза, соответственно. Действительно, повышенная экспрессия белка OCTN2 была обнаружена в печени и сердце тренирующихся мышей. В печени мы наблюдали увеличение экспрессии γ -BBH, тогда как в сердце экспрессия TMDL стимулировалась резкими упражнениями. Взятые вместе, изменения свободного карнитина в плазме, возникающие при физических нагрузках и во время восстановления, согласуются с поглощением и биосинтезом.Кроме того, учитывая критическую роль печени в биосинтезе карнитина [13] и резкое увеличение уровней белка γ -BBH, которое сохранялось в течение 4 часов после выздоровления, вполне вероятно, что восстановление гомеостаза карнитина в плазме было связано с вывод из печени. Наши результаты также подчеркивают влияние острого метаболического стрессора на гомеостаз карнитина, поскольку большинство исследований на сегодняшний день предоставляют механизмы регуляции карнитина, напоминающие хронические изменения окисления ЖК [5–7].Таким образом, как острые, так и хронические стрессоры активируют поглощение и биосинтез карнитина, способствуя окислению ЖК, но, что наиболее примечательно, снижение уровня свободного карнитина в плазме с помощью физических упражнений, по-видимому, является надежным стимулом. Это повышает вероятность того, может ли нарушение гомеостаза карнитина в плазме из-за поглощения OCTN2 для усиления окисления ЖК служить начальным стимулом для активации биосинтеза карнитина тканями. Ранние исследования показали, что биосинтез карнитина и экспрессия OCTN2 в печени зависят от активации PPAR α [14], липид-чувствительного ядерного рецептора, который функционирует как регулятор метаболизма ЖК [15].Доказательства этой важной роли PPAR α в гомеостазе карнитина были подтверждены на гепатоцитах, сверхэкспрессирующих PPAR α , и на мышах с нулевым PPAR α [16], у последних мышей развился дефицит карнитина в результате снижения содержания в печени γ. Экспрессия -BBH и OCTN2 [17]. Недавние данные показывают, что активация транскрипции TMABA-DM, которая обеспечивает γ -бутиробетаин и предположительно TMLD, опосредуется PPAR α [18].Естественным лигандом для активации PPAR α является NEFA из жировой ткани, и с высвобождением этого лиганда во время острой физической нагрузки в результате липолиза синтез генов, связанных с биосинтезом карнитина и его захватом для поддержки метаболизма ЖК, может быть стимулирован [19, 20]. В соответствии с этим механизмом мы продемонстрировали, используя те же условия упражнений, что экстракция NEFA из плазмы была связана с активацией PPAR α и повышенной экспрессией γ -BBH и OCTN2 в почках мыши [9].Недавнее наблюдение, что содержание свободного карнитина в печени увеличивается при физической нагрузке, согласуется с этим механизмом [21]. Повышенное соотношение этерифицированного карнитина и свободного карнитина в плазме и повышенное содержание мРНК CPT-1a в печени отражают увеличение окисления жирных кислот в результате физических упражнений. Уменьшение NEFA в плазме, вызванное физической нагрузкой, указывает на то, что этот субстрат был извлечен из плазмы и, вероятно, активировал PPAR α и OCTN2 в тканях. Интересным открытием этого исследования было то, что острые упражнения увеличивали экспрессию OCTN2 и TMLD в сердце.Изменения в OCTN2 обычно очевидны после хронических стрессовых состояний, включая голодание, ограничение калорийности или упражнения, выполняемые при ожирении, вызванном диетой [5–7]. В этих условиях происходит значительное увеличение экспрессии этого переносчика, что способствует окислению ЖК в тканях. В настоящем исследовании мы показываем, что острые упражнения стимулировали экспрессию этого носителя, что является ожидаемой реакцией, учитывая окислительную природу сердца и зависимость от ЖК в качестве энергетического субстрата, особенно в условиях физических упражнений, когда окисление ЖК повышено [22].Действительно, сокращение увеличивает транслокацию внутриклеточного накопленного FAT / CD36 к плазматической мембране с последующим увеличением поглощения кислоты длинноцепочечной FA в кардиомиоциты, предназначенные для митохондриального β -окисления [23]. Важность карнитина в окислении ЖК в сердце подтверждается исследованиями, изучающими адаптацию к тренировкам, некоторые из которых включают увеличение плотности митохондрий и свободного карнитина, а также улучшение выносливости [24]. Напротив, еще одним подтверждением роли карнитина в окислении ЖК является наблюдение, что здоровые субъекты и крысы, которым вводили пивалоил-конъюгированные антибиотики, которые, как известно, вызывают серьезный системный дефицит карнитина, демонстрируют снижение частоты сердечных сокращений и снижение скорости окисления ЖК, снижение способности к физической нагрузке, и повышенный уровень кетоновых тел в плазме [25, 26].Экспрессия TMLD, первого в пути биосинтеза карнитина, который превращает триметиллизин в 3-гидрокситриметиллизин, также стимулировалась в ответ на сильную физическую нагрузку, эффект, который еще предстоит подтвердить активацией PPAR α [18]. Повышенная экспрессия этой гидроксилазы в сердце потенциально может обеспечить γ -бутиробетаин, прямой предшественник карнитина для окончательного превращения в карнитин печенью или почками [2]. Более ранние исследования показали, что доступность γ -бутиробетаина считается ограничивающим шагом для биосинтеза [27], а повышенные уровни γ -бутиробетаина в сыворотке крови после регулярных физических упражнений у здоровых субъектов отражают повышенное поступление предшественников карнитина из сердца. и скелетные мышцы для биосинтеза карнитина [28]. В заключение мы показываем, что гомеостаз карнитина в плазме крови нарушается при физической нагрузке, но быстро восстанавливается у мышей, что указывает на стимуляцию механизмов биосинтеза карнитина. Возврат FC в плазму в течение периода восстановления согласуется с повышенной экспрессией γ -BBH в печени наряду с возможным косвенным вовлечением TMLD со стороны сердца. Хотя упражнения повышают уровень γ -бутиробетаина [28], а транспортер OCTN2 активно извлекает этот предшественник карнитина из плазмы, гомеостаз карнитина также достигается за счет экспрессии OCTN2 в печени и сердце, хотя это будет рассмотрено в наших будущих исследованиях.Кроме того, поскольку острые упражнения могут стимулировать биосинтез и механизмы поглощения карнитина, частые упражнения могут принести пользу пациентам с синдромами первичной и вторичной недостаточности карнитина. Конфликт интересовАвторы заявляют об отсутствии конфликта интересов. Вклад авторовТом Л. Бродерик задумал и разработал исследование, проанализировал данные, написал и отредактировал рукопись. Фрэнк А. Кузимано и Челси Карлсон провели эксперименты и проанализировали данные.Джеганатан Рамеш Бабу дал концептуальные и редакционные советы и отредактировал рукопись. БлагодарностиЭта работа была поддержана Управлением исследований и спонсируемых программ Среднезападного университета. Произошла ошибка при настройке пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт. Настройка вашего браузера для приема файлов cookieСуществует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
Почему этому сайту требуются файлы cookie? Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie Что сохраняется в файле cookie?Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется. Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт Первичный дефицит карнитина и скрининг новорожденных на нарушения карнитинового цикла — FullText — Annals of Nutrition and Metabolism 2016, Vol. 68, Прил. 3АннотацияКарнитин необходим для переноса длинноцепочечных жирных кислот через внутреннюю митохондриальную мембрану для последующего β-окисления.Карнитин может синтезироваться организмом, а также поступать с пищей из мяса и молочных продуктов. Дефекты транспорта карнитина, например, вызванные дефектной активностью транспортера OCTN2, кодируемого геном SLC22A5 , приводят к первичному дефициту карнитина, и программы скрининга новорожденных могут идентифицировать пациентов с риском этого состояния до необратимого повреждения. Первоначальный биохимический диагноз может быть подтвержден с помощью молекулярного тестирования, хотя прямое исследование транспорта карнитина в фибробластах очень полезно для подтверждения или исключения первичного дефицита карнитина у лиц с генетическими вариациями неизвестной клинической значимости или у которых сохраняется низкий уровень карнитина, несмотря на отрицательные молекулярные анализы. .Генетические дефекты биосинтеза карнитина обычно не приводят к низким уровням карнитина в плазме. Однако делеция гена триметиллизингидроксилазы, ключевого гена биосинтеза карнитина, была связана с недисморфическим аутизмом. Таким образом, появляются новые роли карнитина, не связанные с классическими врожденными ошибками метаболизма. © 2016 S. Karger AG, Базель Карнитин необходим для переноса длинноцепочечных жирных кислот через внутреннюю митохондриальную мембрану для последующего β-окисления [1].Карнитин может быть синтезирован организмом и может быть получен с пищей, потребляя мясо и молочные продукты. Таким образом, генетические дефекты биосинтеза карнитина обычно не приводят к низким уровням карнитина в плазме. Карнитиновый цикл и дефицит карнитина у новорожденныхКарнитин накапливается в клетках и задерживается почками через OCTN2, высокоаффинный переносчик органических катионов, специфичный для карнитина [1]. Генетические дефекты переносчика карнитина OCTN2 приводят к первичному дефициту карнитина, который связан со сниженным накоплением внутриклеточного карнитина, повышенной потерей карнитина с мочой и низким уровнем карнитина в сыворотке.Больные могут иметь гипокетотическую гипогликемию и печеночную энцефалопатию в раннем возрасте, или скелетную и сердечную миопатию, или внезапную смерть от сердечной аритмии в более позднем возрасте, обычно вызванную голоданием или катаболическим состоянием. Хотя дефекты OCTN2 могут приводить к дефициту карнитина, были выявлены и другие состояния, которые могут вызывать дефицит карнитина у новорожденных. К ним относятся диетический дефицит карнитина, полное парентеральное питание без добавления карнитина [2], материнская глутаровая ацидемия типа I [3], материнский дефицит ацилкофермента A (CoA) дегидрогеназы со средней длиной цепи [4], дефицит 3-метилкротонил-CoA карбоксилазы [ 5].Существуют также другие состояния, не связанные напрямую с дефицитом карнитина, которые могут потребовать лечения карнитином, такие как делеции в гене триметиллизингидроксилазы ( TMLHE ) на Xq28, кодирующем ε-N-TMLHE, фактор риска несиндромального аутизма. расстройства спектра у мужчин [6,7]. Необходимость скрининга и лечения первичного дефицита карнитинаПервичный дефицит карнитина является ответом на пероральный прием карнитина, который в фармакологических дозах проникает в клетки с помощью переносчика аминокислот B 0, + [1].Ключевые аспекты дефицита переносчика карнитина показаны на рисунке 1. Рис. 1Ключевые особенности первичного дефицита карнитина. Частота первичного дефицита карнитина колеблется в пределах примерно 1:40 000 новорожденных в Японии [8], 1: 37 000–1: 100 000 новорожденных в Австралии [9] и 1: 142 000 в США [10]. Самый высокий уровень заболеваемости (1: 300) зарегистрирован на Фарерских островах, архипелаге, который веками оставался географически изолированным [11].Снижение внутриклеточного накопления карнитина приводит к нарушению окисления жирных кислот, и, если не принимать добавки карнитина, у пациентов с первичным дефицитом карнитина может развиться ранняя острая метаболическая декомпенсация, или в более позднем возрасте — скелетная и сердечная миопатия или внезапная смерть от аритмии [12]. Программы скрининга новорожденных на первичный дефицит карнитина могут выявить пациентов с риском этого состояния до того, как произойдет необратимый ущерб. Диагноз первичной недостаточности карнитина может быть подтвержден биохимически, демонстрируя низкие уровни свободного карнитина в плазме (<8 мкМ, нормальные 25-50 мкМ) со сниженной почечной реабсорбцией (<90%) и нормальной функцией почек без отклонений в органических кислотах в моче [1 ].Поскольку материнское заболевание также может быть причиной первичной недостаточности карнитина, у матери следует оценивать карнитин в плазме и моче, ацилкарнитиновый профиль плазмы и содержание органических кислот в моче. Диагноз окончательно подтверждается молекулярным тестированием гена SLC22A5 или изучением транспорта карнитина в фибробластах (<20% от нормального контроля). Оценка транспорта карнитина в фибробластахФункциональный анализ (транспорт карнитина в фибробластах) очень полезен для подтверждения или исключения первичного дефицита карнитина у людей с генетическими вариациями неизвестной клинической значимости или у тех, кто продолжает иметь низкие уровни карнитина, несмотря на отрицательные молекулярные анализы.Кроме того, у родителей пораженных детей транспорт карнитина в фибробластах примерно наполовину ниже нормы и может быть низкий уровень карнитина в плазме [13]. Функциональные исследования фибробластов также можно рассматривать как наиболее точный тест, поскольку до 16% мутантных аллелей, вызывающих первичный дефицит карнитина, не могут быть идентифицированы с помощью секвенирования и анализа делеций / дупликаций всех 10 экзонов гена SLC22A5 и фланкирующих областей. . У большинства пациентов есть по крайней мере одна миссенс-мутация в переносчике карнитина OCTN2, и исследования экспрессии в клетках яичника китайского хомячка (СНО) могут подтвердить причинную роль одиночных аминокислотных замен.На рис. 2 показано, что не все миссенс-изменения, выявленные у пациентов с первичной недостаточностью карнитина, нарушают транспорт карнитина, поскольку некоторые вариации обладают такой же активностью, что и OCTN2 дикого типа. Рис. 2Транспорт карнитина клетками СНО, экспрессирующими нормальные и мутантные переносчики карнитина OCTN2. Недостатки скрининга новорожденныхНедавнее исследование Therrell et al. [10] обнаружили, что частота первичного дефицита карнитина среди программ скрининга новорожденных в США составляет 1: 142 000.Однако частота мутаций (только бессмыслица, сплайсинг и выраженный миссенс) у 60000 нормальных людей (носителей) в браузере exac (http://exac.broadinstitute.org/gene/ENSG00000197375) составляет 1: 141 с экстраполированной частотой. пораженных индивидуумов (гомозиготных или сложных гетерозиготных) — 1 из 79 910. Поскольку сообщаемая частота составляет 1 из 142 236, это позволяет предположить, что многие случаи не учитываются при скрининге новорожденных. Возможность того, что при скрининге новорожденных могут быть пропущены случаи дефицита переносчика карнитина, следует учитывать у пациентов со стойкими низкими или пограничными уровнями карнитина или у которых наблюдается снижение уровня карнитина после прекращения приема добавок.Такие люди должны быть обследованы на первичный дефицит карнитина. Стратегии скрининга новорожденныхСуществуют разные стратегии скрининга новорожденных, которые различаются в разных штатах США. В Юте мы проводим 2 обследования, первый в течение примерно 48 часов после рождения, а второй — через 7–21 день жизни. Карнитин передается от матери к ребенку через плаценту, и уровень карнитина может быть нормальным у младенца, если образец собирается вскоре после рождения.В этом случае уровень карнитина может со временем снижаться. Двухэтапный скрининг может позволить лучше выявлять младенцев с первичной недостаточностью карнитина. С другой стороны, первичный дефицит карнитина у матери лучше выявляется по очень низким уровням карнитина при первом обследовании. В таких случаях у большинства матерей имеются симптомы, но они подвержены риску внезапной смерти. Добавки карнитина бессимптомным матерям могут повысить уровень карнитина в плазме и предотвратить сердечную аритмию. Различия в представлении первичного дефицита карнитинаК сожалению, существует небольшая корреляция между типом мутации и временем или типом (метаболическая или кардиомиопатия) проявления у детей с первичным дефицитом карнитина.Более того, даже в пределах одной семьи клинические проявления различаются: у некоторых детей рано проявляется печеночная энцефалопатия, а у других позже развивается сердечная дисфункция. Отсутствие корреляции генотип-фенотип было продемонстрировано в нескольких исследованиях [14,15,16]. Этот аспект был более подробно изучен Rose et al. [17], где было обнаружено, что транспорт карнитина значительно снижен в фибробластах от всех пациентов с первичным дефицитом карнитина, но значительно выше в фибробластах от бессимптомных женщин.Анализ последовательности ДНК обнаружил повышенную частоту бессмысленных мутаций у пациентов с симптомами. Выражение миссенс-мутаций у бессимптомных пациентов в клетках СНО показало, что многие из них сохранили остаточную транспортную активность карнитина, со снижением средней активности миссенс-мутаций, выявленных у пациентов с симптомами по сравнению с бессимптомными пациентами. На основании этих результатов было сделано предположение, что у бессимптомных женщин средний уровень остаточной транспортной активности карнитина выше, чем у пациентов с симптомами, из-за наличия по крайней мере одной миссенс-мутации.Однако не все матери, выявленные при скрининге новорожденных, не имеют симптомов. Chen et al. [18] сообщили о случаях нарушения усвоения карнитина у 13 матерей, выявленных в рамках программы скрининга новорожденных. У одной матери была кардиомиопатия, а другая внезапно умерла через год после родов. Этот последний человек перенес несколько эпизодов обморока с 13 лет, не понимая их этиологии, и диагноз был поставлен ретроспективно. Это подчеркивает необходимость скрининга как младенцев, так и матерей. Фарерские острова: пример из практикиКак упоминалось выше, частота случаев первичного дефицита карнитина на Фарерских островах очень высока. Это небольшой архипелаг в Северной Атлантике, расположенный между Шотландией и Исландией. Фарерские острова географически изолированы и входят в состав Королевства Дания, наряду с собственно Данией и Гренландией. Население Фарерских островов составляет около 50 000 человек, еще 20 000 проживают за границей, в основном в Дании. Он возник в основном в результате колонизации небольшим количеством норвежцев около 1000 лет назад.У коренного населения Фарерских островов очень высокая частота нескольких генетических заболеваний: кистозный фиброз, болезнь накопления гликогена типа IIIA, дефицит холокарбоксилазосинтазы и дефицит 3-метилкротонил-КоА-карбоксилазы. Высокая частота первичного дефицита карнитина связана с мутацией-основателем (p.N32S) [19]. Интересно, что молодые люди (возраст 25-30 лет) часто умирали от фибрилляции желудочков в отсутствие кардиомиопатии. Некоторые люди также жаловались на усталость и слабость, которые улучшились с добавлением карнитина. TMLHE Ген, биосинтез карнитина и аутизм Дефекты синтеза карнитина не являются причиной дефицита карнитина, поскольку большая часть карнитина поступает с пищей. Однако делеция гена TMLHE , который является частью пути синтеза карнитина и расположен на Х-хромосоме, чаще встречается у мужчин с недисморфическим аутизмом [20]. В исследовании Celestino-Soper et al. [20], Дефицит TMLHE был обычным явлением у мужчин контрольной группы (1 из 366) и не увеличивался по частоте у пробандов из семей с симплексным аутизмом (1 из 323).Тем не менее, это было почти в 3 раза чаще у пробандов из семей с множественным аутизмом мужчины-мужчины по сравнению с контрольной группой (1 из 130). Более того, 6 из 7 аутичных братьев и сестер пробандов мужского и мужского пола имели делецию, что позволяет предположить, что дефицит TMLHE является фактором риска аутизма, хотя и с низкой пенетрантностью (по оценкам, 2-4%). Гемизиготная делеция второго гена пути биосинтеза карнитина, BBOX1, также приводит к низко-нормальному уровню карнитина, хотя неясно, связаны ли наблюдаемые фенотипические эффекты (микроцефалия и задержки) напрямую со снижением уровней карнитина или с удалением близлежащих гены [21].Таким образом, возможное нарушение регуляции метаболизма карнитина при недисморфическом аутизме требует дальнейшего изучения. Выводы• Дефицит переносчика карнитина OCTN2 вызывает целый спектр заболеваний, от печеночной энцефалопатии до кардиомиопатии и внезапной смерти. • При скрининге новорожденных можно пропустить младенцев с первичным дефицитом карнитина, отчасти из-за времени проведения скрининга. • Тестирование ДНК выявляет около 85% причинных мутаций, а остальные находятся в неэкзонных областях. • У людей были обнаружены дефекты биосинтеза карнитина, которые приводят к низкому нормальному уровню карнитина и накоплению промежуточных соединений до метаболического блока — такие дефекты могут представлять собой фактор риска недисморфического аутизма. • Новые роли карнитина появляются при нарушениях обмена веществ, которые не связаны с классическими врожденными нарушениями метаболизма. Заявление о раскрытии информацииN.L. получил спонсорскую путевку и гонорар от SigmaTau за участие в симпозиуме по карнитину. Список литературы
Автор КонтактыПроф. Никола Лонго Отделение педиатрии и патологии, лаборатории ARUP Университет Юты, 295 Chipeta Way Солт-Лейк-Сити, UT 84108 (США) Электронная почта [email protected] Подробности статьи / публикацииПредварительный просмотр первой страницы
Опубликовано онлайн: 9 декабря 2016 г.
Количество страниц для печати: 5
ISSN: 0250-6807 (печатный) Для дополнительной информации: https: // www.karger.com/ANM Авторские права / Дозировка препарата / Заявление об ограничении ответственности Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или с помощью какой-либо системы хранения и поиска информации, без письменного разрешения издателя. . Метаболитов месяца — КарнитинЗамечательные факты о карнитинеИстория и эволюция1905: открытие | 1927: выяснение структуры Обнаруженный в мясных экстрактах, карнитин получил свое название от латинского carnis , что означает мясо или плоть.Роль карнитина в метаболизме была первоначально описана у насекомых, где было обнаружено, что он является важным питательным веществом для определенных видов. У многих видов, включая млекопитающих, карнитин играет решающую роль в использовании жирных кислот в качестве источника энергии (Wolf 2006). Карнитин имеет высококонсервативный биосинтетический путь. Энантиомер L-карнитин — это активная форма, обнаруженная у людей и других форм жизни. D-карнитин не встречается в природе. Биосинтез и потребление пищиПо оценкам, только четверть нашего пула карнитина обеспечивается синтезом de novo карнитина, который в основном происходит в печени и почках.Остальное усваивается из нашего рациона (Longo et al., 2016). У человека L-карнитин в основном продуцируется из триметиллизина (TML), продукта разложения лизина, включенного в белок. Гамма-бутиробетаиндиоксигеназа (BBOX) является ключевым ферментом в пути синтеза карнитина и катализирует последний и стереоспецифический этап этого пути. Для синтеза карнитина требуется несколько кофакторов, включая витамины B3 (ниацин), B6 (пиридоксальфосфат), C (аскорбиновая кислота), железо и цинк. Диета может быть обильным источником L-карнитина, особенно если она богата красным мясом, рыбой и молочными продуктами. Диеты, исключающие мясо и / или другие продукты животного происхождения, приводят к снижению уровней циркулирующего карнитина, а также к снижению способности транспортировать карнитин в мышечные ткани (Stephens et al. 2011). Однако было высказано предположение, что вегетарианская / веганская диета может быть богатым источником предшественника карнитина TML (Servillo et al. 2014). Система челнока карнитинаКарнитин в первую очередь описывается как ключевой игрок в деградации длинноцепочечных жирных кислот (LCFA) в митохондриях через систему челнока карнитина.Чтобы вступить в бета-окисление, LCFAs должны сначала транспортироваться через внутреннюю митохондриальную мембрану. Это достигается с помощью карнитин-ацилкарнитиновой транслоказы (CACT), которая переносит их связанную с карнитином форму (ацилкарнитин). Попав в митохондриальный матрикс, ацильная группа ацилкарнитина отщепляется и может вступать в бета-окисление. Конечным метаболитом бета-окисления является ацетил-КоА, который может вступать в цикл трикарбоновых кислот для производства АТФ. Карнитин, не содержащий ацильной группы, может транспортироваться обратно из матрицы с помощью CACT и повторно использоваться для челночного перемещения LCFA.Та же система челночного транспорта может также экспортировать избыток ацетилкарнитина из митохондрий, чтобы ограничить ингибирование пируватдегидрогеназы и сэкономить пул свободного КоА, необходимого для других молекул. Ацилкарнитины и их рольКарнитин является центральным строительным блоком класса метаболитов, называемых ацилкарнитинами, которые связывают молекулу карнитина с ацил-КоА, активированной формой жирных кислот для проникновения в митохондрии. Полученные ацилкарнитины названы в честь исходной жирной кислоты и обычно имеют короткое название, описывающее (i) количество атомов углерода, добавленных к основной структуре карнитина, (ii) количество двойных связей в ацильной группе и (iii) возможное наличие гидроксильной группы.Например, карнитин — это C0 (без ацильной группы), ацетилкарнитин — это C2 (2 атома углерода), декадиеноилкарнитин — это C10: 2 (10 атомов углерода, 2 двойные связи), гидроксиоктадеценоилкарнитин — это C18: 1-OH (18 атомов углерода, 1 двойная связь, 1 гидроксильная группа). Короткоцепочечный ацилкарнитин ацетилкарнитин (C2) имеет особое значение в энергетическом метаболизме, так как он тесно связан с ацетил-КоА (Constantin-Teodosiu et al. 1991). Последний является метаболическим перекрестком, где продукты бета-окисления жирных кислот и метаболизма глюкозы посредством гликолиза могут вступать в цикл трикарбоновых кислот (или цикл Кребса).Повышение уровней ацетил-КоА через любой путь может сильно истощить уровни КоА, необходимые в митохондриальном матриксе для бета-окисления жирных кислот. Описанная выше система челнока карнитина действует как буфер для избытка митохондриального ацетил-КоА, транспортируя ацетильную группу в цитозоль, высвобождая группу КоА в митохондриальном матриксе. Карнитин и микробиотаМолекулы карнитина, которые не всасываются, могут выводиться из организма или метаболизироваться кишечной микробиотой (Ghonimy et al.2018). Бактерии вида Pseudomonas используют карнитин в качестве источника углерода и азота, в то время как Acinetobacter используют только углеродный скелет и выделяют триметиламин (ТМА) в качестве конечного продукта. Многие исследования показали связь между риском сердечно-сосудистых заболеваний и выработкой кишечными бактериями ТМА, который далее превращается в N-оксид триметиламина (ТМАО) печеночными ферментами (Tang et al.2019). Карнитин как пищевая добавкаL-карнитин прославился как пищевая добавка, заявив, что он «превращает жир в энергию».В результате он широко используется как для похудания (Pooyandjoo et al., 2016), так и для бодибилдинга и повышения спортивных результатов (Karlic and Lohninger 2004). Хотя карнитин действительно всасывается в кишечнике, исследования показали, что большая часть добавок L-карнитина непосредственно выводится из организма или быстро выводится почками с мочой. Кроме того, поглощение редко связано с увеличением содержания карнитина в мышечной ткани. Исследования показали, что инсулин или диета с высоким содержанием углеводов могут повышать уровень карнитина в мышечной ткани во время упражнений после приема добавок в течение нескольких недель (Wall et al.2011), что является более тяжелым бременем, чем простой прием таблеток с добавками. Кроме того, необходимо проверить долгосрочные эффекты такой диеты, прежде чем рекомендовать ее для любого применения. Клиническое применение карнитина и его метаболитовАцилкарнитины десятилетиями использовались для ранней диагностики ряда наследственных метаболических нарушений у новорожденных. Этот скрининг новорожденных (NBS) использует абсолютные измерения и соотношения уровней ацилкарнитина в высушенных пятнах крови для выявления условий, которые приводят к дисбалансу уровней (ацил) карнитина в крови.В такие стратегии скрининга обычно включаются несколько наследственных заболеваний, связанных с биосинтезом и транспортом карнитина. Узнайте больше о содержании этих тестов в США и Европе (Bodamer et al. 2007). Ацилкарнитины с короткой цепью привлекли большое внимание в контексте диабета и инсулинорезистентности, при этом ацетилкарнитин снова играет центральную роль в качестве главного регулятора стратегий энергетического метаболизма. Малонилкарнитин (C4-OH) также был предложен в качестве метаболита, представляющего интерес в контексте инсулинорезистентности и стратегий управления метаболизмом липидов (Schooneman et al.2013). В недавно проведенном внутри- и межиндивидуальном исследовании метаболического профиля метаболиты карнитина являются ключевыми молекулярными игроками при диабете 2 типа (Diamanti et al.2019). Редкие болезниБыло показано, что несколько редких заболеваний, приводящих к низким уровням выработки и / или поглощения карнитина, получают большую пользу от добавок карнитина, которые могут помочь достичь физиологического пула карнитина и восстановить соответствующие функции в энергетическом обмене. Например, пациенты с системным первичным дефицитом карнитина (SPCD) имеют дефицит карнитина из-за мутации натрийзависимого транспортера карнитина с высоким сродством к плазматической мембране (OCTN2), который обеспечивает клеточный захват карнитина в сердце, мышцах и почках.Это приводит к недостатку выработки энергии из жирных кислот, что вызывает симптомы, начиная от усталости и гипогликемии (глюкоза широко используется в качестве источника энергии) до накопления жира в печени и других органах, а также повреждения сердечных и мышечных тканей. Прием добавок с высоким уровнем L-карнитина (100-400 мг / кг / день) облегчает большинство симптомов. Точно так же у пациентов с дефицитом карнитин-ацилкарнитинтранслоказы (CACTD) система карнитинового челнока не функционирует, и LCFA не могут транспортироваться внутри митохондриального матрикса для бета-окисления.Это приводит к опасному для жизни расстройству, характеризующемуся гипокетотической гипогликемией, дисфункцией сердца, мышц и печени и энцефалопатией. Здесь диета является важной стратегией управления, и голодание строго следует избегать, чтобы гарантировать достаточный запас глюкозы для энергетического метаболизма. Добавки карнитина также могут помочь пациентам с CACTD, хотя они не устраняют все симптомы. Список литературыБодамер О.А., Хоффманн Г.Ф., Линднер М .: Расширенный скрининг новорожденных в Европе, 2007 г.(2007) J Inherit Metab Dis. | DOI: 10.1007 / s10545-007-0666-z Константин-Теодосиу Д., Карлин Дж., Седерблад Дж., Харрис Р.К., Халтман Е: Накопление ацетильных групп и активность пируватдегидрогеназы в мышцах человека во время дополнительных упражнений (1991) Acta Physiol Scand | DOI: 10.1111 / j.1748-1716.1991.tb09247.x Diamanti K, Cavalli M, Pan G и др .: Внутрииндивидуальное и межиндивидуальное метаболическое профилирование выделяет пути карнитина и лизофосфатидилхолина как ключевые молекулярные дефекты при диабете 2 типа.(2019) Научный представитель | DOI: 10.1038 / s41598-019-45906-5 Ghonimy A, Zhang DM, Farouk MH, Wang Q .: Влияние карнитина на пищевую клетчатку и метаболизм кишечных бактерий и их взаимное взаимодействие при моногастрии. (2018) Int J Mol Sci. | DOI: 10.3390 / ijms1 08 Karlic H, Lohninger A .: Добавка L-карнитина спортсменам: имеет ли это смысл? (2004) Питание | DOI: 10.1016 / j.nut.2004.04.003 Longo N, Frigeni M, Pasquali M .: Транспорт карнитина и окисление жирных кислот.(2016) Biochim Biophys Acta. | DOI: 10.1016 / j.bbamcr.2016.01.023 Pooyandjoo M, Nouhi M, Shab-Bidar S, Djafarian K, Olyaeemanesh A .: Влияние (L-) карнитина на потерю веса у взрослых: систематический обзор и метаанализ рандомизированных контролируемых исследований. (2016) Obes Rev. | doi: 10.1111 / obr.12436 Schooneman MG, Vaz FM, Houten SM, Soeters MR .: Ацилкарнитины: отражают или вызывают инсулинорезистентность? (2013) Диабет | DOI: 10.2337 / db12-0466 Сервильо Л., Джоване А, Каутела Д. | ||||||||||||||||||||||||||