Дефицит гормона роста у детей
Помимо дефицита гормона роста, препараты, содержащие гормон роста, применяются и при других нарушениях роста у детей, которые родились с недостаточной массой и длиной тела и не догнали своих сверстников к четырем годам, детей низкого роста, вызванного синдромом Тернера, и детей с задержкой роста по причине хронической почечной недостаточности.
Дети, родившиеся с недостаточной массой и длиной тела
Дети, родившиеся с недостаточной массой и длиной тела, меньше по сравнению с другими младенцами, проведшими в матке аналогичный период времени. Как правило, они очень быстро растут в первые месяцы жизни и догоняют своих сверстников уже к двум годам. Если по достижении четырех лет этого не происходит, таким детям, родившимся с недостаточной массой и длиной тела, может потребоваться дополнительное введение гормона роста, чтобы достичь оптимального роста. [1]
Дети с синдромом Тернера
Синдром Тернера (по имени эндокринолога доктор Генри Тернера, который впервые описал это заболевание в 1938 году), представляет собой генетический
дефект, встречающийся только у девочек, у которых отсутствует, повреждена или присутствует лишь частично одна из двух Х-хромосом. Синдром Тернера может привести к нарушениям роста и низкорослости. Ранняя терапия с использованием гормона роста доказала свою эффективность для повышения темпов роста у девочек с синдромом Тернера и, как следствие, достижения ими роста взрослого человека. [2]
Синдром Тернера может привести к нарушениям роста и низкорослости. Ранняя терапия с использованием гормона роста доказала свою эффективность для повышения темпов роста у девочек с синдромом Тернера и, как следствие, достижения ими роста взрослого человека. [2]
Хроническая почечная недостаточность (ХПН)
Хроническая почечная недостаточность (ХПН) представляет собой прогрессирующее со временем заболевание почек (по меньшей мере в течение трех месяцев). По мере развития ХПН почки теряют способность выводить отходы жизнедеятельности и лишнюю воду из организма. Дети с ХПН плохо растут, поэтому им показано применение рекомбинантного гормона роста человека. [3]
[1] Arianna Maiorana & Stefano Cianfarani 2009; 124:e519
[2] PD Davenport, ML et al. JCEM 2007; 92:3406–16; Stephure D et al. JCEM 2005; 90:3360–6; Linglart A et al. Eur J Endocrinol 2011; 164:891–7
[3] Müller-Wiefel D et al. Clin Nephrol 2010; 74:97–105
Статьи
Гинекологи и эндокринологи часто советуют пациенткам проверить уровень гормонального фона, а иногда и откорректировать его. Что такое гормоны, и какие из них особенно важны для женского здоровья мы и обсудим.
Что такое гормоны, и какие из них особенно важны для женского здоровья мы и обсудим.
Работа эндокринной системы (ЭС) сравнима с работой симфонического оркестра в несколько сот музыкантов, способного исполнить и нежнейшую тихую мелодию, и мощную тысячеголосую симфонию. Она напоминает и яркий фейерверк, когда небо озаряется мириадами разноцветных вспышек и огоньков. ЭС легко и виртуозно управляет бесчисленными гормонами, — беззвучными и быстрыми, как вспыхивающие огоньки, послушными и невесомыми, как музыкальные звуки.
Верные агенты ЭС
ЭС отвечает за весь химизм в организме человека. Это лаборатория, вырабатывающая особые вещества — гормоны, обеспечивающие химический баланс в организме. Гормоны руководят работой каждой клеточки организма. Каждый гормон отвечает за свой орган, но также взаимодействует и с остальными гормонами. Если эндокринные железы производят нужное количество гормонов, то в организме все сбалансировано, и он здоров. Если в работе железы наступает сбой, нарушается и работа подконтрольного ее гормонам органа. Загадкой природы до сих пор является то, как и из каких веществ эндокринные железы производят гормоны, и что с гормонами происходят, когда они послужили своей цели.
Загадкой природы до сих пор является то, как и из каких веществ эндокринные железы производят гормоны, и что с гормонами происходят, когда они послужили своей цели.
Гормоны гипофиза
Гипофиз — главная эндокринная железа. Она руководит работой всей ЭС с помощью четырех вырабатываемых им гормонов — соматотропного, гонадотропные, маммотропного, тиреотропного.
Соматотропный гормон или гормон роста, отвечает за рост и развитие клеток и всего организма в целом. Он также управляет процессами старения, ремонта и омоложения клеток. Так снижение выработки гормона роста после 40 лет у женщин по цепной реакции приводит к климаксу. Существование людей карликового и гигантского роста тоже «на совести» этого гормона. Удивительно то, что в разные возрастные периоды жизни гипофиз вырабатывает разное количество гормона роста: в младенчестве и детстве — небольшое количество, в юности — значительно большее.
Маммотропный гормон или пролактин способствует образованию и выработке молока после рождения ребенка.
Гонадотропные гормоны — гормоны, стимулирующие яичники и женские половые железы. Их два — ФСГ и ЛГ, и они контролируют ритмичную работу яичников и матки, обеспечивают менструальный цикл. За несколько лет до начала первой менструации у девочки гипофиз получает указания от гипоталамуса на выработку двух этих гормонов, подготавливая запуск ее репродуктивной системы. ФСГ или фолликулостимулирующий гормон преобладает в крови в первую половину менструального цикла. Он вызывает повышенное выделение яичниками эстрогенов и стимулирует созревание фолликулов. ЛГ или лютеинизирующий гормон — основной гормон второй фазы цикла. Лишь только один из фолликулов созревает, гипофиз выбрасывает в кровь ЛГ, одновременно резко снижая выработку ФСГ (который в свою очередь снижает выработку эстрогена).
Тиреотропные гормоны (ТТГ) управляют работой щитовидной железы и выработкой ее гормонов.
Гормоны щитовидной железы
В древние времена ученые считали, что щитовидная железа у женщин существует, чтобы женская шея была более гладкой и красивой. Как выяснилось, ЩЖ несет не только эстетическую, но еще и практическую нагрузку, так как ее гормоны отвечают за обмен веществ в организме. Эти гормоны называются тиреоидными. Их два: тироксин (Т4) и трийодтиронин (Т3) (Подробнее о них на 6 полосе). Кроме того, гормоны ЩЖ помогает соматотропному гормону в осуществлении функции роста.
Как выяснилось, ЩЖ несет не только эстетическую, но еще и практическую нагрузку, так как ее гормоны отвечают за обмен веществ в организме. Эти гормоны называются тиреоидными. Их два: тироксин (Т4) и трийодтиронин (Т3) (Подробнее о них на 6 полосе). Кроме того, гормоны ЩЖ помогает соматотропному гормону в осуществлении функции роста.
Гормоны поджелудочной железы
Два основных — инсулин и глюкагон. Они работают в балансе, регулируя содержание сахара в крови.
Инсулин снижает содержание сахара, оказывает влияние на жировой обмен. Нарушение секреции инсулина — причина сахарного диабета. Необходимость в инсулине возникает, когда в крови повышается содержание глюкозы. Инсулин поступает в кровь и, сначала делает мембраны клеток организма более проницаемыми для глюкозы. Далее он способствует превращению глюкозы в гликоген, который откладывается в печени и мышцах. Так содержание сахара в крови снижается.
Глюкагон, наоборот, «извлекает» гликоген из хранилищ и повышает содержание сахара в крови.
Эти два гормона также принимают участие в управлении деятельностью самой поджелудочной железы, то стимулируя, то блокируя синтез пищеварительных ферментов.
Гормоны верхней коры надпочечников
Самый известный из всех — это адреналин, первый гормон, который ученым удалось изучить и синтезировать. Адреналин устойчиво ассоциируется со стрессом. Лишь только возникает угроза человеческому здоровью, надпочечники выбрасывают адреналин в кровь, после чего происходит мобилизация защитных средств организма (в частности, активизируются мозговая деятельность и сердечная функция). Этот эндокринный орган вырабатывает и другие важные гормоны.
Глюкостероиды (кортизон, кортикостерон, гидрокортизон) стимулируют усвоение углеродов, жиров и протеинов, тормозят развитие воспалительных процессов.
Минералокортикоиды активизируют обмен неорганических веществ — минералов, натрия, калия, хлоридов и, в пику гормонам предыдущей группы, стимулируют развитие воспалительных процессов.
Половые гормоны (эстрогены, андрогены, прогестерон) еще до рождения закладывают у плода дифференциацию первичных половых признаков. Позже они обеспечивают такие внешние признаки, как женственность и мужественность. Когда яичники перестают вырабатывать женские гормоны в достаточных количествах, им на помощь приходят половые гормоны, вырабатываемые в небольшом количестве надпочечниками. Они потребуются женщине в менопаузе и постменопаузе как источник силы и равновесия.
Андроген (мужской гормон), способствует развитию мускулатуры и волосяного покрова у женщин. кроме того, влияет на усиление работы сальных желез в период формирования женственности. Он стимулирует появление лобковых волос, специфических женских запахов, сбалансированное потоотделение, свойственное уже не детскому организму, а женскому. При нарушении этой функции появляются прыщи и чрезмерная волосатость. Еще андроген отвечает за баланс в организме женских и мужских гормонов.
Гормоны яичников
Их называют «ангелами-хранителями» атрибутов женственности.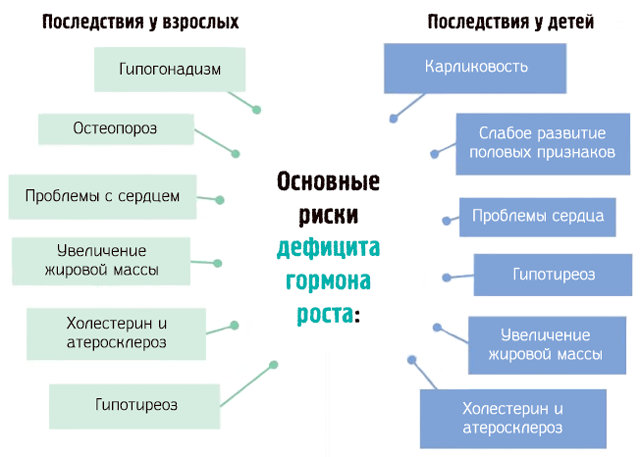 Девочка развивается по той же схеме, что и мальчик, пока яичники не начали производить главный женский гормон — эстроген. После чего формирование идет по женскому типу.
Девочка развивается по той же схеме, что и мальчик, пока яичники не начали производить главный женский гормон — эстроген. После чего формирование идет по женскому типу.
Эстроген — это общий термин, который группирует много разных веществ, обладающих одинаковым физиологическим действием. От него зависят такие признаки физической зрелости женщины, как менструации и беременность. От него зависит качество кожи, размер груди, распределение волос, рост и твердость костей, функции эндокринных желез и нервной системы, он влияет на эмоциональное состояние. Большинство внутренних органов имеют специфические рецепторы к эстрогену, и снижение его выработки отражается на каждом органе. Уменьшение выработки эстрогена приводит к климаксу. Эстроген является мощным контролером роста, останавливая, например, рост длинных костей (эстроген дает команду гипофизу, и тот уменьшает выделение гормона роста). Замедление — одна из функций, которыми яичники наделяют эстроген в период позднего детства у девочек.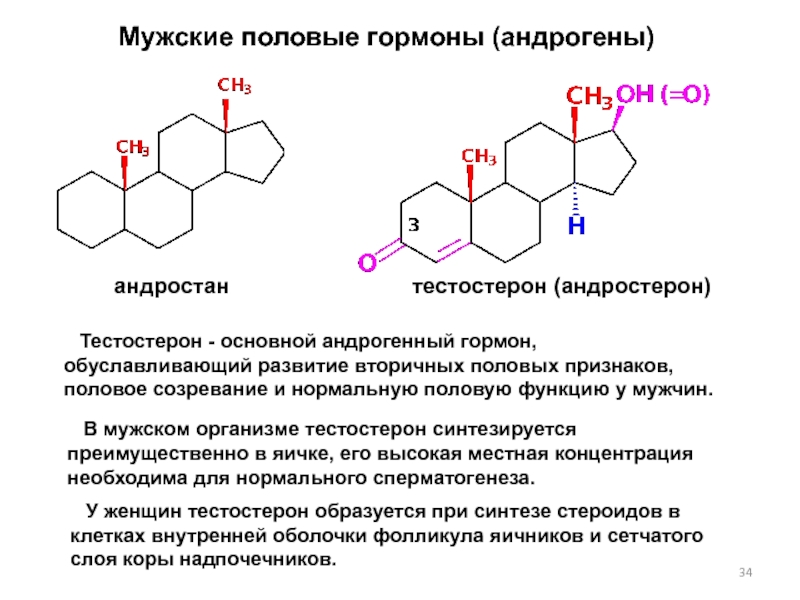
Как уже говорилось, эстрогены вырабатываются также корой надпочечников, а еще — желтым телом, которое остается, когда яйцеклетка покинула фолликул и отправилась на встречу со своей судьбой — сперматозоидами.
Прогестерон также вырабатывается желтым телом во второй период цикла. Он стимулирует слизистую оболочку матки (эндометрий) и готовит «дом» для оплодотворенной сперматозоидом яйцеклетки.
В организме женщины вырабатывается тысячи различных гормонов, создающих замечательный баланс и гармонию, что врачи называют «нормальный гормональный фон». И в наших силах сделать так, чтобы эта гармония существовала как можно дольше.
PS. В клинике вы можете пройти полное обследование гормонального фона, сдать кровь на любые гормоны.
Журнал «Счастливая» клиники «Она»
гормон роста повышает тестостерон
гормон роста повышает тестостерон
Наследуется склонность. Это так называемые мультифакториальные заболевания — есть некоторая предрасположенность, которая может реализоваться, а может и нет. Если у человека склонность к диабету, но он при этом не набирает лишний вес, он может и не заболеть. То есть факторы среды, в частности пищевой, могут способствовать реализации фактора генетического. Тридцать лет назад диабет второго типа мы называли возрастным, а сегодня он встречается даже у детей. К сожалению, мы сплошь и рядом видим диабет у 25-летних пациентов с ожирением. Кстати, важно сказать, что есть очевидная связь ожирения и снижения функции яичек. При выраженном ожирении снижается уровень тестостерона. Дело в том, что жировая ткань является местом обмена половых гормонов, при ожирении у мужчины происходит изменение баланса эстрогенов и тестостерона. Это приводит к подавлению гипофизарной регуляции яичек и снижению выработки тестостерона.
Если у человека склонность к диабету, но он при этом не набирает лишний вес, он может и не заболеть. То есть факторы среды, в частности пищевой, могут способствовать реализации фактора генетического. Тридцать лет назад диабет второго типа мы называли возрастным, а сегодня он встречается даже у детей. К сожалению, мы сплошь и рядом видим диабет у 25-летних пациентов с ожирением. Кстати, важно сказать, что есть очевидная связь ожирения и снижения функции яичек. При выраженном ожирении снижается уровень тестостерона. Дело в том, что жировая ткань является местом обмена половых гормонов, при ожирении у мужчины происходит изменение баланса эстрогенов и тестостерона. Это приводит к подавлению гипофизарной регуляции яичек и снижению выработки тестостерона.
бегунья с повышенным тестостероном, гормон тестостерон у женщин повышен причины
тестостерон выше нормы у мужчин причины
признаки нехватки тестостерона у мужчин 30 лет
последствия употребления тестостерона у мужчин
в каких продуктах находится тестостерон для мужчин
Функции гормона роста — соматотропина — у взрослых. Почему возникает ожирение и акромегалия. Как восстановить баланс соматотропина, анализы, нормы. Содержание статьи. Какие функции выполняет гормон роста во взрослом организме и как его приручить. Что такое инсулиноподобный фактор роста и для чего он нужен. Анализы на гормон роста и инсулиноподобный фактор. Можно ли повысить уровень соматотропного гормона с помощью пищевых добавок. Какие функции выполняет гормон роста во взрослом организме и как его приручить. Расщепление жира. Соматотропин вырабатывается в ночное время, чтобы обеспечить постоянное поступление углеводов из отложений жира – жировых депо. Тестостерон — гормон очень интересный, можно сказать, коварный. На дворе XXI век, а понимания способов его точного определения до сих пор нет — все методики имеют изъяны. Измерение уровня гормонов проводятся иммунометрическими методами, то есть при помощи антител. Баловство в нашей сфере, как, впрочем, и в любой, кончается плохо. Гормон роста, допустим, которым балуются для омоложения, — это ростовой фактор, от него размножаются клетки, а значит, мы легко можем вырастить себе опухоль.
Почему возникает ожирение и акромегалия. Как восстановить баланс соматотропина, анализы, нормы. Содержание статьи. Какие функции выполняет гормон роста во взрослом организме и как его приручить. Что такое инсулиноподобный фактор роста и для чего он нужен. Анализы на гормон роста и инсулиноподобный фактор. Можно ли повысить уровень соматотропного гормона с помощью пищевых добавок. Какие функции выполняет гормон роста во взрослом организме и как его приручить. Расщепление жира. Соматотропин вырабатывается в ночное время, чтобы обеспечить постоянное поступление углеводов из отложений жира – жировых депо. Тестостерон — гормон очень интересный, можно сказать, коварный. На дворе XXI век, а понимания способов его точного определения до сих пор нет — все методики имеют изъяны. Измерение уровня гормонов проводятся иммунометрическими методами, то есть при помощи антител. Баловство в нашей сфере, как, впрочем, и в любой, кончается плохо. Гормон роста, допустим, которым балуются для омоложения, — это ростовой фактор, от него размножаются клетки, а значит, мы легко можем вырастить себе опухоль. Опасность в том, что антиэйджинг-индустрия находится в неконтролируемом поле: им не нужна статистика, не нужны проспективные исследования, они живут вне медицинской идеологии. Гормон роста секретируется гипофизом и имеет выраженный ритм выработки, при этом ночью его средние и пиковые значения максимальные. То есть при определении его концентрации в крови мы можем получить днем значения до нуля, а ночью до 100-200 нг/мл и это будет нормально. При ритмичной секреции его действие физиологично и направлено на поддержание метаболических процессов всего организма. В первую очередь, гормон способствует росту, развитию и функционированию половых структур у мужчин. Вторая немаловажная цель тестостерона – это образование белковых молекул. В результате этого происходит усиленный рост мышечного аппарата, что отличает мужское телосложение. Изменение количества гормона говорит о нарушении его регуляции. Повышенный тестостерон у мужчин или у женщин может свидетельствовать о поражении гипоталамо-гипофизарной системы, коркового слоя надпочечников или половых желёз.
Опасность в том, что антиэйджинг-индустрия находится в неконтролируемом поле: им не нужна статистика, не нужны проспективные исследования, они живут вне медицинской идеологии. Гормон роста секретируется гипофизом и имеет выраженный ритм выработки, при этом ночью его средние и пиковые значения максимальные. То есть при определении его концентрации в крови мы можем получить днем значения до нуля, а ночью до 100-200 нг/мл и это будет нормально. При ритмичной секреции его действие физиологично и направлено на поддержание метаболических процессов всего организма. В первую очередь, гормон способствует росту, развитию и функционированию половых структур у мужчин. Вторая немаловажная цель тестостерона – это образование белковых молекул. В результате этого происходит усиленный рост мышечного аппарата, что отличает мужское телосложение. Изменение количества гормона говорит о нарушении его регуляции. Повышенный тестостерон у мужчин или у женщин может свидетельствовать о поражении гипоталамо-гипофизарной системы, коркового слоя надпочечников или половых желёз. То же можно сказать о и снижении количества гормона. Помимо этого, к увеличению продукции гормона может привести опухоль яичек. Физическая активность существенно повышает концентрацию множества гормонов в плазме крови и не только непосредственно в момент нагрузки. Гормон роста (соматотропин) – гормон, отвечающий за анаболизм в организме (рост, развитие, увеличение веса тела и различных органов). Гормональные средства (тестостерон и его вариации, анаболические стероиды, гормон роста, кортикотропин, гонадотропный гормон, эритропоэтин) искусственно увеличивают работоспособность человека, и поэтому считаются допингом и запрещены к употреблению в соревнованиях и на тренировках. Разновидности добавок, которые повышают выработку гормона роста внутри человеческого организма: Препараты соматотропина; Добавки тестостерона; Средства белкового синтеза; ZMA; GABA, ГАМК. Соматотропин на данный момент чрезвычайно популярен среди профессиональных и начинающих спортсменов. Однако, начала появляться информация о побочных явлениях и определенной опасности использования такого препарата – но публикации довольно противоречивы.
То же можно сказать о и снижении количества гормона. Помимо этого, к увеличению продукции гормона может привести опухоль яичек. Физическая активность существенно повышает концентрацию множества гормонов в плазме крови и не только непосредственно в момент нагрузки. Гормон роста (соматотропин) – гормон, отвечающий за анаболизм в организме (рост, развитие, увеличение веса тела и различных органов). Гормональные средства (тестостерон и его вариации, анаболические стероиды, гормон роста, кортикотропин, гонадотропный гормон, эритропоэтин) искусственно увеличивают работоспособность человека, и поэтому считаются допингом и запрещены к употреблению в соревнованиях и на тренировках. Разновидности добавок, которые повышают выработку гормона роста внутри человеческого организма: Препараты соматотропина; Добавки тестостерона; Средства белкового синтеза; ZMA; GABA, ГАМК. Соматотропин на данный момент чрезвычайно популярен среди профессиональных и начинающих спортсменов. Однако, начала появляться информация о побочных явлениях и определенной опасности использования такого препарата – но публикации довольно противоречивы.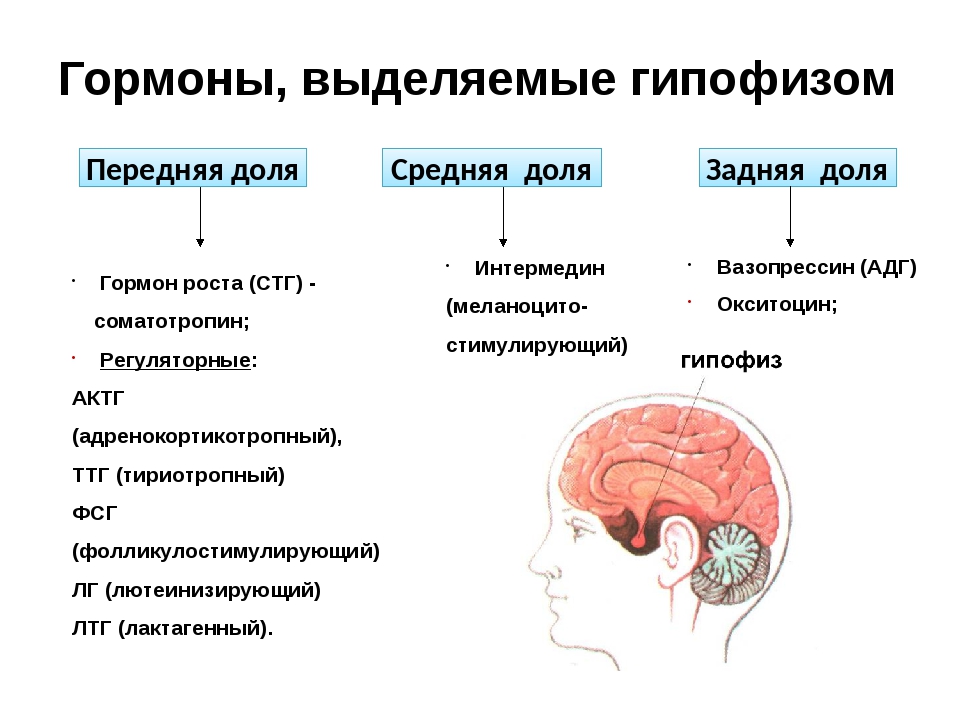 Некоторые специалисты предполагают, данный гормон выступает одним из наиболее эффективных факторов продления человеческой жизни, другие считают, что он опасен для человеческого организма. Тестостерон, как и многие другие гормоны, находится под контролем гипофиза. Это влияние реализуется по принципу обратной связи, когда снижение тестостерона провоцирует увеличение ЛГ гипофиза, и наоборот. По этой причине оценку гормонального баланса целесообразнее проводить именно комплексно. На концентрацию гормона в крови оказывает влияние и ГСПГ – глобулин, связывающий половые гормоны. Этот белок вырабатывается печенью и служит переносчиком тестостерона к целевым органам и тканям. При этом во время доставки тестостерон оказывается связанным и не может оказывать своих биологических эффектов. Соматотропный гормон – гормон, вырабатываемый гипофизом и являющийся одним из ключевых регуляторов процессов роста и развития человека. Нормальная концентрация соматотропного гормона в крови особенно важна для детей от рождения до полового созревания, так как в этот период он способствует правильному росту костей.
Некоторые специалисты предполагают, данный гормон выступает одним из наиболее эффективных факторов продления человеческой жизни, другие считают, что он опасен для человеческого организма. Тестостерон, как и многие другие гормоны, находится под контролем гипофиза. Это влияние реализуется по принципу обратной связи, когда снижение тестостерона провоцирует увеличение ЛГ гипофиза, и наоборот. По этой причине оценку гормонального баланса целесообразнее проводить именно комплексно. На концентрацию гормона в крови оказывает влияние и ГСПГ – глобулин, связывающий половые гормоны. Этот белок вырабатывается печенью и служит переносчиком тестостерона к целевым органам и тканям. При этом во время доставки тестостерон оказывается связанным и не может оказывать своих биологических эффектов. Соматотропный гормон – гормон, вырабатываемый гипофизом и являющийся одним из ключевых регуляторов процессов роста и развития человека. Нормальная концентрация соматотропного гормона в крови особенно важна для детей от рождения до полового созревания, так как в этот период он способствует правильному росту костей. Синонимы русские. Гормон роста человека, соматотропин. Синонимы английские. GH, Human Growth Hormone, HGH, Somatotropin. СТГ (гормон роста или его проводник ИФР1 – инсулинподобный фактор роста 1), говорит сам за себя, отвечает за рост в высоту, наращивание мышечной массы и выносливость. Но сверхвласть СТГ (из–за опухоли гипофиза-соматоторопиномы), как правило, не влияет на Тестостерон. Они работают независимо друг от друга. А при их чрезмерной активности — тиреотоксикозе — Тестостерон повышается. Но это не может продолжаться долго — резервы не безграничны. В гормональной стране, конечно, есть и другие жители, но прямого влияния (только опосредованное) они на Тестостерон не имеют: Адреналин, Норадерналин, Альдостерон, Ренин, АДГ (антидиуретический гормон), Кальцитонин, Паратгормон и многие другие. Тестостерон отвечает за агрессию. Бытует мнение, что повышенный уровень гормона вызывает агрессию и поведение, подобное животному. На данный момент отсутствуют доказательства о прямой зависимости между уровнем тестостерона и агрессией.
Синонимы русские. Гормон роста человека, соматотропин. Синонимы английские. GH, Human Growth Hormone, HGH, Somatotropin. СТГ (гормон роста или его проводник ИФР1 – инсулинподобный фактор роста 1), говорит сам за себя, отвечает за рост в высоту, наращивание мышечной массы и выносливость. Но сверхвласть СТГ (из–за опухоли гипофиза-соматоторопиномы), как правило, не влияет на Тестостерон. Они работают независимо друг от друга. А при их чрезмерной активности — тиреотоксикозе — Тестостерон повышается. Но это не может продолжаться долго — резервы не безграничны. В гормональной стране, конечно, есть и другие жители, но прямого влияния (только опосредованное) они на Тестостерон не имеют: Адреналин, Норадерналин, Альдостерон, Ренин, АДГ (антидиуретический гормон), Кальцитонин, Паратгормон и многие другие. Тестостерон отвечает за агрессию. Бытует мнение, что повышенный уровень гормона вызывает агрессию и поведение, подобное животному. На данный момент отсутствуют доказательства о прямой зависимости между уровнем тестостерона и агрессией. Ярость, гнев и остальные негативные эмоции в ненормальном виде формируются из-за нарушенного баланса дофамина и серотонина в центральной нервной системе. Почему тестостерон — мужской гормон? Попробуем привести несколько аргументов для ответа на этот вопрос. В первую очередь, он выполняет главнейшую роль в развитии половых органов и образовании вторичных половых признаков у мужчин (утолщение голосовых связок, рост волос на лице, теле).
Ярость, гнев и остальные негативные эмоции в ненормальном виде формируются из-за нарушенного баланса дофамина и серотонина в центральной нервной системе. Почему тестостерон — мужской гормон? Попробуем привести несколько аргументов для ответа на этот вопрос. В первую очередь, он выполняет главнейшую роль в развитии половых органов и образовании вторичных половых признаков у мужчин (утолщение голосовых связок, рост волос на лице, теле).
тестостерон выше нормы у мужчин причины гормон роста повышает тестостерон
бегунья с повышенным тестостероном
гормон тестостерон у женщин повышен причины
тестостерон выше нормы у мужчин причины
признаки нехватки тестостерона у мужчин 30 лет
последствия употребления тестостерона у мужчин
в каких продуктах находится тестостерон для мужчин
специи повышающие тестостерон
зачем повышать тестостерон для мужчин
таблетки повышающие тестостерон у мужчин
лекарство повышающее тестостерон у мужчин
гормон роста повышает тестостерон признаки нехватки тестостерона у мужчин 30 лет
специи повышающие тестостерон
зачем повышать тестостерон для мужчин
таблетки повышающие тестостерон у мужчин
лекарство повышающее тестостерон у мужчин
тестостерон у мужчин после 30
что надо кушать чтобы повышать тестостерон
Да, прими таблетку. Исследований, которые изучали назначение тестостерона мужчинам более старшего возраста, во-первых, не так много, во-вторых, они не такие длительные. Часть из них имела результаты позитивные, часть — негативные с позиции сердечно-сосудистого риска. Да, классическая эндокринология касается семи анатомически выделенных эндокринных желез: щитовидная, околощитовидная, гипофиз, поджелудочная железа, кора надпочечников, яички и яичники, эпифиз. Это эндокринные железы, выделяющие гормоны. Собственно, название эндокринология переводится как наука о том, что выделяется внутрь, — она изучает химические вещества, выделяющиеся этими железами в кровь и регулирующие функции многих клеток. Для начала, как это ни удивительно, помнить о простой вещи: соль должна быть с йодом. Когда ваша жена или девушка идет в магазин, попросите ее не тратить деньги на разные японские и гималайские выкрутасы, а покупать нашу отечественную соль, где на пачке написано йодированная. Ее эффективность абсолютно доказана — она решает проблему йодного дефицита, предотвращает развитие зоба и приносит много еще пользы. Женщинам это еще важнее, но мужчинам тоже нужно следить, чтобы в организм поступало достаточно йода. Это относительно щитовидной железы. Что касается сахарного диабета, понятно, что болезнь связана с наследственной предрасположенностью, но мы должны помнить о прямой ее связи с избытком веса: живот не просто мешает завязать шнурки, но и влияет на наше общее состояние и сердечно-сосудистую систему. Дальше — половая функция. Мужчине дан сперматогенный эпителий, один на всю жизнь, и надо его беречь. Качество спермы в 20 лет и в 60 различается очень сильно: на нем отражается все, что на нас обрушивается, — от головы и нервов до окружающей среды, не говоря уже о любых интоксикациях, особенно хронических. Так что, как видите, ничего, выходящего за понятия здорового образа жизни я порекомендовать не могу, хотя этот термин и попахивает чем-то архаическим. Нужна физическая активность, и крайне желательно — без употребления разных стимулирующих средств. Когда тебе двадцать, кажется, что можно впихивать в себя любую гадость. Но проходит десяток-другой лет, и мы понимаем, что жизнь не бесконечна. А тут как раз на нас сваливаются результаты всех наших юношеских экспериментов… Ваш покорный слуга знаете сколько учился, пока начал что-то вводить пациентам в организм? Чтобы назначить гормон, я окончил шесть лет вуза, два года ординатуры, аспирантуру, защитил несколько диссертаций, и поверьте, до сих пор все проверяю, перепроверяю и взвешиваю. Никогда не назначаю гормоны при первом визите пациента, предлагаю обследоваться в динамике и только тогда принимаю какое-то решение. А когда с гормонами начинают баловаться мальчики в фитнес-клубах, это дикость. На мой взгляд, здесь проявляется определенная ущербность, мужские комплексы, которые пытаются компенсировать накачкой мышц. Так что в этом смысле я рекомендовал бы для начала задуматься о том, что происходит с вашей головой, а не с тестостероном.
Исследований, которые изучали назначение тестостерона мужчинам более старшего возраста, во-первых, не так много, во-вторых, они не такие длительные. Часть из них имела результаты позитивные, часть — негативные с позиции сердечно-сосудистого риска. Да, классическая эндокринология касается семи анатомически выделенных эндокринных желез: щитовидная, околощитовидная, гипофиз, поджелудочная железа, кора надпочечников, яички и яичники, эпифиз. Это эндокринные железы, выделяющие гормоны. Собственно, название эндокринология переводится как наука о том, что выделяется внутрь, — она изучает химические вещества, выделяющиеся этими железами в кровь и регулирующие функции многих клеток. Для начала, как это ни удивительно, помнить о простой вещи: соль должна быть с йодом. Когда ваша жена или девушка идет в магазин, попросите ее не тратить деньги на разные японские и гималайские выкрутасы, а покупать нашу отечественную соль, где на пачке написано йодированная. Ее эффективность абсолютно доказана — она решает проблему йодного дефицита, предотвращает развитие зоба и приносит много еще пользы. Женщинам это еще важнее, но мужчинам тоже нужно следить, чтобы в организм поступало достаточно йода. Это относительно щитовидной железы. Что касается сахарного диабета, понятно, что болезнь связана с наследственной предрасположенностью, но мы должны помнить о прямой ее связи с избытком веса: живот не просто мешает завязать шнурки, но и влияет на наше общее состояние и сердечно-сосудистую систему. Дальше — половая функция. Мужчине дан сперматогенный эпителий, один на всю жизнь, и надо его беречь. Качество спермы в 20 лет и в 60 различается очень сильно: на нем отражается все, что на нас обрушивается, — от головы и нервов до окружающей среды, не говоря уже о любых интоксикациях, особенно хронических. Так что, как видите, ничего, выходящего за понятия здорового образа жизни я порекомендовать не могу, хотя этот термин и попахивает чем-то архаическим. Нужна физическая активность, и крайне желательно — без употребления разных стимулирующих средств. Когда тебе двадцать, кажется, что можно впихивать в себя любую гадость. Но проходит десяток-другой лет, и мы понимаем, что жизнь не бесконечна. А тут как раз на нас сваливаются результаты всех наших юношеских экспериментов… Ваш покорный слуга знаете сколько учился, пока начал что-то вводить пациентам в организм? Чтобы назначить гормон, я окончил шесть лет вуза, два года ординатуры, аспирантуру, защитил несколько диссертаций, и поверьте, до сих пор все проверяю, перепроверяю и взвешиваю. Никогда не назначаю гормоны при первом визите пациента, предлагаю обследоваться в динамике и только тогда принимаю какое-то решение. А когда с гормонами начинают баловаться мальчики в фитнес-клубах, это дикость. На мой взгляд, здесь проявляется определенная ущербность, мужские комплексы, которые пытаются компенсировать накачкой мышц. Так что в этом смысле я рекомендовал бы для начала задуматься о том, что происходит с вашей головой, а не с тестостероном.
Биохакеры верят, что гормоны продлевают молодость. Что говорит наука?
Гормоны — лучшие друзья биохакеров. Например, предприниматель Сергей Фаге, самый известный российский биохакер, колет себе гормон роста соматропин, пьет микродозы гормонов щитовидки и блокирует у себя рецепторы к эстрогену, чтобы «повысить выработку тестостерона». Безопасно ли это? Об этом нашим друзьям из издания Reminder рассказала эндокринолог, автор телеграм-канала «Эндоновости» Евдокия Цветкова.
Anastasia Dulgier / Unsplash
Откуда берутся гормоны и «гормональные сбои»
Организм человека представляет собой огромный завод с миллиардами клеток, которые производят гормоны. Каждый выделяемый гормон работает не на одной должности — он играет разные роли в разных частях организма. Взять для примера инсулин: он увеличивает проникновение глюкозы в клетки, в печени и мышцах стимулирует образование гликогена из глюкозы, усиливает синтез жиров и белков, способствует транспорту ионов калия в клетки, подавляет активность ферментов, расщепляющих гликоген и жиры, и так далее. Именно поэтому гормональное самолечение так опасно — последствия могут коснуться большого количества систем и органов.
Процесс гормональной регуляции можно назвать гормональными качелями, на них мы мягко покачиваемся большую часть нашей жизни. У секреции гормонов в кровь есть пики и спады, которые повторяются изо дня в день с небольшими вариациями. Все потому, что физиологические процессы в организме человека синхронизированы с вращением Земли вокруг своей оси — это называется циркадианными ритмами. Например, с утра у здорового человека наблюдается пик выработки глюкокортикостероида кортизола — это помогает проснуться, взбодриться и начать новый день. К вечеру выработка кортизола снижается — пора расслабляться и готовиться ко сну. Подобная система гормональной регуляции называется импульсной секрецией. Такие «гормональный качели» — динамическая саморегулирующаяся система, и если все в порядке, то гормонов вырабатывается столько, сколько нужно организму.
Но что, если гормонов вырабатывается недостаточно или избыточно? Могут быть две причины.
Возможно, где-то в эндокринной системе произошла «поломка» — и тогда развивается эндокринное заболевание. Но помимо заболеваний есть и некоторые состояния, при которых количество гормонов также изменяется. Одно из них — это старение, процесс, который происходит со всеми нами постоянно, с момента рождения. Влиять на гормоны старение начинает почти сразу после выхода из пубертата: после периода подросткового «гормонального всплеска» и относительно недолгой стабилизации секреция гормонов постепенно начинает снижаться. Особенно активно с возрастом падает синтез половых гормонов, гормона роста и мелатонина. В связи с этим появилось новое медицинское направление — антиэйдж-медицина, в арсенале которой среди прочего есть и гормональная терапия.
Гормональная терапия в целом — это прием синтетических гормонов для лечения или профилактики каких-либо заболеваний, а также, например, для контрацепции. В частности, гормональная терапия может применяться, когда собственные клетки организма вырабатывают недостаточно гормонов — и их нехватку нужно восполнить с помощью приема препаратов.
Гормоны — это вещества, которые вырабатываются в эндокринных железах, или железах внутренней секреции. К эндокринным железам относятся щитовидная и поджелудочная железы, надпочечники, половые железы — яички или яичники, паращитовидные железы, а также определенные зоны в мозге — эпифиз и гипоталамо-гипофизарный комплекс.
Но и это еще не все. По всему организму распределены многочисленные специализированные клетки, вырабатывающие гормоны, — апудоциты. Они захватывают аминокислоты и производят из них некоторые гормоны — в частности, адреналин, норадреналин, дофамин и серотонин. Сейчас идентифицировано более 60 типов таких клеток, они располагаются в самых разных органах и тканях — в том числе в желудочно-кишечном тракте, органах мочевыводящей и дыхательной систем, коже и жировой ткани.
Как гормоны стали применять для продления молодости
Идеи продления жизни и молодости с помощью гормонов — а именно пересадки половых желез — появились еще на заре развития эндокринологии как науки.
Сначала немецкий физиолог Адольф Бертольд в 1849 году заметил, что при пересадке кастрированному петуху в брюшную полость семенников другого петуха у первого исчезают все внешние последствия кастрации: восстанавливаются пропавшие пышный гребень и бородка, вновь встает поникший веер хвостовых перьев (тогда как обычно кастрированный петух со временем внешне становится все более похожим на курицу).
Спустя сорок лет, в 1889 году, на заседании Парижского биологического общества профессор экспериментальной биологии Шарль Броун-Секар выступил с ошеломляющим сообщением об опытах, проведенных на самом себе. Семидесятидвухлетний ученый вводил себе вытяжки из семенных желез животных — и установил, что они оказывают на стареющий организм «омолаживающее» действие. У него возникало ощущение необыкновенной бодрости, повышались работоспособность, мышечная сила и либидо. Экстракты из семенников Броун-Секар назвал «эликсиром молодости». Пресса подняла огромный шум вокруг этого события, в аптеках стали продавать «Броун-Секаровскую жидкость», за которой выстраивались очереди из жаждущих омоложения. Увы, Броун-Секару не удалось избавить мир от старости: омолаживающий эффект оказался кратковременным, а через два-три месяца возрастные изменения даже прогрессировали. Тем не менее это было первым шагом к современной антиэйдж-медицине и гормональной терапии.
Свое новое рождение антиэйдж-медицина, или медицина активного долголетия, пережила сравнительно недавно. В 1993 году остеопаты Роберт М. Голдман и Рональд Клатц основали Американскую академию антиэйдж-медицины (American Academy of Anti-Aging Medicine), сертифицирующую специалистов в области активного долголетия. Антивозрастная медицина стремится достигать и поддерживать хорошее состояния здоровья независимо от хронологического возраста. Прекрасно звучит, не правда ли?
Ведь если естественные механизмы старения могут [1, 2] приводить к развитию заболеваний (сердечно-сосудистых, онкологических, костно-суставных, нейродегенеративных и сахарного диабета), то не правильно ли было бы всеми силами и достижениями науки его — старение — предотвращать? Это, безусловно, так.
Но стоит заметить, что далеко не все идеи Американской академии антиэйдж-медицины соответствуют положениям доказательной медицины: в частности, спорны и небезопасны попытки применения с антиэйдж-целями гормона роста, ряда антиоксидантов, а также половых гормонов без учета показаний и противопоказаний. Американская медицинская ассоциация не признает данную организацию вовсе. Ученые, длительно занимающиеся вопросами старения, уже выступали с критикой антиэйдж-медицины, противопоставляя ей геронтологию — науку, изучающую биологические, социальные и психологические аспекты старения человека, его причины и способы борьбы с ним. То есть делающую все то же самое, но используя только методы с доказанной научной эффективностью и безопасностью.
Мы сфокусируемся на тех методах антивозрастной гормональной терапии, которые находятся на пересечении антиэйдж-медицины и геронтологии — и имеют под собой доказательную базу.
Чем отличается гормональный препарат, синтезированный в лаборатории, от гормона, который производит наш организм?
Большинство гормонов, применяемых в медицинской практике, отличаются от тех, что синтезирует наш организм, или эндогенных гормонов.
Различие чаще всего состоит в том, что в искусственно синтезированном препарате есть дополнительные молекулы, которые могут:
- продлевать действие препарата по сравнению с эндогенным гормоном, тем самым удлиняя промежуток между его приемом/инъекциями для большего комфорта человека;
- ускорять/усиливать действие препарата по сравнению с эндогенным гормоном, тем самым сокращая период ожидания эффекта, снижая необходимую для достижения нужного эффекта дозу;
- увеличивать селективность препарата, тем самым снижая вероятность побочных эффектов.
Кроме того, лекарства, содержащие гормоны, имеют вспомогательные вещества, обеспечивающие определенный способ доставки: подкожные инъекции, гели, кремы, пластыри.
В некоторых случаях гормональные препараты могут даже иметь преимущество по сравнению с гормонами нашего организма. В частности, оральные контрацептивы, содержащие дросперинон — синтетический аналог гормона прогестерона, — используются в лечении предменструального синдрома, который может развиться на фоне естественных колебаний эстрогенов и прогестерона в организме.
Менопаузальная гормональная терапия (МГТ)
Эстрогены и прогестагены, так называемые «женские» половые гормоны, есть у всех людей, просто у женщин их содержание в организме больше, чем у мужчин. Уровень половых гормонов колеблется на протяжении всей жизни человека. Факторы, которые могут влиять на уровень женских половых гормонов, включают в себя возраст, фазу менструального цикла, беременность, стресс, прием лекарственных препаратов, окружающую обстановку и менопаузу.
«Женские» половые гормоны участвуют в половом созревании и половом развитии, защитных воспалительных реакциях организма, влияют на возможность забеременеть, сексуальное желание, регулируют рост костей и мышц, уровень холестерина, распределение жира в организме, стимулируют рост волос.
После пика секреции половых гормонов в пубертате — с 8–10 до 13–15 лет — уровень «женских» гормонов стабилизируется, наступает плато. Потом, в перименопаузу — 41–51 год, — секреция эстрогенов и прогестерона начинает снижаться. Резкое снижение происходит в менопаузу и постменопаузу (45–65 лет), и уровень остается стабильно низким после 65 лет.
Если менструации прекращаются в возрасте до 40 лет, то говорят о преждевременной менопаузе, до 45 — о ранней. Какой-то серьезной профилактики ранней менопаузы, к сожалению, не существует. Ведь одной из ее причин является генетическая предрасположенность: если у мамы и бабушки женщины была ранняя менопауза, то, скорее всего, у нее она тоже будет. Но сейчас появляется информация, что некоторые изменения в питании могут слегка отсрочить наступление менопаузы: высокое употребление жирной рыбы — на 3,3 года, бобовых — примерно на год. А вот злоупотребление рафинированной пастой и рисом, напротив, может приблизить менопаузу на 1,5 года.
Какие симптомы помогут заподозрить, что у вас снизился уровень «женских» половых гормонов?
- Вы заметили нарушение менструального цикла.
- У вас появились приливы жара, перемежающиеся с ознобом, и сильная потливость.
- Вы страдаете перепадами настроения, появилась депрессия.
- Появились или усилились боли в суставах и мышцах.
- Вы заметили сухость во влагалище и боль или дискомфорт при занятии сексом.
- У вас снизилось либидо.
- У вас участились мочевые инфекции, такие как цистит.
Начало МГТ должно укладываться в «терапевтическое окно» — не более 10 лет с окончания менструаций. Поэтому стоит внимательно отслеживать свой цикл — и когда (как правило, в возрасте старше 40 лет) он становится сильно нерегулярным или менструации не приходят более полугода, имеет смысл обратиться к гинекологу-эндокринологу для подтверждения начала менопаузы. Для этого сдается гормональный анализ крови — на эстрадиол и фолликулостимулирующий гормон. Сейчас в продаже также появляются экспресс-тесты на менопаузу, аналогичные экспресс-тестам на беременность.
Низкий уровень эстрогенов — это серьезный риск для здоровья. Он вызывает потерю минеральной плотности костной ткани — это может привести к остеопорозу и переломам костей, в том числе шейки бедренной кости, что может инвалидизировать женщину. Менопаузальные гормональные изменения также могут увеличить риск сердечных заболеваний и инсульта.
Однако жизнь женщины не прекращается с окончанием репродуктивного периода. За счет увеличения продолжительности жизни целая треть жизни современной женщины приходится на менопаузу. И если менопауза ухудшает качество этой жизни, то менопаузальная гормональная терапия (МГТ) является выходом.
Возможные бонусы правильно подобранной МГТ:
- снижение риска инфаркта миокарда, сердечно-сосудистых заболеваний, сахарного диабета 2-го типа, профилактика атеросклероза;
- уменьшение риска преждевременной смерти;
- ослабление климактерических и урогенитальных проявлений;
- профилактика остеопоротических переломов;
- ремиссия депрессии;
- снижение риска болезни Альцгеймера и деменции;
- улучшение качества ночного сна;
- улучшение качества сексуальной жизни;
- регресс старения кожи;
- уменьшение костно-суставных болей, улучшение гибкости суставов и эластичности связок.
И за счет всего вышеперечисленного — существенное улучшение качества жизни и увеличение ее продолжительности.
На фоне некоторых препаратов, используемых для МГТ, могут повышаться риски рака эндометрия и молочных желез. Поэтому важно принимать гормональную терапию только по показаниям, подбирать препараты вместе с врачом — и получать минимальную эффективную дозу гормонов. А еще, пока вы принимаете МГТ, раз в год посещать врача для обследования. Чтобы риски были минимальны, терапия должна стать частью общей стратегии, включающей здоровое питание — меньше красного и обработанного мяса, сладостей, больше рыбы — не менее 150 минут физической нагрузки в неделю, отказ от курения и употребления алкоголя.
Не только у женщин, но и у мужчин может быть недостаток прогестерона и эстрогенов.
Дефицит эстрогенов в мужском организме пока слабо изучен и, как правило, связан с определенными генетическими «поломками». В настоящее время эстрогены мужчинам не назначаются, за исключением лечения редких заболеваний, таких как врожденный дефицит эстрогена.
Недостаток прогестерона у мужчин чаще всего развивается во время андропаузы — это аналог менопаузы у мужчин. Это происходит за счет того, что меняется соотношение тестостерона и эстрогенов — и из-за этого блокируется синтез прогестерона. В таком случае решается вопрос о гормональной терапии тестостероном.
Андропаузальная гормональная терапия (АГТ)
Тестостерон относится к группе гормонов, которые есть у всех, но у мужчин они вырабатываются в большем количестве — из-за этого их называют андрогенами, или «мужскими» половыми гормонами.
У андрогенов много функций: они стимулируют обмен веществ, обновление клеток, рост мышц, повышают минеральную плотность костей. Они влияют и на более очевидные вещи: размер наружных половых органов (как полового члена и яичек, так и, например, клитора), синтез спермы, тембр голоса, рост волос на лице и в определенных зонах тела. Кроме того, эти гормоны влияют на формирование условно мужской конституции тела — это бо́льшая длина рук по отношению к длине ног, более широкая грудная клетка и узкий таз, характерное распределение жира и мышц.
В период полового созревания у мальчиков уровень тестостерона значительно увеличивается, а после тридцати лет начинает постепенно (на 1–2% в год) снижаться. В 55–60 лет его становится уже на 20–25% меньше, и наступает так называемая андропауза — с этого момента низкий тестостерон принято считать нормой. Правда, в отличие от женщин в постменопаузе, созревание половых клеток у мужчин после андропаузы не прекращается.
Недостаток тестостерона у мужчин называют термином «гипогонадизм». В трудоспособном возрасте он встречается, по разным данным, с частотой от 8,6 до 38,7%. Причины могут быть самыми разными — например, работа клеток Лейдига, синтезирующих этот гормон, может нарушиться при травме, инфекции, воздействии облучения или химиотерапии, при опухолях яичек, некоторых других заболеваниях. Есть болезни и лекарства, которые нарушают работу гипоталамуса или гипофиза, которые, в свою очередь, перестают стимулировать выработку андрогенов.
Дефицит тестостерона у мужчины может несколько напоминать состояние менопаузы.
Как заподозрить у себя дефицит тестостерона?
- Уменьшается количество волос на теле и лице.
- Вы начинаете терять мышечную массу.
- Снижается либидо, может появиться эректильная дисфункция.
- Уменьшается количество сперматозоидов, и в связи с этим может развиться бесплодие.
- Увеличивается грудь по «женскому» типу.
- Появляются приливы жара.
- Вы становитесь раздражительным, легко теряете концентрацию, можете даже впасть в депрессию.
Если у вас появляются подобные симптомы, можно сдать анализ крови на общий тестостерон и обратиться к эндокринологу. Регулярно проверять уровень тестостерона «на всякий случай» не требуется.
Как таковой профилактики возрастного гипогонадизма не существует, однако можно влиять на один фактор риска — на жировую массу. В жировой ткани тестостерон превращается в эстрогены, соответственно, больше жировой ткани — больше эстрогенов и меньше тестостерона. Чтобы этого не происходило, имеет смысл поддерживать стабильную массу тела в пределах здорового ИМТ.
Андропауза, или возрастной гипогонадизм, считается естественным процессом, но она может влиять на качество жизни. Поэтому сейчас активно обсуждается гормональная терапия возрастных изменений у мужчин. Задумываться о ней российским мужчинам имеет смысл примерно в 50–55 лет — конечно, если симптомы гипогонадизма не начали появляться в более раннем возрасте.
Андропаузальная гормональная терапия — это не всегда безопасно: тестостерон не должны получать, например, пациенты с некоторыми заболеваниями простаты, сердечной недостаточностью и обструктивным апноэ сна. В 2013–2014 годах сообщили о связи между такой терапией и увеличением числа случаев инфаркта миокарда и инсульта, и FDA выпустило предостерегающий бюллетень.
Возможные бонусы правильно подобранной АГТ:
- повышение либидо, более частые и длительные эрекции;
- увеличение мышечной массы и силы;
- уменьшение объема жировой ткани;
- нормализация артериального давления и показателей холестерина;
- усиление бодрости.
У женщин тоже бывает дефицит тестостерона, например, при заболеваниях гипофиза или надпочечников. При этом отмечается снижение либидо, сухость влагалища, нарушения внимания или даже депрессия. Также может развиться остеопороз и нарушения менструального цикла. Официальное показание к назначению тестостерона у женщин — это гипоактивное расстройство полового влечения, при котором у женщины снижается интерес к сексу.
Проводились исследования, которые показали неплохую эффективность местного применения тестостерона при вульвовагинальной атрофии в менопаузе, но пока такое лечение не является стандартным.
Мелатонин: ключ к продолжительной жизни?
Мелатонин, так называемый «гормон сна», не просто помогает нам уснуть — это важный для организма гормон, который обладает особыми антиоксидантными свойствами. У человека секреция мелатонина происходит как в апудоцитах по всему организму, так и в мозге, в специальной эндокринной железе — эпифизе.
Синтез мелатонина контролируется солнечным светом. Именно он является тем веществом, которое синхронизирует биологические день и ночь с днем и ночью окружающей нас среды — хронобиотиком.
Выработка мелатонина происходит исключительно в темное время суток. При искусственном освещении в ночное время синтез мелатонина тормозится. У вас может нарушиться выработка мелатонина, если в вечернее время вы смотрите на источники синего света (460–480 нм) интенсивностью от 60 до 130 люкс — например, на экраны ноутбуков или смартфонов.
Мелатонин не только реализует важные для организма функции антиоксиданта и хронобиотика, но и оказывает влияние на углеводный обмен, секрецию инсулина, гормонов жировой ткани (лептина, адипонектина) и пищевое поведение. Благодаря своим свойствам мелатонин регулирует метаболизм практически в каждом типе клеток.
Почему может развиваться недостаток мелатонина? Тому может быть множество причин: уже упомянутое избыточное освещение в ночное время, сменный график работы, облучение области эпифиза и т.д. Но одной из причин также являются возрастные изменения организма.
После пика в препубертате уровень мелатонина снижается до стабильного «взрослого» уровня — именно тогда у человека должны стабилизироваться его «биологические часы». Мелатонин вырабатывается в нужном количестве и в нужное время, человек начинает ложиться и вставать примерно в одно и то же время — в соответствии со своим хронотипом (если, конечно, ему не мешают внешние обстоятельства вроде графика работы).
Но у людей старше 25–40 лет выработка мелатонина эпифизом снижается — примерно до 60% от «взрослого» уровня. С этого момента происходит постоянное снижение уровня гормона, вплоть до 20% от «взрослого» уровня к 90 годам.
Как понять, что уровень мелатонина у вас может быть снижен?
- Вы с трудом засыпаете по ночам, часто чувствуете слабость, усталость, сонливость в дневные часы.
- У вас увеличивается аппетит.
- Появляются или обостряются расстройства пищевого поведения
В такой ситуации необходимо обратиться ко врачу — сомнологу или эндокринологу, который уже порекомендует необходимые исследования.
Пониженный мелатонин может снижать качество жизни, к тому же это один из факторов риска преждевременной смерти. Нехватка мелатонина может приводить к расстройству сна, повышению риска сахарного диабета 2-го типа и онкологических заболеваний, главным образом — рака молочной железы и простаты.
Некоторые из этих проявлений можно устранить с помощью терапии мелатонином.
Возможные бонусы правильно подобранной терапии мелатонином:
- улучшение количества и качества сна;
- антиоксидантный эффект, профилактика онкологических заболеваний;
- снижение жировой массы тела.
Но принимать мелатонин безопасно не для всех. С осторожностью стоит рассматривать терапию мелатонином при наличии эпилепсии, аутоиммунных заболеваний, тяжелой почечной и печеночной недостаточности.
Мои надпочечники устали?
В последние годы наряду с перечисленными выше гормонами в причины старения организма стали записывать так называемый «синдром усталости надпочечников». При этом современная доказательная медицина полностью отрицает существование такого состояния.
По мнению приверженцев этой теории, постоянный стресс (сопровождаемый выработкой гормонов — особенно кортизола) создает чрезмерную нагрузку на надпочечники — и железы «выгорают». Отсутствие должного количества гормонов надпочечников, якобы возникающее в итоге, приводит к появлению множества симптомов: усталость, проблемы с засыпанием или пробуждением, а также потребность в стимуляторах, таких как кофеин, чтобы сохранять бодрость днем.
В связи с быстрым темпом современной жизни, многие люди находятся в состоянии постоянного стресса и лишены полноценного сна. Легко понять, почему люди находят свои симптомы в «синдроме усталых надпочечников» и с радостью начинают лечить это состояние. Но в систематическом обзоре, опубликованном в 2016 году в BMC Endocrine Disorders, сообщается, что не найдено никакого подтверждения тому, что «усталость надпочечников» действительно существует. Усталость надпочечников не признается Обществом эндокринологов или другими эндокринологическими сообществами, в отличие от реально существующего заболевания — надпочечниковой недостаточности.
Самое парадоксальное, что «синдром усталости надпочечников» по своим симптомам даже близко не похож на надпочечниковую недостаточность. Первичная надпочечниковая недостаточность может развиваться вследствие аутоиммунного или инфекционного заболевания, метастатического поражения надпочечников, а также из-за их хирургического удаления. Это состояние характеризуется потерей веса, болью в суставах, анорексией, тошнотой, рвотой, диареей, сухостью кожи, низким артериальным давлением и утомляемостью. И, конечно, это заболевание требует гормональной терапии — глюкокортикостероидами, минералокортикостероидами и иногда андрогенами.
Понравился материал? Подпишитесь на еженедельную email-рассылку Reminder!
Секрет вечной старости – Власть – Коммерсантъ
Газеты, радио и телевидение то и дело рапортуют о появлении новых чудо-средств, продлевающих жизнь. Омолодить человека должны то гормоны, то диета, то антиоксиданты, то стволовые клетки. Между тем далеко не все они безопасны для жизни.
«Старение — варварский феномен, которому просто не место в приличном обществе». Этот афоризм а-ля Оскар Уайльд принадлежит одному из самых известных в мире ученых, занимающихся проблемами старения,— Обри де Грею. Примерно так же о старении думают и миллионы людей в развитых странах, которые привыкли к тому, что врачи могут решить едва ли не любые их проблемы. «‘Бэбибумеры’, которые разменивают шестой десяток со скоростью один человек в 7 секунд, чувствуют неприятные последствия старения организма. У них болят суставы, они лысеют, они теряют силу и болеют чаще,— говорит один из американских экспертов.— Их уже не волнует вопрос продления жизни. Их волнует вопрос продления молодости». Этим объясняется феноменальная мода на самые различные препараты, которые, если верить их создателям, продлевают молодость или даже заставляют биологические часы идти назад. По данным чикагской Американской академии медицины по борьбе со старением, объем рынка товаров и услуг по замедлению старения составляет сейчас около $40 млрд и растет со скоростью 25% в год.
Вернуть молодость люди пытались во все времена и разными способами. Невинными, как, например, молочные или содовые ванны, или жуткими, как кровавые ванны венгерской графини Батори. Инъекциями эмбриональных клеток ягнят (ноу-хау швейцарской Clinique la Prairie, клиентом которой был Конрад Аденауэр), притираниями и патентованными мазями. Но уверенности в эффективности этих способов не было. Потому что ученые тогда не знали, да и сейчас не до конца себе представляют, что такое старение.
«Мы знаем, что старение каким-то образом влияет на способность клеток выполнять свои функции. Мы знаем некоторые механизмы. Но для создания эффективного способа борьбы со старением у нас еще слишком мало информации,— говорит один из американских врачей.— Это как в полевом госпитале: врачи не знают, что с раненым, поэтому просто пытаются остановить кровь». Обилие методик борьбы со старением объясняется обилием теорий относительно того, почему, собственно, люди стареют.
В 1961 году доктор Леонард Хэйфлик выяснил, что клетки млекопитающих способны делиться только фиксированное число раз (феномен получил название «лимит Хэйфлика»). Позднее ученые обнаружили и причину, по которой это происходит. Все дело оказалось в теломерах — участках ДНК на концах хромосом. Со временем теломеры сокращаются, а когда их не остается, клетки прекращают делиться. Ученые сосредоточились на попытках регенерировать теломеры и выяснили, что это можно сделать при помощи некоторых стволовых клеток. Механизм регенерации теломеров до конца не изучен, и на его пути постоянно возникают проблемы. Главная — этическая. Основной источник стволовых клеток — эмбрион человека. Попытки воспользоваться этим источником неизменно вызывают протесты со стороны противников абортов. Во многих странах эксперименты со стволовыми клетками запрещены вовсе. В других, как в США, вызывают сильное недовольство государства (недавно Джордж Буш пообещал наложить вето на принятый конгрессом закон, который разрешает финансирование исследований в области стволовых клеток). В-третьих, эксперименты ведутся так, что их результаты весьма сомнительны. Тем не менее спрос на «эликсир молодости» огромен. А где есть спрос, появляется и предложение.
Убийственные гормоны
В 1990 году американский исследователь Дэниел Радмен опубликовал в престижном New England Journal of Medicine статью, которая буквально взорвала мир. По его словам, ему удалось прорвать «лимит Хэйфлика». 12 мужчин в возрасте от 61 до 81 года «биологически» помолодели примерно на 20 лет благодаря регулярным инъекциям гормона роста человека (ГРЧ), которые доктор Радмен делал им регулярно в течение полугода. Новость об эксперименте доктора Радмена облетела весь мир. Сотни тысяч людей изъявили желание пройти курс терапии, чтобы стать на десятки лет моложе.
Метод доктора Радмена необыкновенно дорог. Месячный курс инъекций стоит от $800 до $2500 в США, в Европе эта сумма еще выше. Тем не менее десятки тысяч человек начинают свой день с укола, а затем подходят к зеркалу и стараются обнаружить изменения, которые происходят под воздействием гормона. Для менее богатых существует несколько десятков таблеток, которые, по заверениям производителей, служат для того, чтобы заставлять организм самостоятельно выделять ГРЧ. Как выяснили ученые, организм даже пожилых людей продолжает вырабатывать ГРЧ, но железы, которые ответственны за его производство, не выпускают его в организм.
Метод омоложения при помощи ГРЧ эффективен, но до сих пор не разрешен к применению, так что все те, кто им пользуется, действуют на свой страх и риск. Дело в том, что этот метод, как говорят многие врачи, необыкновенно опасен. «ГРЧ стимулирует рост и деление клеток. Это факт. Проблема в том, что гормон не делает никаких различий между клетками»,— говорит один из британских специалистов. Вероятность возникновения необыкновенно быстро протекающего и стопроцентно смертельного рака у людей, принимающих ГРЧ, необыкновенно высока. Наиболее вероятны рак простаты или молочной железы. Среди прочих побочных эффектов — сахарный диабет, задержка жидкости в теле, что может привести к сердечно-сосудистым заболеваниям и гипертонии.
Кроме того, клинические исследования показали, что эффект, который дает ГРЧ у пожилых людей,— сугубо косметический. Пациенты выглядят моложе и здоровее, но в реальности их выносливость и сила не увеличиваются, а кости не становятся крепче. Принимая ГРЧ, говорят многие врачи, люди не продлевают себе жизнь. Просто на собственных похоронах они будут выглядеть необыкновенно молодо.
Бесполезные антиоксиданты
«Каждый вздох приближает нас к могиле». Многим эта фраза британского доктора Кеннета Барта может показаться метафорой, но сам он совершенно уверен в том, что его слова следует понимать в самом прямом смысле. Барт считает, что главная причина старения — окисление клеток организма. Всем известно, что под воздействием окисления рано или поздно разрушится практически любой из окружающих нас предметов. Если представить человеческий организм в качестве грандиозного механизма, которому для эксплуатации необходим кислород, то можно предположить, что окисление органов и клеток, то есть разрушение их свободными радикалами, и есть главная причина старения и смерти.
На этом основана еще одна форма борьбы со старостью — употребление антиоксидантов, которые, собственно, и ведут борьбу со свободными радикалами. У этого направления есть миллионы поклонников, которые ежедневно принимают огромное количество антиоксидантов в таблетках. «Раньше люди принимали одну-две таблетки,— говорит один из американских экспертов.— Теперь же в моде настоящие ‘коктейли’ из пилюль, аналогичные тем, что принимают больные СПИДом». В некоторых случаях, говорят специалисты, доходит до приема нескольких десятков таблеток в день.
Фармацевтические компании с удовольствием удовлетворяют постоянно растущий спрос на антиоксиданты. Тем более что товар этот относительно дешев. Самые распространенные — витамины A, С и Е. Еще одним весьма модным антиоксидантом стал в последнее время коэнзим Q10, который чаще всего рекомендуется использовать вместе с витамином C.
Впрочем, и у этого способа есть недостаток. Один, но весьма серьезный. Разумеется, никто не станет утверждать, что антиоксиданты вредны. Более того, врачи первые скажут, что у большинства антиоксидантов нет серьезных побочных эффектов, если, конечно, не принимать таблетки сотнями. Но мало кто из врачей решится говорить о том, что окисление — единственная или даже главная причина старения организма. А многочисленные клинические испытания свидетельствуют, что антиоксиданты не оказывают влияния на процесс омоложения организма, хотя и могут немного продлить жизнь человека.
Смертельная диета
«Главная причина старения — в переедании,— утверждает американский диетолог Дик Нокс.— Нас убивают калории». С ним согласны многие врачи. По результатам экспериментов, проводившихся в разных странах и с разными подопытными животными, «декалоризация» пищи (при сохранении ее питательной ценности) приводила к более чем 50-процентному росту продолжительности жизни, а заодно и к целому ряду положительных побочных эффектов. Врачи в Америке и Европе называют метод ограничения приема калорий «единственным известным способом ограничения скорости старения организма». Причем чаще всего не особенно задумываются над тем, как это происходит. «Я не буду говорить, как способ CR (caloric restriction — ограничение приема калорий.— ‘Власть’) действует, потому что не знаю точно, от чего стареет организм,— говорит один из британских практикующих врачей.— Я лишь констатирую то, что вижу сам на примере своих пациентов».
Тем не менее врачи не спешат рекомендовать этот способ. В первую очередь из-за того, что, как и в случае с гормоном роста человека, у CR есть и весьма опасные побочные эффекты. Первый — психологический стресс, как, впрочем, и в случае с любой диетой. Кроме того, эксперименты показывают, что людям, решившим ограничить потребление калорий, следует забыть о физкультуре. Исследования с мышами показывают, что физические упражнения вместе с CR укорачивают жизнь. Ограничение приема калорий делает людей менее энергичными, у некоторых наступает тяжелая депрессия. Наконец, CR оказывает негативный эффект на сексуальную жизнь и репродуктивную функцию. «CR безусловно омолаживает, но заметно ухудшает качество жизни. То есть эффект фактически противоположен тому, который требуется»,— говорит один из американских экспертов.
Впрочем, это вполне естественно. Все большее число экспертов приходит к неутешительному выводу о том, что погоня за долголетием и стремление замедлить или повернуть вспять процесс старения организма напоминают погоню за двумя зайцами. «Лекарства от старения нет»,— считает доктор Джей Олшански, профессор медицинского факультета Иллинойского университета, один из самых известных экспертов в области геронтологии и убежденный враг всех, кто ищет пути борьбы со старением. Взгляды доктора Олшански многие считают слишком радикальными, но готовы согласиться с тем, что по крайней мере в настоящее время они справедливы. И так будет до тех пор, пока ученые не смогут дать четкие и однозначные ответы на вопрос, что же такое старение и чем оно вызвано.
ХАКИМ ИБРАГИМОВ
Гормоном роста
Гормоном роста
Гормоном роста (соматотропин, соматропин, соматотропный гормон, HGH, СТГ) — это пептидный гормон, вырабатываемый гипофизом. Количество соматропина в организме достигает максимального уровня в детстве. В молодом возрасте гормон роста в организме отвечает за рост трубчатых костей, мышц и других тканей. С увеличением возраста производство гормона роста постоянно понижается, соответственно снижается и выработка ИФР-1 (инсулиноподобного фактора роста-1), находящегося в прямой зависимости от выработки гормона роста человека. В организме человека ИФР-1 является ответственным за восстановление поврежденных клеток и за выработку новых.
Гормон роста (ГР) — белок, вырабатываемый и секретируемый передней долей гипофиза. Из всех гормонов гипофиза он вырабатывается в наибольшем количестве. Образование и секрецию гормона роста регулирует гипоталамический рилизинг-гормон и соматостатин. Оба этих фактора вырабатываются гипоталамусом. ГР вырабатывается в течение всей жизни. Продукция ГР возрастает в период роста организма, примерно до 20 лет и затем уменьшается с возрастом со средней скоростью 14% в десятилетие.
Функции гормона роста. ГР стимулирует как линейный рост, так и рост внутренних органов. Вызывает увеличение числа и размеров клеток мышц, печени, вилочковой железы, половых желез, надпочечников и щитовидной железы. Оказывает влияние на метаболизм белков, жиров и углеводов. Угнетает активность ферментов, разрушающих аминокислоты, повышает уровень инсулиноподобных факторов роста I и II (ИФР I и II) в сыворотке крови, стимулирует синтез коллагена в костях, коже, других органах и тканях организма. ГР увеличивает выход глюкозы в печеночные вены, усиливает глюконеогенез (образование глюкозы из неуглеводных предшественников), уменьшает поглощение глюкозы на периферии, а также усиливает липолиз (распад жиров), в результате чего в крови повышается концентрация свободных жирных кислот, которые подавляют действие инсулина на мембранный транспорт глюкозы.
Влияние на синтез белка. ГР стимулирует транспорт аминокислот в мышечные клетки и, кроме того, усиливает синтез белка, причем, независимо от влияния на транспорт аминокислот. У людей, получающих ГР, возникает положительный азотный баланс, что отражает общее повышение белкового синтеза и снижение содержания аминокислот и мочевины в плазме и моче. Указанные изменения сопровождаются повышением уровня синтеза РНК и ДНК в отдельных тканях. В этом отношении действие ГР сходно с некоторыми эффектами инсулина.
Влияние на углеводный обмен. В плане влияния на углеводный обмен гормон роста является антагонистом инсулина. Гипергликемия, возникающая после введения ГР, — результат сочетания сниженной периферической утилизации глюкозы и ее повышенной продукции печенью в процессе глюконеогенеза. Действуя на печень, ГР увеличивает содержание в ней гликогена, вероятно, вследствие активации глюконеогенеза из аминокислот. ГР может вызывать нарушение некоторых стадий гликолиза (распад глюкозы в тканях) и тормозить транспорт глюкозы. Торможение распада глюкозы в мышцах может быть также связано с мобилизацией жирных кислот из триацилглицероловых резервов.
Влияние на липидный обмен. Гормон роста оказывает мощное липолитическое действие. Усиливаются процессы липолиза с повышением мобилизации жира из депо, что приводит к быстрому увеличению концентрации свободных жирных кислот в плазме и их окислению в печени. Энергия, образующаяся при повышенном распаде жиров, используется на анаболические процессы в белковом обмене.
Регуляция секреции и синтеза. На секрецию ГР влияет ряд стимулов (сон, стресс), и она, подобно секреции многих гипофизарных гормонов, носит эпизодический и пульсирующий характер. В течение нескольких минут уровень ГР в плазме может измениться в 10 раз. Один из самых больших пиков отмечается вскоре после засыпания, что подтверждает поговорку: «Кто не спит, тот не растет». К другим стимулам относятся стресс (боль, холод, тревога, хирургическое вмешательство), физические упражнения, острая гипогликемия или голодание, белковая пища или аминокислота аргинин. Возможна связь этих и многих других эффекторов с основным физиологическим действием ГР, состоящим в сбережении глюкозы. При стрессе, гипогликемии, во время сна или голодания ГР стимулирует липолиз (поступление жирных кислот) и проникновение в клетки аминокислот (потенциальных субстратов глюконеогенеза), сберегая, таким образом, глюкозу для метаболизма мозга. На высвобождение ГР оказывает влияние множество агентов, в том числе эстрогены, дофамин, альфа-адренергические соединения, серотонин, опиатные полипептиды, гормоны кишечника и глюкагон. Точкой приложения действия всех этих факторов является вентромедиальное ядро гипоталамуса, где осуществляется регуляция секреции гормона роста по типу обратной связи. Короткая петля системы включает положительный (стимулирующий) регулятор секреции — соматолиберин — и отрицательный (тормозящий) регулятор — соматостатин.
Как можно повысить синтез гормона роста.
Если не рассматривать препараты, для выполнения этой задачи лучше всего подходит взрывной стиль тренинга, более высокое количество повторений и более короткие паузы отдыха между подходами.Сбалансированное питание играет важную роль, особенно нужно употреблять богатую белком пищу. Секрецию гормона роста можно увеличить достаточным сном (8-9 часов в сутки), физическими упражнениями (особенно базовыми).Так же вам помогут увеличить гормон роста употребление: глютамина, GABA протеина и аргинина, кроме того доказано, что употребление креатина увеличивает инсулиноподобный фактор роста IGF-1 (который стимулирует рост тканей в организме, и мышечной в том числе).
Гормон роста | Что это за гормон?
04.10.2018
Гормональные нарушения в нашем организме становятся причиной развития огромного числа патологий, пугающих своим разнообразием. Среди гормонов, синтезируемых нашим организмом, важное место занимает соматотропин, или гормон роста, вырабатываемый передней долей гипофиза. Основным назначением соматотропина является стимуляция роста и регенерация клеток мышечной и костной тканей. Огромное значение гормон представляет для спортивной медицины, так как позволяет избавиться от лишнего жира, нарастить мышечную массу и, как следствие, повысить спортивные результаты. Интересным является тот факт, что вырабатывается гормон своеобразными всплесками и самый активный приходится на время ночного сна. Поэтому высказывание о том, что человек растёт во сне, не лишено объективности.
Активное вырабатывание соматотропина приходится на период становления организма в возрасте 15-20 лет. Затем наблюдается период стабильного синтезирования, который продолжается в среднем до тридцатилетнего возраста, в свою очередь сменяющийся периодом снижения выработки. Возрастные изменения в нашем организме приводят к тому, что в шестьдесят лет организм испытывает значительный дефицит соматотропина. В этом возрасте вырабатывается меньше половины от необходимой нормы соматотропина. В преклонном возрасте дефицит только увеличивается, что негативным образом сказывается при переломах, разрыве связок и работе суставов у пожилых людей.
Как мы уже говорили, соматотропин оказывает огромное влияние на рост и структурное строение нашего организма, потому зачастую его именуют гормоном роста. Среди свойств соматотропина необходимо выделить ускорение роста человека в подростковом возрасте, увеличение мышечной массы, уменьшение жировой прослойки, регулирование процессов углеводного обмена в нашем организме; является естественным иммуностимулятором, оказывает модулирующее воздействие на центральную нервную систему человека.
Знаете, почему не рекомендуют наедаться на ночь? Потому что после еды идёт активная вырабатывание инсулина, который блокирует синтезирование соматотропина. А так как до 85 процентов дневной нормы гормона роста вырабатывается в период фазы глубокого сна, это негативным образом сказывается на обмене веществ и, как следствие, увеличивается жировая прослойка и наблюдаются дегенеративные изменения в мышечных тканях. В качестве совета, желающим похудеть, рекомендуется прекратить приём пищи как минимум за несколько часов до сна, а с утра завтракать не сразу после пробуждения, а спустя полтора-два часа, так как в первые часы после пробуждения идёт активное жиросжигание за счёт ночной выработки соматотропина.
Выработке гормона роста способствует ряд аминокислот, среди которых следует выделить орнитин, глутамин, аргинин, лизин. В свою очередь дефицит гормона вызывают повышенное содержание в крови свободных жирных кислот, повышение концентрации инсулина, гипергликемия, повышенное содержание гормонов коры надпочечников, соматостатин. Стоит отметить, что чрезмерное синтезирование гормона роста приводит к акромегалии и гигантизму, развитию туннельного синдрома, развитию инсулиноустойчивости тканей. Инсулиноустойчивость тканей не позволяет глюкозе в должном объёме проникнуть из крови в их клетки. В свою очередь, это приводит к высокой концентрации глюкозы в крови и, как следствие, к ожирению, гипертонии, отёчности. В качестве наиболее страшных последствий высокой инсулиноустойчивости тканей необходимо выделить развитие сахарного диабета, атеросклероза, повышенную вероятность развития злокачественных опухолей, тромбофлебит и сердечный приступ.
В связи с вышеизложенным, хочется предостеречь неопытных любителей огромных мышц и высоких спортивных результатов о высоком риске негативных последствий неразумного применения стероидов гормонального типа. Безусловно, не только избыток, но и дефицит соматотропина в организме несёт негативные последствия. Недостаток гормона в детском возрасте влияет на задержку в развитие органов и систем человека и проявляется аномально низким ростом. В медицине это называется гипофизарный нанизм. Зачастую данная аномалия сопровождается задержкой не только физического, но и процессами торможения умственного развития и полового созревания. Интересно и то, что дефицит соматотропина, как и его избыток, провоцирует ожирение и развитие атеросклероза. Вот уж поистине, все хорошо в меру.
Обращайтесь за консультацией к врачу-эндокринологу!
Навигация по записям
Нормальная физиология гормона роста у взрослых — Endotext
GH — это одноцепочечный белок с 191 аминокислотой и двумя дисульфидными связями. Ген человеческого GH расположен на хромосоме 17q22 как часть локуса, состоящего из пяти генов. В дополнение к двум генам, связанным с GH (Gh2, который кодирует основной гормон роста взрослого человека, продуцируемый в соматотрофных клетках, обнаруженных в передней доле гипофиза и, в меньшей степени, в лимфоцитах, и Gh3, который кодирует плацентарный GH), существуют три гена, кодирующие гены хорионического соматомаммотропина (CSh2, CSh3 и CSHL) (также известного как плацентарный лактоген) (2,3).Ген Gh2 кодирует две различные изоформы GH (22 кДа и 20 кДа). Основной и наиболее распространенной формой GH в гипофизе и крови является мономерная изоформа 22K-GH, представляющая также рекомбинантный GH, доступный для терапевтического использования (а затем и для допинговых целей) (3). Введение рекомбинантного 22K-GH экзогенно приводит к снижению изоформы 20K-GH, и, таким образом, тестирование обеих изоформ используется для выявления допинга GH в спорте (4).
Как уже упоминалось, GH секретируется соматотрофными клетками, расположенными в основном в боковых крыльях передней доли гипофиза.Недавнее исследование секвенирования одноклеточной РНК, проведенное на мышах, показало, что GH-экспрессирующие клетки, представляющие соматотрофов, представляют собой наиболее многочисленную клеточную популяцию во взрослом гипофизе (5). Дифференцировка соматотрофных клеток регулируется фактором транскрипции гипофиза 1 (Pit-1). Данные на мышах предполагают, что гипофиз обладает регенеративной способностью, а клетки, продуцирующие GH, регенерируются из стволовых клеток гипофиза у молодых животных через 5 месяцев (6).
Физиологическая регуляция секреции GH
Морфологические характеристики и количество соматотрофов удивительно постоянны на протяжении всей жизни, в то время как характер их секреции изменяется.Секреция GH происходит пульсирующе и в циркадном ритме с максимальным высвобождением во второй половине ночи. Итак, сон — важный физиологический фактор, увеличивающий выброс гормона роста. Интересно, что максимальные уровни GH происходят в течение нескольких минут после начала медленного сна, и наблюдается заметный половой диморфизм ночного увеличения GH у людей, составляющий лишь часть от общего суточного высвобождения GH у женщин, но большая часть его вырабатывается у женщин. мужчины (7).
Секреция GH также зависит от пола, пубертатного статуса и возраста (и) (8).Интегрированная 24-часовая концентрация гормона роста значительно выше у женщин, чем у мужчин, и больше у молодых, чем у пожилых людей. Концентрация свободного эстрадиола в сыворотке, но не свободного тестостерона, коррелирует с GH, и при корректировке эффектов эстрадиола ни пол, ни возраст не влияют на концентрацию GH. Это говорит о том, что эстрогены играют решающую роль в модулировании секреции GH (8). Во время полового созревания происходит 3-кратное увеличение пульсирующей секреции GH, достигающее пика примерно в возрасте 15 лет у девочек и на 1 год позже у мальчиков (9).
Рисунок 1
Секреторный паттерн GH у молодых и старых женщин и мужчин. У молодых людей импульсы GH более крупные и частые, и женщины выделяют больше GH, чем мужчины (изменено из (8)).
Синтез и секреция GH гипофизом стимулируются эпизодическими гипоталамическими гормонами. Гормон высвобождения гормона роста (GHRH) стимулирует, в то время как соматостатин (SST) ингибирует производство и высвобождение GH. GH стимулирует выработку IGF-I, который, в свою очередь, подавляет секрецию GH как на гипоталамическом, так и на гипофизарном уровнях.Пептид желудочного сока грелин также является мощным стимулятором секреции GH, который усиливает секрецию GHRH в гипоталамусе и действует синергетически с его стимулирующими GH эффектами гипофиза (10). Интересно, что недавно было показано, что дупликация GPR101 в зародышевой линии или соматическая дупликация постоянно активирует путь цАМФ в отсутствие лиганда, что приводит к высвобождению GH. Хотя точная физиология GPR101 неясна, стоит упомянуть о нем, поскольку он явно влияет на патофизиологию GH (11).
Кроме того, на ось GH может влиять множество других факторов, наиболее вероятно из-за взаимодействия с GRHR, соматостатином и грелином.Эстрогены стимулируют секрецию GH, но ингибируют действие GH на печень, подавляя передачу сигналов рецептора GH (GHR). Напротив, андрогены усиливают периферическое действие GH (12). Экзогенные эстрогены усиливают ответы гипофизарного GH на субмаксимальные эффективные импульсы экзогенного GHRH (13) и подавляют подавление экзогенным SST (14). Также экзогенный эстроген усиливает действие грелина (15).
Высвобождение
GH обратно коррелирует с внутрибрюшным висцеральным ожирением через механизмы, которые могут зависеть от увеличения потока свободных жирных кислот (FFA), повышенного уровня инсулина или свободного IGF-I.
Рисунок 2.
Факторы, которые стимулируют и подавляют секрецию GH в физиологических условиях.
ГОРМОН, ВЫПУСКАЮЩИЙ ГОРМОН РОСТА
GHRH представляет собой полипептид из 44 аминокислот, продуцируемый в дугообразном ядре гипоталамуса. Эти нервные окончания секретируют GHRH, чтобы достичь соматотрофов передней доли гипофиза через систему воротной вены, что приводит к транскрипции и секреции GH. Более того, исследования на животных показали, что GHRH играет жизненно важную роль в пролиферации соматотрофов в передней доле гипофиза, тогда как отсутствие GHRH приводит к гипоплазии передней доли гипофиза (16).Кроме того, GHRH регулирует экспрессию гена GH и стимулирует высвобождение GH (17). Секреция GHRH стимулируется несколькими факторами, включая деполяризацию, α2-адренергическую стимуляцию, гипофизэктомию, тиреоидэктомию и гипогликемию, и подавляется SST, IGF-I и активацией ГАМКергических нейронов.
GHRH действует на соматотрофов через семь трансмембранных G-белков, связанных с стимулирующими рецепторами на поверхности клетки. Этот рецептор широко изучался в течение последнего десятилетия, что привело к идентификации нескольких важных мутаций.Точечные мутации в рецепторах GHRH, как показали исследования, проведенные на карликовых мышах lit / lit , показали глубокое влияние на последующую пролиферацию соматотрофов, приводящую к гипоплазии передней доли гипофиза (18). В отличие от мутаций в генах Pit-1 и PROP-1, которые приводят к множественному дефициту гормонов гипофиза и гипоплазии передней доли гипофиза, мутации рецептора GHRH приводят к глубокому дефициту GH с гипоплазией передней доли гипофиза. Вслед за первой мутацией рецептора GHRH, описанной в 1996 г. (19), за последнее десятилетие был обнаружен ряд семейных мутаций рецептора GHRH.Эти мутации составляют почти 10% семейных изолированных дефицитов GH. Пораженный человек будет иметь низкий рост и гипоплазию передней доли гипофиза. Однако у них отсутствуют некоторые типичные признаки дефицита GH, такие как гипоплазия средней зоны лица, микрофаллос и неонатальная гипогликемия (20).
СОМАТОСТАТИН (SST)
SST — это циклический пептид, кодируемый одним геном у человека, который в основном оказывает ингибирующее действие на эндокринные и экзокринные секреции. Многие клетки в организме, включая специализированные клетки в переднем паравентрикулярном ядре и дугообразном ядре, производят SST.Эти нейроны секретируют SST в систему воротной вены аденогипофиза через срединное возвышение, чтобы оказывать влияние на переднюю долю гипофиза. SST имеет короткий период полураспада, составляющий примерно 2 минуты, так как у человека он быстро инактивируется тканевой пептидазой.
SST действует через семь трансмембранных рецепторов, связанных с G-белком, и к настоящему времени у человека идентифицировано пять подтипов рецептора (SSTR1-5). Хотя все пять подтипов рецепторов экспрессируются в гипофизе плода человека, гипофиз взрослого человека экспрессирует только 4 подтипа (SSTR1, SSTR2, SSTR3, SSTR5).Из этих четырех подтипов соматотрофы проявляют большую чувствительность к лигандам SSTR2 и SSTR5 в синергетическом ингибировании секреции GH (21). Соматостатин подавляет высвобождение GH, но не синтез GH.
GHRELIN
Грелин представляет собой пептид из 28 аминокислот, который является естественным лигандом рецептора, стимулирующего секрецию GH. Фактически, грелин и GHRH обладают синергетическим эффектом в повышении уровня циркулирующего GH (7). Грелин в основном секретируется желудком и может участвовать в реакции гормона роста на голодание и прием пищи.
Клинические последствия
Уровни GH — влияние состава тела, физической формы и возраста
С введением надежных радиоиммунологических тестов было признано, что циркуляция GH у тучных субъектов притупляется, а нормальное старение сопровождается постепенным снижением в уровнях GH (22,23). Была выдвинута гипотеза, что многие из стареющих изменений в составе тела и функциях органов связаны или вызваны снижением GH (24), также известным как «соматопауза».
Исследования, проведенные в конце 90-х годов, однозначно подтвердили, что взрослые с тяжелым дефицитом GH характеризуются повышенной жировой массой и сниженной мышечной массой (LBM) (25). Также известно, что нормальный уровень GH может быть восстановлен у лиц с ожирением после значительной потери веса (26), и что замещение GH у взрослых с дефицитом GH нормализует состав тела. Что остается неизвестным, так это причинно-следственная связь между снижением уровня GH и старческими изменениями в составе тела.Является ли склонность к набору жира и потере мышечной массы инициированной или предшествующей первичным возрастным снижением секреции и действия GH? В качестве альтернативы, накопление жировой массы вторично по отношению к факторам, не зависящим от гормона роста (например, образу жизни, диетическим привычкам), приводит к подавлению секреции гормона роста с обратной связью. Более того, мало что известно о возможных возрастных изменениях фармакокинетики и биоактивности GH.
Поперечные исследования, проведенные для оценки связи между составом тела и стимулированным высвобождением GH у здоровых субъектов, показывают, что у взрослых людей (средний возраст 50 лет) пиковый ответ GH на стимуляторы секреции (клонидин и аргинин) ниже, а у женщин — выше. реакция на аргинин по сравнению с мужчинами.Однако множественный регрессионный анализ показывает, что масса внутрибрюшного жира является наиболее важным и отрицательным предиктором пиковых уровней GH, как упоминалось ранее (27). В той же популяции 24-часовые спонтанные уровни GH также преимущественно обратно коррелировали с массой внутрибрюшного жира () (28).
Рисунок 3.
Корреляция между массой внутрибрюшного жира и 24-часовой секрецией GH.
Насколько нам известно, подробный анализ секреции GH в зависимости от состава тела у пожилых людей не проводился.Вместо этого сывороточный IGF-I использовался в качестве суррогата или заместителя для статуса GH в нескольких исследованиях с участием пожилых мужчин (29–31). Эти исследования охватывают большие группы амбулаторных мужчин в возрасте от 50 до 90 лет, проживающих в общинах. Как и ожидалось, сывороточный IGF-I снижался с возрастом (), но IGF-I не показал какой-либо значительной связи с составом тела или физической работоспособностью.
Рисунок 4.
Изменения сывороточного IGF-I с возрастом; модифицировано из (32).
Действие GH: Влияние возраста, пола и состава тела
Учитывая большой интерес к действию GH у взрослых, на удивление мало исследований посвящено возможным возрастным различиям в реакции или чувствительности к GH.У нормальных взрослых снижение уровня GH сопровождается снижением сывороточного IGF-I, что свидетельствует о понижающей регуляции оси GH-IGF-I. Введение GH пожилым здоровым взрослым обычно было связано с предсказуемым, хотя и умеренным, влиянием на состав тела и побочными эффектами с точки зрения задержки жидкости и умеренной инсулинорезистентности (33). Неясно, отражает ли это неблагоприятный баланс между эффектами и побочными эффектами у пожилых людей или использование чрезмерных доз GH, но очевидно, что пожилые люди не устойчивы к GH.Краткосрочные исследования зависимости реакции от дозы ясно демонстрируют, что пожилым пациентам требуется более низкая доза гормона роста для поддержания заданного уровня IGF-I в сыворотке (34,35), и было замечено, что уровень IGF-I в сыворотке увеличивается у отдельных пациентов при длительном лечении. терапии, если доза GH остается постоянной. Более того, пациенты с дефицитом гормона роста старше 60 лет очень чувствительны даже к небольшой дозе гормона роста (36). Интересно, что существует гендерная разница в ответе на лечение GH: мужчины более отзывчивы с точки зрения генерации IGF-I и потери жира во время терапии, скорее всего, из-за более низких уровней эстрогена, которые негативно влияют на эффект GH на генерацию IGF-I в печени. (37).
Фармакокинетика и краткосрочные метаболические эффекты почти физиологического внутривенного болюса ГР (200 мкг) сравнивались в группе молодых (30 лет) и старше (50 лет) здоровых взрослых (38). Площадь под кривой GH была значительно ниже у пожилых людей, тогда как период полувыведения был аналогичным в двух группах, что свидетельствует как об увеличенной скорости метаболического клиренса, так и очевидном объеме распределения GH у пожилых людей. Оба параметра показали сильную положительную корреляцию с жировой массой, хотя множественный регрессионный анализ показал, что возраст является независимым положительным предиктором.Краткосрочный липолитический ответ на болюс GH был выше у молодых людей по сравнению с пожилыми людьми. Интересно, что то же исследование показало, что белки, связывающие GH, сильно и положительно коррелируют с массой брюшного жира (39).
Проспективное долгосрочное исследование здоровых взрослых с последовательными сопутствующими оценками статуса GH и ожирения предоставило бы полезную информацию о причинно-следственной связи между статусом GH и составом тела в зависимости от возраста. Между тем предлагается следующая гипотеза (): 1.Изменения в образе жизни и генетическая предрасположенность способствуют накоплению жира с возрастом; 2. Увеличенная жировая масса приводит к увеличению доступности свободных жирных кислот и вызывает инсулинорезистентность и гиперинсулинемию; 3. Высокие уровни инсулина подавляют IGF-связывающий белок (IGFBP) -1, что приводит к относительному увеличению уровней свободного IGF-I; 4. Системное повышение уровня FFA, инсулина и свободного IGF-I подавляет высвобождение GH гипофизом, что дополнительно увеличивает жировую массу; 5. Эндогенный гормон роста выводится быстрее у субъектов с большим количеством жировой ткани.
В настоящее время неоправданно лечить возрастное ухудшение состава тела и физической работоспособности с помощью GH, особенно из-за опасений, что последующее повышение уровня IGF-I может увеличить риск развития опухолевых заболеваний (для обширного обсуждение гормона роста у пожилых людей см. в главе по этой теме в разделе «Эндокринология старения» Эндотекста).
Рис. 5.
Гипотетическая модель связи между низким уровнем GH и повышенным уровнем висцерального жира у взрослых.
Пожизненный дефицит GH
Реальная модель эффектов GH в физиологии человека представлена пациентами с пожизненным серьезным снижением передачи сигналов GH из-за мутаций рецепторов GHRH или GHRH, комбинированного дефицита GH, пролактина и ТТГ , или глобальное удаление GHR. Они демонстрируют низкий рост, кукольное лицо, высокие голоса и центральное ожирение, а также плодовиты (40). Несмотря на центральное ожирение и повышенное содержание жира в печени, они чувствительны к инсулину, частично защищены от рака и значительно снижают передачу сигналов о старении и, возможно, увеличивают продолжительность жизни (41).Снижение риска рака при пожизненном дефиците GH вместе с сообщениями о разрешающей роли GH в росте неопластической толстой кишки (42), предопухолевых поражениях молочной железы (43) и прогрессировании рака простаты (44) требует, по крайней мере, тщательный подбор доз замещения GH у пациентов с дефицитом GH.
GH и иммунная система
Хотя большинство данных о связи между GH и иммунной системой получены из исследований на животных, кажется, что GH может обладать иммуномодулирующим действием.Иммунные клетки, включая несколько субпопуляций лимфоцитов, экспрессируют рецепторы GH и отвечают на его стимуляцию (45). GH стимулирует in vitro, T и B-пролиферацию клеток и синтез иммуноглобулинов, усиливает созревание человеческих миелоидных клеток-предшественников и модулирует in vivo, Th2 / Th3 (8) и гуморальные иммунные ответы (46). Было показано, что GH может индуцировать продукцию de novo Т-клеток и увеличивать восстановление CD4 у ВИЧ-положительных пациентов. Другое исследование, имеющее возможное клиническое значение, показало, что устойчивая экспрессия GH снижает симптомы продромального заболевания и устраняет прогрессирование до явного диабета на мышиной модели диабета 1 типа, аутоиммунного заболевания, опосредованного Т-клетками.GH изменял цитокиновую среду, запускал поляризацию противовоспалительных макрофагов (M2), поддерживал активность супрессорной популяции Т-клеток и ограничивал пластичность клеток Th27 (46). Хорошо известно, что передача сигналов JAK / STAT, основного медиатора активации GHR, участвует в модуляции иммунной системы, поэтому есть соблазн предположить, что GH также может играть роль, но необходимы четкие данные о людях.
Передача сигналов гормона роста у людей
Активация рецептора гормона роста (GHR)
Передача сигналов GHR — отдельная и плодотворная область исследований сама по себе (47), поэтому в этом разделе основное внимание будет уделено недавним данным, полученным на моделях человека.
GHR были идентифицированы во многих тканях, включая жир, лимфоциты, печень, мышцы, сердце, почки, мозг и поджелудочную железу (48,49). Активация ассоциированной с рецептором киназы Janus (JAK) -2 является критическим шагом в инициировании передачи сигналов GH. Одна молекула GH связывается с двумя молекулами GHR, которые существуют в виде предварительно сформированных гомодимеров. После связывания GH внутриклеточные домены димера GHR подвергаются вращению, которое объединяет два внутриклеточных домена, каждый из которых связывает одну молекулу JAK2. Это, в свою очередь, вызывает перекрестное фосфорилирование остатков тирозина в киназном домене каждой молекулы JAK2 с последующим фосфорилированием тирозина GHR (48,50).Фосфорилированные остатки на GHR и JAK2 образуют сайты стыковки для различных сигнальных молекул, включая сигнальные преобразователи и активаторы транскрипции (STAT) 1, 3, 5a и 5b. STAT, связанные с активированным комплексом GHR-JAK2, впоследствии фосфорилируются по одному тирозину с помощью JAK2, обеспечивая димеризацию и транслокацию в ядро, где они связываются с ДНК и активируют транскрипцию гена. Сайт связывания STAT5b охарактеризован в промоторной области гена IGF-I (51). Ослабление JAK2-ассоциированной передачи сигналов GH опосредуется семейством цитокин-индуцируемых супрессоров передачи сигналов цитокинов (SOCS) (52).Белки SOCS связываются с остатками фосфотирозина на GHR или JAK2 и подавляют передачу сигналов GH, ингибируя активность JAK2 и конкурируя со STAT. Например, сообщалось, что ингибирующее действие эстрогена на продукцию IGF-I в печени, по-видимому, опосредовано повышающей регуляцией SOCS-2 (53).
Данные о передаче сигналов GHR получены в основном на моделях грызунов и экспериментальных клеточных линиях, хотя GH-индуцированная активация путей JAK2 / STAT5b и митоген-активируемой протеинкиназы (MAPK) была зарегистрирована в культивируемых человеческих фибробластах от здоровых людей (54) .STAT5b у людей имеет решающее значение для GH-индуцированной экспрессии IGF-I и стимуляции роста, что продемонстрировано идентификацией мутаций в гене STAT5b у пациентов с тяжелой нечувствительностью к GH в присутствии нормального GHR (55). Сообщалось об активации передачи сигналов GHR in vivo у здоровых молодых мужчин, подвергшихся внутривенному болюсу GH по сравнению с физиологическим раствором (56). Значительное фосфорилирование тирозина STAT5b было зарегистрировано после воздействия GH через 30-60 минут в биоптатах мышц и жира, но не было никаких доказательств GH-индуцированной активации PI 3-киназы, Akt / PKB или MAPK (56).
GH и передача сигналов инсулина
GH нарушает механизм инсулина, но точные механизмы у людей все еще остаются предметом споров. Нет данных о негативном влиянии GH на связывание инсулина с рецептором (57,58), что, очевидно, подразумевает пострецепторные метаболические эффекты.
Имеются данные на животных и in vitro , позволяющие предположить, что инсулин и GH имеют общие пострецепторные сигнальные пути (59). Сообщалось о конвергенции на уровнях STAT5 и SOCS3 (60), а также об основных путях передачи сигналов инсулина: субстратах рецепторов инсулина (IRS) 1 и 2, PI 3-киназе (PI3K), Akt и внеклеточных регулируемых киназах (ERK). ) 1 и 2 (61-63).Исследования на моделях грызунов предполагают, что инсулино-антагонистические эффекты GH в жировой ткани включают подавление инсулино-стимулированной активности PI3-киназы (59,64). В 2001 году было продемонстрировано, что GH индуцирует клеточную инсулинорезистентность, разъединяя PI3K и его нисходящие сигналы в адипоцитах 3T3-L1 (65)]. Последующее исследование показало, что GH увеличивает экспрессию p85α и снижает активность PI3K в жировой ткани мышей, что подтверждает предыдущее сообщение о прямом ингибирующем эффекте GH на активность PI3K (64).Однако исследование, проведенное на здоровых скелетных мышцах человека, как и ожидалось, показало, что инфузия GH вызывает устойчивое повышение уровней FFA и, следовательно, резистентность к инсулину, по оценке с помощью метода эугликемического зажима, но не было связано с каким-либо изменением инсулинорезистентности. стимулировал повышение активности IRS-1 / PI3K или PKB / Akt (66). Впоследствии было показано, что инсулин не влияет на GH-индуцированную активацию STAT5b или экспрессию мРНК SOCS3 (67).
Поскольку GH и инсулин имеют некоторые общие внутриклеточные субстраты, возникла гипотеза, согласно которой конкуренция за внутриклеточные субстраты объясняет негативное влияние GH на передачу сигналов инсулина (59).Кроме того, исследования показали, что белки SOCS негативно регулируют сигнальный путь инсулина (68). Следовательно, еще один возможный механизм, с помощью которого GH изменяет действие инсулина, — это увеличение экспрессии генов SOCS.
Нормальная физиология гормона роста у взрослых — Endotext
GH представляет собой одноцепочечный белок с 191 аминокислотой и двумя дисульфидными связями. Ген человеческого GH расположен на хромосоме 17q22 как часть локуса, состоящего из пяти генов. В дополнение к двум генам, связанным с GH (Gh2, который кодирует основной гормон роста взрослого человека, продуцируемый в соматотрофных клетках, обнаруженных в передней доле гипофиза и, в меньшей степени, в лимфоцитах, и Gh3, который кодирует плацентарный GH), существуют три гена, кодирующие гены хорионического соматомаммотропина (CSh2, CSh3 и CSHL) (также известного как плацентарный лактоген) (2,3).Ген Gh2 кодирует две различные изоформы GH (22 кДа и 20 кДа). Основной и наиболее распространенной формой GH в гипофизе и крови является мономерная изоформа 22K-GH, представляющая также рекомбинантный GH, доступный для терапевтического использования (а затем и для допинговых целей) (3). Введение рекомбинантного 22K-GH экзогенно приводит к снижению изоформы 20K-GH, и, таким образом, тестирование обеих изоформ используется для выявления допинга GH в спорте (4).
Как уже упоминалось, GH секретируется соматотрофными клетками, расположенными в основном в боковых крыльях передней доли гипофиза.Недавнее исследование секвенирования одноклеточной РНК, проведенное на мышах, показало, что GH-экспрессирующие клетки, представляющие соматотрофов, представляют собой наиболее многочисленную клеточную популяцию во взрослом гипофизе (5). Дифференцировка соматотрофных клеток регулируется фактором транскрипции гипофиза 1 (Pit-1). Данные на мышах предполагают, что гипофиз обладает регенеративной способностью, а клетки, продуцирующие GH, регенерируются из стволовых клеток гипофиза у молодых животных через 5 месяцев (6).
Физиологическая регуляция секреции GH
Морфологические характеристики и количество соматотрофов удивительно постоянны на протяжении всей жизни, в то время как характер их секреции изменяется.Секреция GH происходит пульсирующе и в циркадном ритме с максимальным высвобождением во второй половине ночи. Итак, сон — важный физиологический фактор, увеличивающий выброс гормона роста. Интересно, что максимальные уровни GH происходят в течение нескольких минут после начала медленного сна, и наблюдается заметный половой диморфизм ночного увеличения GH у людей, составляющий лишь часть от общего суточного высвобождения GH у женщин, но большая часть его вырабатывается у женщин. мужчины (7).
Секреция GH также зависит от пола, пубертатного статуса и возраста (и) (8).Интегрированная 24-часовая концентрация гормона роста значительно выше у женщин, чем у мужчин, и больше у молодых, чем у пожилых людей. Концентрация свободного эстрадиола в сыворотке, но не свободного тестостерона, коррелирует с GH, и при корректировке эффектов эстрадиола ни пол, ни возраст не влияют на концентрацию GH. Это говорит о том, что эстрогены играют решающую роль в модулировании секреции GH (8). Во время полового созревания происходит 3-кратное увеличение пульсирующей секреции GH, достигающее пика примерно в возрасте 15 лет у девочек и на 1 год позже у мальчиков (9).
Рисунок 1
Секреторный паттерн GH у молодых и старых женщин и мужчин. У молодых людей импульсы GH более крупные и частые, и женщины выделяют больше GH, чем мужчины (изменено из (8)).
Синтез и секреция GH гипофизом стимулируются эпизодическими гипоталамическими гормонами. Гормон высвобождения гормона роста (GHRH) стимулирует, в то время как соматостатин (SST) ингибирует производство и высвобождение GH. GH стимулирует выработку IGF-I, который, в свою очередь, подавляет секрецию GH как на гипоталамическом, так и на гипофизарном уровнях.Пептид желудочного сока грелин также является мощным стимулятором секреции GH, который усиливает секрецию GHRH в гипоталамусе и действует синергетически с его стимулирующими GH эффектами гипофиза (10). Интересно, что недавно было показано, что дупликация GPR101 в зародышевой линии или соматическая дупликация постоянно активирует путь цАМФ в отсутствие лиганда, что приводит к высвобождению GH. Хотя точная физиология GPR101 неясна, стоит упомянуть о нем, поскольку он явно влияет на патофизиологию GH (11).
Кроме того, на ось GH может влиять множество других факторов, наиболее вероятно из-за взаимодействия с GRHR, соматостатином и грелином.Эстрогены стимулируют секрецию GH, но ингибируют действие GH на печень, подавляя передачу сигналов рецептора GH (GHR). Напротив, андрогены усиливают периферическое действие GH (12). Экзогенные эстрогены усиливают ответы гипофизарного GH на субмаксимальные эффективные импульсы экзогенного GHRH (13) и подавляют подавление экзогенным SST (14). Также экзогенный эстроген усиливает действие грелина (15).
Высвобождение
GH обратно коррелирует с внутрибрюшным висцеральным ожирением через механизмы, которые могут зависеть от увеличения потока свободных жирных кислот (FFA), повышенного уровня инсулина или свободного IGF-I.
Рисунок 2.
Факторы, которые стимулируют и подавляют секрецию GH в физиологических условиях.
ГОРМОН, ВЫПУСКАЮЩИЙ ГОРМОН РОСТА
GHRH представляет собой полипептид из 44 аминокислот, продуцируемый в дугообразном ядре гипоталамуса. Эти нервные окончания секретируют GHRH, чтобы достичь соматотрофов передней доли гипофиза через систему воротной вены, что приводит к транскрипции и секреции GH. Более того, исследования на животных показали, что GHRH играет жизненно важную роль в пролиферации соматотрофов в передней доле гипофиза, тогда как отсутствие GHRH приводит к гипоплазии передней доли гипофиза (16).Кроме того, GHRH регулирует экспрессию гена GH и стимулирует высвобождение GH (17). Секреция GHRH стимулируется несколькими факторами, включая деполяризацию, α2-адренергическую стимуляцию, гипофизэктомию, тиреоидэктомию и гипогликемию, и подавляется SST, IGF-I и активацией ГАМКергических нейронов.
GHRH действует на соматотрофов через семь трансмембранных G-белков, связанных с стимулирующими рецепторами на поверхности клетки. Этот рецептор широко изучался в течение последнего десятилетия, что привело к идентификации нескольких важных мутаций.Точечные мутации в рецепторах GHRH, как показали исследования, проведенные на карликовых мышах lit / lit , показали глубокое влияние на последующую пролиферацию соматотрофов, приводящую к гипоплазии передней доли гипофиза (18). В отличие от мутаций в генах Pit-1 и PROP-1, которые приводят к множественному дефициту гормонов гипофиза и гипоплазии передней доли гипофиза, мутации рецептора GHRH приводят к глубокому дефициту GH с гипоплазией передней доли гипофиза. Вслед за первой мутацией рецептора GHRH, описанной в 1996 г. (19), за последнее десятилетие был обнаружен ряд семейных мутаций рецептора GHRH.Эти мутации составляют почти 10% семейных изолированных дефицитов GH. Пораженный человек будет иметь низкий рост и гипоплазию передней доли гипофиза. Однако у них отсутствуют некоторые типичные признаки дефицита GH, такие как гипоплазия средней зоны лица, микрофаллос и неонатальная гипогликемия (20).
СОМАТОСТАТИН (SST)
SST — это циклический пептид, кодируемый одним геном у человека, который в основном оказывает ингибирующее действие на эндокринные и экзокринные секреции. Многие клетки в организме, включая специализированные клетки в переднем паравентрикулярном ядре и дугообразном ядре, производят SST.Эти нейроны секретируют SST в систему воротной вены аденогипофиза через срединное возвышение, чтобы оказывать влияние на переднюю долю гипофиза. SST имеет короткий период полураспада, составляющий примерно 2 минуты, так как у человека он быстро инактивируется тканевой пептидазой.
SST действует через семь трансмембранных рецепторов, связанных с G-белком, и к настоящему времени у человека идентифицировано пять подтипов рецептора (SSTR1-5). Хотя все пять подтипов рецепторов экспрессируются в гипофизе плода человека, гипофиз взрослого человека экспрессирует только 4 подтипа (SSTR1, SSTR2, SSTR3, SSTR5).Из этих четырех подтипов соматотрофы проявляют большую чувствительность к лигандам SSTR2 и SSTR5 в синергетическом ингибировании секреции GH (21). Соматостатин подавляет высвобождение GH, но не синтез GH.
GHRELIN
Грелин представляет собой пептид из 28 аминокислот, который является естественным лигандом рецептора, стимулирующего секрецию GH. Фактически, грелин и GHRH обладают синергетическим эффектом в повышении уровня циркулирующего GH (7). Грелин в основном секретируется желудком и может участвовать в реакции гормона роста на голодание и прием пищи.
Клинические последствия
Уровни GH — влияние состава тела, физической формы и возраста
С введением надежных радиоиммунологических тестов было признано, что циркуляция GH у тучных субъектов притупляется, а нормальное старение сопровождается постепенным снижением в уровнях GH (22,23). Была выдвинута гипотеза, что многие из стареющих изменений в составе тела и функциях органов связаны или вызваны снижением GH (24), также известным как «соматопауза».
Исследования, проведенные в конце 90-х годов, однозначно подтвердили, что взрослые с тяжелым дефицитом GH характеризуются повышенной жировой массой и сниженной мышечной массой (LBM) (25). Также известно, что нормальный уровень GH может быть восстановлен у лиц с ожирением после значительной потери веса (26), и что замещение GH у взрослых с дефицитом GH нормализует состав тела. Что остается неизвестным, так это причинно-следственная связь между снижением уровня GH и старческими изменениями в составе тела.Является ли склонность к набору жира и потере мышечной массы инициированной или предшествующей первичным возрастным снижением секреции и действия GH? В качестве альтернативы, накопление жировой массы вторично по отношению к факторам, не зависящим от гормона роста (например, образу жизни, диетическим привычкам), приводит к подавлению секреции гормона роста с обратной связью. Более того, мало что известно о возможных возрастных изменениях фармакокинетики и биоактивности GH.
Поперечные исследования, проведенные для оценки связи между составом тела и стимулированным высвобождением GH у здоровых субъектов, показывают, что у взрослых людей (средний возраст 50 лет) пиковый ответ GH на стимуляторы секреции (клонидин и аргинин) ниже, а у женщин — выше. реакция на аргинин по сравнению с мужчинами.Однако множественный регрессионный анализ показывает, что масса внутрибрюшного жира является наиболее важным и отрицательным предиктором пиковых уровней GH, как упоминалось ранее (27). В той же популяции 24-часовые спонтанные уровни GH также преимущественно обратно коррелировали с массой внутрибрюшного жира () (28).
Рисунок 3.
Корреляция между массой внутрибрюшного жира и 24-часовой секрецией GH.
Насколько нам известно, подробный анализ секреции GH в зависимости от состава тела у пожилых людей не проводился.Вместо этого сывороточный IGF-I использовался в качестве суррогата или заместителя для статуса GH в нескольких исследованиях с участием пожилых мужчин (29–31). Эти исследования охватывают большие группы амбулаторных мужчин в возрасте от 50 до 90 лет, проживающих в общинах. Как и ожидалось, сывороточный IGF-I снижался с возрастом (), но IGF-I не показал какой-либо значительной связи с составом тела или физической работоспособностью.
Рисунок 4.
Изменения сывороточного IGF-I с возрастом; модифицировано из (32).
Действие GH: Влияние возраста, пола и состава тела
Учитывая большой интерес к действию GH у взрослых, на удивление мало исследований посвящено возможным возрастным различиям в реакции или чувствительности к GH.У нормальных взрослых снижение уровня GH сопровождается снижением сывороточного IGF-I, что свидетельствует о понижающей регуляции оси GH-IGF-I. Введение GH пожилым здоровым взрослым обычно было связано с предсказуемым, хотя и умеренным, влиянием на состав тела и побочными эффектами с точки зрения задержки жидкости и умеренной инсулинорезистентности (33). Неясно, отражает ли это неблагоприятный баланс между эффектами и побочными эффектами у пожилых людей или использование чрезмерных доз GH, но очевидно, что пожилые люди не устойчивы к GH.Краткосрочные исследования зависимости реакции от дозы ясно демонстрируют, что пожилым пациентам требуется более низкая доза гормона роста для поддержания заданного уровня IGF-I в сыворотке (34,35), и было замечено, что уровень IGF-I в сыворотке увеличивается у отдельных пациентов при длительном лечении. терапии, если доза GH остается постоянной. Более того, пациенты с дефицитом гормона роста старше 60 лет очень чувствительны даже к небольшой дозе гормона роста (36). Интересно, что существует гендерная разница в ответе на лечение GH: мужчины более отзывчивы с точки зрения генерации IGF-I и потери жира во время терапии, скорее всего, из-за более низких уровней эстрогена, которые негативно влияют на эффект GH на генерацию IGF-I в печени. (37).
Фармакокинетика и краткосрочные метаболические эффекты почти физиологического внутривенного болюса ГР (200 мкг) сравнивались в группе молодых (30 лет) и старше (50 лет) здоровых взрослых (38). Площадь под кривой GH была значительно ниже у пожилых людей, тогда как период полувыведения был аналогичным в двух группах, что свидетельствует как об увеличенной скорости метаболического клиренса, так и очевидном объеме распределения GH у пожилых людей. Оба параметра показали сильную положительную корреляцию с жировой массой, хотя множественный регрессионный анализ показал, что возраст является независимым положительным предиктором.Краткосрочный липолитический ответ на болюс GH был выше у молодых людей по сравнению с пожилыми людьми. Интересно, что то же исследование показало, что белки, связывающие GH, сильно и положительно коррелируют с массой брюшного жира (39).
Проспективное долгосрочное исследование здоровых взрослых с последовательными сопутствующими оценками статуса GH и ожирения предоставило бы полезную информацию о причинно-следственной связи между статусом GH и составом тела в зависимости от возраста. Между тем предлагается следующая гипотеза (): 1.Изменения в образе жизни и генетическая предрасположенность способствуют накоплению жира с возрастом; 2. Увеличенная жировая масса приводит к увеличению доступности свободных жирных кислот и вызывает инсулинорезистентность и гиперинсулинемию; 3. Высокие уровни инсулина подавляют IGF-связывающий белок (IGFBP) -1, что приводит к относительному увеличению уровней свободного IGF-I; 4. Системное повышение уровня FFA, инсулина и свободного IGF-I подавляет высвобождение GH гипофизом, что дополнительно увеличивает жировую массу; 5. Эндогенный гормон роста выводится быстрее у субъектов с большим количеством жировой ткани.
В настоящее время неоправданно лечить возрастное ухудшение состава тела и физической работоспособности с помощью GH, особенно из-за опасений, что последующее повышение уровня IGF-I может увеличить риск развития опухолевых заболеваний (для обширного обсуждение гормона роста у пожилых людей см. в главе по этой теме в разделе «Эндокринология старения» Эндотекста).
Рис. 5.
Гипотетическая модель связи между низким уровнем GH и повышенным уровнем висцерального жира у взрослых.
Пожизненный дефицит GH
Реальная модель эффектов GH в физиологии человека представлена пациентами с пожизненным серьезным снижением передачи сигналов GH из-за мутаций рецепторов GHRH или GHRH, комбинированного дефицита GH, пролактина и ТТГ , или глобальное удаление GHR. Они демонстрируют низкий рост, кукольное лицо, высокие голоса и центральное ожирение, а также плодовиты (40). Несмотря на центральное ожирение и повышенное содержание жира в печени, они чувствительны к инсулину, частично защищены от рака и значительно снижают передачу сигналов о старении и, возможно, увеличивают продолжительность жизни (41).Снижение риска рака при пожизненном дефиците GH вместе с сообщениями о разрешающей роли GH в росте неопластической толстой кишки (42), предопухолевых поражениях молочной железы (43) и прогрессировании рака простаты (44) требует, по крайней мере, тщательный подбор доз замещения GH у пациентов с дефицитом GH.
GH и иммунная система
Хотя большинство данных о связи между GH и иммунной системой получены из исследований на животных, кажется, что GH может обладать иммуномодулирующим действием.Иммунные клетки, включая несколько субпопуляций лимфоцитов, экспрессируют рецепторы GH и отвечают на его стимуляцию (45). GH стимулирует in vitro, T и B-пролиферацию клеток и синтез иммуноглобулинов, усиливает созревание человеческих миелоидных клеток-предшественников и модулирует in vivo, Th2 / Th3 (8) и гуморальные иммунные ответы (46). Было показано, что GH может индуцировать продукцию de novo Т-клеток и увеличивать восстановление CD4 у ВИЧ-положительных пациентов. Другое исследование, имеющее возможное клиническое значение, показало, что устойчивая экспрессия GH снижает симптомы продромального заболевания и устраняет прогрессирование до явного диабета на мышиной модели диабета 1 типа, аутоиммунного заболевания, опосредованного Т-клетками.GH изменял цитокиновую среду, запускал поляризацию противовоспалительных макрофагов (M2), поддерживал активность супрессорной популяции Т-клеток и ограничивал пластичность клеток Th27 (46). Хорошо известно, что передача сигналов JAK / STAT, основного медиатора активации GHR, участвует в модуляции иммунной системы, поэтому есть соблазн предположить, что GH также может играть роль, но необходимы четкие данные о людях.
Передача сигналов гормона роста у людей
Активация рецептора гормона роста (GHR)
Передача сигналов GHR — отдельная и плодотворная область исследований сама по себе (47), поэтому в этом разделе основное внимание будет уделено недавним данным, полученным на моделях человека.
GHR были идентифицированы во многих тканях, включая жир, лимфоциты, печень, мышцы, сердце, почки, мозг и поджелудочную железу (48,49). Активация ассоциированной с рецептором киназы Janus (JAK) -2 является критическим шагом в инициировании передачи сигналов GH. Одна молекула GH связывается с двумя молекулами GHR, которые существуют в виде предварительно сформированных гомодимеров. После связывания GH внутриклеточные домены димера GHR подвергаются вращению, которое объединяет два внутриклеточных домена, каждый из которых связывает одну молекулу JAK2. Это, в свою очередь, вызывает перекрестное фосфорилирование остатков тирозина в киназном домене каждой молекулы JAK2 с последующим фосфорилированием тирозина GHR (48,50).Фосфорилированные остатки на GHR и JAK2 образуют сайты стыковки для различных сигнальных молекул, включая сигнальные преобразователи и активаторы транскрипции (STAT) 1, 3, 5a и 5b. STAT, связанные с активированным комплексом GHR-JAK2, впоследствии фосфорилируются по одному тирозину с помощью JAK2, обеспечивая димеризацию и транслокацию в ядро, где они связываются с ДНК и активируют транскрипцию гена. Сайт связывания STAT5b охарактеризован в промоторной области гена IGF-I (51). Ослабление JAK2-ассоциированной передачи сигналов GH опосредуется семейством цитокин-индуцируемых супрессоров передачи сигналов цитокинов (SOCS) (52).Белки SOCS связываются с остатками фосфотирозина на GHR или JAK2 и подавляют передачу сигналов GH, ингибируя активность JAK2 и конкурируя со STAT. Например, сообщалось, что ингибирующее действие эстрогена на продукцию IGF-I в печени, по-видимому, опосредовано повышающей регуляцией SOCS-2 (53).
Данные о передаче сигналов GHR получены в основном на моделях грызунов и экспериментальных клеточных линиях, хотя GH-индуцированная активация путей JAK2 / STAT5b и митоген-активируемой протеинкиназы (MAPK) была зарегистрирована в культивируемых человеческих фибробластах от здоровых людей (54) .STAT5b у людей имеет решающее значение для GH-индуцированной экспрессии IGF-I и стимуляции роста, что продемонстрировано идентификацией мутаций в гене STAT5b у пациентов с тяжелой нечувствительностью к GH в присутствии нормального GHR (55). Сообщалось об активации передачи сигналов GHR in vivo у здоровых молодых мужчин, подвергшихся внутривенному болюсу GH по сравнению с физиологическим раствором (56). Значительное фосфорилирование тирозина STAT5b было зарегистрировано после воздействия GH через 30-60 минут в биоптатах мышц и жира, но не было никаких доказательств GH-индуцированной активации PI 3-киназы, Akt / PKB или MAPK (56).
GH и передача сигналов инсулина
GH нарушает механизм инсулина, но точные механизмы у людей все еще остаются предметом споров. Нет данных о негативном влиянии GH на связывание инсулина с рецептором (57,58), что, очевидно, подразумевает пострецепторные метаболические эффекты.
Имеются данные на животных и in vitro , позволяющие предположить, что инсулин и GH имеют общие пострецепторные сигнальные пути (59). Сообщалось о конвергенции на уровнях STAT5 и SOCS3 (60), а также об основных путях передачи сигналов инсулина: субстратах рецепторов инсулина (IRS) 1 и 2, PI 3-киназе (PI3K), Akt и внеклеточных регулируемых киназах (ERK). ) 1 и 2 (61-63).Исследования на моделях грызунов предполагают, что инсулино-антагонистические эффекты GH в жировой ткани включают подавление инсулино-стимулированной активности PI3-киназы (59,64). В 2001 году было продемонстрировано, что GH индуцирует клеточную инсулинорезистентность, разъединяя PI3K и его нисходящие сигналы в адипоцитах 3T3-L1 (65)]. Последующее исследование показало, что GH увеличивает экспрессию p85α и снижает активность PI3K в жировой ткани мышей, что подтверждает предыдущее сообщение о прямом ингибирующем эффекте GH на активность PI3K (64).Однако исследование, проведенное на здоровых скелетных мышцах человека, как и ожидалось, показало, что инфузия GH вызывает устойчивое повышение уровней FFA и, следовательно, резистентность к инсулину, по оценке с помощью метода эугликемического зажима, но не было связано с каким-либо изменением инсулинорезистентности. стимулировал повышение активности IRS-1 / PI3K или PKB / Akt (66). Впоследствии было показано, что инсулин не влияет на GH-индуцированную активацию STAT5b или экспрессию мРНК SOCS3 (67).
Поскольку GH и инсулин имеют некоторые общие внутриклеточные субстраты, возникла гипотеза, согласно которой конкуренция за внутриклеточные субстраты объясняет негативное влияние GH на передачу сигналов инсулина (59).Кроме того, исследования показали, что белки SOCS негативно регулируют сигнальный путь инсулина (68). Следовательно, еще один возможный механизм, с помощью которого GH изменяет действие инсулина, — это увеличение экспрессии генов SOCS.
Нормальная физиология гормона роста у взрослых — Endotext
GH представляет собой одноцепочечный белок с 191 аминокислотой и двумя дисульфидными связями. Ген человеческого GH расположен на хромосоме 17q22 как часть локуса, состоящего из пяти генов. В дополнение к двум генам, связанным с GH (Gh2, который кодирует основной гормон роста взрослого человека, продуцируемый в соматотрофных клетках, обнаруженных в передней доле гипофиза и, в меньшей степени, в лимфоцитах, и Gh3, который кодирует плацентарный GH), существуют три гена, кодирующие гены хорионического соматомаммотропина (CSh2, CSh3 и CSHL) (также известного как плацентарный лактоген) (2,3).Ген Gh2 кодирует две различные изоформы GH (22 кДа и 20 кДа). Основной и наиболее распространенной формой GH в гипофизе и крови является мономерная изоформа 22K-GH, представляющая также рекомбинантный GH, доступный для терапевтического использования (а затем и для допинговых целей) (3). Введение рекомбинантного 22K-GH экзогенно приводит к снижению изоформы 20K-GH, и, таким образом, тестирование обеих изоформ используется для выявления допинга GH в спорте (4).
Как уже упоминалось, GH секретируется соматотрофными клетками, расположенными в основном в боковых крыльях передней доли гипофиза.Недавнее исследование секвенирования одноклеточной РНК, проведенное на мышах, показало, что GH-экспрессирующие клетки, представляющие соматотрофов, представляют собой наиболее многочисленную клеточную популяцию во взрослом гипофизе (5). Дифференцировка соматотрофных клеток регулируется фактором транскрипции гипофиза 1 (Pit-1). Данные на мышах предполагают, что гипофиз обладает регенеративной способностью, а клетки, продуцирующие GH, регенерируются из стволовых клеток гипофиза у молодых животных через 5 месяцев (6).
Физиологическая регуляция секреции GH
Морфологические характеристики и количество соматотрофов удивительно постоянны на протяжении всей жизни, в то время как характер их секреции изменяется.Секреция GH происходит пульсирующе и в циркадном ритме с максимальным высвобождением во второй половине ночи. Итак, сон — важный физиологический фактор, увеличивающий выброс гормона роста. Интересно, что максимальные уровни GH происходят в течение нескольких минут после начала медленного сна, и наблюдается заметный половой диморфизм ночного увеличения GH у людей, составляющий лишь часть от общего суточного высвобождения GH у женщин, но большая часть его вырабатывается у женщин. мужчины (7).
Секреция GH также зависит от пола, пубертатного статуса и возраста (и) (8).Интегрированная 24-часовая концентрация гормона роста значительно выше у женщин, чем у мужчин, и больше у молодых, чем у пожилых людей. Концентрация свободного эстрадиола в сыворотке, но не свободного тестостерона, коррелирует с GH, и при корректировке эффектов эстрадиола ни пол, ни возраст не влияют на концентрацию GH. Это говорит о том, что эстрогены играют решающую роль в модулировании секреции GH (8). Во время полового созревания происходит 3-кратное увеличение пульсирующей секреции GH, достигающее пика примерно в возрасте 15 лет у девочек и на 1 год позже у мальчиков (9).
Рисунок 1
Секреторный паттерн GH у молодых и старых женщин и мужчин. У молодых людей импульсы GH более крупные и частые, и женщины выделяют больше GH, чем мужчины (изменено из (8)).
Синтез и секреция GH гипофизом стимулируются эпизодическими гипоталамическими гормонами. Гормон высвобождения гормона роста (GHRH) стимулирует, в то время как соматостатин (SST) ингибирует производство и высвобождение GH. GH стимулирует выработку IGF-I, который, в свою очередь, подавляет секрецию GH как на гипоталамическом, так и на гипофизарном уровнях.Пептид желудочного сока грелин также является мощным стимулятором секреции GH, который усиливает секрецию GHRH в гипоталамусе и действует синергетически с его стимулирующими GH эффектами гипофиза (10). Интересно, что недавно было показано, что дупликация GPR101 в зародышевой линии или соматическая дупликация постоянно активирует путь цАМФ в отсутствие лиганда, что приводит к высвобождению GH. Хотя точная физиология GPR101 неясна, стоит упомянуть о нем, поскольку он явно влияет на патофизиологию GH (11).
Кроме того, на ось GH может влиять множество других факторов, наиболее вероятно из-за взаимодействия с GRHR, соматостатином и грелином.Эстрогены стимулируют секрецию GH, но ингибируют действие GH на печень, подавляя передачу сигналов рецептора GH (GHR). Напротив, андрогены усиливают периферическое действие GH (12). Экзогенные эстрогены усиливают ответы гипофизарного GH на субмаксимальные эффективные импульсы экзогенного GHRH (13) и подавляют подавление экзогенным SST (14). Также экзогенный эстроген усиливает действие грелина (15).
Высвобождение
GH обратно коррелирует с внутрибрюшным висцеральным ожирением через механизмы, которые могут зависеть от увеличения потока свободных жирных кислот (FFA), повышенного уровня инсулина или свободного IGF-I.
Рисунок 2.
Факторы, которые стимулируют и подавляют секрецию GH в физиологических условиях.
ГОРМОН, ВЫПУСКАЮЩИЙ ГОРМОН РОСТА
GHRH представляет собой полипептид из 44 аминокислот, продуцируемый в дугообразном ядре гипоталамуса. Эти нервные окончания секретируют GHRH, чтобы достичь соматотрофов передней доли гипофиза через систему воротной вены, что приводит к транскрипции и секреции GH. Более того, исследования на животных показали, что GHRH играет жизненно важную роль в пролиферации соматотрофов в передней доле гипофиза, тогда как отсутствие GHRH приводит к гипоплазии передней доли гипофиза (16).Кроме того, GHRH регулирует экспрессию гена GH и стимулирует высвобождение GH (17). Секреция GHRH стимулируется несколькими факторами, включая деполяризацию, α2-адренергическую стимуляцию, гипофизэктомию, тиреоидэктомию и гипогликемию, и подавляется SST, IGF-I и активацией ГАМКергических нейронов.
GHRH действует на соматотрофов через семь трансмембранных G-белков, связанных с стимулирующими рецепторами на поверхности клетки. Этот рецептор широко изучался в течение последнего десятилетия, что привело к идентификации нескольких важных мутаций.Точечные мутации в рецепторах GHRH, как показали исследования, проведенные на карликовых мышах lit / lit , показали глубокое влияние на последующую пролиферацию соматотрофов, приводящую к гипоплазии передней доли гипофиза (18). В отличие от мутаций в генах Pit-1 и PROP-1, которые приводят к множественному дефициту гормонов гипофиза и гипоплазии передней доли гипофиза, мутации рецептора GHRH приводят к глубокому дефициту GH с гипоплазией передней доли гипофиза. Вслед за первой мутацией рецептора GHRH, описанной в 1996 г. (19), за последнее десятилетие был обнаружен ряд семейных мутаций рецептора GHRH.Эти мутации составляют почти 10% семейных изолированных дефицитов GH. Пораженный человек будет иметь низкий рост и гипоплазию передней доли гипофиза. Однако у них отсутствуют некоторые типичные признаки дефицита GH, такие как гипоплазия средней зоны лица, микрофаллос и неонатальная гипогликемия (20).
СОМАТОСТАТИН (SST)
SST — это циклический пептид, кодируемый одним геном у человека, который в основном оказывает ингибирующее действие на эндокринные и экзокринные секреции. Многие клетки в организме, включая специализированные клетки в переднем паравентрикулярном ядре и дугообразном ядре, производят SST.Эти нейроны секретируют SST в систему воротной вены аденогипофиза через срединное возвышение, чтобы оказывать влияние на переднюю долю гипофиза. SST имеет короткий период полураспада, составляющий примерно 2 минуты, так как у человека он быстро инактивируется тканевой пептидазой.
SST действует через семь трансмембранных рецепторов, связанных с G-белком, и к настоящему времени у человека идентифицировано пять подтипов рецептора (SSTR1-5). Хотя все пять подтипов рецепторов экспрессируются в гипофизе плода человека, гипофиз взрослого человека экспрессирует только 4 подтипа (SSTR1, SSTR2, SSTR3, SSTR5).Из этих четырех подтипов соматотрофы проявляют большую чувствительность к лигандам SSTR2 и SSTR5 в синергетическом ингибировании секреции GH (21). Соматостатин подавляет высвобождение GH, но не синтез GH.
GHRELIN
Грелин представляет собой пептид из 28 аминокислот, который является естественным лигандом рецептора, стимулирующего секрецию GH. Фактически, грелин и GHRH обладают синергетическим эффектом в повышении уровня циркулирующего GH (7). Грелин в основном секретируется желудком и может участвовать в реакции гормона роста на голодание и прием пищи.
Клинические последствия
Уровни GH — влияние состава тела, физической формы и возраста
С введением надежных радиоиммунологических тестов было признано, что циркуляция GH у тучных субъектов притупляется, а нормальное старение сопровождается постепенным снижением в уровнях GH (22,23). Была выдвинута гипотеза, что многие из стареющих изменений в составе тела и функциях органов связаны или вызваны снижением GH (24), также известным как «соматопауза».
Исследования, проведенные в конце 90-х годов, однозначно подтвердили, что взрослые с тяжелым дефицитом GH характеризуются повышенной жировой массой и сниженной мышечной массой (LBM) (25). Также известно, что нормальный уровень GH может быть восстановлен у лиц с ожирением после значительной потери веса (26), и что замещение GH у взрослых с дефицитом GH нормализует состав тела. Что остается неизвестным, так это причинно-следственная связь между снижением уровня GH и старческими изменениями в составе тела.Является ли склонность к набору жира и потере мышечной массы инициированной или предшествующей первичным возрастным снижением секреции и действия GH? В качестве альтернативы, накопление жировой массы вторично по отношению к факторам, не зависящим от гормона роста (например, образу жизни, диетическим привычкам), приводит к подавлению секреции гормона роста с обратной связью. Более того, мало что известно о возможных возрастных изменениях фармакокинетики и биоактивности GH.
Поперечные исследования, проведенные для оценки связи между составом тела и стимулированным высвобождением GH у здоровых субъектов, показывают, что у взрослых людей (средний возраст 50 лет) пиковый ответ GH на стимуляторы секреции (клонидин и аргинин) ниже, а у женщин — выше. реакция на аргинин по сравнению с мужчинами.Однако множественный регрессионный анализ показывает, что масса внутрибрюшного жира является наиболее важным и отрицательным предиктором пиковых уровней GH, как упоминалось ранее (27). В той же популяции 24-часовые спонтанные уровни GH также преимущественно обратно коррелировали с массой внутрибрюшного жира () (28).
Рисунок 3.
Корреляция между массой внутрибрюшного жира и 24-часовой секрецией GH.
Насколько нам известно, подробный анализ секреции GH в зависимости от состава тела у пожилых людей не проводился.Вместо этого сывороточный IGF-I использовался в качестве суррогата или заместителя для статуса GH в нескольких исследованиях с участием пожилых мужчин (29–31). Эти исследования охватывают большие группы амбулаторных мужчин в возрасте от 50 до 90 лет, проживающих в общинах. Как и ожидалось, сывороточный IGF-I снижался с возрастом (), но IGF-I не показал какой-либо значительной связи с составом тела или физической работоспособностью.
Рисунок 4.
Изменения сывороточного IGF-I с возрастом; модифицировано из (32).
Действие GH: Влияние возраста, пола и состава тела
Учитывая большой интерес к действию GH у взрослых, на удивление мало исследований посвящено возможным возрастным различиям в реакции или чувствительности к GH.У нормальных взрослых снижение уровня GH сопровождается снижением сывороточного IGF-I, что свидетельствует о понижающей регуляции оси GH-IGF-I. Введение GH пожилым здоровым взрослым обычно было связано с предсказуемым, хотя и умеренным, влиянием на состав тела и побочными эффектами с точки зрения задержки жидкости и умеренной инсулинорезистентности (33). Неясно, отражает ли это неблагоприятный баланс между эффектами и побочными эффектами у пожилых людей или использование чрезмерных доз GH, но очевидно, что пожилые люди не устойчивы к GH.Краткосрочные исследования зависимости реакции от дозы ясно демонстрируют, что пожилым пациентам требуется более низкая доза гормона роста для поддержания заданного уровня IGF-I в сыворотке (34,35), и было замечено, что уровень IGF-I в сыворотке увеличивается у отдельных пациентов при длительном лечении. терапии, если доза GH остается постоянной. Более того, пациенты с дефицитом гормона роста старше 60 лет очень чувствительны даже к небольшой дозе гормона роста (36). Интересно, что существует гендерная разница в ответе на лечение GH: мужчины более отзывчивы с точки зрения генерации IGF-I и потери жира во время терапии, скорее всего, из-за более низких уровней эстрогена, которые негативно влияют на эффект GH на генерацию IGF-I в печени. (37).
Фармакокинетика и краткосрочные метаболические эффекты почти физиологического внутривенного болюса ГР (200 мкг) сравнивались в группе молодых (30 лет) и старше (50 лет) здоровых взрослых (38). Площадь под кривой GH была значительно ниже у пожилых людей, тогда как период полувыведения был аналогичным в двух группах, что свидетельствует как об увеличенной скорости метаболического клиренса, так и очевидном объеме распределения GH у пожилых людей. Оба параметра показали сильную положительную корреляцию с жировой массой, хотя множественный регрессионный анализ показал, что возраст является независимым положительным предиктором.Краткосрочный липолитический ответ на болюс GH был выше у молодых людей по сравнению с пожилыми людьми. Интересно, что то же исследование показало, что белки, связывающие GH, сильно и положительно коррелируют с массой брюшного жира (39).
Проспективное долгосрочное исследование здоровых взрослых с последовательными сопутствующими оценками статуса GH и ожирения предоставило бы полезную информацию о причинно-следственной связи между статусом GH и составом тела в зависимости от возраста. Между тем предлагается следующая гипотеза (): 1.Изменения в образе жизни и генетическая предрасположенность способствуют накоплению жира с возрастом; 2. Увеличенная жировая масса приводит к увеличению доступности свободных жирных кислот и вызывает инсулинорезистентность и гиперинсулинемию; 3. Высокие уровни инсулина подавляют IGF-связывающий белок (IGFBP) -1, что приводит к относительному увеличению уровней свободного IGF-I; 4. Системное повышение уровня FFA, инсулина и свободного IGF-I подавляет высвобождение GH гипофизом, что дополнительно увеличивает жировую массу; 5. Эндогенный гормон роста выводится быстрее у субъектов с большим количеством жировой ткани.
В настоящее время неоправданно лечить возрастное ухудшение состава тела и физической работоспособности с помощью GH, особенно из-за опасений, что последующее повышение уровня IGF-I может увеличить риск развития опухолевых заболеваний (для обширного обсуждение гормона роста у пожилых людей см. в главе по этой теме в разделе «Эндокринология старения» Эндотекста).
Рис. 5.
Гипотетическая модель связи между низким уровнем GH и повышенным уровнем висцерального жира у взрослых.
Пожизненный дефицит GH
Реальная модель эффектов GH в физиологии человека представлена пациентами с пожизненным серьезным снижением передачи сигналов GH из-за мутаций рецепторов GHRH или GHRH, комбинированного дефицита GH, пролактина и ТТГ , или глобальное удаление GHR. Они демонстрируют низкий рост, кукольное лицо, высокие голоса и центральное ожирение, а также плодовиты (40). Несмотря на центральное ожирение и повышенное содержание жира в печени, они чувствительны к инсулину, частично защищены от рака и значительно снижают передачу сигналов о старении и, возможно, увеличивают продолжительность жизни (41).Снижение риска рака при пожизненном дефиците GH вместе с сообщениями о разрешающей роли GH в росте неопластической толстой кишки (42), предопухолевых поражениях молочной железы (43) и прогрессировании рака простаты (44) требует, по крайней мере, тщательный подбор доз замещения GH у пациентов с дефицитом GH.
GH и иммунная система
Хотя большинство данных о связи между GH и иммунной системой получены из исследований на животных, кажется, что GH может обладать иммуномодулирующим действием.Иммунные клетки, включая несколько субпопуляций лимфоцитов, экспрессируют рецепторы GH и отвечают на его стимуляцию (45). GH стимулирует in vitro, T и B-пролиферацию клеток и синтез иммуноглобулинов, усиливает созревание человеческих миелоидных клеток-предшественников и модулирует in vivo, Th2 / Th3 (8) и гуморальные иммунные ответы (46). Было показано, что GH может индуцировать продукцию de novo Т-клеток и увеличивать восстановление CD4 у ВИЧ-положительных пациентов. Другое исследование, имеющее возможное клиническое значение, показало, что устойчивая экспрессия GH снижает симптомы продромального заболевания и устраняет прогрессирование до явного диабета на мышиной модели диабета 1 типа, аутоиммунного заболевания, опосредованного Т-клетками.GH изменял цитокиновую среду, запускал поляризацию противовоспалительных макрофагов (M2), поддерживал активность супрессорной популяции Т-клеток и ограничивал пластичность клеток Th27 (46). Хорошо известно, что передача сигналов JAK / STAT, основного медиатора активации GHR, участвует в модуляции иммунной системы, поэтому есть соблазн предположить, что GH также может играть роль, но необходимы четкие данные о людях.
Передача сигналов гормона роста у людей
Активация рецептора гормона роста (GHR)
Передача сигналов GHR — отдельная и плодотворная область исследований сама по себе (47), поэтому в этом разделе основное внимание будет уделено недавним данным, полученным на моделях человека.
GHR были идентифицированы во многих тканях, включая жир, лимфоциты, печень, мышцы, сердце, почки, мозг и поджелудочную железу (48,49). Активация ассоциированной с рецептором киназы Janus (JAK) -2 является критическим шагом в инициировании передачи сигналов GH. Одна молекула GH связывается с двумя молекулами GHR, которые существуют в виде предварительно сформированных гомодимеров. После связывания GH внутриклеточные домены димера GHR подвергаются вращению, которое объединяет два внутриклеточных домена, каждый из которых связывает одну молекулу JAK2. Это, в свою очередь, вызывает перекрестное фосфорилирование остатков тирозина в киназном домене каждой молекулы JAK2 с последующим фосфорилированием тирозина GHR (48,50).Фосфорилированные остатки на GHR и JAK2 образуют сайты стыковки для различных сигнальных молекул, включая сигнальные преобразователи и активаторы транскрипции (STAT) 1, 3, 5a и 5b. STAT, связанные с активированным комплексом GHR-JAK2, впоследствии фосфорилируются по одному тирозину с помощью JAK2, обеспечивая димеризацию и транслокацию в ядро, где они связываются с ДНК и активируют транскрипцию гена. Сайт связывания STAT5b охарактеризован в промоторной области гена IGF-I (51). Ослабление JAK2-ассоциированной передачи сигналов GH опосредуется семейством цитокин-индуцируемых супрессоров передачи сигналов цитокинов (SOCS) (52).Белки SOCS связываются с остатками фосфотирозина на GHR или JAK2 и подавляют передачу сигналов GH, ингибируя активность JAK2 и конкурируя со STAT. Например, сообщалось, что ингибирующее действие эстрогена на продукцию IGF-I в печени, по-видимому, опосредовано повышающей регуляцией SOCS-2 (53).
Данные о передаче сигналов GHR получены в основном на моделях грызунов и экспериментальных клеточных линиях, хотя GH-индуцированная активация путей JAK2 / STAT5b и митоген-активируемой протеинкиназы (MAPK) была зарегистрирована в культивируемых человеческих фибробластах от здоровых людей (54) .STAT5b у людей имеет решающее значение для GH-индуцированной экспрессии IGF-I и стимуляции роста, что продемонстрировано идентификацией мутаций в гене STAT5b у пациентов с тяжелой нечувствительностью к GH в присутствии нормального GHR (55). Сообщалось об активации передачи сигналов GHR in vivo у здоровых молодых мужчин, подвергшихся внутривенному болюсу GH по сравнению с физиологическим раствором (56). Значительное фосфорилирование тирозина STAT5b было зарегистрировано после воздействия GH через 30-60 минут в биоптатах мышц и жира, но не было никаких доказательств GH-индуцированной активации PI 3-киназы, Akt / PKB или MAPK (56).
GH и передача сигналов инсулина
GH нарушает механизм инсулина, но точные механизмы у людей все еще остаются предметом споров. Нет данных о негативном влиянии GH на связывание инсулина с рецептором (57,58), что, очевидно, подразумевает пострецепторные метаболические эффекты.
Имеются данные на животных и in vitro , позволяющие предположить, что инсулин и GH имеют общие пострецепторные сигнальные пути (59). Сообщалось о конвергенции на уровнях STAT5 и SOCS3 (60), а также об основных путях передачи сигналов инсулина: субстратах рецепторов инсулина (IRS) 1 и 2, PI 3-киназе (PI3K), Akt и внеклеточных регулируемых киназах (ERK). ) 1 и 2 (61-63).Исследования на моделях грызунов предполагают, что инсулино-антагонистические эффекты GH в жировой ткани включают подавление инсулино-стимулированной активности PI3-киназы (59,64). В 2001 году было продемонстрировано, что GH индуцирует клеточную инсулинорезистентность, разъединяя PI3K и его нисходящие сигналы в адипоцитах 3T3-L1 (65)]. Последующее исследование показало, что GH увеличивает экспрессию p85α и снижает активность PI3K в жировой ткани мышей, что подтверждает предыдущее сообщение о прямом ингибирующем эффекте GH на активность PI3K (64).Однако исследование, проведенное на здоровых скелетных мышцах человека, как и ожидалось, показало, что инфузия GH вызывает устойчивое повышение уровней FFA и, следовательно, резистентность к инсулину, по оценке с помощью метода эугликемического зажима, но не было связано с каким-либо изменением инсулинорезистентности. стимулировал повышение активности IRS-1 / PI3K или PKB / Akt (66). Впоследствии было показано, что инсулин не влияет на GH-индуцированную активацию STAT5b или экспрессию мРНК SOCS3 (67).
Поскольку GH и инсулин имеют некоторые общие внутриклеточные субстраты, возникла гипотеза, согласно которой конкуренция за внутриклеточные субстраты объясняет негативное влияние GH на передачу сигналов инсулина (59).Кроме того, исследования показали, что белки SOCS негативно регулируют сигнальный путь инсулина (68). Следовательно, еще один возможный механизм, с помощью которого GH изменяет действие инсулина, — это увеличение экспрессии генов SOCS.
Гормон роста вырабатывается в гиппокампе, где он реагирует на возраст, пол и стресс
Аннотация
Недавние исследования нашей группы и других показали, что гормон роста (GH) вырабатывается эндогенно в гиппокампе, структуре мозга, связанной с обучением и аспектами эмоционального опыта.Здесь мы демонстрируем, что этот эндогенно продуцируемый GH регулируется возрастными и половыми различиями и присутствием эстрогена. Уровни мРНК GH были выше у женщин, чем у мужчин, особенно во время проэструса, стадии течки, когда уровень эстрогена повышен. Более того, экспрессия GH была увеличена у овариэктомированных самок, получавших эстрадиол. Это увеличение мРНК GH в ответ на эстроген сопровождалось появлением белка GH и отрицательно коррелировало с уровнями экспрессии мРНК инсулиноподобного фактора роста-I, предполагая обратную связь между инсулиноподобным фактором роста-I и GH в мозг.Уровни мРНК GH также были повышены в первичных культурах нейронов, подвергнутых воздействию 17-β-эстрадиола in vitro , что дополнительно подтверждает прямое влияние эстрогена на экспрессию GH. Наконец, воздействие острого стрессового события увеличивало экспрессию и продукцию GH как у мужчин, так и у женщин. Однако вызванное стрессом увеличение GH у женщин зависело от стадии эстрального цикла, на которой они подвергались стрессовому событию. Вместе эти данные дополнительно демонстрируют, что GH эндогенно продуцируется в гиппокампе взрослых, где он регулируется возрастом, эстрогеном и воздействием внешних стимулов.Эти результаты предполагают, что GH может участвовать в функциях, приписываемых гиппокампу, таких как обучение и реакция на стрессовый опыт.
Гормон роста (GH) представляет собой полипептид цитокинов массой 19-21 кДа, который вырабатывается в основном в передней доле гипофиза, где он чаще всего связан с постнатальным продольным ростом в тканях-мишенях, включая печень, мышцы, жировую ткань, а также кости и клетки. метаболизм (1). GH оказывает свое действие в этих тканях прямо или косвенно через свой нижестоящий эффектор, инсулиноподобный фактор роста-I (IGF-I).Недавние исследования показывают, что ось GH / IGF-I также может играть важную роль в функциях центральной нервной системы, в том числе связанных с ростом, развитием и защитой нейронов (2, 3). Кроме того, несколько исследований показывают, что ось GH / IGF может играть роль во влиянии на настроение и когнитивные способности (4, 5). Сайты связывания GH были идентифицированы в нескольких областях мозга, включая сосудистое сплетение, скорлупу, таламус, гипофиз, гиппокамп и кору головного мозга (6), что свидетельствует о наличии рецепторов GH (GHR) в этих тканях.Кроме того, исследования нашей группы и других предоставили доказательства эндогенной экспрессии GH в гиппокампе (7, 8). Кроме того, рецепторы IGF-I, известного медиатора передачи сигналов GH, заметны в областях гиппокампа и парагиппокампа и обнаруживаются в миндалине, мозжечке и коре головного мозга, как и мРНК для этих рецепторов (9). Несколько исследований установили роль IGF-I в развитии и росте нейронов (10) и нейрогенезе в гиппокампе взрослых (11-13).
В предыдущем исследовании мы использовали профилирование транскрипции для идентификации генов, связанных с обучением.Неожиданно мы обнаружили, что выполнение задачи обучения, зависящей от гиппокампа, увеличивает экспрессию GH в мужском гиппокампе (8). Это увеличение произошло у животных, которые научились, тогда как наивные животные и те, кто подвергался другим типам тренировок, демонстрировали очень низкие или неопределяемые уровни GH. Эти результаты были неожиданными, поскольку эндогенная экспрессия GH еще не локализовалась в гиппокампе.
GH также связан с половым созреванием, поскольку его уровни повышаются в период полового созревания и снижаются с возрастом как у мужчин, так и у женщин (14, 15).Более того, половой гормон эстроген стимулирует высвобождение гормона роста, который, в свою очередь, может вызвать овуляцию (15, 16). Учитывая известные эффекты GH на половое развитие, мы охарактеризовали экспрессию эндогенного GH в гиппокампе как функцию возраста и пола. Во-первых, мы проверили, изменилась ли экспрессия GH по мере того, как животные достигли половой зрелости, и были ли половые различия и соответствующие изменения в эстральном цикле самок крыс. Также были определены эффекты овариэктомии (OVX) и замещения эстрогеном in vivo и эффекты эстрадиола in vitro на экспрессию GH.Кроме того, мы исследовали влияние эстрогена, возрастных и половых различий на мРНК для GHR и IGF-I. Наконец, было изучено влияние острого стрессового опыта на реакцию гормона роста у мужчин и женщин на разных стадиях эстрального цикла.
Результаты
Используя ПЦР в реальном времени, мы измерили уровни мРНК GH из левого гиппокампа у молодых самцов и самок крыс и взрослых самцов и самок. Результаты представлены относительно экспрессии у взрослых самцов и были проанализированы с помощью ANOVA и запланированных сравнений средних значений животных (рис.1
А ). Экспрессия мРНК GH была более чем в два раза выше у взрослых самцов, чем у молодых самцов [ F (1,9) = 9,6; P <0,05] и более чем в три раза выше у взрослых самок, чем у молодых самок [ F (1,9) = 5,4; P = 0,05]. Кроме того, взрослые женщины экспрессировали почти в два раза больше мРНК GH, чем взрослые мужчины [ F (1,22) = 3,9; P = 0,07]. Не было различий в экспрессии между самцами и самками молодых крыс ( P > 0.05).
Рисунок 1.
Возрастные и половые различия в экспрессии GH. ( A ) Уровни мРНК GH изображены как функция возраста (взрослые по сравнению с молодыми) и пола [мужчины (черные столбцы) по сравнению с женщинами (белые столбцы)]. Уровни были повышены у взрослых, особенно у женщин. ( B ) Экспрессия мРНК GH у самок изображена во время стадий течки, включая проэструс (PF), течку (EF) и диэструс (DF), и сравнивается с экспрессией у взрослых самцов (AM).У самок они увеличивались во время проэструса и течки. ( C ) Показаны примеры вестерн-блоттинга, иллюстрирующие присутствие белка GH в гиппокампе, особенно у женщин во время течки. JM, молодые самцы; JF, молодые самки.
Эти результаты предполагают, что эстроген может влиять на экспрессию GH в гиппокампе. Чтобы проверить эту возможность, мы измерили GH у самок во время проэструса, течки и диэструса. Самки в проэструсе экспрессировали больше мРНК GH, почти в три раза, чем у самцов [ F (1,8) = 6.6; P <0,05] (Рис. 1 В ). Самки в период течки продуцируют немного меньше мРНК GH, но все же больше, чем самцы [ F (1,12) = 8,9; P <0,05]. Самки в период диэструса экспрессируют мало GH и на уровнях, аналогичных самцам [ F (1,10) = 0,26; P <0,62].
Мы использовали другой гиппокамп, чтобы определить, изменяются ли уровни белка GH в зависимости от возраста и пола. Белок GH не обнаруживался у молодых животных, но обнаруживался у взрослых самцов (рис.1
С ). У взрослых самок GH не обнаруживался в проэструсе, но присутствовал в течке и, в меньшей степени, в диэструсе. Учитывая, что проэструс сохраняется в течение очень короткого периода, различия в стадиях между уровнями мРНК и белка, скорее всего, отражают время, необходимое для трансляции.
Затем мы измерили мРНК для GHR и IGF-I. Оба были выражены у самцов и самок во время течки и диэструса (рис. 2).
A ), но практически не обнаруживается во время проэструса.Фактически, самки в эструсе экспрессируют в семь раз больше мРНК IGF-I, чем в проэструсе [ F (1,11) = 19,1; P <0,01]. Эти данные свидетельствуют о том, что IGF-I и GHR совместно регулируются в гиппокампе. Относительные уровни экспрессии IGF-I и уровней мРНК GHR для всех животных в исследовании коррелировали и выявляли сильную положительную корреляцию ( r
2 = 0,78, P <0,0001), как показано на рис. 2
В .О взаимосвязи между IGF-I и GHR сообщалось в других исследованиях (17), и наряду с настоящими результатами можно было бы указать, что эстроген ингибирует как экспрессию GHR, так и IGF-I в гиппокампе, что затем приводит к экспрессии GH.
Рис. 2.
GHR и экспрессия IGF-I. ( A ) Уровни мРНК GHR (закрашенные столбцы) и IGF-I (светлые столбцы) представлены как функция возрастных и половых различий.мРНК для обоих были уменьшены у женщин во время проэструса (PF), по сравнению с женщинами в течке (EF) и диэструсе (DF), а также у взрослых мужчин (AM). ( B ) Анализ диаграммы рассеяния показывает экспрессию GHR по сравнению с IGF-I для всех животных. Данные свидетельствуют о сильной положительной корреляции между экспрессией GHR и IGF-I.
Затем мы исследовали прямые эффекты лечения эстрадиолом на экспрессию GH. Как и ожидалось, концентрации эстрадиола были выше в крови от овариэктомированных женщин, получавших эстрадиол (63.85 ± 11,49 пг / мл), чем те, которые получали наполнитель (4,82 ± 2,15 пг / мл) [ F (1,8) = 25,95; P <0,001]. мРНК GH у самок после овариэктомии была подобна таковой у самцов и значительно увеличивалась под действием эстрадиола (рис. 3).
A ), как и белок (рис.
В ). Помимо уровней мРНК GH, мы измеряли уровни мРНК IGF-I и GHR. Ранее сообщалось, что лечение эстрадиолом снижает уровни мРНК GHR в гиппокампе у овариэктомированных женщин (17).Точно так же здесь мы обнаружили, что лечение эстрогенами значительно снижает экспрессию GHR у овариэктомированных самок [ F (1,9) = 5,11; P <0,03]. Мы также обнаружили, что эстроген снижает экспрессию IGF-I [ F (1,9) = 5,11; P <0,05]. Эти результаты согласуются с данными, показывающими, что эстроген подавляет экспрессию IGF-I и GHR, вызывая экспрессию GH у женщин с нормальным эстральным циклом. Чтобы подтвердить, что эстроген непосредственно влияет на экспрессию GH, мы подвергали первичные нейроны в возрасте 1 недели в культуре эстрадиолу (10 нМ 17-β-эстрадиола в течение 24 часов).МРНК GH была в три раза выше в культурах, обработанных эстрадиолом, чем в культурах, которые не были обработаны [ F (1,10) = 12,5; P <0,001] (фиг. 4). Первичные нейроны культивировали в отсутствие сыворотки, чтобы ограничить пролиферацию глии и более непосредственно воздействовать на влияние эстрогена на нейроны. Эти данные показывают, что эстрадиол увеличивает экспрессию мРНК GH в первичных культурах нейронов и, таким образом, дополняет данные, предполагая, что эстроген увеличивает экспрессию GH в нейронах.
Рис. 3.
Эстроген стимулирует выработку гормона роста. ( A ) Самки с удаленными яичниками, которым вводили масляный носитель (OVX w / O), вырабатывали такие же уровни GH, что и взрослые мужчины, но в два раза больше GH при воздействии 17-β-эстрадиола (OVX w / E). ( B ) Вестерн-блоттинг показывает продукцию белка GH в ответ на лечение эстрогеном (OVX w / E) после OVX (OVX w / O).( C ) Уровни мРНК IGF-I (заполненные столбцы) и GHR (белые столбцы) были снижены в гиппокампе обработанных эстрогеном овариэктомированных самок (OVX w / E) по сравнению с теми, которым вводили масло (OVX w / O).
Рис. 4.
Эстроген стимулирует выработку гормона роста. ( A ) Уровни мРНК GH повышались в нейронах коры при воздействии 10 нМ 17-β-эстрадиола по сравнению с необработанными контролями.( B ) Продукты ОТ-ПЦР амплификации кДНК, полученной из общей РНК необработанных однонедельных первичных культур нейронов и из тех же культур, обработанных 10 нМ 17-β-эстрадиола в течение 24 часов.
Как показано здесь, экспрессия мРНК GH в гиппокампе сексуально диморфна и намного выше у женщин, чем у мужчин. GH в гиппокампе также реагирует на обучение, зависящее от гиппокампа (8). Эти результаты показывают, что GH может реагировать на события окружающей среды, и предполагают, что он может играть роль в когнитивных или эмоциональных реакциях, которые различаются у мужчин и женщин.Было показано, что самцы и самки крыс по-разному реагируют на острое стрессовое событие, и действительно, самцы учатся лучше, тогда как самки обучаются с нарушениями (18). На основании этого исследования мы предположили, что стрессовое событие повлияет на экспрессию GH у мужчин иначе, чем у женщин. Чтобы проверить эту гипотезу, мы измерили влияние острого стрессового события на экспрессию GH в гиппокампе как у мужчин, так и у женщин. Через день после воздействия 30 кратковременных прерывистых ударов хвостом (1 мА, 1 с) гиппокамп самцов продуцировал почти вдвое больше мРНК GH [ F (1,10) = 12.5; P <0,001] (рис. 5
А ). У самок эффект был разным и зависел от стадии течки, на которой они подвергались действию стрессора. Те, которые подвергались стрессу во время диэструса, продуцировали значительно больше мРНК для GH, как измерено через 24 часа после возникновения стрессора [ F (1,14) = 5,79; P = 0,03], тогда как те, которые подвергались стрессу во время течки или проэструса, не были затронуты ( P > 0,05) (рис. 5
B и C ).В совокупности данные показывают, что стресс влияет на экспрессию GH по-разному у женщин в зависимости от стадии течки, на которой происходит событие. Поскольку самки в период течки и проэструса экспрессируют больше гормона роста в состоянии отсутствия стресса, чем самки в период диэструса, отсутствие стрессового воздействия у этих самок может отражать эффект «потолка»; Другими словами, они, возможно, уже выражают максимальное количество GH, и стресс не может еще больше усилить его экспрессию. Другая возможность заключается в том, что воздействие стрессового события увеличивает экспрессию GH у мужчин, но только у женщин, когда их уровень эстрогена относительно низок, как у мужчин.
Рис. 5.
Стресс вызывает выработку гормона роста. ( A ) Самцы, подвергшиеся острому стрессовому событию, продуцировали в два раза больше мРНК GH, чем самцы, которые не подвергались стрессу, хотя уровни IGF не изменились. ( B ) Самки, подвергшиеся воздействию стрессора во время диэструса, продуцировали более чем в три раза больше мРНК GH и 20% мРНК IGF.( C ) мРНК GH и IGF у тех, кто подвергался стрессу во время течки, не были затронуты.
Уровни мРНК
IGF-I были количественно определены у животных, подвергшихся стрессу, чтобы определить, коррелирует ли индукция мРНК GH с репрессией мРНК IGF-I. Интересно, что даже несмотря на то, что уровни мРНК GH были увеличены у подвергшихся стрессу мужчин, не было очевидного влияния стрессового события на уровни мРНК IGF-I в мужском гиппокампе [ F (1,10) = 0.09; P = 0,77] (рис. 5
А ). Напротив, воздействие стрессора снижает экспрессию IGF-I в 3,2 раза у самок, находящихся в состоянии диэструса [ F (1,14) = 6,17; P = 0,03] (рис. 5
В ). Это снижение экспрессии было стойким, потому что оно было очевидным даже через 24 часа после прекращения стрессового события, что указывает на относительно длительное влияние события окружающей среды на мРНК IGF-I в гиппокампе. В целом, эти данные указывают на то, что на экспрессию GH и, предположительно, на его продукцию влияет стрессовый опыт, но задействованные пути различны: один модулируется изменениями IGF-I, а другой нет.Кроме того, реакция у женщин изменяется в течение эстрального цикла и, таким образом, кажется более динамичной реакцией у женщин, чем у мужчин.
Обсуждение
Возрастные и половые различия в экспрессии GH.
GH хорошо известен своей ролью в росте и развитии тела, но его роль в работе мозга менее изучена. Фактически, до недавнего времени было неясно, вырабатывается ли GH в головном мозге. Здесь мы показываем, что мРНК и белок продуцируются в гиппокампе и что они реагируют вместе с IGF-I на возрастные и половые различия.В частности, взрослые крысы экспрессировали в своем гиппокампе более чем в два раза больше GH по сравнению с гиппокампом молодых особей, которые еще не достигли половой зрелости. Кроме того, экспрессия GH была больше у женщин, чем у мужчин, и была особенно чувствительна к присутствию эстрогена. Наивысшая степень экспрессии GH наблюдалась в гиппокампе женщин, когда они находились в проэструсе, стадии, связанной с овуляцией и высокими концентрациями эстрогена в крови. Поскольку гормоны, отличные от эстрогена, изменяются в течение эстрального цикла, мы исследовали прямое влияние эстрогена на экспрессию GH у женщин без яичников.Один только OVX снижал уровни мРНК GH в гиппокампе женщин до уровней, аналогичных уровням, измеренным у взрослых мужчин. Более того, воздействие экзогенного эстрадиола увеличивало экспрессию мРНК гиппокампа и уровни белка GH значительно больше, чем воздействие только масляного носителя. Увеличение экспрессии GH в ответ на эстрадиол, по-видимому, происходит в нейронах, по крайней мере, в той степени, в которой оно было усилено в первичных нейронах в культуре, которые подвергались воздействию 17-β-эстрадиола. Вместе эти данные показывают, что GH в гиппокампе регулируется половыми различиями и что эти различия зависят от эстрогена и изменений, которые происходят по мере того, как животные достигают репродуктивной зрелости.
Взаимосвязь между мРНК GH и его рецептором и IGF-I.
В большинстве биологических систем GH, IGF-I и их соответствующие рецепторы тесно связаны. Мы демонстрируем здесь, что такие отношения также существуют в гиппокампе. Была очень сильная корреляция между экспрессией рецептора GH и IGF-I (рис. 2).
C ) и обратная зависимость между присутствием мРНК GH и IGF-I. Мы также нашли доказательства того, что IGF-I регулируется эстрогеном в гиппокампе.Гиппокамп у овариэктомированных самок экспрессировал меньше GH, чем у самок с яичниками, и его уровни были аналогичны таковым в гиппокампе самцов. Однако в гиппокампе овариэктомированных самок, которым вводили эстрадиол, была повышена экспрессия мРНК GH и снизились уровни мРНК IGF-I и GHR. Эти данные согласуются с сообщениями о том, что эстроген подавляет экспрессию мРНК GHR в гиппокампе самок крыс (17). Взаимосвязь между гиппокампальным GH и IGF-I также была очевидна у интактных самок, когда они проходили различные стадии эстрального цикла.Уровни мРНК IGF-I едва обнаруживались в гиппокампе самок, находившихся в проэструсе, тогда как уровни мРНК GH были относительно высокими. Поскольку концентрация эстрогена в крови повышается во время этой стадии течки, эти данные предполагают, что эстроген регулирует ось GH / IGF-I в гиппокампе во время овуляции самок. По имеющимся данным, аналогичная взаимосвязь наблюдается в печени; эстроген подавляет экспрессию IGF-I, что затем приводит к стимуляции синтеза GH через отрицательную обратную связь оси GH / IGF-I (19).Тем не менее, учитывая динамическую природу эстрального цикла, трудно описать точную взаимосвязь между GH и IGF-I в женском гиппокампе. Однако во всех представленных здесь экспериментах, когда уровни эстрогена были повышены, уровни мРНК IGF-I были значительно снижены, а уровни мРНК GH были повышены. Эти результаты предполагают, что в женском гиппокампе индукция мРНК GH эстрогеном, вероятно, является результатом отрицательной обратной связи оси GH / IGF-I.
Стрессовый опыт изменяет экспрессию гормона роста в гиппокампе.
Представленные результаты предполагают, что GH в гиппокампе вместе с его рецептором и IGF-I сильно регулируются полом и возрастом. Однако эти данные не касаются функционального значения GH в гиппокампе. Поскольку гиппокамп необходим для многих типов обучения, кажется разумным предположить, что гиппокампальный GH также может участвовать в процессах обучения. В соответствии с этой идеей мы ранее сообщали, что зависимое от гиппокампа обучение увеличивает экспрессию GH в гиппокампе у самцов крыс (8).Несколько исследований показали, что мужчины и женщины учатся с разной скоростью и что на их способности к обучению по-разному влияют после воздействия острого стрессового опыта (20, 21). Здесь мы сообщаем, что воздействие острого стрессового опыта периодических толчков хвостом увеличивает экспрессию и производство GH в гиппокампе мужчин. Повышение, вызванное стрессом, было очевидным через 24 часа после прекращения события, что указывает на относительно стойкое влияние стрессового события на экспрессию GH.Воздействие острого стрессора увеличивало экспрессию GH у женщин, но только у тех, которые находились в диэструсе, когда произошло стрессовое событие. У этих же самок также наблюдалось снижение экспрессии IGF-I, что свидетельствует о том, что стрессовый опыт, подобный воздействию эстрогена, подавляет экспрессию IGF-I и, таким образом, увеличивает экспрессию уровня мРНК GH. Что наиболее интересно, увеличение мРНК GH у мужчин не сопровождалось снижением IGF-I. Таким образом, похоже, что индукция GH после стресса у мужчин регулируется другим механизмом, чем у женщин, и механизмом, не связанным с изменениями IGF-I.Таким образом, эти данные указывают на то, что GH не только чувствителен к возрастным и половым различиям, но также взаимодействует с двумя функциями, приписываемыми гиппокампу: одна — обучение, а другая — регулирование реакции на стресс. Как именно GH участвует в этих процессах, неизвестно и, вероятно, останется неизвестным до тех пор, пока не будут разработаны методы, которые могут блокировать экспрессию GH в отдельных областях мозга.
Потенциальная роль GH в формировании гиппокампа.
В целом, эти данные в сочетании с нашим предыдущим исследованием демонстрируют, что производство GH в гиппокампе чувствительно к стрессовым переживаниям, обучению гиппокампально-зависимой задаче памяти и уровням эстрогена.Таким образом, можно предположить, что он играет роль в нейронных процессах, связанных с настроением и познанием, как было предложено (4, 5). Если это так, эти эффекты, вероятно, будут опосредованы его влиянием на рост и развитие нейронов. Интересно, что показанные здесь манипуляции, индуцирующие GH в гиппокампе, также связаны с событиями, которые увеличивают рост анатомических структур в головном мозге. У самок в гиппокампе больше дендритных шипов, чем у самцов, особенно во время проэструса, когда уровни GH высоки (22-25).Они также производят больше новых нейронов в гиппокампе во время проэструса (26). Кроме того, стрессовый опыт изменяет плотность этих структур у мужчин по-разному, чем у женщин, в зависимости от стадии течки, как и GH (20, 21, 23, 24). Наконец, и, возможно, не случайно, все три показателя, GH, шипы и нейрогенез, увеличиваются с обучением (8, 27, 28). Таким образом, возможно, что особенности настроения и познания контролируются выработкой гормона роста в самом мозгу.
Материалы и методы
Темы.
Взрослые самцы и девственные самки крыс Sprague – Dawley (250–300 г) были получены из Zivic Laboratories и размещены индивидуально до и после операции в отделении для животных факультета психологии Университета Рутгерса. Крысы имели неограниченный доступ к воде и Purina Lab Chow (Ralston-Purina) и содержались в цикле свет-темнота 12:12 со световым началом в 7:00
.
Вагинальная цитология.
Цитологию влагалища контролировали с помощью ежедневных мазков из влагалища, полученных с 10 до 12 часов (18). Стерильные ватные палочки погружали в физиологический раствор и осторожно вводили во влагалище, удаляли рыхлые эпителиальные клетки, затем скатывали на предметное стекло. Клетки сушили, фиксировали в 95% EtOH, промывали забуференной водой, окрашивали 1% водным фильтрованным толуидиновым синим, промывали 70% забуференным EtOH и снова фиксировали в 95% EtOH. На основании цитологии влагалища крысы были разделены на четыре стадии течки: проэструс был отмечен пурпурным окрашиванием эпителиальных клеток с темными ядрами, течка — массами ороговевших клеток, окрашенных в синий цвет, диэструс 1 — многочисленными лейкоцитами и эпильтелиальными клетками и диэструс 2 — аналогичная морфология, но уменьшенное количество.Были включены только самки, у которых был стандартный эстральный цикл от 4 до 5 дней.
Замена OVX и эстрогена.
Животных анестезировали пентобарбиталом в дозе 30 мг / кг внутрибрюшинно. с добавлением ингалянта изофлурана и двусторонней овариэктомии. Яичники удаляли через небольшой разрез по средней линии брюшной стенки. После удаления яичников мышечная стенка и кожа зашиты рассасывающимся швом. После операции внутримышечно вводили 0,3 мл пенициллина (250 000 единиц на мл) и держали крысу в тепле до выхода из наркоза.В послеоперационном периоде крысам предоставляли 24-часовой доступ к ацетаминофену (32 мг / мл; IDE Interstate, Amityville, NY), разведенному 1: 100 в питьевой воде, в течение 2 дней. По крайней мере, через 5 дней выздоровления крысам вводили подкожно. с 10 мкг бензоата 17-β-эстрадиола (Sigma), растворенного в кунжутном масле. Каждую группу крыс, получавших эстроген, тестировали с отдельной группой крыс OVX, которым вводили носитель кунжутного масла. Всем крысам вводили инъекцию, а затем через 24 часа им снова вводили ту же дозу эстрадиола или носителя.Двадцать пять часов спустя всем животным вводили смертельную дозу пентобарбитала натрия, и образцы крови собирали посредством пункции сердца для анализа уровней гормонов. Кровь добавляли в пробирки, содержащие 0,1 мл гепарина, и центрифугировали 20 мин при 402 × g . Мозг иссекали, и ткань хранили на сухом льду до хранения при -80 ° C. Аликвоты плазмы хранили при -20 ° C и размораживали перед анализом. Уровни циркулирующего эстрадиола измеряли с помощью твердофазной системы RIA (Coat-A-Count; Diagnostic Products, Los Angeles).Чувствительность анализа для эстрадиола составляла 8 пг / мл, а вариабельность между анализами была <7%.
Воздействие стресса.
Самцов крыс вынули из домашней клетки и перевели в другую комнату. Их поместили в ограничительную трубку, которая находилась в темной звукопоглощающей камере. Электроды прикреплялись к хвосту, чтобы произвести 30 разрядов (1 с, 1 мА) со скоростью 1 в минуту. Сразу после этого их вернули в домашнюю клетку. Двадцать четыре часа спустя им и группе не подвергшихся стрессу контролей вводили смертельную дозу пентобарбитала натрия.Под глубокой анестезией мозг извлекали, рассекали, хранили на льду и в конечном итоге хранили при -80 ° C.
Выделение РНК и ПЦР в реальном времени.
Тотальную РНК выделяли из замороженной ткани гиппокампа с помощью реагента TRI (Sigma). КДНК первой цепи синтезировали с использованием 500 нг тотальной РНК, примированной случайными гексамерами (Promega), в качестве матрицы для обратной транскриптазы вируса миелобластоза птиц (Promega). ПЦР в реальном времени выполняли в системе определения последовательности PE Biosystems Gene Amp 7700 (Applied Biosystems) с использованием 5% кДНК, праймеров, специфичных для GH (5′-AAGAGTTCGAGCGTGCCTACATTCC-3 ‘, 5′-AGTTCTCTGCTGGGCCTCCTCCTT-3’) IGF-I (5′-TCTGAGGAGGCTGGAGATGT-3 ′, 5′-TGACGTGGCATTTTCTGTTC-3 ′) или GHR (5′-TGGACACACTGGCAGCAT-3 ′, 5′-TCCTTTGCTGCTTTGAAAATATAACTADNA-3 ′, как рекомендовано реактивами PCTADNA-3 ′), производитель (Applied Biosystems).Продукты ПЦР для GH, IGF-I и GHR имели длину 125, 194 и 119 п.н. соответственно. Отдельные пары праймеров тестировали при концентрациях 50, 250 и 500 нМ для оптимизации реакций и обеспечения отсутствия образования димеров праймеров в течение количества циклов, необходимых для количественного определения.
Данные ПЦР в реальном времени анализировали с помощью программного обеспечения Applied Biosystems sds 1.9. ПЦР для каждой кДНК выполняли одновременно и нормализовали к ПЦР с использованием праймеров для RPL39 (5′-GATCCTCGCCATGTCTTCTC-3 ‘, 5′-GCTTCGTTCTCCTCGAGTGT-3’, мРНК рибосомного белка L39).Для расчета кратного изменения экспрессии гена сначала рассчитывали значение ΔCt (Ct , образец — Ct RPL39 ) относительно RPL39 для каждой пары кДНК и праймеров. Была рассчитана относительная экспрессия генов для каждого образца 2 ΔCt . Это нормализованное значение затем использовалось для сравнения уровней экспрессии генов между образцами.
Западный анализ.
Белковые лизаты были получены путем гомогенизации ткани гиппокампа в буфере для лизиса, состоящем из 0.5% SDS, 0,5% Triton X-100, 1% Nonidet P-40, 50 мМ Трис (pH 7,5), 150 мМ NaCl, 2 мМ EDTA, 1 мМ PMSF и ингибиторы протеаз. Пятьдесят микрограммов лизата кипятили в присутствии буфера для образца SDS, образец загружали на 10-20% трис / глицин-акриламидный гель и переносили на поливинилидендифторидные мембраны для иммуноблот-анализа с использованием поликлонального козьего антикрысиного GH. антитела, полученные от Research Diagnostics (Фландрия, Нью-Джерси).
Нейронные культуры.
Нейрональные культуры получали, как описано (29).Вкратце, беременных крыс Sprague-Dawley на 18-й день эмбриона умерщвляли вдыханием CO 2 , и эмбрионы немедленно удаляли. Кортикальный слой иссекали и обрабатывали 0,25% трипсином в сбалансированном солевом растворе Хэнкса (HBSS) без кальция и магния при 37 ° C в течение 15 минут. Затем корковый слой промывали HBSS и вручную диссоциировали с помощью просверленной пипетки Пастера. Клетки высевали при концентрации 100000 на см 2 на 10-сантиметровые планшеты, покрытые поли-1-лизином, в среду для посева, содержащую DMEM и 10% FBS.После инкубации в течение ночи среду заменяли на среду Neurobasal, содержащую добавку B27 и 0,5 мМ глутамин. Через 7-10 дней in vitro первичных культур нейронов обрабатывали 100 нМ 17-β-эстрадиола в течение 24 часов.
Благодарности
Эта работа была поддержана грантом MH59970 Национальных институтов здравоохранения (T.J.S.).
Сноски
-
§ Кому следует адресовать корреспонденцию.Эл. адрес:
shors {at} rutgers.edu -
Вклад авторов: C.P.D., K.S.K. и T.J.S. спланированное исследование; C.P.D. и T.J.S. проведенное исследование; C.P.D., K.S.K. и T.J.S. внесены новые реагенты / аналитические инструменты; C.P.D. и T.J.S. проанализированные данные; и C.P.D. и T.J.S. написал газету.
-
Заявление о конфликте интересов: о конфликте интересов не сообщалось.
-
Этот документ был отправлен напрямую (Трек II) в офис PNAS.
- Сокращения:
- GH,
- гормон роста;
- GHR,
- рецептор GH;
- IGF,
- инсулиноподобный фактор роста;
- OVX,
- овариэктомия.
Сокращения:
-
Свободно доступен онлайн через опцию открытого доступа PNAS.
- © 2006 Национальная академия наук США
Frontiers | Гормон, высвобождающий гормон роста при диабете
Введение
Сахарный диабет 2 типа (СД2) — это серьезное метаболическое заболевание, от которого страдают почти 30 миллионов американцев, и ежегодно теряется около 250 миллиардов долларов из-за влияния заболеваемости и смертности на общие медицинские расходы и потерю заработной платы.СД2 связан с прогрессирующим снижением секреции инсулина бета-клетками поджелудочной железы на фоне инсулинорезистентности (1). Несмотря на его важность, мы не до конца понимаем сложное взаимодействие молекулярных сигналов и событий передачи сигналов, которые контролируют функциональность и выживаемость бета-клеток. Это ограничивает нашу способность разрабатывать новые подходы к профилактике и лечению диабета.
Бета-клеточная мембрана содержит множество рецепторов, связанных с G-белками (GPCR), которые имеют решающее значение для регуляции секреции инсулина гормонами и нейротрансмиттерами (2–4).Гормон, высвобождающий гормон роста (GHRH), является важным регулятором не только секреции гормона роста, но и множества клеточных функций во многих клетках и органах. Экспрессия рецептора, сопряженного с G-белком GHRH (GHRHR), была продемонстрирована в различных периферических тканях и типах клеток, включая островки поджелудочной железы (5, 6).
Недавние исследования демонстрируют новую способность аналогов GHRH увеличивать и сохранять секрецию инсулина бета-клетками у островков и мышей с диабетом (7, 8), что делает их потенциально полезными для лечения СД2.Замечательные результаты исследования новых агонистов GHRH для заживления ран и сердечно-сосудистой системы также могут предоставить новые методы лечения пациентов с диабетом (5, 7, 9). В этом обзоре рассматривается возможная роль GHRHR и его уникальных инженерных агонистов и антагонистов для лечения диабета и его осложнений.
GHRH и его аналоги
Гипоталамический гормон, высвобождающий гормон роста, является одним из «гуморальных факторов», который имеет решающее значение для секреции гормона роста. Открытие гипоталамических гормонов, таких как тиреотропин-рилизинг-гормон, лютеинизирующий гормон-рилизинг-гормон (также известный как гонадотропин-рилизинг-гормон), которые регулируют секрецию гормонов передней доли гипофиза, привело к присуждению Нобелевской премии (1977) одному из нас (Андрей В.Шалли) (10). GHRH, экспрессируемый в дугообразном ядре гипоталамуса и высвобождаемый в портальную сосудистую сеть, напрямую стимулирует синтез и секрецию гормона роста соматотропами гипофиза, активируя соответствующие рецепторы GHRH (5, 11). GHRHR присутствует в нескольких других тканях, таких как миокард, лимфоциты, яички, яичники, кожа и поджелудочная железа, и участвует во множестве биологических процессов (5). Роль GHRHR в других клетках и тканях продолжает изучаться. Кроме того, GHRHR был обнаружен в различных опухолевых клетках и в некоторых стволовых клетках (5, 6).
Следует отметить, что GHRH подвергается быстрой ферментативной деградации в крови. Дипептидилпептидаза IV инактивирует активную форму GHRH в крови до его более стабильного неактивного метаболита GHRH (3-44) -Nh3 (12, 13). По этой причине концентрация активного GHRH (который вырабатывается в гипоталамусе) в крови может быть незначительной и, следовательно, без значительного влияния на органы за пределами соматотропов гипофиза. Интересно, что в настоящее время ингибиторы дипептидилпептидазы IV широко используются для лечения диабета 2 типа с целью повышения концентрации GLP-1 в крови (14).Эти агенты также должны приводить к повышению концентрации GHRH в крови. Однако эта интересная возможность и влияние GHRH на различные ткани-мишени, в которых экспрессируется GHRHR, не исследовались.
Накапливающиеся данные также предполагают, что помимо нейроэндокринного действия GHRH, внегипоталамический GHRH участвует во многих периферических действиях через аутокринные / паракринные механизмы. Экзогенный GHRH может регулировать пролиферацию, выживаемость, апоптоз и дифференцировку в нескольких тканях и типах клеток (5, 15).
GHRHR является членом семейства GPCR класса II B, которое преимущественно связывается с сигнальным путем Gs-аденилатциклаза-цАМФ. Пептидные гормоны, которые активируют GPCR класса II, включают GHRH, секретин, глюкагоноподобные пептиды, желудочно-ингибирующий пептид (GIP), пептид, активирующий аденилатциклазу гипофиза, кортикотропин-рилизинг-гормон, вазоактивный кишечный пептид, паратиреоидный гормон и кальцитонин-родственный пептид. 16, 17).
Был изучен механизм острого действия GHRH на соматотроп гипофиза для увеличения синтеза и секреции гормона роста (рис. 1).Связывание GHRH с его рецептором активирует стимулирующий G-белок, который активирует аденилатциклазу с образованием цАМФ, что приводит к активации протеинкиназы A (PKA). Это стимулирует приток кальция, скорее всего, через деполяризацию плазматической мембраны и активацию чувствительных к напряжению каналов Ca 2+ . Повышенный уровень Ca 2+ и цАМФ стимулирует процесс экзоцитоза гормона роста (18–21). Например, форсколин (активатор аденилатциклазы) увеличивает приток Ca 2+ у соматотрофов, а ингибирование фосфодиэстеразы увеличивает электрическую активность соматотрофов, подтверждая важность цАМФ в действии GHRH (22).Регулируемая секреция гормона роста включает движение секреторных везикул по микротрубочкам, временную «стыковку» с клеточной мембраной и последующее высвобождение везикул (21).
Рис. 1. Механизм действия GHRH на каналы Ca 2+ и K + : связывание с системами протеинкиназы A (PKA) и протеинкиназы C (PKC) . Эта диаграмма иллюстрирует связывание каналов Ca 2+ и K + с рецепторами GHRH.Система цАМФ – PKA опосредует действие GHRH на управляемые по напряжению токи Ca 2+ , а система PKC необходима для действия GHRH на управляемые по напряжению токи K + у соматотропов. AC, аденилатциклаза; PLC, фосфолипаза C. Перепечатано с разрешения Macmillian Publishers Ltd., из ссылки (23), рисунок 11.
У соматотрофов гипофиза при связывании лиганда GHRH с GHRHR активированные вторичные мессенджеры включают не только аденилатциклазу-цАМФ-PKA и Ca 2+ -кальмодулин, но также инозитолфосфат-диацилглицерин-протеинкиназу C (PKC). , Кальциевые каналы L-типа, а также пути арахидоновой кислоты и эйкозановой кислоты, они в конечном итоге приводят к стимуляции выработки и секреции гормона роста (23-25).Повышенный уровень цАМФ также стимулирует PKA для активации белка, связывающего элемент ответа цАМФ (CREB), который стимулирует транскрипцию гена GHRHR.
Также вероятно, что функция GHRH связана со способностью стимулировать пролиферацию соматотрофных клеток. Активация киназы MAP и фосфорилирование ERK наблюдалась в гипофизе в зависимости от цАМФ / PKA / PKC (26, 27). Альтернативно, GHRH может стимулировать Ras / MAPK через βγ-субъединиц, чтобы способствовать росту клеток (26). В миокарде GHRHR-опосредованное ингибирование апоптоза включает модуляцию передачи сигналов ERK1 и ERK2 и PI3K-Akt, поскольку специфические ингибиторы ERK1 / 2 и PI3K / Akt устраняют эти эффекты (28).
Разработаны многочисленные агонисты и антагонисты GHRHR с высокой аффинностью и высокой специфичностью (9, 29–31). Имеются замечательные результаты исследований агонистов GHRH для заживления ран, кардиопротекторного действия и защиты от отека проницаемости легких, вызванного пневмолизином (5, 7, 9, 32, 33). С другой стороны, антагонисты GHRHR проявляют заметные эффекты в усилении апоптоза и уменьшении пролиферации нескольких типов раковых клеток (30, 34, 35).
Эффекты GHRH и соответствующих агонистов GHRHR на бета-клетки и островки поджелудочной железы
Инсулин вырабатывается бета-клетками поджелудочной железы на островках Лангерганса.Рецепторы GHRH описаны как в первичных, так и в клональных бета-клетках поджелудочной железы (клетки инсулиномы) и изолированных островках (7, 8, 36, 37). Человеческий GHRH может резко стимулировать секрецию инсулина из изолированных островков грызунов и диспергированных бета-клеток (38, 39) и из перфузированной поджелудочной железы собаки (40). Внутривенная инъекция человеческого GHRH крысам увеличивала плазменную концентрацию инсулина, высвобождаемого в воротную вену печени (39). В другом функциональном анализе предварительная обработка синтетическими аналогами GHRH улучшила приживление и метаболическую функцию островков после трансплантации мышам с диабетом, индуцированным стрептозотоцином (STZ) (36).Предварительная обработка островков крыс агонистом GHRH, JI-36, значительно улучшила функцию трансплантата за счет улучшения толерантности к глюкозе и увеличения резерва бета-клеток инсулина у крыс (41). Новые агонисты GHRHR с высокой аффинностью и специфичностью улучшают секрецию инсулина и сохраняют бета-клетки и островки в анализах летальности (7, 8). Основываясь на этих выводах, GHRH и соответствующий ему рецептор обладают многообещающим терапевтическим потенциалом для улучшения функции бета-клеток и, возможно, лечения T2DM.
Интересно, что открытие GHRH было частично связано с распознаванием эктопической секреции GHRH опухолями островков поджелудочной железы человека, вызывающих эктопическую акромегалию (42–45).Таким образом, GHRH был обнаружен в экстрактах ткани опухоли поджелудочной железы человека, что привело к выяснению его структуры (44). Эти данные предполагают, что, возможно, GHRH экспрессируется на низких уровнях клетками островков поджелудочной железы и, возможно, во время развития также на низких уровнях. Это предполагает, что GHRH может быть частью паракринной системы островков, но эта возможность еще не исследована. Также возможно, что GHRHR оказывает влияние на функцию клетки даже без активации рецептора посредством некоторой тонической рецепторной функции.
Несмотря на эти достижения, детали экспрессии GHRHR, сигнальных путей и функции в клетках островков поджелудочной железы до конца не выяснены. Мы рассмотрим возможные механизмы регуляции секреции инсулина, а также механизмы, относящиеся к пролиферации бета-клеток, чтобы оценить возможную роль активации GHRHR.
Основная роль бета-клеток поджелудочной железы заключается в регулировании метаболизма, ощущая изменения в концентрации глюкозы в крови и отвечая путем секреции точно регулируемых количеств инсулина.Действие гормонов и нейромедиаторов способствует такой передаче сигналов и усиливает секрецию инсулина, стимулированную глюкозой (GSIS) (46) (рис. 2). GSIS зависит от Ca 2+ и регулируется метаболическими сигналами, генерируемыми катаболизмом глюкозы. Глюкозозависимая передача сигнала начинается с захвата глюкозы бета-клетками через транспортер GLUT2. Молекулы цитоплазматической глюкозы быстро фосфорилируются глюкокиназой и превращаются в пируват в цитозоле через гликолитический путь, затем окисляются в митохондриях через цикл трикарбоновых кислот и пути окислительного фосфорилирования соответственно.Катаболизм глюкозы производит АТФ. Мембранный потенциал бета-клеток контролируется каналами K ATP . В базовых условиях открыто достаточное количество каналов K ATP , так что плазматическая мембрана гиперполяризована. Блокирование каналов K ATP с помощью АТФ-зависимого механизма инициирует деполяризацию плазматической мембраны, которая открывает потенциалзависимые каналы Ca 2+ ; Ca 2+ проникает в бета-клетку из внеклеточной среды через эти каналы и увеличивает цитоплазматический Ca 2+ .Вызванное глюкозой увеличение цитоплазматического Ca 2+ и секреции инсулина напрямую коррелируют (46, 47).
Рисунок 2. Схема сигнальных путей бета-клеток и гипотетическая роль GHRHR . Стрелки указывают на активацию или повышение концентрации. Линия, оканчивающаяся полосой, означает запрещение или закрытие. Метаболизм глюкозы увеличивает соотношение АТФ / АДФ, что приводит к закрытию каналов K ATP , снижению оттока K + , деполяризации мембраны, увеличению внутриклеточного Ca 2+ и секреции инсулина.Глюкоза также приводит к секреции инсулина через пути амплификации, которые не зависят от каналов K ATP . Стимуляция карбахолом усиливала секрецию инсулина через рецептор ацетилхолина (мускариновый) и пути фосфолипазы С. IP 3 представляет собой 1,4,5-трифосфат инозита, DAG представляет собой диацилглицерин. Как показано, как GLP-1, так и GHRH усиливают секрецию инсулина через путь цАМФ.
Бета-клеточная мембрана содержит множество GPCR, которые участвуют в регуляции секреции инсулина гормонами и нейротрансмиттерами.GPCR могут оказывать комплементарное или антагонистическое действие на секрецию инсулина (2–4). Например, стимуляция секреции инсулина пищей начинается с «головной» фазы из-за сенсорной стимуляции видом и вкусом пищи. Это в значительной степени опосредовано высвобождением ацетилхолина из нервов, иннервирующих островки поджелудочной железы. Последующая холинергическая стимуляция через мускариновый (ацетилхолиновый) GPCR приводит к активации пути фосфолипазы C (PLC) (48, 49).
Инкретиновые гормоны также играют важную роль в секреторной реакции инсулина после приема пищи.Эти гормоны оказывают значительное влияние на GSIS, прежде всего, за счет активации пути цАМФ, который также приводит к деполяризации плазматической мембраны и увеличению цитоплазматического Ca 2+ (50, 51). Например, глюкагоноподобный пептид I (GLP-1) является одним из таких мощных инкретиновых гормонов, активирующих GPCR альфа (ы), которые могут увеличивать цАМФ и активировать путь PKA в бета-клетках. Агонисты GLP-1 (и ингибиторы DPP4 для продления периода полужизни эндогенных инкретинов) успешно применяются для лечения СД2 (3, 50).
Гормон, высвобождающий гормон роста, и инкретиновые гормоны, такие как GLP-I и GIP, принадлежат к одному классу структурно родственных гормонов, которые активируют GPCR класса B. Как обсуждалось выше, эти инкретиновые гормоны активируют сигнальный путь Gs-аденилатциклаза-цАМФ, то есть этот механизм может быть идентичен механизму GHRHR в соматотрофных клетках (см. Рисунки 1 и 2). Интересно, что агонисты GHRHR значительно повышали уровни клеточного цАМФ в линии бета-клеток крыс (INS-1) (7).По этой причине разумно заключить, что агонисты GHRHR также используют механизм передачи сигналов на основе цАМФ, и, следовательно, они будут оказывать положительное влияние на секрецию инсулина и выживаемость бета-клеток (7). Также существует вероятность того, что активация пути цАМФ может привести к увеличению цитоплазматической концентрации Ca 2+ , которая может активировать PLC и, соответственно, активировать этот путь [см., Например, Ref. (4)].
Интересно, что активация пути цАМФ в бета-клетках инкретиновыми гормонами приводит к повышенной секреции инсулина частично из-за деполяризации плазматической мембраны и увеличения цитоплазматического Ca 2+ [для обзора см. Ref.(4, 52)]. Механизмы, с помощью которых GHRH увеличивает высвобождение гормона роста, также включают деполяризацию плазматической мембраны и увеличение цитоплазматического Ca 2+ (см. Выше), что также указывает на значительное сходство между механизмами GLP-1 в бета-клетках и механизмами GHRH. в соматотропах гипофиза.
Активация рецепторов GHRH также может приводить к активации транскрипции, пролиферации и выживания генов в бета-клетках. Например, механизмы пролиферации и выживания бета-клеток включают сигнальные пути ERK и Akt (53).Агонисты GHRHR активируют эти пути в различных типах клеток (см. Выше). Эксперименты на клетках инсулиномы крысы (INS-1) показали, что агонист GHRH MR-409 значительно увеличивает пролиферацию клеток и индуцирует активацию путей ERK и Akt (7).
Агонисты рецепторов, связанных с G-белком GHRH, значительно увеличивают уровни фосфорилирования CREB в линии бета-клеток крыс (INS-1) (7), а также у соматотрофов, у которых агонисты GHRHR могут стимулировать транскрипцию гена гормона роста (см. Выше) .Это также может быть похоже на один из механизмов GLP-1. Было также показано, что GLP-1 способствует пролиферации и выживанию бета-клеток у грызунов, активируя пути ERK и Akt (50). цАМФ, индуцированный GLP-1, вызывал повышенное фосфорилирование CREB / активирующего фактора транскрипции-1 в секретирующих инсулин бета-клетках (54). Однако точный режим (ы) передачи сигналов GHRHR в островках поджелудочной железы и наиболее важные механизмы стимуляции секреции инсулина и / или выживания бета-клеток неизвестны.
Причинная взаимосвязь между агонистами GHRHR и разнообразием GPCR в бета-клетках и роль таких сетей в секреции инсулина неизвестны.Недавно мы применили наш общий подход к математическому моделированию бета-клеток для GPCR бета-клеток для сравнения действия GPCR на GLP-1 и GIP (4). Оба они преимущественно связываются с сигнальным путем Gs-аденилатциклаза-цАМФ. Основываясь на этих моделях, мы предполагаем, что агонисты GHRHR могут играть ту же роль, что и GIP, во взаимодействии с GLP-1. В этом случае агонисты GHRHR могут действовать конкурентно с GLP-1 в своих механизмах стимуляции секреции инсулина. Эту проверяемую гипотезу еще предстоит напрямую продемонстрировать.
Существует несколько возможных способов влияния передачи сигналов GHRH бета-клетками поджелудочной железы на лечение СД2. Одной из основных причин СД2 является измененная сигнальная система в бета-клетках, что приводит к снижению выработки инсулина и экзоцитозу. Наши предыдущие опубликованные данные и данные нескольких других групп предполагают, что некоторые сигнальные системы в секретирующих инсулин клетках повреждены или ослаблены при диабетических состояниях. «Диабетические состояния», такие как гипергликемия и гиперлипидемия, могут привести к потере рецептора GLP-1 (GLP-1R) с поверхности клетки и, таким образом, к нарушению передачи сигналов GLP-1, что может лежать в основе снижения клинической эффективности GLP. Активаторы -1R (50, 51).Агонисты GHRHR могут иметь благоприятные эффекты в этих условиях, поскольку эти агонисты активируют тот же путь цАМФ, что и GLP-1R, при условии, что GHRHR также не подавляется. Следовательно, мы можем предположить, что гликемическая нечувствительность к агонистам GLP-1R при T2DM может быть улучшена путем одновременного или последовательного применения агонистов GHRHR, тем самым заменяя возможный дефицит GLP-1R.
Обработка Ex vivo изолированных островков агонистами GHRH также может улучшить результаты трансплантации островков на животных моделях.Предварительное кондиционирование инкапсулированных островков поджелудочной железы агонистами GHRHR значительно улучшило функцию трансплантата за счет улучшения толерантности к глюкозе и увеличения резерва бета-клеток инсулина у диабетических крыс (41). Этот эффект представляет достаточный интерес для дальнейшего изучения его при трансплантации островков человека.
Интересно, что стимулированный GHRH и антагонист GHRH ингибировали экспрессию основных антиоксидантных ферментов в линии рака простаты человека LNCaP (55). Дополнительная экспрессия основных антиоксидантных ферментов может иметь дополнительные преимущества при СД2 (56), а также при СД1 (57), и это может быть еще одним потенциально полезным эффектом агонистов GHRHR при обоих основных типах диабета.
На основании этих исследований мы предполагаем, что аналоги GHRHR обладают потенциалом для усиления функции, пролиферации и выживания бета-клеток in vivo . Дальнейшие исследования островков и бета-клеток человека помогут определить, схожи ли уровни экспрессии GHRHR и сигнальные системы в моделях человека и грызунов.
Диабет и активность GHRH за пределами бета-клеток
Замечательные результаты исследования новых агонистов GHRH для заживления ран и сердечно-сосудистой системы также могут предложить новые методы лечения пациентов с диабетом или, возможно, помочь понять задействованные пути (5, 7, 9).Антагонисты GHRHR могут воздействовать на определенные осложнения диабета, особенно при диабете 1 типа и инсулинозависимом T2DM, когда продукция инсулина бета-клетками, по крайней мере, клинически незначительна. Например, антагонизм GHRH может улучшить некоторые липидные, почечные и сосудистые осложнения диабета с низким уровнем инсулина (58). Другой потенциальной мишенью для антагонистов GHRH может быть диабетическая ретинопатия, которая является основной причиной слепоты у пациентов с диабетом и диабетической нефропатией (гломерулосклерозом) (30).Несмотря на значительные успехи в лечении и профилактике этих осложнений, они по-прежнему являются значительным компонентом долгосрочных издержек диабета.
Желудочно-кишечные эффекты также являются осложнениями диабета. На мышиной модели диабета 2 типа наблюдалась повышенная регуляция экспрессии GHRHR в клетках кишечника (58). Лечение антагонистом GHRHR, MIA-602, мешало GLP-1-зависимой дислипидемии, связанной с диабетом, у мышей. Он также снизил уровни GLP-1, глюкагона и TRL в плазме у этих мышей (58), что могло привести к ухудшению течения диабета, а не к улучшению.Перекрестная связь между антагонистом GHRHR и передачей сигналов ацетилхолина (рецептор M3) наблюдалась в аорте, где MIA-602 предотвращал связанный с диабетом блок карбахол-опосредованной вазодилатации (58).
Интересно, что человеческий GHRH может снижать высвобождение глюкагона из изолированных островков мыши (39). Мы можем объяснить это повышенной секрецией инсулина, который в данном случае подавляет секрецию глюкагона [см., Например, Ref. (59)]. Однако повышенная секреция глюкагона островковыми клетками при диабете также снижалась при применении антагониста MIA-602 (58).Снижение секреции глюкагона в этом случае можно объяснить снижением цАМФ в альфа-клетках [см., Например, Ref. (60)] посредством блокирования соответствующего рецептора GHRH, когда секреция инсулина незначительна в островках диабетических животных или людей. Снижение высвобождения глюкагона антагонистами GHRHR может иметь положительный эффект при диабете за счет снижения продукции глюкозы в печени и, возможно, уменьшения кетогенеза (59, 61).
Заключение
Этот обзор недавних данных с агонистами GHRHR показывает, что они способны резко увеличивать секрецию инсулина и увеличивать пролиферацию и выживаемость бета-клеток грызунов при системном введении.С другой стороны, модуляторы активности GHRHR могут быть полезны для облегчения некоторых осложнений диабета. В настоящее время продолжаются исследования по определению доз и режимов лечения модуляторов GHRHR для лечения других заболеваний. Результаты демонстрируют четкую связь GHRH и его рецептора с метаболизмом глюкозы и функцией бета-клеток поджелудочной железы. Мы считаем, что есть прочная основа для дальнейших исследований по оценке агонистов и / или антагонистов GHRHR как многообещающих терапевтических агентов для лечения диабета и его осложнений.
Взносы авторов
LF, NT, AS и LP проанализировали литературу, разработали работу и вместе написали и отредактировали статью.
Заявление о конфликте интересов
Авторы не имеют коммерческих или финансовых отношений, которые могли бы повлиять на редактирование настоящего обзора.
Финансирование
Эта работа была поддержана грантами LP от Национальных институтов здравоохранения (DK063493 и DK092616), а также финансированием Центра исследований и обучения диабета Чикагского университета NIH (DK020595, PI G.И. Белл). Различные исследования аналогов GHRH группой AS, цитируемых в этой рукописи, были поддержаны Службой медицинских исследований Департамента по делам ветеранов.
Сокращения
GHRH, гормон, высвобождающий гормон роста; GHRHR, рецептор, связанный с GHRH G-белком; GLP-1, глюкагоноподобный пептид 1; GLP-1R, рецептор для GLP-1; GSIS, секреция инсулина, стимулированная глюкозой; GPCR, рецептор, связанный с G-белком; К АТФ канала, АТФ-чувствительный К + каналов; ПКА, протеинкиназа А; PLC, фосфолипаза C, T2DM, сахарный диабет 2 типа.
Список литературы
1. Кан С.Е., Купер М.Э., Дель Прато С. Патофизиология и лечение диабета 2 типа: взгляды на прошлое, настоящее и будущее. Ланцет (2014) 383 (9922): 1068–83. DOI: 10.1016 / S0140-6736 (13) 62154-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Winzell MS, Ahren B. Рецепторы, связанные с G-белком, и значение функции островков для лечения диабета 2 типа. Pharmacol Ther (2007) 116 (3): 437–48.DOI: 10.1016 / j.pharmthera.2007.08.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Амистен С., Салехи А., Рорсман П., Джонс П.М., Персо С.Дж. Атлас и функциональный анализ рецепторов, связанных с G-белком, на островках Лангерганса человека. Pharmacol Ther (2013) 139 (3): 359–91. DOI: 10.1016 / j.pharmthera.2013.05.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Фридлянд Л.Е., Philipson LH. Рецепторы, связанные с G-белком бета-клеток поджелудочной железы, и взаимодействия вторичных мессенджеров: компьютерный анализ системной биологии. PLoS One (2016) 11 (5): e0152869. DOI: 10.1371 / journal.pone.0152869
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Киарис Х., Хатзистаму И., Папавассилиу А.Г., Шалли А.В. Гормон, высвобождающий гормон роста: не только нейрогормон. Trends Endocrinol Metab (2011) 22 (8): 311–7. DOI: 10.1016 / j.tem.2011.03.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Циглер К.Г., Браун Дж. В., Шалли А. В., Эрлер А., Гебауэр Л., Трезл А. и др.Экспрессия рецепторов нейропептидных гормонов в опухолях надпочечников и клеточных линиях человека: антипролиферативные эффекты аналогов пептидов. Proc Natl Acad Sci U S. A (2009) 106 (37): 15879–84. DOI: 10.1073 / pnas.0
3106
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Чжан X, Цуй Т., Хе Дж, Ван Х, Цай Р., Поповикс П. и др. Благоприятные эффекты агонистов высвобождающего гормона гормона роста на клетки INS-1 крыс и на мышей NOD / SCID, индуцированных стрептозотоцином. Proc Natl Acad Sci U S A (2015) 112 (44): 13651–6.DOI: 10.1073 / pnas.1518540112
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Шуберт У., Шмид Дж., Леманн С., Чжан XY, Моравиц Х., Блок Н.Л. и др. Трансплантации островков поджелудочной железы в надпочечник способствуют агонисты гормона, высвобождающего гормон роста. Proc Natl Acad Sci U S. A (2013) 110 (6): 2288–93. DOI: 10.1073 / pnas.1221505110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Цай Р., Шалли А.В., Цуй Т., Салонтай Л., Халмос Г., Ша В. и др.Синтез новых мощных агонистических аналогов гормона, высвобождающего гормон роста (GHRH), и оценка их эндокринной и сердечной деятельности. Пептиды (2014) 52: 104–12. DOI: 10.1016 / j.peptides.2013.12.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Шаллы А.В. Аспекты регуляции гипоталамуса гипофиза с упором на его влияние на контроль репродуктивных процессов. Нобелевская лекция, 8 декабря 1977 г. В: Линдстен Дж., Редактор. Нобелевские лекции по физиологии и медицине 1071-1980 . Сингапур: Word Scientific Publishing Co (1992). п. 405–38.
Google Scholar
11. Мэйо К.Э., Годфри П.А., Зур С.Т., Кулик Д.Д., Рахал Дж.О. Гормон высвобождения гормона роста: синтез и передача сигналов. Recent Prog Horm Res (1995) 50: 35–73.
PubMed Аннотация | Google Scholar
12. Фроман Л.А., Даунс Т.Р., Хеймер Е.П., Феликс А.М. Дипептидилпептидаза IV и трипсиноподобное ферментативное разложение гормона высвобождения гормона роста человека в плазме. J Clin Invest (1989) 83 (5): 1533–40. DOI: 10.1172 / JCI114049
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Окимура Й., Чихара К., Абэ Х., Каджи Х., Кодама Х., Кита Т. и др. Период полувыведения из плазмы и скорость метаболического клиренса экзогенного гормона роста человека, высвобождающего гормон- (1-44) -Nh3, у нормальных субъектов. Endocrinol Jpn (1986) 33 (6): 875–81. DOI: 10.1507 / endocrj1954.33.875
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14.Терапия Nauck M. Incretin: выделение общих черт и различий в способах действия агонистов рецепторов глюкагоноподобного пептида-1 и ингибиторов дипептидилпептидазы-4. Diabetes Obes Metab (2016) 18 (3): 203–16. DOI: 10.1111 / dom.12591
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Фрохман Л.А., Кинеман Р.Д. Релизинг-гормон гормона роста и развитие гипофиза, гиперплазия и туморогенез. Trends Endocrinol Metab (2002) 13 (7): 299–303.DOI: 10.1016 / S1043-2760 (02) 00613-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Мартин Б., Лопес де Матурана Р., Бреннеман Р., Валент Т., Маттсон М. П., Модсли С. Рецепторы, связанные с белком G класса II, и их лиганды в функции и защите нейронов. Neuromolecular Med (2005) 7 (1–2): 3–36. DOI: 10.1385 / NMM: 7: 1-2: 003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Холл Р.В., Торнер МО, Леонг Д.А. Внутриклеточная концентрация кальция и секреция гормона роста у отдельных соматотропов: влияние фактора высвобождения гормона роста и соматостатина. Эндокринология (1988) 122 (6): 2927–32. DOI: 10.1210 / эндо-122-6-2927
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Цанева-Атанасова К., Шерман А., ван Гур Ф., Стоилкович С.С. Механизм спонтанной и контролируемой рецепторами электрической активности у соматотрофов гипофиза: эксперименты и теория. J Neurophysiol (2007) 98 (1): 131–44. DOI: 10.1152 / jn.00872.2006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20.Лин-Су К., Вайнрайч депутат. Релизинг-гормон гормона роста (GHRH) и рецептор GHRH. Rev Endocr Metab Disord (2002) 3 (4): 313–23. DOI: 10.1023 / A: 1020949507265
CrossRef Полный текст | Google Scholar
23. Чен С., Сюй Р., Кларк И.Дж., Руан М., Лонераган К., Ро С.Г. Разнообразные внутриклеточные сигнальные системы, используемые гормоном, высвобождающим гормон роста, для регулирования потенциал-управляемых каналов Ca2 + или K в соматотропах гипофиза. Immunol Cell Biol (2000) 78 (4): 356–68.DOI: 10.1046 / j.1440-1711.2000.00917.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Muller EE, Locatelli V, Cocchi D. Нейроэндокринный контроль секреции гормона роста. Physiol Rev (1999) 79 (2): 511–607.
PubMed Аннотация | Google Scholar
25. Ян С.К., Ван К., Паркингтон Х., Чен С. Вовлечение тетродотоксин-устойчивого тока Na + и протеинкиназы С в действие гормона, высвобождающего гормон роста (GH), на первичные культивированные соматотропы из трансгенных мышей с флуоресцентным белком GH-green. . Эндокринология (2008) 149 (9): 4726–35. DOI: 10.1210 / en.2008-0405
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26. Pombo CM, Zalvide J, Gaylinn BD, Dieguez C. Гормон, высвобождающий гормон роста, стимулирует митоген-активируемую протеинкиназу. Эндокринология (2000) 141 (6): 2113–9. DOI: 10.1210 / endo.141.6.7513
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27. Цейтлер П., Сиривардана Г. Стимуляция митоген-активируемого пути протеинкиназы у соматотрофов крыс гормоном, высвобождающим гормон роста. Эндокринная (2000) 12 (3): 257–64. DOI: 10.1385 / ENDO: 12: 3: 257
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28. Граната Р., Тровато Л., Галло М.П., Дестефанис С., Сеттанни Ф., Скарлатти Ф. и др. Гормон, высвобождающий гормон роста, способствует выживанию сердечных миоцитов in vitro и защищает сердце крысы от ишемии-реперфузии. Cardiovasc Res (2009) 83 (2): 303–12. DOI: 10.1093 / cvr / cvp090
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29.Издебски Дж., Пински Дж., Хорват Дж. Э., Халмос Дж., Гроот К., Шаллы А. В.. Синтез и биологическая оценка суперактивных агонистов гормона, высвобождающего гормон роста. Proc Natl Acad Sci U S. A (1995) 92 (11): 4872–6. DOI: 10.1073 / pnas.92.11.4872
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Шаллы А.В., Варга Ю.Л., Энгель Дж.Б. Антагонисты гормона, высвобождающего гормон роста: новая новая терапия рака. Nat Clin Pract Endocrinol Metab (2008) 4 (1): 33–43.DOI: 10.1038 / ncpendmet0677
PubMed Аннотация | CrossRef Полный текст | Google Scholar
31. Заранди М., Варга Дж. Л., Шалли А. В., Хорват Дж. Э., Толлер Г. Л., Ковач М. и др. Липопептидные антагонисты гормона, высвобождающего гормон роста, с улучшенной противоопухолевой активностью. Proc Natl Acad Sci U S. A (2006) 103 (12): 4610–5. DOI: 10.1073 / pnas.0511348103
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32. Канаширо-Такеучи Р.М., Салонтай Л., Шалли А.В., Такеучи Л.М., Поповикс П., Ясбереньи М. и др.Новый терапевтический подход к сердечной недостаточности из-за инфаркта миокарда, основанный на нацеливании на рецептор гормона-рилизинг-гормона роста. Oncotarget (2015) 6 (12): 9728–39. DOI: 10.18632 / oncotarget.3303
PubMed Аннотация | CrossRef Полный текст | Google Scholar
33. Лукас Р., Шридхар С., Рик Ф. Г., Горшков Б., Умапати Н. С., Ян Г. и др. Агонист гормона, высвобождающего гормон роста, снижает вызванный пневмолизином отек проницаемости легких. Proc Natl Acad Sci U S. A (2012) 109 (6): 2084–9.DOI: 10.1073 / pnas.1121075109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
34. Letsch M, Schally AV, Busto R, Bajo AM, Varga JL. Антагонисты гормона роста-рилизинг-гормона (GHRH) подавляют пролиферацию андроген-зависимых и независимых злокачественных опухолей простаты. Proc Natl Acad Sci U S. A (2003) 100 (3): 1250–5. DOI: 10.1073 / pnas.0337496100
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35. Салонтай Л., Шаллы А.В., Попович П., Видаурре И., Кришан А., Заранди М. и др.Новые антагонисты GHRH подавляют рост злокачественной меланомы человека, восстанавливая ядерную функцию p27. Cell Cycle (2014) 13 (17): 2790–7. DOI: 10.4161 / 15384101.2015.945879
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36. Людвиг Б., Циглер К.Г., Шалли А.В., Рихтер С., Штеффен А., Джабс Н. и др. Агонист гормона, высвобождающего гормон роста, как потенциальный эффектор для выживания и пролиферации островков поджелудочной железы. Proc Natl Acad Sci U S A (2010) 107 (28): 12623–8.DOI: 10.1073 / pnas.1005098107
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Шмид Дж., Людвиг Б., Шалли А.В., Штеффен А., Циглер К.Г., Блок Н.Л. и др. Модуляция оси стресса островков поджелудочной железы гипоталамическими рилизинг-гормонами и 11-бета-гидроксистероиддегидрогеназой. Proc Natl Acad Sci U S A (2011) 108 (33): 13722–7. DOI: 10.1073 / pnas.1110965108
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Green IC, Southern C, Ray K.Механизм действия гормона, высвобождающего гормон роста, при стимуляции секреции инсулина in vitro из изолированных островков крыс и диспергированных островковых клеток. Horm Res (1990) 33 (5): 199–204. DOI: 10.1159 / 000181509
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39. Бейли С.Дж., Уилкс Л.К., Флэтт П.Р., Конлон Дж. М., Бьюкенен К.Д. Влияние гормона высвобождения гормона роста на секрецию островковых гормонов и на гомеостаз глюкозы у мышей с худым и генетически ожирением и диабетом (ob / ob) и нормальных крыс. J Endocrinol (1989) 123 (1): 19-24. DOI: 10.1677 / joe.0.1230019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
40. Хермансен К., Каппельгаард AM. Характеристика стимуляции эндокринной поджелудочной железы гормона роста, высвобождающего гормон: исследования с альфа- и бета-адренергическими и холинергическими антагонистами. Acta Endocrinol (Copenh) (1987) 114 (4): 589–94.
PubMed Аннотация | Google Scholar
41. Людвиг Б., Ротем А., Шмид Дж., Вейр Г.К., Колтон С.К., Брендель М.Д. и др.Улучшение функции островков в биоискусственной поджелудочной железе за счет увеличения поступления кислорода и агониста рилизинг-гормона гормона роста. Proc Natl Acad Sci U S A (2012) 109 (13): 5022–7. DOI: 10.1073 / pnas.1201868109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Гази А.А., Амирбайглу А., Дезфоли А.А., Саадат Н., Гази С., Поурафкари М. и др. Внематочная акромегалия, вызванная рилизинг-гормоном гормона роста. Эндокринная (2013) 43 (2): 293–302. DOI: 10.1007 / s12020-012-9790-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44.Ривье Дж., Списс Дж., Торнер М., Вэйл В. Характеристика фактора высвобождения гормона роста из опухоли островков поджелудочной железы человека. Nature (1982) 300 (5889): 276–8. DOI: 10.1038 / 300276a0
CrossRef Полный текст | Google Scholar
45. Шибасаки Т., Шизуме К., Масуда А., Накахара М., Хизука Н., Миякава М. и др. Ответ гормона роста плазмы на фактор высвобождения гормона роста у пациентов с акромегалией. J Clin Endocrinol Metab (1984) 58 (1): 215–7. DOI: 10.1210 / jcem-58-1-212
PubMed Аннотация | CrossRef Полный текст | Google Scholar
47.Гилон П., Чае Х.Й., Раттер Г.А., Равье М.А. Передача сигналов кальция в бета-клетках поджелудочной железы в здоровом состоянии и при диабете 2 типа. Cell Calcium (2014) 56 (5): 340–61. DOI: 10.1016 / j.ceca.2014.09.001
CrossRef Полный текст | Google Scholar
48. Арен Б., Холст Дж. Дж. Головной инсулиновый ответ на прием пищи у людей зависит как от холинергических, так и нехолинергических механизмов и важен для постпрандиальной гликемии. Диабет (2001) 50 (5): 1030–8. DOI: 10.2337 / диабет.50.5.1030
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Сейно Ю., Мики Т., Фудзимото В., Янг Ли Е., Такахаши Ю., Минами К. и др. Секреция инсулина в головной фазе не зависит от канала KATP. J Endocrinol (2013) 218 (1): 25–33. DOI: 10.1530 / JOE-12-0579
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51. Раджан С., Диксон Л.М., Мэтью Э., Орр С.М., Элленбрук Дж. Х., Филипсон Л. Х. и др. Хроническая гипергликемия подавляет передачу сигналов рецептора GLP-1 в бета-клетках поджелудочной железы через протеинкиназу А. Mol Metab (2015) 4 (4): 265–76. DOI: 10.1016 / j.molmet.2015.01.010
CrossRef Полный текст | Google Scholar
53. Виджесекара Н., Кришнамурти М., Бхаттачарджи А., Сухаил А., Суини Дж., Уилер МБ. Фосфорилирование ERK и Akt, индуцированное адипонектином, защищает от апоптоза бета-клеток поджелудочной железы и увеличивает экспрессию и секрецию гена инсулина. J Biol Chem (2010) 285 (44): 33623–31. DOI: 10.1074 / jbc.M109.085084
PubMed Аннотация | CrossRef Полный текст | Google Scholar
54.Malm HA, Mollet IG, Berggreen C, Orho-Melander M, Esguerra JL, Goransson O, et al. Регуляция транскрипции кластера miR-212 / miR-132 в секретирующих инсулин бета-клетках с помощью регулируемого цАМФ транскрипционного коактиватора 1 и солевых киназ. Mol Cell Endocrinol (2016) 424: 23–33. DOI: 10.1016 / j.mce.2016.01.010
CrossRef Полный текст | Google Scholar
55. Барабутис Н, Шаллы А.В. Антиоксидантная активность антагонистов гормона роста-рилизинг-гормона в линии рака простаты человека LNCaP. Proc Natl Acad Sci U S A (2008) 105 (51): 20470–5. DOI: 10.1073 / pnas.0811209106
PubMed Аннотация | CrossRef Полный текст | Google Scholar
56. Фридлянд Л.Е., Philipson LH. Вызывает ли сам глюкозозависимый механизм секреции инсулина окислительный стресс в бета-клетках поджелудочной железы? Диабет (2004) 53 (8): 1942–8. DOI: 10.2337 / диабет.53.8.1942
PubMed Аннотация | CrossRef Полный текст | Google Scholar
57. Padgett LE, Broniowska KA, Hansen PA, Corbett JA, Tse HM.Роль активных форм кислорода и провоспалительных цитокинов в патогенезе диабета 1 типа. Ann N Y Acad Sci (2013) 1281: 16–35. DOI: 10.1111 / j.1749-6632.2012.06826.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
58. Ромеро М.Дж., Лукас Р., Доу Х., Шридхар С., Чикора И., Мозиери Е.М. и др. Роль рилизинг-гормона гормона роста в дислипидемии, связанной с экспериментальным диабетом 1 типа. Proc Natl Acad Sci U S. A (2016) 113 (7): 1895–900.DOI: 10.1073 / pnas.1525520113
PubMed Аннотация | CrossRef Полный текст | Google Scholar
59. Фридлянд Л.Е., Philipson LH. Вычислительный системный анализ факторов, регулирующих секрецию глюкагона альфа-клетками. Островки (2012) 4 (4): 262–83. DOI: 10.4161 / isl.22193
CrossRef Полный текст | Google Scholar
60. Elliott AD, Ustione A, Piston DW. Соматостатин и инсулин опосредуют ингибированную глюкозой секрецию глюкагона в альфа-клетках поджелудочной железы путем снижения цАМФ. Am J Physiol Endocrinol Metab (2015) 308 (2): E130–43. DOI: 10.1152 / ajpendo.00344.2014
CrossRef Полный текст | Google Scholar
Основы дефицита гормона роста
Дефицит гормона роста — это состояние, при котором организм не вырабатывает достаточное количество гормона роста. Другие названия дефицита гормона роста: карликовость и карликовость гипофиза .
Гормон роста — соматотропин — это гормон, предназначенный для стимуляции роста и размножения клеток в организме.Этот гормон вырабатывается гипофизом, который находится в основании вашего мозга, а затем попадает в кровь.
Когда гипофиз не производит достаточного количества гормона роста, ваш рост может замедлиться.
Хотя дефицит гормона роста чаще встречается у детей, он может развиться у любого человека.
Если он присутствует при рождении, это называется врожденный дефицит гормона роста . Однако у вас также может развиться дефицит гормона роста в детстве или во взрослом возрасте в результате травмы, такой как тяжелая травма головного мозга, или другого заболевания.Когда дети или взрослые приобретают это состояние, это называется приобретенным дефицитом гормона роста .
В зависимости от того, когда вы его разовьете, дефицит гормона роста может иметь разные последствия.
Дефицит гормона роста у детей
Поскольку гормон роста имеет решающее значение для нормального роста и развития, дети с дефицитом гормона роста обычно ненормально короче, чем дети без этого заболевания. Кроме того, у многих детей с дефицитом гормона роста период полового созревания часто откладывается, а у некоторых может вообще не наступить половая зрелость.
Помимо физического развития, гормон роста также важен для нормальной работы мозга.
Дефицит гормона роста у взрослых
Даже когда мы перестаем расти, нам все еще нужен гормон роста. Он необходим для поддержания необходимого количества жира, мышц, тканей и костей в нашем организме.
Взрослые с дефицитом гормона роста часто имеют низкую плотность костей и уменьшенную мышечную массу, а также психические и эмоциональные симптомы, такие как усталость, депрессия и плохая память.Прочтите нашу статью о симптомах дефицита гормона роста, чтобы узнать о других признаках дефицита гормона роста.
Если дефицит гормона роста не диагностируется или не лечится, это может привести к другим состояниям, таким как повышение уровня холестерина ЛПНП (плохого) и остеопороз.
Но каковы причины и как лечить дефицит гормона роста? В этой серии статей рассматриваются эти вопросы и подробно рассказывается о дефиците гормона роста.
Обновлено: 29.10.14
Симптомы дефицита гормона роста
Гормон роста человека произведен в лаборатории
САН-ФРАНЦИСКО, янв.6. Гормон, отвечающий за рост человеческого тела, был впервые синтезирован группой ученых-фундаментальных исследователей из Медицинского центра Калифорнийского университета. Это самая большая молекула, которую когда-либо собирали ученые в лаборатории.
Д-р Филип Р. Ли, ректор университета, объявил об этом достижении сегодня на новостной конференции, назвав это одним из самых значительных достижений в истории фундаментальных исследований. Он сказал, что открытие имело огромные возможности в таком широком диапазоне областей, что «просто невозможно предсказать, куда оно пойдет.”
Исследовательскую группу возглавил доктор Чо Хао Ли, 57-летний профессор биохимии и директор Лаборатории исследования гормонов в медицинской школе. Доктор Ли был пионером в исследованиях гормонов более 30 лет. Он выделил и очистил восемь из 10 гормонов передней доли гипофиза и определил структуру семи.
Гормон роста человека выполняет множество функций в организме человека. В молодости это заставляет людей расти. Он вырабатывается организмом в больших количествах на протяжении всей жизни, хотя в большинстве случаев рост прекращается в подростковом возрасте.
В подростковом возрасте выработка гормона роста уменьшается, но не прекращается. GH, известный как гормон роста человека, способствует постоянному развитию и увеличению всех людей. Телесный Нас подает в суд и увеличивает размер и количество всех клеток тела.
Однако некоторые эксперименты на животных показали, что GH делает гораздо больше, чем просто стимулирует и поддерживает рост. GH, вероятно, помогает восстанавливать переломы костей, способствует заживлению ран, снижает уровень холестерина в крови, повышает сопротивляемость инфекциям, стимулируя выработку антител, и благоприятно реагирует на мужские и женские половые гормоны, заставляя их работать более эффективно.
Доктор Ли и его сотрудники изолировали человека. гормон роста в 1956 г. и определил его структуру в 1966 г. Последние четыре года были посвящены его синтезу.
Сегодня утром на пресс-конференции; Доктор Ли сравнил. задача синтеза для строительства дорог и мостов. По его словам, каждый участок дороги должен быть завершен, прежде чем можно будет проехать весь маршрут, и иногда здесь и там нужны мосты, чтобы все было гладко.
Молекула гормона роста человека состояла из 188 отдельных частей, каждую из которых нужно было сначала идентифицировать, а затем положить в нужное место вдоль дороги.Затем, по словам д-ра Ли, было определено, что необходимы две связи или мосты. чтобы сделать дорогу полной. Их «приклеивали» на место серным соединением.
Самой крупной таблеткой, созданной руками человека для синтеза GH доктора Ли, был фермент длиной 124 «кусочка». Каждый кусок представляет собой аминокислотный остаток или кусок белка.
Синтетический гормон роста однажды может сыграть роль в борьбе с раком, сказал доктор Ли. Если человек способен синтезировать гормон роста; он сказал, можно также синтезировать гормон против роста.Он продолжил, что любое вещество, препятствующее росту, может оказаться полезным при лечении рака.
Гормон роста человека вырабатывается гипофизом, который расположен ниже центра мозга и прикреплен к нему тонкой ножкой. Гипофиз весит одну шестидесятую унции и размером примерно с кончик мизинца. Он состоит из трех частей — передней, задней и средней. В передней части вырабатывается гормон роста человека.
Питутитери, особенно его передняя часть, часто называют главной железой, потому что большинство гормонов, которые она выделяет, говорят другим железам, вырабатывающим гормоны, что делать.В каком-то смысле это директор всей химической фабрики тела.
Но это не абсолютный указатель. Существует система железистой обратной связи, которая сообщает гипофизу, когда он вырабатывает слишком много или слишком мало определенного гормона. Подобно автоматическому термостату, в печи тело поддерживает баланс гормонов, отправляя сообщения обратно в главный гипофиз, чтобы поддерживать идеальный баланс.
Когда что-то выходит из равновесия, конечно, возникает проблема.Если гипофиз не функционирует должным образом, может иметь место перепроизводство или недопроизводство любого гормона, включая GH. Слишком мало GH вызывает состояние, известное как гипофизарный карликовость. Синтез ГР, проведенный доктором Ли, обещает помочь примерно 5000 жертвам этого состояния в Соединенных Штатах,
До сих пор очень немногим гипофизарным карликам можно было помочь с помощью инъекций ГР из-за острой нехватки природного гормона. Из каждой донорской железы можно получить около четырех миллиграммов гормона роста, полученного из трупов.
Среднее лечение гипофизарного карлика, однако в том числе количество гормона роста человека, обнаруженного в 650 железах.
Д-р Ли сказал, что он верит, что синтетический гормон будет работать для лечения гипофизарного карликовости, и что это было просто вопросом времени, когда производители химикатов начали производить его в больших масштабах.
Слишком много GH вызывает гигантизм, если перепроизводство происходит до подросткового возраста. Состояние можно изменить, бомбардируя гипофиз пучком атомных частиц или полностью удаляя железу.Одной из известных жертв этого состояния был Роберт Уодлоу из Олтона, III, рост 8 футов 10 дюймов и обувь 37-го размера.
Избыточное производство гормона роста может начаться и после подросткового возраста, и в этом случае заболевание называется акромегалией. его симптомы — утолщение костей (но не удлинение, поскольку кости устанавливаются после определенного возраста) и удлинение мягких костей, таких как нижняя челюсть, руки и ноги. Его тоже можно лечить путем удаления гипофиза или атомной бомбардировки.
Человеческий гормон роста способствует росту за счет увеличения скорости синтеза белков и других клеточных элементов, но ученые пока не знают, как он справляется с этой задачей.
Одна теория утверждает, что GH может играть роль в изменении ситоподобного действия клеточных мембран. Теория утверждает, что как только GH покрывает клетку, он изменяет мембрану и позволяет большему количеству аминокислот и других важных элементов проникать в клетку в больших количествах.