Аэробные нагрузки
Аэробные нагрузки сжигают жир
Правда, жир начинает сгорать не сразу, а только когда истощаются запасы гликогена. Первые 20 минут тренировки жир почти не сгорает и только после 40 минут тренировки жир становится основным источником энергии!
Во время аэробных тренировок расходуется много калорий
В результате, при соблюдении диеты, можно похудеть. В чем же подвох? Казалось бы, бегай 40 минут в неделю и худей. Но дело в том, что организм очень быстро привыкает к аэробным нагрузкам. Через 2 недели Вы будете тратить на получасовую пробежку намного меньше калорий, чем вначале.
Похудеть, используя только аэробные упражнения, крайне тяжело
Если в течение первого месяца, при условии регулярных тренировок и соблюдении диеты, вы и можете потерять 2-3 кг, то дальше процесс затормозится.
Если же говорить о «чисто» аэробных тренировках, то они способствуют не только сгоранию жира, но и потере мышечной массы, что крайне нежелательно. «Больше» не всегда значит «лучше». С аэробными упражнениями важно не перестараться! Избыток аэробных упражнений воспринимается организмом как шок, вызывая гормональную реакцию, приводящую к распаду мышечной ткани. Если подробней, повышается уровень кортизола, вызывающего распад мышц и понижается уровень тестостерона, ответственного за их рост.
В то же время, очевидна польза умеренных аэробных упражнений для здоровья:
- Повышают общую выносливость организма
- Предупреждают сердечно — сосудистые заболевания
- Снижают уровень холестерина
- Повышают уровень гемоглобина
- Улучшают состояния центральной нервной системы
- Повышают иммунитет
- Помогают очищению организма от шлаков
- Способствуют очищению кожи
Автор материала: персональный тренер групповых программ Казанцев Сергей
Остеопороз (потеря костной массы) является широко распространенным заболеванием.

Что такое остеопороз
Остеопороз, также известный как потеря костной массы, является метаболическим заболеванием скелета, при котором кости теряют свою прочность. Они становятся пористыми и хрупкими. Заболевание протекает бессимптомно. Первым симптомом может стать перелом позвоночника или шейки бедра.
По данным Всемирной организации здравоохранения (ВОЗ), остеопороз является одним из самых распространенных заболеваний нашего времени. Остеопорозом страдает приблизительно каждая четвертая женщина старше 50 лет. Частота остеопороза превышает частоту рака молочной железы, инсульта и инфаркта.1
Основная задача для врачей и пациентов — как можно быстрее выявить заболевание. Если остеопороз диагностируется на ранней стадии, его проявления можно эффективно устранить, хотя излечение пока что невозможно.
Физические упражнения и здоровое питание (витамин D и кальций) являются эффективными мерами Предшественником остеопороза является остеопения (уменьшение плотности кости).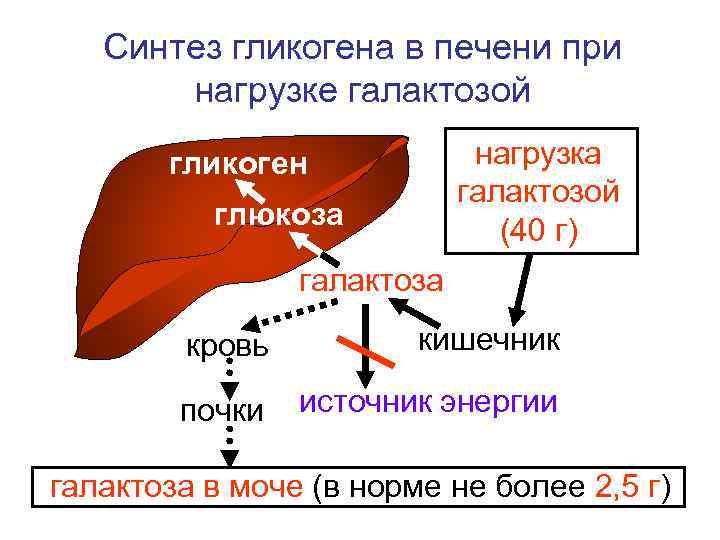 При регулярном наблюдении и выполнении рекомендаций врача остеопения может никогда не перейти в остеопороз. В случае прогрессирования возникает остеопороз и необходимость снова посетить врача, чтобы он назначил соответствующую терапию.
При регулярном наблюдении и выполнении рекомендаций врача остеопения может никогда не перейти в остеопороз. В случае прогрессирования возникает остеопороз и необходимость снова посетить врача, чтобы он назначил соответствующую терапию.
Как развивается остеопороз?
Некоторые считают, что кости — это прочные структуры, не подверженные изменениям. На самом деле, это не так. Кость постоянно обновляется путем посредством одновременного разрушения костного вещества и образования нового. Гормоны, витамины и другие активные вещества контролируют этот процесс (ремоделирование кости). В юности и молодости процесс костеообразование преобладает над разрушением. С возрастом образование кости замедляется. После смещения равновесия в сторону разрушения костной ткани кость постепенно утрачивает свою прочность.
Оценить плотность костей можно с помощью специального исследования — денситометрии.
Остеопороз разделяют на две формы: первичный и вторичный.
Первичный остеопороз
Первичный остеопороз
Приблизительно 95 % случаев потери костной массы обусловлено первичным остеопорозом.
Остеопороз I типа:
Первый тип остеопороза развивается у женщин в постменопаузе (постменопаузальный остеопороз). При данном типе остеопороза переломам наиболее подвержены позвонки.
Остеопороз II типа:
Остеопороз II типа обычно возникает после 70 лет (сенильный остеопороз). При данном типе остеопороза чаще всего ломаются позвонки, бедренные кости и кости предплечья.
Факторы риска первичного остеопороза:
- Старение
- Изменение гормонального фона (позднее менархе, ранняя менопауза)
- Гиподинамия
- Длительный период иммобилизации
- Дефицит массы тела
- Диета с недостаточным поступлением кальция или диета с высоким потреблением фосфатов (еда в сетях быстрого питания, сладкие газированные напитки)
- Злоупотребление алкоголем, кофе
- Курение
Вторичный остеопороз
Вторичный остеопороз
Вторичный остеопороз возникает в результате других заболеваний или является побочным действием определенных медикаментозных препаратов:
- Противовоспалительные гормональные препараты для лечения астмы или ревматизма (кортизон)
- Нарушения гормональной регуляции, например гипертиреоз
- Опухолевые заболевания
Факторы риска вторичного остеопороза:
- Длительный прием гормональных препаратов (астма, ревматизм)
- Длительный прием производных кумарина (маркумар)
- Систематическое нарушение работы желудочно-кишечного тракта, в том числе при заболеваниях поджелудочной железы, кишечника, печени
- Хронические заболевания почек
- Нарушение обмена гормонов щитовидной железы (гипотиреоз) и поджелудочной железы (диабет)
- Онкологические заболевания
Диагностика остеопороза
Правильно и быстро поставленный диагноз имеет решающее значение для немедленного начала лечения. Поэтому рекомендуется регулярно посещать врача и проводить скрининговые исследования (денситометрия) при наличии факторов риска. Это касается женщин в постменопаузе, а также мужчин пожилого и старческого возраста. Всякий раз при наличии подозрений на снижение костной массы эти подозрения должны быть подтверждены или опровергнуты инструментальными методами диагностики. Симптомами, позволяющими заподозрить остеопороз, являются:
Поэтому рекомендуется регулярно посещать врача и проводить скрининговые исследования (денситометрия) при наличии факторов риска. Это касается женщин в постменопаузе, а также мужчин пожилого и старческого возраста. Всякий раз при наличии подозрений на снижение костной массы эти подозрения должны быть подтверждены или опровергнуты инструментальными методами диагностики. Симптомами, позволяющими заподозрить остеопороз, являются:
- снижение роста и формирование гиперкифоза грудного отдела позвоночника (горб)
- выраженные хронические боли в спине или грудине
- Переломы костей без видимых причин, особенно переломы позвоночника под тяжестью собственного веса
Профилактика остеопороза
Существуют различные способы замедлить процесс разрушения костной ткани. Профилактику остеопороза нужно начинать уже в юности, когда есть возможность сформировать более массивные кости, на ослабление которых спустя десятилетия потребуется дополнительное время. К профилактическим мерам относятся:
Профилактику остеопороза нужно начинать уже в юности, когда есть возможность сформировать более массивные кости, на ослабление которых спустя десятилетия потребуется дополнительное время. К профилактическим мерам относятся:
- регулярная гимнастика и умеренные мышечные тренировки (специальные упражнения для тренировки разных групп мышц замедляют потерю костной массы),
- здоровое и сбалансированное питание с достаточным потреблением витаминов, белков и кальция.
Комбинация физической активности и правильного питания позволяет на долгие годы сохранить кости и мышцы здоровыми.
Лечение остеопороза
Лечение остеопороза направлено на улучшение качества жизни пациентов. Терапия заключается в комбинировании нескольких подходов, которые профильными специалистами объединены в клинические рекомендации по остеопорозу. Эффективная терапия остеопороза должна быть многокомпонентной:
Медикаментозная терапия
Для лечения остеопороза используются следующие группы препаратов:
СМРЭ
СМРЭ (селективные модуляторы рецепторов эстрогена) по своей химической структуре похожи на гормон эстроген, выработка которого понижается после наступления менопаузы. СМРЭ активизируют рецепторы эстрогена и увеличивают образование костной ткани. При этом данная группа препаратов в отличие от эстрогена не повышает риск рака молочной железы и сердечно-сосудистых заболеваний.
СМРЭ активизируют рецепторы эстрогена и увеличивают образование костной ткани. При этом данная группа препаратов в отличие от эстрогена не повышает риск рака молочной железы и сердечно-сосудистых заболеваний.
Бифосфонаты
Бисфосфонаты замедляют деградацию костной ткани и таким образом замедляют процесс потери костной массы.
Кальций и витамин D
Кальция и витамин D. Кальций является основным элементом минерального компонента костной ткани. Он должен поступать в организм в достаточном количестве с питанием. При недостаточном потреблении кальция рекомендуется прием препаратов кальция. Витамин D облегчает всасывание кальция из желудочно-кишечного тракта и встраивание элемента в структуру кости.
Паратиреоидный гормон / терипаратид
Паратиреоидный гормон / терипаратид стимулирует образование остеобластов и повышает их активность. Остеобласты — это специальные клетки, ответственные за образование костной и ремоделирование костной ткани.
Остеобласты — это специальные клетки, ответственные за образование костной и ремоделирование костной ткани.
Анальгетики
Обезболивающие препараты уменьшают боль непосредственно после переломов (в остром периоде) и облегчают хроническую боль, возникающую в результате переломов позвонков. Как известно, боль ограничивает активность, поэтому пациенты с остеопорозом должны получать адекватную обезболивающую терапию.
Двигательный режим
Физические упражнения являются методом лечения остеопороза. Специальные физические упражнения, разработанные специалистами по лечебной физкультуре и врачами, повышают двигательную активность, улучшают функциональное состояние мышц и координацию, положительно влияют на общее эмоциональное состояние.
Лечебная гимнастика, особенно упражнения на тренировку силы мышц туловища, должны выполняться постоянно.
Специальный тренажер-корректор, работающий по принципу биологической обратной связи, поддерживает позвоночник в физиологическом положении и тренирует мышцы брюшного пресса и спины. В дополнение к лечебной физкультуре пациентам с остеопорозом рекомендуются следующие виды физической активности:
Идеальным сочетанием является сочетание тренировок силы и выносливости. Чем больше мышечная масса, тем лучше прогноз относительно качества костной ткани.
Упражнения на свежем воздухе особенно эффективны, так как солнечный свет стимулирует естественное образование в коже витамина D.
Важная информация: Пациенты с остеопорозом всегда должны согласовывать с врачом уровень своей физической активности и упражнения лечебной физкультуры.
Силовые тренировки способствует формированию костной ткани
Силовые тренировки создают биомеханические и биохимические стимулы для образования костной ткани. Одновременно, эти упражнения способствуют формированию хорошей осанки. Сильные мышцы работают гармонично и скоординировано.
Одновременно, эти упражнения способствуют формированию хорошей осанки. Сильные мышцы работают гармонично и скоординировано.
Тренажер-корректор Spinomed при правильном использовании также тренирует мышцы. Система ремней и алюминиевая шина создают усилие, которое стимулирует собственную мускулатуру. Таким образом, изделие работает практически на подсознательном уровне. Использование Spinomed согласовывается с клиническими рекомендациями по лечению остеопороза.3
Планирование тренировок
Идеальным является сочетание разных видов спортивной активности. В результате повышается мышечная масса, улучшается качество кости, общее состояние и чувство равновесия. Подобрать подходящие Вам виды спорта и физические упражнения поможет лечащий врач или врач лечебной физкультуры.
Функциональное ортезирование
Работа костной и мышечной систем тесно связана, поэтому обычно происходит одновременная потеря костной и мышечной массы.
По это причине лечение переломов позвоночника должно быть функциональным, а не только медикаментозным. Перелом позвонка резко увеличивает вероятность последующего перелома и является причиной хронической боли, низкой физической активности и связанной с этим потерей мышечной массы. Современные средства реабилитации при переломе позвоночника одновременно тренируют мышцы и исправляют осанку одновременно.
В прошлом практиковалась иммобилизация после переломов позвоночника в жестких корсетах, но это приводило лишь к прогрессированию остеопороза. В настоящее время от использования жестких корсетов при переломах позвоночника на фоне остеопороза отказывается все большее число врачей, ведь есть современные средства, например тренажер-корректор Spinomed.
Продукция medi: ортезирование при остеопорозе
Переломы позвонков при остеопорозе сопровождаются хроническими болями в спине, что сильно ограничивает двигательную активность пациентов и ведет к еще большему прогрессированию заболевания. Тренажер-корректор Spinomed тренирует мышцы и уменьшает болевые ощущения, что было подтверждено в проведенных клинических исследованиях.4,5
Тренажер-корректор Spinomed тренирует мышцы и уменьшает болевые ощущения, что было подтверждено в проведенных клинических исследованиях.4,5
Эффективность Spinomed и Spinomed active подтверждена в нескольких клинических исследованиях 5,6:
- сила мышц живота и туловища увеличивается на 73 и 56 %, соответственно,
- уменьшается отклонение тела от вертикальной оси на 25 %,
- происходит уменьшение угла грудного гиперкифоза на 11 %,
- происходит уменьшение интенсивности боли на 47 %,
- физическая активность становится более комфортной — на 18 %,
- дыхательная функция легких улучшается на 19 %.
Тренажер-корректоры Spinomed и Spinomed active разработаны профессором Гельмутом Ф. Минне (Helmut W. Minne) в сотрудничестве с компанией medi. Spinomed по дизайну схож с рюкзаком. Spinomed active выполнен в виде боди и может использоваться под верхней одеждой. Все модели Spinomed оказывают свое действие по принципу обратной биологической связи.
Источники
1 Epidemiologie der Osteoporose: Bone Evaluation Study, Deutsches Ärzteblatt 2013,4, 52 ff.
2 Hadji P et al. Dtsch Arztebl Int 2013;110(4):52–57.
3 Лесняк О.М., Беневоленская Л.И. Остеопороз. Диагностика, профилактика и лечение. Клинические рекомендации. Изд. 2-е. — М.: «ГЕОТАР-МЕД», 2010.
4 Pfeifer M et al. Die Wirkungen einer neu entwickelten Rückenorthese auf Körperhaltung, Rumpfmuskelkraft und Lebensqualität bei Frauen mit postmenopausaler Osteoporose. Eine randomisierte Studie. Am J Phys Med Rehabil 2004;83(3):177-186.
5 Pfeifer M et al. Die Wirkungen von zwei neu entwickelten Rückenorthesen auf Rumpfmuskelkraft, Körperhaltung und Lebensqualität bei Frauen mit postmenopausaler Osteoporose. Eine randomisierte Studie. Am J Phys Med Rehabil 2011;90(5):805-815.
Советы по продукции
Тренажер-корректор для лечения остеопороза
medi Spinomed
Диагностика и лечение
Типы, причины и лечение болей в спине
Боль в спине
Сдать анализ на миоглобин в крови, цена в Лаборатории KDL
Миоглобин – белок, содержащийся в сердце и скелетных мышцах. Он задерживает кислород в мышечных клетках, позволяя им вырабатывать энергию, необходимую для сокращения мышц. При повреждении сердца или скелетных мышц миоглобин выделяется в кровь, где циркулирует в течение нескольких часов. Затем он отфильтровывается из крови почками и выводится из организма с мочой. Большая концентрация миоглобина токсична для почек, и при серьезных травмах выброс миоглобина в кровь может привести к почечной недостаточности.
Он задерживает кислород в мышечных клетках, позволяя им вырабатывать энергию, необходимую для сокращения мышц. При повреждении сердца или скелетных мышц миоглобин выделяется в кровь, где циркулирует в течение нескольких часов. Затем он отфильтровывается из крови почками и выводится из организма с мочой. Большая концентрация миоглобина токсична для почек, и при серьезных травмах выброс миоглобина в кровь может привести к почечной недостаточности.
Миоглобин может быть использован как вспомогательный тест при диагностике инфаркта миокарда, однако он не является специфичным для этого заболевания, поскольку он выделяется в кровь при повреждении любых мышц. Одна из распространенных причин резкого повышения миоглобина в крови – рабдомиолиз, стремительный распад мышечной ткани. Он может быть вызван тяжелыми травмами (например, при автокатастрофе), поражении электрическим током, ожогами, тромбозом, интоксикации, некоторыми инфекциями (ВИЧ, грипп, стрептококк), неконтролируемым диабетом, гипо- и гипертиреозом, мышечными дистрофиями на поздних стадиях.
В каких случаях обычно назначают исследование?
- При травмах, ранениях, ожогах, других серьезных повреждениях мышц;
- При диагностике мышечной дистрофии;
- При подозрении на инфаркт миокарда вместе с анализом на тропонин и креатинкиназу-МВ.
Что именно определяется в процессе анализа?
Происходит измерение концентрации миоглобина в образце сыворотки крови пациента методом иммунотурбидиметрии/
Что означают результаты теста?
Содержание миоглобина в крови здорового человека ничтожно. Повышение уровня этого вещества указывает на повреждение мышечной ткани и может быть вызвано инфарктом миокарда, травмой, ранением, судорогами, хирургическими вмешательствами. Миоглобин повышается при рабдомиолизе, мышечных дистрофиях и миозитах (воспаление скелетных мышц).
Для оценки функции почек при повышении миоглобина в крови в некоторых случаях измеряют также концентрацию миоглобина в моче. Чем выше его уровень в моче, тем серьезнее риск развития острой почечной недостаточности и отказа почек. Помимо травм и других вышеописанных причин, миоглобин в моче может повышаться после чрезмерной физической активности у нетренированных спортсменов, при вирусных инфекциях, воздействии токсинов или лекарственных препаратов.
Сроки выполнения теста.
Обычно результат анализа можно получить на следующий день после взятия крови.
Как подготовиться к анализу?
Следует придерживаться общих правил подготовки к взятию крови из вены. С подробной информацией можно ознакомиться в соответствующем разделе статьи.
Креатинин — Клиника 1
Креатинин – это продукт неферментативного распада креатина и креатина фосфата, образующийся в мышцах. Он выводится из организма почками.
Креатин входит в цикл, обеспечивающий организм энергией для сокращения мышц. После 7 секунд интенсивной физической активности креатинфосфат превращается в креатин, затем переходящий в креатинин, фильтрующийся в почках и выделяющийся с мочой. Креатин и креатинин стабильно продуцируются нашим телом в постоянном количестве. Почти весь креатинин выделяется почками, поэтому его концентрация в крови является хорошим показателем их функции. Количество продуцируемого креатинина зависит от общей массы тела и, в частности, мышечной массы. Поэтому, например, уровни креатинина у мужчин будут значительно выше, чем у женщин и детей.
Для чего используется исследование?
- Для оценки функции почек.
- Для оценки функции основных органов и систем (в комплексе с другими исследованиями).
- Для оценки нарушения функции почек и эффективности его лечения, если креатинин или мочевина выходят за пределы нормы и у пациента есть какое-то основное хроническое заболевание, например диабет, течение которого влияет на состояние почек.
- Если известен уровень креатинина в крови и в моче, можно подсчитать клиренс креатинина (проба Реберга) – этот тест показывает, насколько эффективно почки фильтруют из крови маленькие молекулы, такие как креатинин.
- Для подсчета скорости клубочковой фильтрации, чтобы подтвердить повреждения почек.
Когда назначается исследование?
- Через определенные промежутки времени при уже известном заболевании почек или заболевании, способном вызвать ухудшение функции почек (совместно с тестом на мочевину и на микроальбуминурию).
- При диагностике заболеваний скелетных мышц.
- Перед проведением процедуры гемодиализа и после нее.
- При симптомах дисфункции почек:
- слабость, утомляемость, снижение внимания, плохой аппетит, проблемы со сном,
- отеки на лице, запястьях, лодыжках, асцит,
- пенистая, красного или кофейного цвета моча,
- снижение диуреза,
- проблемы с актом мочеиспускания: жжение, прерывистость, изменение частоты (преобладание ночного диуреза),
- боль в поясничной области (особенно по бокам от позвоночника), под ребрами,
- высокое давление.
- При любых патологических состояниях, сопровождающихся дегидратацией.
- При подготовке к компьютерной томографии.
- Перед назначением лекарственных средств, способных вызывать повреждение почечной ткани.
Стоимость исследования
Миопатия: причины, симптомы, лечение. в Солнцево
Миопатией называют совокупность симптомов, возникающих в результате повреждения мышц. В отличие от заболеваний периферической нервной системы, (при которых мышцы также повреждены, но это связано с предшествующим повреждением снабжающих их нервов), при миопатиях болезненный процесс локализуется в самой мышце.
Беспокоит слабость в конечностях? Записывайтесь к неврологу!
Миопатии представляют собой очень большую группу заболеваний с различными причинами, разным течением и прогнозом. Общей чертой является мышечная слабость — поражение мышц бедер и рук, хотя мышцы лица также могут быть ослаблены. Сенсорные расстройства при миопатиях не встречаются. Мышечная слабость обычно двусторонняя и симметричная с самого начала, то есть сходна с обеих сторон тела — левой и правой.
Миопатии могут быть генетическими или приобретенными. Генетически обусловленные миопатии включают, например, мышечные дистрофии, которые характеризуются аномальной структурой мышечных клеток (например, из-за врожденного недостатка любого из его компонентов). С другой стороны, приобретенные миопатии имеют воспаление (воспалительные миопатии), могут сопровождать эндокринные заболевания (например, гипотиреоз), а также могут возникать в результате повреждения мышц некоторыми лекарственными средствами или токсичными соединениями (например, алкоголем).
Насколько распространена миопатия?
Термин «миопатия» очень широк и охватывает множество различных заболеваний. Поэтому общую заболеваемость миопатией трудно определить. Как правило, миопатии являются редкими заболеваниями.
Как проявляется миопатия?
Основным симптомом миопатии является мышечная слабость. Чаще всего это касается мышц бедер и рук — пациентам, например, трудно подниматься по лестнице, вставать из положения сидя, сидеть или выполнять действия с поднятыми руками (например, повесить шторы или делать прическу). Мышечная слабость может сопровождаться болью. При некоторых миопатиях участвуют мышцы лица или горла. Может быть опущение век, снижение подвижности глазных яблок, невнятная речь, затрудненное глотание. Иногда мышцы шеи слабые — тогда не держится голова. При некоторых миопатиях может возникнуть слабость дыхательных мышц, приводящая к одышке. Иногда при миопатиях наблюдаются проблемы с расслаблением мышц, например, пациент не может быстро разжать пальцы после сжимания кулака. При прогрессирующих и длительных миопатиях возникает атрофия мышц. Эти симптомы могут сопровождаться признаками повреждения других тканей и органов вне мышечной системы.
Что делать, если появились симптомы миопатии (слабости в конечностях)?
Если замечены какие-либо симптомы, которые могут указывать на миопатию, нужно обратиться к врачу общей практики или терапевту, который затем направит пациента к специалисту, обычно неврологу. Если симптомы длятся недолго (к примеру, несколько недель) и быстро нарастают, следует как можно скорее прийти к врачу.
Как врач диагностирует миопатию?
Врач собирает историю болезни пациента и проводит тест, который обычно показывает парез мышц (бедра, руки, иногда лица), иногда также ослабление рефлексов, вызванных при постукивании с помощью неврологического молотка. Затем он заказывает дополнительные тесты. Обычно это лабораторные анализы крови, в том числе уровни электролита, ТТГ, воспаления и креатинкиназы. Это чувствительный показатель разрушения мышц, и его уровень повышается у большинства пациентов с миопатией. Он также может быть увеличен при заболеваниях, когда повреждение мышц вызвано повреждением нервов, таких как боковой амиотрофический склероз или полинейропатия, а иногда и у здоровых людей, например, после физической нагрузки или травмы мышц. Электромиография (ЭМГ) является еще одним дополнительным тестом, важным для диагностики. ЭМГ позволяет подтвердить миопатию или указывает на другое заболевание, которое вызывает аналогичные симптомы. Окончательный диагноз миопатии, то есть определение ее типа и причины, чаще всего возможен после теста среза мышечной ткани (для этой цели берут маленький фрагмент ткани под местной анестезией для микроскопического исследования) или генетического анализа из образца крови, взятого у пациента. Генетическое тестирование проводится только для некоторых генетических миопатий.
Как лечить миопатию?
Как и в случае с полиневропатией, можно выделить причинно-следственное и симптоматическое лечение. Возможно причинное лечение, например, при воспалительных миопатиях. В этих случаях используются глюкокортикоиды (стероидные гормоны), иммунодепрессанты или внутривенные иммуноглобулины. Причинное лечение миопатии, возникающей при эндокринных заболеваниях (например, заболевание щитовидной железы, гиперпаратиреоз или гиперадренокортицизм), включает лечение гормональных нарушений. При лекарственной или токсической миопатии нужно попытаться перестать принимать лекарство или прекратить воздействие токсического соединения, которое вызвало повреждение мышц. В редких случаях генетической миопатии, суть которой заключается в отсутствии одного из ферментов, необходимых для правильного функционирования мышц, возможно причинное лечение в виде введения недостающего фермента.
Симптоматическое лечение — это прежде всего реабилитация. В случае, если для пациента с быстрым мышечным расслаблением возникают обременительные трудности, фармакологическое лечение используется для смягчения этого симптома. При некоторых заболеваниях мышц поражаются другие органы, такие как сердечная мышца. Тогда для пациентов важно регулярно проходить осмотры у кардиолога. Кроме того, генетическое консультирование следует давать пациентам с генетической миопатией.
Можно ли полностью вылечить миопатию?
При генетических миопатиях полное выздоровление невозможно. Прогноз для приобретенных миопатий зависит от их причины: например, при воспалительных миопатиях мышечная сила обычно улучшается после начала лечения, а в миопатии, вызванной гормональными нарушениями, мышечные симптомы обычно исчезают после излечения основного заболевания.
Обращайтесь в поликлинику Медсемья в Солнцево — наш врач-невролог проведет диагностику и назначит правильное лечение!
Азотистый обмен
В Клинико-диагностической лаборатории производится определение следующих параметров азотистого обмена:
Мочевина
Мочевина – конечный продукт метаболизма белков в организме. При патологии сдвиги в уровне мочевины крови зависят от соотношения процессов мочевинообразования и ее выведения. Пониженная концентрация мочевины не имеет диагностического значения.
Три группы причин, приводящих к увеличению содержания мочевины в крови:
1. Надпочечная азотемия:
- При потреблении очень большого количества белковой пищи.
- При различных воспалительных процессах с выраженным усилением катаболизма белков.
- При обезвоживании в результате рвоты, поноса и др.
2. Почечная азотемия (наиболее частая, при нарушении функции почек):
- При острых и хронических гломерулонефритах.
- При хронических пиелонефритах.
- При нефросклерозах, вызванных отравлениями солями ртути и другими токсическими веществами.
- При синдроме длительного сдавливания.
- При гидронефрозе.
- При острой почечной недостаточности.
3. Подпочечная азотемия:
- При задержке выделения мочи какими-либо препятствиями в мочевыводящих путях (камень, опухоль).
Креатинин
Креатинин – является конечным продуктом распада креатина, который играет важную роль в энергетическом обмене мышечной и других тканей. Определение креатинина широко используется в диагностике заболеваний почек.
Креатинин в меньшей степени зависит от уровня катаболизма, не реабсорбируется в почках, поэтому в большей мере отражает степень нарушения выделительной и фильтрационной функции почек.
Автоматический биохимический анализатор высокой мощности AU680
с ISE модулем и станцией пробоподготовки AutoMate 1200
производства Beckman Coulter Inc., США
Креатинин в моче – суточное выделение креатинина с мочой относительно постоянно, эквивалентно суточному образованию и непосредственно зависит от массы мышц и выделительной функции почек.
Параллельное определение концентрации креатинина в крови и моче значительно расширяет диагностические возможности оценки функционального состояния почек.
Проба Реберга
Проба Реберга – позволяет судить о клубочковой фильтрации и канальцевой реабсорбции в почках. Проба основана на том, что креатинин фильтруется только клубочками, практически не всасывается и не секретируется канальцами.
Порядок проведения пробы: утром пациент мочится, выпивает 200 мл воды, и затем натощак в состоянии полного покоя собирает мочу за точно определенное непродолжительное время (2 часа). Посередине этого отрезка времени берут кровь из вены. Определяют концентрацию креатинина в крови и в моче, собранной за 2 часа. Затем по формулам вычисляют величину клубочковой фильтрации (КФ) и канальцевой реабсорбции (КР).
КФ – чувствительный показатель функционального состояния почек. Снижение ее наблюдается при острых и хронических гломерулонефритах, нефросклерозах, являясь одним из ранних симптомов нарушения функции почек. Повышению способствует хронический гломерулонефрит с нефротическим синдромом, нефрозы.
КР – может значительно меняться в физиологических условиях, снижаясь до 90% при водной нагрузке. Выраженное снижение реабсорбции происходит при форсированном диурезе, вызванном мочегонными средствами. Наибольшее снижение канальцевой реабсорбции наблюдается у больных несахарным диабетом.
Стойкое снижение происходит при хронических пиелонефритах. Повышение КФ сопутствует нефриту, нефротическому синдрому.
Мочевая кислота
Мочевая кислота – продукт обмена пуриновых оснований, входящих в состав сложных белков – нуклеопротеидов. Образовавшаяся мочевая кислота выделяется почками.
Мочевая кислота во внеклеточной жидкости присутствует в виде солей натрия (ураты) в концентрации, близкой к насыщению, поэтому существует возможность кристаллизации урата натрия, если концентрация мочевой кислоты превысит максимум нормальных значений.
Повышение уровня мочевой кислоты – гиперурикемия – имеет большое значение для диагностики подагры.
Определение мочевой кислоты в моче необходимо проводить совместно с ее определением в крови. Это позволяет во многих случаях установить патологический механизм, лежащий в основе подагры у пациента (избыточная продукция мочевой кислоты в организме или нарушение ее выведения).
Материал для исследования
- Cыворотка крови;
- Моча.
Цистатин
Исследования показали, что уровень цистатина С является более точным маркером почечной функции, чем уровень креатинина.
Цистатин C (наряду с инулином) на сегодняшний день рассматривается как «золотой стандарт» определения скорости клубочковой фильтрации как интегрального показателя функции почек.
В отличие от креатинина, на темп синтеза цистатина C не влияют такие факторы, как возраст, пол, мышечная масса, характер питания, наличие воспалительных реакций.
Бета-2- микроглобулин
Уровень бета-2 микроглобулина в крови возрастает при почечной недостаточности (снижении почечного клиренса).
При повреждении клеток проксимальных канальцев вследствие заболевания почек, лекарственной интоксикации, токсического воздействия тяжёлых металлов и т. д. экскреция бета-2 микроглобулина с мочой возрастает.
Поэтому определение бета-2 микроглобулина мочи используют в качестве маркёра поражения проксимальных канальцев почек; этот тест может быть полезен при дифференциальной диагностике инфекции верхних и нижних отделов мочевого тракта.
Страница не найдена |
Страница не найдена |
404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
2930
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Метки
Настройки
для слабовидящих
Рабдомиолиз: симптомы, лечение
Обзор
Что такое рабдомиолиз?
Рабдомиолиз может быть опасным для жизни состоянием, вызванным разрушением мышц и их гибелью. Это опасное повреждение мышц может быть результатом перенапряжения, травмы, токсичных веществ или болезни.
Когда мышечные клетки распадаются, они выделяют в кровь белок, называемый миоглобином. Почки отвечают за удаление этого миоглобина из крови, чтобы моча могла вымыть его из организма.
В больших количествах миоглобин может повредить почки. Если почки не могут достаточно быстро избавиться от шлаков, может произойти почечная недостаточность и смерть.
Насколько распространен рабдомиолиз?
Рабдомиолиз (также называемый рабдо) встречается относительно редко. Ежегодно это заболевание заболевает около 26000 человек.
Кто страдает рабдомиолизом?
Хотя рабдомиолиз может случиться с кем угодно, определенные группы имеют более высокий риск развития этого состояния, чем другие.К людям с повышенным риском развития рабдомиолиза относятся:
- Спортсмены на выносливость: Марафонцы, люди, занимающиеся спиннингом, и другие, кто выполняет высокоинтенсивные интервальные упражнения, имеют более высокий риск развития рабдомиолиза. Эти группы могут слишком сильно напрягаться, не отдыхая.
- Пожарные: Состояние пожарных может развиться после физических нагрузок при высоких температурах. Перегрев может вызвать рабдомиолиз.
- Военнослужащие: Военнослужащие, особенно те, кто находится в учебном лагере или проходят интенсивную подготовку, имеют повышенный риск развития рабдомиолиза.
- Пожилые люди: Люди, которые падают, не могут встать и долгое время не обнаруживаются, могут получить рабдомиолиз.
Симптомы и причины
Как люди заболевают рабдомиолизом?
Несколько факторов могут привести к рабдомиолизу. Причины рабдомиолиза включают:
- Упражнения высокой интенсивности: Слишком быстрое выполнение программы упражнений может привести к рабдомиолизу, когда мышцы не успевают восстановиться после интенсивной тренировки.
- Сильное обезвоживание и перегрев: Тепло вызывает более быстрое разрушение мышц. Ваши почки не могут избавиться от всех отходов без большого количества жидкости.
- Травма: Тяжелый ожог, удар молнии или раздавливание могут вызвать быстрое разрушение мышечных волокон.
- Лекарства: Некоторые лекарства могут вызывать разрушение мышц, в том числе антипсихотические, антидепрессанты и противовирусные препараты. Прием статинов также может привести к рабдомиолизу, особенно у людей с диабетом или заболеваниями печени.
- Незаконные наркотики и алкоголь: Героин, ЛСД, кокаин и чрезмерное употребление алкоголя токсичны для организма и могут вызвать разрушение мышц.
- Длительные периоды бездействия: У людей, которые падают, теряют сознание и не могут подняться в течение длительного времени, может развиться рабдо.
Может ли рабдомиолиз передаваться по наследству?
Сам по себе рабдомиолиз не может передаваться по наследству (передается в семье). Но определенные генетические нарушения могут увеличить риск развития этого состояния.Люди могут получить рабдомиолиз в результате наследственного мышечного заболевания (например, мышечной дистрофии).
Люди с определенными метаболическими или митохондриальными нарушениями также имеют более высокий риск рабдомиолиза. Нарушение обмена веществ влияет на то, как энергия поступает в клетки. Митохондриальные нарушения возникают, когда ваше тело неправильно вырабатывает энергию для ваших клеток.
Каковы симптомы рабдомиолиза?
Симптомы рабдомиолиза могут варьироваться от легких до тяжелых.Симптомы обычно развиваются через один-три дня после мышечной травмы, хотя некоторые люди могут даже не замечать мышечную болезненность. К основным признакам рабдомиолиза относятся:
- Мышечный отек.
- Слабые, болезненные и болезненные мышцы.
- Темная моча коричневого, красного или чайного цвета.
Некоторые люди также испытывают обезвоживание или уменьшение мочеиспускания, тошноту или потерю сознания.
Диагностика и тесты
Как диагностируется рабдомиолиз?
Чтобы диагностировать рабдомиолиз, ваш врач будет:
- Осмотрите вас и спросите о недавней физической активности, лекарствах, отпускаемых по рецепту, а также об употреблении алкоголя или наркотиков.
- Закажите анализ мочи, чтобы проверить уровень миоглобина в моче.
- Возьмите образец крови, чтобы измерить уровень креатининкиназы, белка, который выделяется мышцами при распаде.
После диагностики рабдомиолиза врачи могут назначить биопсию мышцы, чтобы определить причину. Для биопсии мышцы ваш врач:
- Онемение области.
- Возьмите небольшой образец вашей мышцы.
- Отправьте образец в лабораторию для тестирования.
Ваш врач может также порекомендовать сделать анализ крови, чтобы узнать, есть ли у вас генетическое заболевание, повышающее риск развития рабдомиолиза.
Как узнать, что у меня рабдомиолиз?
Если через несколько дней после тренировки у вас очень болезненные или слабые мышцы, у вас может быть рабдомиолиз. Вам также следует обратить внимание на опухоль мышц и темную мочу. Если у вас есть эти симптомы, немедленно обратитесь к врачу, чтобы пройти обследование и пройти курс лечения от рабдомиолиза.
Ведение и лечение
Какие методы лечения рабдомиолиза?
Для лечения рабдомиолиза врач сначала введет вам жидкости и электролиты внутривенно (через вену).Эти жидкости для внутривенного вливания выводят токсины из вашего организма. Возможно, вам придется остаться в больнице на несколько дней. После лечения физиотерапия может помочь вам укрепить мышцы после начального периода отдыха.
Если рабдомиолиз достаточно серьезен, чтобы вызвать повреждение почек, вам может потребоваться диализ. Диализ извлекает (удаляет) часть вашей крови, выводит токсины и возвращает отфильтрованную кровь.
Каковы побочные эффекты лечения рабдомиолиза?
Во время диализа у некоторых людей падает артериальное давление, что может вызвать тошноту, рвоту и головные боли.Эти побочные эффекты обычно проходят при повторных процедурах диализа. Вы можете чувствовать усталость или слабость в течение нескольких часов после процедуры диализа.
Какие осложнения связаны с рабдомиолизом?
Если рабдомиолиз тяжелый, он может повредить почки и привести к почечной недостаточности. Рабдомиолиз может быть смертельным, если его не лечить.
Что я могу сделать, чтобы облегчить симптомы рабдомиолиза?
Если у вас есть симптомы рабдомиолиза, не пытайтесь их облегчить.Вам следует немедленно обратиться к врачу.
Рабдомиолиз опасен для жизни. Ранняя диагностика и лечение необходимы для выздоровления.
Профилактика
Как предотвратить рабдомиолиз?
Возможно, вы не сможете предотвратить рабдомиолиз, возникший в результате несчастного случая. Но вы можете снизить риск развития рабдомиолиза, вызванного физической нагрузкой. Чтобы снизить риск развития рабдомиолиза, вам следует:
- Начинайте программу упражнений медленно и прислушивайтесь к своему телу.Если вы чувствуете особую боль или усталость во время тренировки, остановитесь и отдохните. Не выходите за пределы безопасного.
- Избегайте обезвоживания и перегрева. Делайте перерывы в тени, если занимаетесь физическими упражнениями в жару.
- Не злоупотребляйте алкоголем и не принимайте запрещенные наркотики.
- Поговорите со своим врачом о любых принимаемых вами лекарствах, которые могут повысить риск развития рабдомиолиза. Будьте особенно осторожны, если у вас диабет или заболевание печени.
Перспективы / Прогноз
Каковы перспективы пациентов с рабдомиолизом?
Многие люди выздоравливают после лечения рабдомиолиза.Но у большинства людей мышечная слабость сохраняется в течение нескольких недель после травмы. Почти в 50% случаев рабдомиолиза люди испытывают острое повреждение почек. Некоторым людям требуется длительный диализ, если их почки не работают.
Жить с
Когда мне следует позвонить своему врачу по поводу рабдомиолиза?
Если через несколько дней после тренировки вы продолжаете испытывать мышечную боль, слабость или отек, немедленно обратитесь к врачу. Рабдомиолиз — серьезное заболевание, требующее немедленной медицинской помощи.
Рабдомиолиз: симптомы, лечение
Обзор
Что такое рабдомиолиз?
Рабдомиолиз может быть опасным для жизни состоянием, вызванным разрушением мышц и их гибелью. Это опасное повреждение мышц может быть результатом перенапряжения, травмы, токсичных веществ или болезни.
Когда мышечные клетки распадаются, они выделяют в кровь белок, называемый миоглобином. Почки отвечают за удаление этого миоглобина из крови, чтобы моча могла вымыть его из организма.
В больших количествах миоглобин может повредить почки. Если почки не могут достаточно быстро избавиться от шлаков, может произойти почечная недостаточность и смерть.
Насколько распространен рабдомиолиз?
Рабдомиолиз (также называемый рабдо) встречается относительно редко. Ежегодно это заболевание заболевает около 26000 человек.
Кто страдает рабдомиолизом?
Хотя рабдомиолиз может случиться с кем угодно, определенные группы имеют более высокий риск развития этого состояния, чем другие.К людям с повышенным риском развития рабдомиолиза относятся:
- Спортсмены на выносливость: Марафонцы, люди, занимающиеся спиннингом, и другие, кто выполняет высокоинтенсивные интервальные упражнения, имеют более высокий риск развития рабдомиолиза. Эти группы могут слишком сильно напрягаться, не отдыхая.
- Пожарные: Состояние пожарных может развиться после физических нагрузок при высоких температурах. Перегрев может вызвать рабдомиолиз.
- Военнослужащие: Военнослужащие, особенно те, кто находится в учебном лагере или проходят интенсивную подготовку, имеют повышенный риск развития рабдомиолиза.
- Пожилые люди: Люди, которые падают, не могут встать и долгое время не обнаруживаются, могут получить рабдомиолиз.
Симптомы и причины
Как люди заболевают рабдомиолизом?
Несколько факторов могут привести к рабдомиолизу. Причины рабдомиолиза включают:
- Упражнения высокой интенсивности: Слишком быстрое выполнение программы упражнений может привести к рабдомиолизу, когда мышцы не успевают восстановиться после интенсивной тренировки.
- Сильное обезвоживание и перегрев: Тепло вызывает более быстрое разрушение мышц. Ваши почки не могут избавиться от всех отходов без большого количества жидкости.
- Травма: Тяжелый ожог, удар молнии или раздавливание могут вызвать быстрое разрушение мышечных волокон.
- Лекарства: Некоторые лекарства могут вызывать разрушение мышц, в том числе антипсихотические, антидепрессанты и противовирусные препараты. Прием статинов также может привести к рабдомиолизу, особенно у людей с диабетом или заболеваниями печени.
- Незаконные наркотики и алкоголь: Героин, ЛСД, кокаин и чрезмерное употребление алкоголя токсичны для организма и могут вызвать разрушение мышц.
- Длительные периоды бездействия: У людей, которые падают, теряют сознание и не могут подняться в течение длительного времени, может развиться рабдо.
Может ли рабдомиолиз передаваться по наследству?
Сам по себе рабдомиолиз не может передаваться по наследству (передается в семье). Но определенные генетические нарушения могут увеличить риск развития этого состояния.Люди могут получить рабдомиолиз в результате наследственного мышечного заболевания (например, мышечной дистрофии).
Люди с определенными метаболическими или митохондриальными нарушениями также имеют более высокий риск рабдомиолиза. Нарушение обмена веществ влияет на то, как энергия поступает в клетки. Митохондриальные нарушения возникают, когда ваше тело неправильно вырабатывает энергию для ваших клеток.
Каковы симптомы рабдомиолиза?
Симптомы рабдомиолиза могут варьироваться от легких до тяжелых.Симптомы обычно развиваются через один-три дня после мышечной травмы, хотя некоторые люди могут даже не замечать мышечную болезненность. К основным признакам рабдомиолиза относятся:
- Мышечный отек.
- Слабые, болезненные и болезненные мышцы.
- Темная моча коричневого, красного или чайного цвета.
Некоторые люди также испытывают обезвоживание или уменьшение мочеиспускания, тошноту или потерю сознания.
Диагностика и тесты
Как диагностируется рабдомиолиз?
Чтобы диагностировать рабдомиолиз, ваш врач будет:
- Осмотрите вас и спросите о недавней физической активности, лекарствах, отпускаемых по рецепту, а также об употреблении алкоголя или наркотиков.
- Закажите анализ мочи, чтобы проверить уровень миоглобина в моче.
- Возьмите образец крови, чтобы измерить уровень креатининкиназы, белка, который выделяется мышцами при распаде.
После диагностики рабдомиолиза врачи могут назначить биопсию мышцы, чтобы определить причину. Для биопсии мышцы ваш врач:
- Онемение области.
- Возьмите небольшой образец вашей мышцы.
- Отправьте образец в лабораторию для тестирования.
Ваш врач может также порекомендовать сделать анализ крови, чтобы узнать, есть ли у вас генетическое заболевание, повышающее риск развития рабдомиолиза.
Как узнать, что у меня рабдомиолиз?
Если через несколько дней после тренировки у вас очень болезненные или слабые мышцы, у вас может быть рабдомиолиз. Вам также следует обратить внимание на опухоль мышц и темную мочу. Если у вас есть эти симптомы, немедленно обратитесь к врачу, чтобы пройти обследование и пройти курс лечения от рабдомиолиза.
Ведение и лечение
Какие методы лечения рабдомиолиза?
Для лечения рабдомиолиза врач сначала введет вам жидкости и электролиты внутривенно (через вену).Эти жидкости для внутривенного вливания выводят токсины из вашего организма. Возможно, вам придется остаться в больнице на несколько дней. После лечения физиотерапия может помочь вам укрепить мышцы после начального периода отдыха.
Если рабдомиолиз достаточно серьезен, чтобы вызвать повреждение почек, вам может потребоваться диализ. Диализ извлекает (удаляет) часть вашей крови, выводит токсины и возвращает отфильтрованную кровь.
Каковы побочные эффекты лечения рабдомиолиза?
Во время диализа у некоторых людей падает артериальное давление, что может вызвать тошноту, рвоту и головные боли.Эти побочные эффекты обычно проходят при повторных процедурах диализа. Вы можете чувствовать усталость или слабость в течение нескольких часов после процедуры диализа.
Какие осложнения связаны с рабдомиолизом?
Если рабдомиолиз тяжелый, он может повредить почки и привести к почечной недостаточности. Рабдомиолиз может быть смертельным, если его не лечить.
Что я могу сделать, чтобы облегчить симптомы рабдомиолиза?
Если у вас есть симптомы рабдомиолиза, не пытайтесь их облегчить.Вам следует немедленно обратиться к врачу.
Рабдомиолиз опасен для жизни. Ранняя диагностика и лечение необходимы для выздоровления.
Профилактика
Как предотвратить рабдомиолиз?
Возможно, вы не сможете предотвратить рабдомиолиз, возникший в результате несчастного случая. Но вы можете снизить риск развития рабдомиолиза, вызванного физической нагрузкой. Чтобы снизить риск развития рабдомиолиза, вам следует:
- Начинайте программу упражнений медленно и прислушивайтесь к своему телу.Если вы чувствуете особую боль или усталость во время тренировки, остановитесь и отдохните. Не выходите за пределы безопасного.
- Избегайте обезвоживания и перегрева. Делайте перерывы в тени, если занимаетесь физическими упражнениями в жару.
- Не злоупотребляйте алкоголем и не принимайте запрещенные наркотики.
- Поговорите со своим врачом о любых принимаемых вами лекарствах, которые могут повысить риск развития рабдомиолиза. Будьте особенно осторожны, если у вас диабет или заболевание печени.
Перспективы / Прогноз
Каковы перспективы пациентов с рабдомиолизом?
Многие люди выздоравливают после лечения рабдомиолиза.Но у большинства людей мышечная слабость сохраняется в течение нескольких недель после травмы. Почти в 50% случаев рабдомиолиза люди испытывают острое повреждение почек. Некоторым людям требуется длительный диализ, если их почки не работают.
Жить с
Когда мне следует позвонить своему врачу по поводу рабдомиолиза?
Если через несколько дней после тренировки вы продолжаете испытывать мышечную боль, слабость или отек, немедленно обратитесь к врачу. Рабдомиолиз — серьезное заболевание, требующее немедленной медицинской помощи.
4 факта о рабдомиолизе, которого вы не знали (он же рабдо)
Несколько лет назад большое внимание привлекло странное состояние, называемое рабдомиолизом, как страшный — и, возможно, смертельный — побочный эффект очень интенсивных тренировок, таких как кроссфит. Если бы вы увлекались подобными вещами, возможно, вы немного нервничали. В противном случае вы, вероятно, продолжили свою жизнь.
Но в июле The New York Times сообщила об увеличении случаев рабдомиолиза после занятий спортом, вернув его в центр внимания.То, что когда-то было условием, предназначенным для самых хардкорных людей, теперь заставило всех нас задуматься: «А может ли это случиться со мной?»
Рабдомиолиз, также известный как рабдо, по сути, представляет собой разрушение мышц. Когда вы тренируетесь, некоторые мышцы разрушаются — это нормально и является частью процесса становления сильнее, — объясняет Наян Арора, доктор медицины, научный сотрудник нефрологии Вашингтонского университета.
Когда люди более нагружают свои мышцы, они подвергаются риску разрушения мышечной ткани настолько, что он высвобождает белок миоглобин в кровоток.Миоглобин токсичен для почек, поэтому рабдо может привести к повреждению почек или полной почечной недостаточности, если его не лечить, объясняет Арора.
Несмотря на то, что рабдо — это серьезно — и по-настоящему устрашающе, — он все еще довольно редко встречается. Это означает, что вы не должны позволять ему мешать вам тренироваться, но вы должны видеть это на вашем радаре. Вот четыре вещи, которые вам нужно знать о рабдомиолизе.
1. Это не только из-за тяжелых тренировок.
Арора говорит, что наблюдается небольшой всплеск случаев рабдо, связанного с физическими упражнениями, вероятно, в результате роста популярности изнурительных тренировок, от высокоинтенсивных интервальных тренировок до спиннинга и ультра бега.Но напряжение мышц — не единственная причина. Состояние также может быть результатом злоупотребления алкоголем, приема лекарств, включая статины и преднизон, употребления запрещенных наркотиков, мышечных заболеваний, травм, определенных состояний здоровья и генетических проблем, судорог и неподвижности, как показывают исследования.
Рабдомиолиз впервые широко изучался во время Второй мировой войны, когда исследователи обследовали солдат, получивших тяжелые травмы в результате лондонского блица 1940 года, говорит Арора.
«Интересно, что в Библии упоминаются симптомы рабдо.Когда евреи переходили пустыню, они ели много перепелов », — говорит он. Исследователи полагают, что птицы, возможно, съели болиголов, что привело к рабдомиолизу в результате случайного отравления болиголовом.
Упражнения в жарких и влажных условиях или во время приема креатиновых добавок, таблеток для похудения из эфедры или энергетических напитков с высокими дозами кофеина также увеличивают риск, говорит Арора.
2. Обезвоживание подвергает вас повышенному риску.
Обычно тяжелая тренировка не приводит к попаданию в больницу, — говорит Арора.Большинство людей, страдающих рабдо от физических упражнений, делали что-то действительно интенсивное. и не пили достаточно воды до и во время какой-либо активности.
«Возвращаясь к 1940 году с жертвами тяжелых травм, именно люди, не имевшие доступа к воде, подвергались наибольшему риску», — говорит Арора.
Вот почему внутривенное введение жидкости — это метод лечения рабдомиолиза №1 для предотвращения повреждения почек, — говорит он. Чтобы защитить себя от рабдо, в первую очередь, убедитесь, что вы увлажняете, увлажняете, увлажняете.
Сколько воды вам следует пить, зависит от множества факторов, включая ваш вес, уровень физической подготовки и продукты, которые вы едите в течение дня, — говорит Арора. Но хорошее практическое правило во время упражнений — пить немного воды каждый раз, когда вы делаете перерыв, и делать себе эти перерывы, даже если вы находитесь в классе, который не способствует отдыху.
3. Вы не будете мочиться кровью.
Один из симптомов рабдомиолиза — моча красного или коричневого цвета, которую пациенты часто принимают за кровь, говорит Арора.То, что выглядит как кровь, на самом деле является миоглобином, тем токсином, который может привести к повреждению почек. «Когда это происходит, ваше состояние становится серьезным, и важно немедленно обратиться за медицинской помощью», — говорит он.
4. Установка может занять три дня.
Вы можете ожидать, что вскоре после или даже во время тренировки вы узнаете, что что-то не так. Но пик рабдо обычно наступает через 24-72 часа после тренировки или травмы, говорит Арора. По его словам, отсроченная мышечная болезненность, или DOMS, является нормальным явлением после тяжелой тренировки, и иногда бывает трудно отличить DOMS от рабдомиолиза.
Если вы испытываете мышечную боль или слабость в одной группе мышц, которая кажется непропорциональной тренировке, это может быть рабдо, — говорит Арора. Другими возможными признаками являются отек или ощущение спазма, которое не проходит, особенно в одной группе мышц. Он говорит, что если у вас все болит, вы, вероятно, в порядке, но всегда лучше проявить осторожность, если вы обеспокоены.
Лечение и профилактика рабдомиолиза
Если вы подозреваете, что у вас может быть рабдомиолиз, немедленно обратитесь в отделение неотложной помощи.«Рабдо может быть смертельным, если его не лечить», — говорит Арора.
«По сути, весь смысл лечения заключается в том, чтобы предотвратить повреждение почек, и это можно сделать с помощью огромных доз жидкости», — говорит он.
В зависимости от степени высвобождения токсинов, жидкости обычно вводятся в течение двух-пяти дней. К этому моменту большинство людей выздоровеет. Врач порекомендует пациентам сделать перерыв на физические упражнения. Это может быть от пары недель до пары месяцев, но будет зависеть от многих факторов, включая тяжесть состояния и уровень физической подготовки человека.По словам Арора, всегда рекомендуется возвращаться к консультациям с врачом.
The Takeaway
В конце концов, ни одна тренировка не стоит того, чтобы от нее умирать. Слушайте свое тело, переходите к новым тренировкам, обращайте внимание на гидратацию, делайте регулярные перерывы и сразу же обращайтесь за помощью, если после тренировки что-то не так, — говорит Арора.
Рабдомиолиз, индуцированный повторяющимися упражнениями низкой интенсивности
Case Rep Emerg Med. 2015; 2015: 281540.
Мина Тран
1 Бейлорский медицинский колледж, отделение неотложной медицины, 1504 Тауб-Луп, Хьюстон, Техас 77030, США
Николас Хайден
2 Бейлорский медицинский колледж, отделение неотложной помощи Медицина, летняя медицинская и исследовательская подготовка (SMART), 1504 Taub Loop, Houston, TX 77030, USA
Brandon Garcia
2 Медицинский колледж Бейлора, Секция неотложной медицины, Летняя медицинская и исследовательская подготовка (SMART), 1504 Тауб-Луп, Хьюстон, Техас 77030, США
Вероника Туччи
1 Бейлорский медицинский колледж, отделение неотложной медицины, 1504 Тауб-Луп, Хьюстон, Техас 77030, США
1 Бейлорский медицинский колледж, отделение Emergency Medicine, 1504 Taub Loop, Houston, TX 77030, USA
2 Медицинский колледж Бейлора, отделение неотложной медицины, летняя медицинская и исследовательская подготовка (SMART), 1504 Taub Loop, Housto n, TX 77030, USA
Академический редактор: Аристоменис К.Exadaktylos
Поступила 1 сентября 2015 г .; Принято 11 ноября 2015 г.
Это статья в открытом доступе, распространяемая по лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.
Реферат
Рабдомиолиз — редкое заболевание, вызванное попаданием белков поврежденных мышечных клеток в кровоток и повреждением почек.Общие симптомы рабдомиолиза — мышечные боли и усталость в сочетании с темной мочой; Поражение почек — частый симптом среди этих пациентов. Мы представляем случай 23-летней женщины, у которой наблюдалась миалгия в верхних конечностях, вызванная упражнениями с низкой интенсивностью и частым повторением. Ей успешно поставили диагноз и вылечили рабдомиолиз при физической нагрузке. У этого пациента не было серьезной истории болезни, которая могла бы вызвать это состояние. Мы настоятельно призываем сообщество скорой медицинской помощи наблюдать и контролировать пациентов, которые жалуются на миалгию, чтобы убедиться, что они не страдают рабдомиолизом даже в атипичных случаях.
1. Пример из практики
За три дня до прибытия в отделение неотложной помощи, здоровая 23-летняя пациентка сделала упражнения на бицепс низкой интенсивности с большим числом повторений с отягощением 10–15 фунтов после перерыва в несколько раз. месяцы. Пациентка сообщила о приеме добавок креатина во время тренировки. На следующий день она заметила сильную болезненность и напряжение в верхних конечностях, особенно в бицепсах. Пациентка сообщила о неспособности полностью вытянуть руки и отметила, что ее моча была очень темной и «чайного цвета [ред]».Она отрицала наличие дизурии, лихорадки, озноба, боли в груди и боли в животе. Тем не менее, пациентка сообщила о легкой парестезии в руках до госпитализации с улучшением до обследования.
При немедленном физикальном обследовании у пациента было повышенное артериальное давление (142/115). Ее бицепсы были выпуклыми и напряженными, у нее была небольшая потеря чувствительности, а моча соответствовала описанию как «цвет чая [ред]». Информация из анамнеза пациента и физикального обследования в значительной степени свидетельствует о том, что пациент страдал рабдомиолизом.
После рабочего диагноза лаборатория сообщила, что уровень креатинкиназы в крови пациента составлял 156 339 Ед / л, а анализ мочи показал 3+ крови и 1 эритроцит. Наличие крови без эритроцитов в моче свидетельствует о рабдомиолизе. Пациент начал лечение рабдомиолиза с агрессивной жидкостной реанимации и строгого мониторинга мочи. Эти вмешательства привели к снижению уровня ее креатинкиназы до 68 4281 Ед / л.Благодаря агрессивной жидкостной реанимации уровень креатинкиназы пациента стабилизировался, и ближайший к выписке уровень креатинкиназы составил 16 245 Ед / л. Пациент выписан через 4 дня после поступления. На протяжении всего пребывания в больнице она была гемодинамически стабильной, несмотря на первоначальную госпитализацию в отделение интенсивной терапии.
Используя корреляцию лабораторных данных, истории болезни пациента и физикального обследования, у нас есть доказательства того, что мы были успешными в выявлении и лечении тяжелого случая рабдомиолиза при физической нагрузке, приобретенного с помощью упражнений с низкой интенсивностью и частым повторением [1] .
2. Обсуждение
Рабдомиолиз — это заболевание, вызванное быстрым разрушением мышечной ткани, попадающей в кровоток. Миоглобин, компонентный белок скелетной мышечной ткани, в больших количествах может вызывать почечную недостаточность, накапливаясь в почках и препятствуя правильному функционированию этого органа [2]. Разрушение мышечной ткани может быть вызвано множеством действий, таких как сильное растяжение мышц, раздавливание, поражение электрическим током и употребление наркотиков [3]. Пациенты, у которых развивается рабдомиолиз, часто чувствуют сильную боль в области гибели мышц и показывают темную концентрированную мочу, а также тошноту, трудности с концентрацией внимания, слабость или утомляемость.Если лечить быстро, результат лечения положительный.
Рабдомиолиз впервые был связан с почечной недостаточностью в отчете, написанном Байуотерсом и Биллом во время битвы за Британию в 1940 году [4]. Они заметили, что пациенты, оказавшиеся под разрушенной инфраструктурой, страдали почечной недостаточностью даже в тех случаях, когда почки пациентов не были повреждены. В ходе исследования Байуотерс и Билл обнаружили, что миоглобин, белок, связывающий железо и кислород, обнаруженный в мышечных волокнах, накапливался в крови до уровней, превышающих уровни, которые могут быть должным образом отфильтрованы почками [4].Затем миоглобин начал собираться, что привело к острой почечной недостаточности.
Заболевание довольно редко встречается в общей популяции, проявляясь примерно у 0,0001% (25/25 миллионов) пациентов в период с 1990 по 1999 гг. [5]. Раннее изучение рабдомиолиза стало возможным благодаря изучению жертв стихийных бедствий и травм, но было проведено множество исследований, демонстрирующих, что чрезмерное напряжение мышц также может вызывать болезнь. В ретроспективном исследовании 2015 г., проведенном с 2007 по 2013 г., д-р Имстепф и др.проверяли поступление в отделения неотложной помощи после тренировок и обследовали инциденты с пациентами. Они обнаружили, что 45% госпитализированных пациентов были в возрасте от 17 до 30 лет, и количество пациентов с рабдомиолизом составляло небольшую часть от общего числа госпитализированных пациентов. В сочетании с последними данными это тематическое исследование предполагает, что молодые пациенты получают значительную часть травм в результате тренировок и что среди населения присутствуют пациенты, страдающие рабдомиолизом [6].
Спортсмены, как профессиональные, так и любители, подвержены рабдомиолизу после экстремальных тренировок.Чрезмерное разрушение мышц, вызванное интенсивным поднятием тяжестей, высвобождает миоглобин в кровоток и может привести к его накоплению в почках [7]. Этот риск в настоящее время принимается медицинским сообществом для пациентов, которые являются заядлыми спортсменами, поднимающими большие веса. Однако представленный нами случай демонстрирует, что серьезное напряжение мышц не обязательно должно быть вызвано большим весом, чтобы развиться рабдомиолиз; поднятие небольшого веса с большим количеством повторений может привести к разрушению мышц и вызвать рабдомиолиз.
Тренировки с малым весом и большим числом повторений могут вызвать такую же нагрузку на мышечные волокна, как и тренировки с большим весом. Основная причина рабдомиолиза, крайнего разрушения мышечных волокон и выброса миоглобина в кровоток, на самом деле может быть вызвана многими факторами [3]. Врачи должны заботиться о симптомах и не должны сбрасывать со счетов потенциальный диагноз рабдомиолиза, когда спортсмен допускает использование небольшого веса в своих тренировках или отрицает использование тяжелых весов.Врачи скорой помощи должны включать в свои протоколы учет рабдомиолиза всякий раз, когда у пациента появляются миалгия, утомляемость, слабость и другие симптомы, связанные с этим заболеванием.
Как было описано на примере 23-летней пациентки, миалгия, вызванная низкоинтенсивными тренировками, может привести к рабдомиолизу. Когда у пациента наблюдается тяжелая миалгия конечностей, следует назначить лабораторные анализы для проверки уровня креатина в крови, чтобы определить, есть ли у пациента рабдомиолиз [3].Пациентам, которые соответствуют критериям возможного рабдомиолиза, следует вводить жидкости внутривенно и наблюдать за ними в течение 24–48 часов [7].
3. Заключение
Хотя рабдомиолиз при физической нагрузке обычно вызывается тренировками с большим весом, заболевание также может быть вызвано тренировками с низким весом, как показано в этом случае. Рабдомиолиз может быть вызван интенсивностью тренировки, а не используемым весом. Врачи должны знать об этом, когда обследуют пациентов, жалующихся на мышечные боли и слабость, связанные с рабдомиолизом.Основная причина заболевания — отмирание мышц, которое может быть вызвано множеством способов.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Ссылки
1. Ли Г. Рабдомиолиз, вызванный физической нагрузкой. Медицинский журнал Род-Айленда . 2014. 97 (11): 22–24. [PubMed] [Google Scholar] 2. Кнохель Дж. П. Катастрофические медицинские события с изнурительными упражнениями: «рабдомиолиз белых воротничков» Kidney International .1990. 38 (4): 709–719. DOI: 10,1038 / ки.1990.263. [PubMed] [CrossRef] [Google Scholar] 5. Блэк С., Джик Х. Этиология и частота рабдомиолиза. Фармакотерапия: журнал фармакологии человека и лекарственной терапии . 2015; 22 (12): 1524–1526. DOI: 10.1592 / phco.22.17.1524.34130. [PubMed] [CrossRef] [Google Scholar] 6. Имстепф В. А., Браун К. Т., Риклин М. Э., Эксадактилос А. К. Время для перерыва: госпитализация в городское отделение неотложной помощи после тренировки — ретроспективное исследование из Швейцарии. BioMed Research International . 2015; 2015: 7. doi: 10.1155 / 2015 / 610137.610137 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 7. Титце Д. С., Борхерс Дж. Рабдомиолиз при физической нагрузке у спортсмена: клинический обзор. Спортивное здоровье: мультидисциплинарный подход . 2014. 6 (4): 336–339. DOI: 10.1177 / 1941738114523544. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Рабдомиолиз — Американский семейный врач
1. Иллюстрированный медицинский словарь Дорланда.29 изд. Филадельфия: Сондерс, 2000 ….
2. Абасси З.А.,
Хоффман А,
Лучше ОС.
Острая почечная недостаточность, осложняющая раздавливание мышц. Семин Нефрол .
1998. 18: 558–65.
3. Graves EJ,
Gillum BS.
Подробные диагнозы и процедуры, Национальное обследование выписки из больниц, 1995. Vital Health Stat .
1997. 13 (130): 1–146.
4. Дейган CJ,
Вонг К.М.,
Маклафлин К.Дж.,
Харден П.
Рабдомиолиз и острая почечная недостаточность в результате злоупотребления алкоголем и наркотиками. QJM .
2000. 93: 29–33.
5. Хойс Р,
Экарт Р,
Синкович А,
Хойс-Фабьян Т.
Рабдомиолиз и острая почечная недостаточность в отделении интенсивной терапии. Ren Fail .
1999; 21: 675–84.
6. Knochel JP.
Механизмы рабдомиолиза. Curr Opin Rheumatol .
1993; 5: 725–31.
7. Габов П.А.,
Kaehny WD,
Kelleher SP.
Спектр рабдомиолиза. Медицина [Балтимор] .1982; 61: 141–52.
8. Харпер Дж.
Рабдомиолиз и миоглобинурическая почечная недостаточность. Медсестра интенсивной терапии .
1990. 10 (3): 32–6.
9. Бесса О.
Алкогольный рабдомиолиз: обзор. Conn Med .
1995; 59: 519–21.
10. Линия РЛ,
Ржавчина GS.
Острый рабдомиолиз при физической нагрузке. Врач Фам .
1995; 52: 502–6.
11. Бисвас S,
Гнанасекаран I,
Иватуры р-н,
Саймон Р,
Патель АН.Преувеличенный рабдомиолиз, связанный с положением при литотомии. Am Surg .
1997; 63: 361–4.
12. Алехандро Д.С.,
Петерсон Дж.
Острая миоглобинурическая почечная недостаточность у пациента с трансплантатом сердца, принимающего ловастатин и циклоспорин. Дж. Ам Соц Нефрол .
1994; 5: 153–60.
13. Horowitz BZ,
Паначек Е.А.,
Jouriles NJ.
Тяжелый рабдомиолиз с почечной недостаточностью после интраназального употребления кокаина. J Emerg Med .1997; 15: 833–7.
14. Дар К.Дж.,
McBrien ME.
МДМА-индуцированная гипертермия: отчет о летальном исходе и обзор текущей терапии. Intensive Care Med .
1996; 22: 995–6.
15. Pedrozzi NE,
Рамелли ГП,
Tomasetti R,
Нобиле-Буэтти Л,
Bianchetti MG.
Рабдомиолиз и анестезия: отчет о двух случаях и обзор литературы. Педиатр Нейрол .
1996; 15: 254–7.
16. Брамбак Р.А.,
Отзыв DL,
Пиявка RW.Рабдомиолиз после поражения электрическим током. Семин Нейрол .
1995; 15: 329–34.
17. Ван А.Ю.,
Ли ПК,
Луи СФ,
Лай К.Н.
Почечная недостаточность и тепловой удар. Ren Fail .
1995; 17: 171–17.
18. Могтадер Дж.,
Брэди WJ,
Бонадио В.
Рабдомиолиз при физической нагрузке у спортсмена-подростка. Скорая педиатрическая помощь .
1997; 13: 382–5.
19. Синкелер ИП,
Веверс Р.А.,
Йостен Э.М.,
Бинкхорст РА,
Oei LT,
Вант Хоф М.А.,
и другие.Улучшение скрининга миалгии при физической нагрузке с помощью стандартизированного ишемического теста предплечья. Мышечный нерв .
1986; 9: 731–7.
20. Акмал М,
Массри С.Г.
Обратимая печеночная дисфункция, связанная с рабдомиолизом. Ам Дж. Нефрол .
1990; 10: 49–52.
21. Палата ММ.
Факторы, позволяющие прогнозировать острую почечную недостаточность при рабдомиолизе. Arch Intern Med .
1988; 148: 1553–7.
22. Шварц Ю.Т.,
Brumback RJ,
Лакатош Р,
Пока А,
Батон GH,
Берджесс AR.Синдром острого компартмента бедра. Спектр травм. Хирургия костного сустава J [Am] .
1989. 71: 392–400.
23. Одех М.
Роль реперфузионного повреждения в патогенезе синдрома раздавливания. N Engl J Med .
1991; 324: 1417–22.
24. Синерт Р,
Коль Л,
Райноне Т,
Скалея Т.
Рабдомиолиз, вызванный физической нагрузкой. Энн Эмерг Мед .
1994; 23: 1301–6.
25. Загер Р.А.Рабдомиолиз и острая миоглобин-мочевая почечная недостаточность [От редакции]. Почки Инт .
1996; 49: 314–26.
26. Лучшая ОС,
Рубинштейн I,
Winaver JM,
Knochel JP.
Повторный визит к маннитолотерапии (1940–1997). Почки Инт .
1997. 52: 886–94.
27. Homsi E,
Баррейро М.Ф.,
Орландо Дж. М.,
Higa EM.
Профилактика острой почечной недостаточности у больных рабдомиолизом. Ren Fail .1997; 19: 283–8.
28. Загер Р.А.
Комбинированная терапия маннитом и дефероксамином при миоглобинурическом поражении почек и оксидантном канальцевом стрессе. Механические и терапевтические последствия. Дж. Клин Инвест .
1992; 90: 711–9.
29. Акмаль м.,
Епископ И.Е.,
Телфер Н,
Норман А.В.,
Массри С.Г.
Гипокальциемия и гиперкальциемия у пациентов с рабдомиолизом с острой почечной недостаточностью и без нее. Дж. Клин Эндокринол Метаб .1986; 63: 137–42.
Механизмы атрофии и гипертрофии мышц: последствия для здоровья и болезней
Баскин К. К., Виндерс Б. Р. и Олсон Э. Н. Мышцы как «посредник» системного метаболизма. Cell Metab. 21 , 237–248 (2015).
CAS
PubMed
PubMed Central
Статья
Google ученый
Sandri, M. et al. PGC-1alpha защищает скелетные мышцы от атрофии, подавляя действие FoxO3 и транскрипцию специфичных для атрофии генов. Proc. Natl Acad. Sci. США 103 , 16260–16265 (2006).
ADS
CAS
PubMed
Статья
PubMed Central
Google ученый
Brocca, L. et al. FoxO-зависимые атрогены различаются в зависимости от катаболических состояний и играют ключевую роль в атрофии мышц, вызванной подвешиванием задних конечностей. J. Physiol. 595 , 1143–1158 (2017).
CAS
PubMed
Статья
PubMed Central
Google ученый
Grumati, P. et al. Физические упражнения стимулируют аутофагию в нормальных скелетных мышцах, но вредны для мышц с дефицитом коллагена VI. Аутофагия 7 , 1415–1423 (2011).
CAS
PubMed
PubMed Central
Статья
Google ученый
Лю, Г. Ю. и Сабатини, Д. М. mTOR на стыке питания, роста, старения и болезней. Нат. Rev. Mol. Cell Biol. 21 , 183–203 (2020).
CAS
PubMed
Статья
PubMed Central
Google ученый
Musaro, A. et al. Локальная экспрессия трансгена Igf-1 поддерживает гипертрофию и регенерацию стареющих скелетных мышц. Нат. Genet. 27 , 195–200 (2001).
CAS
PubMed
Статья
PubMed Central
Google ученый
Ascenzi, F. et al.Влияние изоформ IGF-1 на рост мышц и саркопению. Ячейка старения 18 , e12954 (2019).
PubMed
PubMed Central
Статья
CAS
Google ученый
Murgia, M. et al. Ras участвует в зависимой от нервной активности регуляции мышечных генов. Нат. Cell Biol. 2 , 142–147 (2000).
CAS
PubMed
Статья
PubMed Central
Google ученый
Pallafacchina, G., Calabria, E., Serrano, A. L., Kalhovde, J. M. & Schiaffino, S. Зависимый от протеинкиназы B и чувствительный к рапамицину путь контролирует рост скелетных мышц, но не определение типа волокна. Proc. Natl Acad. Sci. США 99 , 9213–9218 (2002).
ADS
CAS
PubMed
Статья
PubMed Central
Google ученый
Blaauw, B. et al. Индуцируемая активация Akt увеличивает массу и силу скелетных мышц без активации сателлитных клеток. Faseb J. 23 , 3896–3905 (2009).
CAS
PubMed
Статья
Google ученый
Bentzinger, C.F. et al. Специфическая абляция скелетных мышц хищника, но не риктора, вызывает метаболические изменения и приводит к мышечной дистрофии. Cell Metab. 8 , 411–424 (2008).
CAS
PubMed
Статья
Google ученый
Risson, V. et al. Мышечная инактивация mTOR вызывает метаболические и дистрофиновые дефекты, приводящие к тяжелой миопатии. J. Cell Biol. 187 , 859–874 (2009).
CAS
PubMed
PubMed Central
Статья
Google ученый
You, J. S. et al. Роль хищника в индуцированной механической нагрузкой регуляции передачи сигналов mTOR, синтеза белка и гипертрофии скелетных мышц. FASEB J. 33 , 4021–4034 (2019).
CAS
PubMed
Статья
Google ученый
Zhang, Q. et al. Недостаток мышечной активности киназы mTOR вызывает раннее начало миопатии и нарушает гомеостаз всего тела. J. Cachexia Sarcopenia Muscle 10 , 35–53 (2019).
PubMed
Статья
Google ученый
Castets, P. et al. Устойчивая активация mTORC1 в скелетных мышцах подавляет конститутивную аутофагию и аутофагию, вызванную голоданием, и вызывает тяжелую миопатию с поздним началом. Cell Metab. 17 , 731–744 (2013).
CAS
PubMed
Статья
Google ученый
Макферрон, А. К., Лоулер, А. М. и Ли, С. Дж. Регулирование массы скелетных мышц у мышей новым членом суперсемейства TGF-бета. Nature 387 , 83–90 (1997).
ADS
CAS
PubMed
Статья
Google ученый
Sartori, R. et al. Факторы транскрипции Smad2 и 3 контролируют мышечную массу в зрелом возрасте. Am. J. Physiol. Cell Physiol. 296 , C1248 – C1257 (2009).
CAS
PubMed
Статья
Google ученый
Winbanks, C.E. et al. Фоллистатин-опосредованная гипертрофия скелетных мышц регулируется Smad3 и mTOR независимо от миостатина. J. Cell Biol. 197 , 997–1008 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Sartori, R. et al. Передача сигналов BMP контролирует мышечную массу. Нат. Genet. 45 , 1309–1318 (2013).
CAS
PubMed
Статья
Google ученый
Traore, M. et al. Эмбриональная изоформа CaVbeta1 способствует поддержанию мышечной массы посредством передачи сигналов GDF5 у взрослых мышей. Sci. Пер. Med. 11 , eaaw1131 (2019).
CAS
PubMed
Статья
Google ученый
Winbanks, C.E. et al. Доставка гена Smad7 предотвращает мышечное истощение, связанное с раковой кахексией у мышей. Sci. Пер. Med. 8 , 348ra398 (2016).
Артикул
CAS
Google ученый
Дэви, Дж.R. et al. Комплексный анализ экспрессии мышечной гипертрофии определяет Asb2 как негативный регулятор мышечной массы. JCI Insight 1 , e85477 (2016).
PubMed
PubMed Central
Статья
Google ученый
Winbanks, C.E. et al. Ось костного морфогенетического белка является положительным регулятором массы скелетных мышц. J. Cell Biol. 203 , 345–357 (2013).
CAS
PubMed
PubMed Central
Статья
Google ученый
Клайн, У. О., Панаро, Ф. Дж., Янг, Х. и Бодин, С. С. Рапамицин подавляет рост и эффекты кленбутерола в плане сохранения мышц. J. Appl. Physiol. 102 , 740–747 (2007).
CAS
PubMed
Статья
Google ученый
Goncalves, D. A. et al. Передача сигналов инсулина / IGF1 опосредует эффекты бета2-адренергического агониста на протеостаз и рост мышц. J. Cachexia Sarcopenia Muscle 10 , 455–475 (2019).
PubMed
PubMed Central
Статья
Google ученый
Benoit, B. et al. Фактор роста фибробластов 19 регулирует массу скелетных мышц и уменьшает мышечное истощение у мышей. Нат. Med. 23 , 990–996 (2017).
CAS
PubMed
Статья
Google ученый
Ост, Л. Дж., Кустерманн, М., Армани, А., Блаау, Б. и Романелло, В.Фактор роста фибробластов 21 контролирует митофагию и мышечную массу. J. Cachexia Sarcopenia Muscle 10 , 630–642 (2019).
PubMed
PubMed Central
Статья
Google ученый
Коэн, С., Ли, Д., Чжай, Б., Гайги, С. П. и Голдберг, А. Л. Trim32 снижает передачу сигналов PI3K-Akt-FoxO при мышечной атрофии, способствуя диссоциации плакоглобина-PI3K. J. Cell Biol. 204 , 747–758 (2014).
CAS
PubMed
PubMed Central
Статья
Google ученый
Summermatter, S. et al. Блокада металлотионеинов 1 и 2 увеличивает массу и силу скелетных мышц. Мол. Cell Biol. 37 , e00305-16 (2017).
Wang, G. et al. Метастатический рак способствует развитию кахексии за счет активации ZIP14 в скелетных мышцах. Нат. Med. 24 , 770–781 (2018).
CAS
PubMed
PubMed Central
Статья
Google ученый
Mammucari, C. et al. Митохондриальный унипортер кальция контролирует трофику скелетных мышц in vivo. Cell Rep. 10 , 1269–1279 (2015).
CAS
PubMed
PubMed Central
Статья
Google ученый
Ruas, J. L. et al. Изоформа PGC-1альфа, индуцированная тренировкой с отягощениями, регулирует гипертрофию скелетных мышц. Ячейка 151 , 1319–1331 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
White, J. P. et al. Рецептор 56, связанный с G-белком, регулирует гипертрофию мышц, вызванную механической перегрузкой. Proc. Natl Acad. Sci. США 111 , 15756–15761 (2014).
ADS
CAS
PubMed
Статья
Google ученый
Das, S. et al. Цитратлиаза АТФ улучшает функцию митохондрий в скелетных мышцах. Cell Metab. 21 , 868–876 (2015).
CAS
PubMed
Статья
Google ученый
Cai, X. et al. Альфа-кетоглутарат способствует гипертрофии скелетных мышц и синтезу белка через сигнальные пути Akt / mTOR. Sci. Отчет 6 , 26802 (2016).
ADS
CAS
PubMed
PubMed Central
Статья
Google ученый
Lahiri, S. et al. Микробиота кишечника влияет на массу и функцию скелетных мышц у мышей. Sci. Пер. Med. 11 , eaan5662 (2019).
Hunt, L.C. et al. Ключевая роль убиквитинлигазы UBR4 в гипертрофии миофибрилл у дрозофилы и мышей. Cell Rep. 28 , 1268–1281 e1266 (2019).
CAS
PubMed
PubMed Central
Статья
Google ученый
Conte, M. et al. Мышечно-специфическое подавление перилипина2 влияет на метаболизм липидов и вызывает гипертрофию миофибрилл. J. Cachexia Sarcopenia Muscle 10 , 95–110 (2019).
PubMed
Статья
Google ученый
Bodine, S.C. et al. Идентификация убиквитинлигаз, необходимых для атрофии скелетных мышц. Наука 294 , 1704–1708 (2001).
ADS
CAS
PubMed
Статья
Google ученый
Pankiv, S. et al. p62 / SQSTM1 связывается непосредственно с Atg8 / LC3, облегчая деградацию убиквитинированных белковых агрегатов за счет аутофагии. J. Biol. Chem. 282 , 24131–24145 (2007).
CAS
PubMed
Статья
Google ученый
Сандри, М. Распад белка при мышечном истощении: роль аутофагии-лизосомы и убиквитин-протеасомы. Внутр. J. Biochem Cell Biol. 45 , 2121–2129 (2013).
CAS
PubMed
PubMed Central
Статья
Google ученый
Коэн, С., Натан, Дж. А. и Голдберг, А. Л. Мышечное истощение при болезни: молекулярные механизмы и перспективные методы лечения. Нат. Rev. Drug Discov. 14 , 58–74 (2015).
CAS
PubMed
Статья
Google ученый
Cadena, S. M. et al. Скелетные мышцы мышей, нулевых по MuRF1, не защищены в условиях низкой гравитации, что указывает на то, что атрофия происходит с помощью уникальных механизмов в космосе. Sci. Отчетность 9 , 9397 (2019).
ADS
PubMed
PubMed Central
Статья
CAS
Google ученый
Баер, Л. М., Ферлоу, Дж. Д. и Бодин, С. С. Сохранение мускулов в мышцах, нулевых по кольцу 1-го пальца мыши: ответ на синтетические глюкокортикоиды. J. Physiol. 589 , 4759–4776 (2011).
CAS
PubMed
PubMed Central
Статья
Google ученый
Хви, Д. Т., Баер, Л. М., Филп, А., Баар, К. и Бодин, С. С. Поддержание мышечной массы и индуцированный нагрузкой рост в мышцах нулевых мышей RING Finger 1 с возрастом. Ячейка старения 13 , 92–101 (2014).
CAS
PubMed
Статья
PubMed Central
Google ученый
Sandri, M. et al. Сигнальные пути, регулирующие мышечную массу в стареющих скелетных мышцах. Роль пути IGF1-Akt-mTOR-FoxO. Биогеронтология 14 , 303–323 (2013).
CAS
PubMed
Статья
PubMed Central
Google ученый
Cohen, S., Zhai, B., Gygi, S.P. & Goldberg, A.L. Убиквитилирование с помощью Trim32 вызывает сопряженную потерю десмина, Z-полос и тонких волокон при мышечной атрофии. J. Cell Biol. 198 , 575–589 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Di Rienzo, M. et al. Для индукции аутофагии в атрофических мышечных клетках требуется активация ULK1 с помощью TRIM32 через незакрепленные цепи полиубиквитина, связанные с K63. Sci. Adv. 5 , eaau8857 (2019).
ADS
CAS
PubMed
PubMed Central
Статья
Google ученый
Paul, P. K. et al. Целенаправленное удаление TRAF6 подавляет истощение скелетных мышц у мышей. J. Cell Biol. 191 , 1395–1411 (2010).
CAS
PubMed
PubMed Central
Статья
Google ученый
Paul, P. K. et al. Убиквитинлигаза E3 TRAF6 вмешивается в вызванную голоданием атрофию скелетных мышц посредством множества механизмов. Мол. Cell Biol. 32 , 1248–1259 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Карнио, С.и другие. Нарушение аутофагии в мышцах вызывает дегенерацию нервно-мышечных соединений и преждевременное старение. Cell Rep. 8 , 1509–1521 (2014).
CAS
PubMed
PubMed Central
Статья
Google ученый
Bujak, A. L. et al. AMPK-активация мышечной аутофагии предотвращает гипогликемию и миопатию, вызванные голоданием, во время старения. Cell Metab. 21 , 883–890 (2015).
CAS
PubMed
PubMed Central
Статья
Google ученый
Raben, N. et al. Подавление аутофагии в скелетных мышцах раскрывает накопление убиквитинированных белков и их потенциальную роль в повреждении мышц при болезни Помпе. Гум. Мол. Genet. 17 , 3897–3908 (2008).
CAS
PubMed
PubMed Central
Статья
Google ученый
Немазаный И.И. и др. Дефекты Vps15 в скелетных мышцах приводят к аутофагической вакуолярной миопатии и лизосомной болезни. EMBO Mol. Med. 5 , 870–890 (2013).
CAS
PubMed
PubMed Central
Статья
Google ученый
Fuqua, J. D. et al. ULK2 необходим для деградации убиквитинированных белковых агрегатов и гомеостаза в скелетных мышцах. FASEB J 33 , 11735–12745 (2019).
Ryu, D. et al. Уролитин А вызывает митофагию и увеличивает продолжительность жизни у C.elegans и увеличивает мышечную функцию у грызунов. Нат. Med. 22 , 879–888 (2016).
CAS
PubMed
Статья
Google ученый
Milan, G. et al. Регуляция аутофагии и убиквитин-протеасомной системы транскрипционной сетью FoxO во время мышечной атрофии. Нат. Commun. 6 , 6670 (2015).
ADS
CAS
PubMed
PubMed Central
Статья
Google ученый
Ли Д., Такаяма С. и Голдберг А. Л. ZFAND5 / ZNF216 является активатором протеасомы 26S, который стимулирует общую деградацию белка. Proc. Natl Acad. Sci. США 115 , E9550 – E9559 (2018).
CAS
PubMed
Статья
Google ученый
VerPlank, J. J. S., Lokireddy, S., Zhao, J. & Goldberg, A. L. 26S протеасомы быстро активируются различными гормонами и физиологическими состояниями, которые повышают цАМФ и вызывают фосфорилирование Rpn6. Proc. Natl Acad. Sci. США 116 , 4228–4237 (2019).
Piccirillo, R. & Goldberg, A. L. АТФаза p97 / VCP имеет решающее значение при атрофии мышц и ускоренной деградации мышечных белков. EMBO J. 31 , 3334–3350 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Wang, C. et al. Метилтрансферазоподобный 21c метилирует и стабилизирует белок теплового шока Hspa8 в миофибриллах I типа у мышей. J. Biol. Chem. 294 , 13718–13728 (2019).
CAS
PubMed
PubMed Central
Статья
Google ученый
Wiederstein, J. L. et al. Метилтрансфераза METTL21C, специфичная для скелетных мышц, триметилирует p97 и регулирует распад белка, связанный с аутофагией. Cell Rep. 23 , 1342–1356 (2018).
CAS
PubMed
Статья
Google ученый
O’Neill, B.T. et al. Факторы транскрипции FoxO являются критическими регуляторами мышечной атрофии, связанной с диабетом. Диабет 68 , 556–570 (2019).
PubMed
Статья
CAS
Google ученый
Segales, J. et al. Сестрин предотвращает атрофию вышедших из употребления и стареющих мышц, интегрируя анаболические и катаболические сигналы. Нат. Commun. 11 , 189 (2020).
ADS
CAS
PubMed
PubMed Central
Статья
Google ученый
Beharry, A. W. et al. HDAC1 активирует FoxO и является достаточным и необходимым для атрофии скелетных мышц. J. Cell Sci. 127 , 1441–1453 (2014).
CAS
PubMed
PubMed Central
Статья
Google ученый
Bertaggia, E., Coletto, L., Sandri, M. Посттрансляционные модификации контролируют активность FoxO3 во время денервации. Am. J. Physiol. Cell Physiol. 302 , C587 – C596 (2012).
CAS
PubMed
Статья
Google ученый
Браулт, Дж. Дж., Джесперсен, Дж. Г. и Голдберг, А. Л. Гамма-коактиватор рецептора, активируемого пролифератором пероксисом, гиперэкспрессия 1альфа или 1бета ингибирует деградацию мышечного белка, индукцию убиквитинлигаз и атрофию неиспользования. J. Biol. Chem. 285 , 19460–19471 (2010).
CAS
PubMed
PubMed Central
Статья
Google ученый
Raffaello, A. et al. Фактор транскрипции JunB поддерживает массу скелетных мышц и способствует гипертрофии. J. Cell Biol. 191 , 101–113 (2010).
CAS
PubMed
PubMed Central
Статья
Google ученый
Yin, J. et al. Dkk3-зависимая регуляция транскрипции контролирует возрастную атрофию скелетных мышц. Нат. Commun. 9 , 1752 (2018).
ADS
PubMed
PubMed Central
Статья
CAS
Google ученый
Shimizu, N. et al. Перекрестные помехи между рецептором глюкокортикоидов и датчиком питания mTOR в скелетных мышцах. Cell Metab. 13 , 170–182 (2011).
CAS
PubMed
Статья
Google ученый
Cai, D. et al. Активация IKKbeta / NF-kappaB вызывает у мышей тяжелое мышечное истощение. Cell 119 , 285–298 (2004).
CAS
PubMed
Статья
Google ученый
Mittal, A. et al. Система TWEAK-Fn14 является критическим регулятором вызванной денервацией атрофии скелетных мышц у мышей. J. Cell Biol. 188 , 833–849 (2010).
CAS
PubMed
PubMed Central
Статья
Google ученый
Bonetto, A. et al. Ингибирование пути JAK / STAT3 блокирует истощение скелетных мышц ниже IL-6 и при экспериментальной раковой кахексии. Am. J. Physiol. Эндокринол.Метаб. 303 , E410 – E421 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Ebert, S. M. et al. Вызванная стрессом экспрессия Gadd45a в скелетных мышцах перепрограммирует миоядра и вызывает атрофию мышц. J. Biol. Chem. 287 , 27290–27301 (2012).
CAS
PubMed
PubMed Central
Статья
Google ученый
Gallot, Y. S. et al. PERK регулирует массу скелетных мышц и сократительную функцию у взрослых мышей. FASEB J. 33 , 1946–1962 (2019).
CAS
PubMed
Статья
Google ученый
Bohnert, K. R. et al. Ось передачи сигналов toll-подобного рецептора / MyD88 / XBP1 опосредует истощение скелетных мышц во время раковой кахексии. Мол. Ячейка Биол . 39 , e00184-19 (2019).
Tezze, C. et al. Связанная с возрастом потеря OPA1 в мышцах влияет на мышечную массу, метаболический гомеостаз, системное воспаление и старение эпителия. Cell Metab. 25 , 1374–1389 e1376 (2017).
CAS
PubMed
PubMed Central
Статья
Google ученый
Favaro, G. et al. DRP1-опосредованная форма митохондрий контролирует гомеостаз кальция и мышечную массу. Нат. Commun. 10 , 2576 (2019).
ADS
PubMed
PubMed Central
Статья
CAS
Google ученый
Choi, S. et al. Специфическая для скелетных мышц делеция Prmt1 вызывает атрофию мышц за счет нарушения регуляции оси PRMT6-FOXO3. Аутофагия 15 , 1069–1081 (2019).
CAS
PubMed
PubMed Central
Статья
Google ученый
Сегатто, М.и другие. Эпигенетическое нацеливание на белок бромодомена BRD4 противодействует раковой кахексии и продлевает выживаемость. Нат. Commun. 8 , 1707 (2017).
ADS
PubMed
PubMed Central
Статья
CAS
Google ученый
Bowman, C.J., Ayer, D. E. & Dynlacht, B.D. Белки Foxk подавляют запуск программ атрофии и аутофагии, вызванных голоданием. Нат. Cell Biol. 16 , 1202–1214 (2014).
CAS
PubMed
PubMed Central
Статья
Google ученый
Sun, L. et al. Длинная некодирующая РНК Atrolnc-1 способствует истощению мышц у мышей с хроническим заболеванием почек. J. Cachexia Sarcopenia Muscle 9 , 962–974 (2018).
PubMed
PubMed Central
Статья
Google ученый
Kravic, B. et al. В скелетных мышцах млекопитающих фосфорилирование TOMM22 протеинкиназой CSNK2 / CK2 контролирует митофагию. Аутофагия 14 , 311–335 (2018).
CAS
PubMed
PubMed Central
Статья
Google ученый
Pin, F. et al. PDK4 вызывает метаболические изменения и атрофию мышц при раковой кахексии. FASEB J. 33 , 7778–7790 (2019).
CAS
PubMed
PubMed Central
Статья
Google ученый
He, W. A. et al. Опосредованная NF-kappaB нарушение регуляции Pax7 в мышечном микроокружении способствует раковой кахексии. J. Clin. Расследование. 123 , 4821–4835 (2013).
CAS
PubMed
Статья
Google ученый
Parajuli, P. et al. Активация Twist1 в мышечных клетках-предшественниках вызывает потерю мышечной массы, подобную раковой кахексии. Dev. Ячейка 45 , 712–725 e716 (2018).
CAS
PubMed
PubMed Central
Статья
Google ученый
Madaro, L. et al. Активированная денервацией передача сигналов STAT3-IL-6 в фибро-адипогенных предшественниках способствует атрофии и фиброзу миофибрилл. Нат. Cell Biol. 20 , 917–927 (2018).
CAS
PubMed
PubMed Central
Статья
Google ученый
Zhang, G. et al. Опухоль вызывает истощение мышц у мышей за счет высвобождения внеклеточных Hsp70 и Hsp90. Нат. Commun. 8 , 589 (2017).
ADS
PubMed
PubMed Central
Статья
CAS
Google ученый
Ekelund, U. et al. Уменьшает ли физическая активность или даже устраняет вредную связь времени сидения со смертностью? Гармонизированный мета-анализ данных более чем 1 миллиона мужчин и женщин. Ланцет 388 , 1302–1310 (2016).
Артикул
Google ученый
Чакраварти, Э. Ф., Хуберт, Х. Б., Лингала, В. Б. и Фрис, Дж. Ф. Снижение инвалидности и смертности среди стареющих бегунов: 21-летнее продольное исследование. Arch. Междунар. Med. 168 , 1638–1646 (2008).
PubMed
PubMed Central
Статья
Google ученый
Hall, D. T. et al. Агонист AMPK 5-аминоимидазол-4-карбоксамид рибонуклеотид (AICAR), но не метформин, предотвращает связанное с воспалением кахектическое истощение мышц. EMBO Mol. Med. 10 , e8307 (2018).
PubMed
PubMed Central
Статья
CAS
Google ученый
Mills, K. F. et al. Длительное введение никотинамидмононуклеотида снижает физиологический спад у мышей, связанный с возрастом. Cell Metab. 24 , 795–806 (2016).
CAS
PubMed
PubMed Central
Статья
Google ученый
Wagner, K. R. et al. Испытание фазы I / II MYO-029 у взрослых с мышечной дистрофией. Ann. Neurol. 63 , 561–571 (2008).
CAS
PubMed
Статья
Google ученый
Golan, T. et al. LY2495655, антитело к антимиостатину, при раке поджелудочной железы: рандомизированное исследование фазы 2. J. Cachexia Sarcopenia Muscle 9 , 871–879 (2018).
PubMed
PubMed Central
Статья
Google ученый
Porporato, P.E. et al. Ацилированный и неацилированный грелин ухудшают атрофию скелетных мышц у мышей. J. Clin. Расследование. 123 , 611–622 (2013).
CAS
PubMed
Google ученый
Garcia, J. M. et al. Анаморелин для пациентов с раковой кахексией: комплексный анализ двух рандомизированных плацебо-контролируемых двойных слепых исследований фазы 2. Ланцет Онкол. 16 , 108–116 (2015).
CAS
PubMed
Статья
Google ученый
Baraldo, M. et al. Скелетная мышца mTORC1 регулирует стабильность нервно-мышечного соединения. J. Cachexia Sarcopenia Muscle 11 , 208–225 (2019).
Pietrocola, F. et al. Спермидин вызывает аутофагию, ингибируя ацетилтрансферазу EP300. Cell Death Differ. 22 , 509–516 (2015).
CAS
PubMed
Статья
Google ученый
Koeberl, D. D. et al. Коррекция биохимических нарушений и улучшение мышечной функции в клинических испытаниях фазы I / II кленбутерола при болезни Помпе. Мол. Ther. 26 , 2304–2314 (2018).
CAS
PubMed
PubMed Central
Статья
Google ученый
Adams, V. et al. Опосредованное низкими молекулами химическое подавление MuRF1 / MuRF2 и ослабление дисфункции диафрагмы при хронической сердечной недостаточности. J. Cachexia Sarcopenia Muscle 10 , 1102–1115 (2019).
PubMed
PubMed Central
Статья
Google ученый
Границы | Атрофия мышц из-за повреждения нервов сопровождается повышенной скоростью синтеза миофибриллярных белков
Введение
Скелетная мышца — самый большой орган человеческого тела, составляющий не менее 40% его массы и содержащий 50–75% всех белков организма (Frontera and Ochala, 2015).Это имеет решающее значение для здоровья и передвижения, а недостаток мышечной массы и силы связан с серьезным снижением независимости, качества жизни и ожидаемой продолжительности жизни (Metter et al., 2002; Wannamethee et al., 2007). Многие клинические состояния сопровождаются потерей мышечной массы, например, рак, ХОБЛ или сердечная недостаточность (Rosenberg, 1997; Al-Majid and McCarthy, 2001; Marquis et al., 2002; Thomas, 2007). В настоящее время не существует лекарственного лечения мышечной атрофии, при этом упражнения и обильное потребление белка являются единственными добросовестными вмешательствами, направленными на медленную потерю мышечной массы (Sepulveda et al., 2015; Гарбер, 2016). Однако бывают ситуации с потерей мышечной массы, когда физическая активность недопустима. Например, у пациентов с переломами, у пациентов в критическом состоянии или у пациентов с повреждением нервов. Повреждение периферических нервов — часто встречающееся клиническое состояние, которое может быть вызвано болезнью или травмой (Dyck, 2005). Распространенной моделью для изучения повреждения периферического нерва является хроническое повреждение нерва сужением (Bennett and Xie, 1988). Хроническое сужение нерва сопровождается изнурительными симптомами, такими как невропатическая боль, нарушение двигательной функции и атрофия скелетных мышц (Bennett and Xie, 1988).Несмотря на то, что нервная функция может восстановиться, это часто переживается ухудшающимся воздействием на мышечную ткань. Хотя хроническое сужение нерва хорошо изучено в отношении его последствий для боли у животных, очень мало известно о физиологии мышечного истощения.
Мышечная масса определяется балансом между синтезом мышечного белка (MPS) и распадом мышечного белка (MPB). Любая сторона баланса может быть нарушена. Следовательно, предполагается, что большинство мышечных атрофий демонстрируют комбинацию снижения MPS и увеличения MPB (McKinnell and Rudnicki, 2004).Тем не менее, индивидуальный вклад снижения MPS может различаться для разных типов атрофий. Например, при атрофии неиспользования у людей снижение показателей МПС, по-видимому, является преобладающей причиной снижения мышечной массы (Wall et al., 2013a, b, 2016). Аналогичным образом, снижение MPS было зарегистрировано при голодании, саркопении, кахексии и других состояниях мышечной атрофии, что указывает на потенциальную пользу вмешательств, которые увеличивают MPS (Emery et al., 1984; Yarasheski et al., 1993; Hector et al., 2018).При атрофии, вызванной повреждением нервов, ранние исследования предполагали различные эффекты денервации на MPS. В зависимости от момента времени у очень молодых крыс после перерезки нерва было обнаружено как снижение, так и кратковременное повышение показателей МПС (Goldspink, 1976, 1978; Goldspink et al., 1983). Неизвестно, как хроническое сужение нервов у взрослых животных влияет на показатели MPS. Кроме того, предыдущие исследования, в которых использовалось мечение стабильных изотопов с использованием метода непрерывной инфузии с затоплением или примированной дозой, были ограничены периодом оценки MPS в несколько часов, что уменьшало их способность прогнозировать абсолютные изменения мышечной массы (Mitchell et al., 2014; Reid et al., 2014). Однако повторное появление оксида дейтерия (D 2 O) в качестве средства изучения интегрированного MPS in vivo в течение нескольких дней или недель предлагает привлекательное решение этой проблемы (Busch et al., 2006; Wilkinson et al. ., 2014; Дамас и др., 2016).
Поэтому мы решили исследовать влияние хронического сужения нерва на МПС. Мы объединили долгосрочные эксперименты с D 2 O-опосредованным индикатором на взрослых крысах с абсолютными изменениями мышечной массы, иммуногистохимическим анализом и данными экспрессии белка.Мы предположили, что сужение нерва приведет к снижению частоты MPS. Однако мы обнаружили, что, несмотря на значительную потерю мышечной массы, атрофия, вызванная повреждением нервов, сопровождается хронически повышенной, а не сниженной скоростью синтеза миофибриллярного белка (MPS).
Материалы и методы
Этическое одобрение и эксперименты на животных
Эксперименты на животных были одобрены местными властями (Landesamt für Gesundheit und Soziales, Берлин, Германия) под номером G 0083/15 и проводились в отделении по уходу за животными Центра молекулярной медицины Макса Дельбрюка (MDC, Берлин).
Модель повреждения нервов
Десять крыс-самцов Sprague-Dawley [Crl: CD (SD), Charles River, Sulzfeld, Germany] в возрасте 20–21 недель содержали в индивидуальных клетках. Животные получали корм из 20 г корма (ssniff Spezialdiäten GmbH, Soest, Германия) (дополнительный рисунок 1), эквивалентный 79 ккал * день -1 для замедления обычно происходящего набора веса. Повреждение нерва было вызвано хроническим сужением седалищного нерва (Sommer, 2013). Крыс анестезировали путем ингаляции изофлураном (~ 2.5%) и лечили инъекцией 4–5 мг карпрофена * кг -1 массы тела для уменьшения послеоперационной боли. Разрез был сделан вдоль бедренной кости, и латеральная широкая мышца бедра была отсоединена от двуглавой мышцы бедра тупым рассечением. Седалищный нерв обнажали выше точки трифуркации, и повреждение сужения было вызвано имплантацией манжеты вокруг нерва. Для дальнейшего уменьшения послеоперационной боли животные получали метамизол в дозе 100 мг * кг -1 .В течение последних 2 недель животных дважды в неделю подвергали электростимуляции для поддержания повреждения нерва и ухудшения восстановления, как было описано ранее (Baptista et al., 2008; Gigo-Benato et al., 2010). Животных вскрывали через 4 недели после операции, в возрасте от 24 до 25 недель. В голодном состоянии животных помещали под глубокую анестезию посредством ингаляции изофлурана (~ 3,5%) и собирали TA и длинных разгибателей пальцев (EDL). Мышцы быстро взвешивали и разрезали пополам, причем одну часть немедленно замораживали в жидком азоте, а другую часть погружали в трагакантовую камедь для гистологического анализа и замораживали в изопентане.
D
2 O Протокол маркировки
Мы использовали протокол маркировки, подходящий для обнаружения обогащения дейтерия ( 2 H) аланином миофибриллярной белковой фракции скелетных мышц с помощью ГХ-МС, аналогичный тому, который был опубликован ранее (Busch et al., 2006; Gasier et al. , 2009). Вкратце, через 2 недели после операции животным внутрибрюшинно вводили 0,014 мл * г -1 массы тела D 2 O (99,8% + Atom D, Euriso-Top GmbH Saarbrücken) и 0.9% NaCl. Эта инъекция примировала животных и повысила уровень воды в их организме приблизительно до 2,5% D 2 O. Для поддержания указанной концентрации крысы получали питьевую воду с обогащением 4% 2 H 2 O.
Экстракция миофибриллярного белка
Выделение миофибриллярного белка выполняли, как описано ранее (Burd et al., 2012). Вкратце, 80–120 мг мышечного образца ТА крысы ( n = 10) взвешивали в пробирке Эппендорфа и хранили на льду.Стандартный буферный раствор добавляли к каждому образцу в количестве 10 мкл * мг -1 и мышечную ткань тщательно гомогенизировали. Ножницы использовали для измельчения ткани перед последующей гомогенизацией пластиковыми пестиками. Для фракционирования осадка, богатого миофибриллярными и другими структурными белками, образец центрифугировали при 700 г в течение 10 минут при 4 ° C. Оставшийся осадок дважды промывали буфером и dH 2 O, супернатант удаляли и к осадку добавляли 1 мл 0,3 NaOH для дальнейшей солюбилизации миофибриллярных белков и выделения их из коллагена.Образцы нагревали при 50 ° C в течение 30 мин. Затем образец центрифугировали при 10000 г в течение 5 минут при 4 ° C и супернатант, содержащий миофибриллярный белок, переносили в 4 мл стеклянные флаконы с завинчивающейся крышкой. В каждую стеклянную пробирку добавляли один миллилитр 1M PCA для денатурации оставшихся белков. После центрифугирования супернатант удаляли и осадок дважды промывали 500 мкл 70% EtOH. После удаления EtOH добавляли 1,5 мл 6M HCl для гидролиза образцов в течение ночи при 110 ° C.На следующий день образцы помещали в нагревательный блок (120 ° C) и сушили в атмосфере азота. Для дальнейшей очистки аминокислот образцы перед дериватизацией пропускали через обменную смолу Dowex (смола AG 50W-X8, Bio-Rad). После очистки стеклянные флаконы осторожно встряхивали и помещали в пар азота для сушки перед дериватизацией. Затем образцы, содержащие свободные аминокислоты фракции миофибриллярного белка, были преобразованы в их производные трет-бутилдиметилсилила (TBDMS) путем добавления к образцу 50 мкл N-трет-бутилдиметилсилил-N-метилтрифторацетамида (MTBSTFA) и 50 мкл ацетонитрила. .Затем каждый образец инкубировали в течение 1 ч при 70 ° C. Затем образец переносили во флаконы с хромаколовым колпачком на 2 мл (Thermo Fisher Scientific, Шверте, Германия), подходящие для инъекции методом ГХ-МС.
Экстракция белков плазмы
Для осаждения белков плазмы 40 мкл хлорной кислоты (20%) добавляли к 360 мкл образца плазмы. После встряхивания свободные аминокислоты отделяли от связанных с белком аминокислот центрифугированием (3500 об / мин, 20 мин, 4 ° C). Осадок собирали и трижды промывали 1 мл хлорной кислоты (2%) перед гидролизом в течение ночи, как описано выше.После гидролиза образцы очищали и обрабатывали для введения ГХ-МС, как описано выше. Значения немеченых образцов использовали в качестве базового контроля для обогащения 2 H аланином, связанным с белками плазмы.
Обогащение свободного аланина в плазме
Образцы плазмы размораживали на льду, и к образцу добавляли сухую 5-сульфосалициловую кислоту для депротеинизации, как описано ранее (Trommelen et al., 2016). После встряхивания образец вращали при 1000 г в течение 15 мин.Супернатант собирали, а затем очищали, обрабатывали и измеряли с помощью ГХ-МС, как описано в разделах выше.
Измерение методом ГХМС и анализ обогащения стабильными изотопами
Обогащение аланином определяли методом электронно-ионизационной газовой хроматографии-масс-спектрометрии (ГХ-МС; Agilent 6890N GC / 5973N MSD) с использованием выбранного ионного мониторинга масс 232, 233, 234, 235 и 236 для их немеченого и меченого h3-аланина. . Мы применили стандартные кривые регрессии для оценки линейности масс-спектрометра и для контроля потери индикатора.
Иммуноблоттинг
Примерно 400 мкм образца вырезали из гистологического блока и гомогенизировали в стандартном лизирующем буфере с использованием пестика. Концентрации белка в образцах определяли с использованием набора для анализа бицинхониновой кислоты (BCA) (Thermo Fisher Scientific, Schwerte, Германия). Требуемый объем 40 мкг белка на образец рассчитывали, разделяли на аликвоты и добавляли SDSPP (6 ×) и SDSPP в H 2 O (1 ×) до общего объема 15 мкл. Для разделения белков в каждом образце использовали коммерческие гели SDS (Invitrogen NuPAGE Bis-Tris Gel, Thermo Fisher Scientific, Schwerte, Германия) и электрофорез (130–200 В).Для переноса использовали технику полусухого блоттинга (45 мин при 18 В). Мембраны блокировали в TBS-T (4% сухое молоко) в течение 1 ч при комнатной температуре. Затем мембраны инкубировали с первым антителом в TBS-T (4% сухого молока) или BSA в течение ночи (дополнительная фигура 9). На следующий день образцы промывали TBS-T и добавляли второе антитело на 60 мин при комнатной температуре. После отмывки для проявления полос использовали хемилюминесценцию (ECL). Уровни экспрессии интересующих белковых полос непосредственно анализировали с помощью Image Studio Lite (LI-Cor, Lincoln, NE, США).Загрузка и перенос белка контролировали с помощью окрашивания по Понсо (дополнительный рисунок 2).
Гистохимия и иммунофлуоресценция
Окрашивание
Гомори трихромом и толуидиновым синим АТФазой проводили в соответствии с установленным протоколом (Engel and Cunningham, 1963; Ogilvie and Feeback, 1990). Для распределения типов волокон было измерено столько волокон на срез, сколько четко различимо по окрашиванию толуидиновым синим. Для волокон типа 2 это было примерно 50 на слайд, для гораздо менее распространенных волокон типа 1 — примерно 10.
Для иммунофлуоресцентного окрашивания свежесрезанные криосрезы оставляли на 1 час при комнатной температуре для высыхания, а затем фиксировали в 3,7% параформальдегиде. Затем срезы промывали и блокировали 3% BSA / PBS. После этого срезы инкубировали с антителом против GLUT4 (дополнительная фигура 9), CT-3, -3 / 5; 1: 1000 в PBS (1% BSA) в течение 1 ч при комнатной температуре. Срезы инкубировали с биотином против кролика (1: 200) в PBS и стрептавидином-Cy3 (1: 200). Ядра визуализировали с помощью Hoechst (1: 1000 в PBS) перед размещением на предметных стеклах с помощью Aqua Mount (Thermo Fisher Scientific, Schwerte, Германия).
Изображения были получены с использованием конфокального микроскопа Zeiss LSM 700 (Zeiss, Йена, Германия) и соответствующего программного обеспечения производителя Zen 2012. Мозаичные изображения ТА были созданы с помощью микроскопа Leica DFC 420 (Leica Microsystems, Ветцлар, Германия). Количество волокон анализировали путем подсчета каждого волокна в секции.
Анализ состава тела
Состав тела измеряли с помощью анализатора ЯМР во временной области Minispec LF90 II (6,5 мГц, Bruker Optics, США).Крыс помещали в ограничительную трубку и вставляли в прибор, который измерял массу жира, массу без жира и содержание жидкости в животном.
Расчеты скорости фракционного синтеза
Скорость синтеза миофибриллярного белка
рассчитывалась с использованием метода предшественник-продукт (Wall et al., 2013b).
FSR (% * d − 1) = (ΔMPEmyo / (ΔMPEplasma * t)) * 100
, где FSR — скорость фракционного синтеза миофибриллярных белков, ΔMPE myo — изменение обогащения 2 H аланином, связанным с мышечным белком, ΔMPE плазма — изменение обогащения 2 H аланином, обнаруженное в плазме и t — время.
Статистика
Статистические тесты применялись по мере необходимости в зависимости от количества выборки и группы. Данные представлены в виде точечной диаграммы разброса с линией, обозначающей среднее значение, среднее значение ± стандартное отклонение, или плавающих столбцов (от минимального до максимального значения) с линией, обозначающей среднее значение. После проверки нормальности данных применяли тест Стьюдента t или ANOVA с апостериорным тестом Тьюки в зависимости от количества групп. p — Значения ниже 0.05 были признаны значительными.
Результаты
Повреждение нерва вызывает значительную потерю мышц
Мы индуцировали повреждение седалищного нерва у здоровых самцов крыс SD. Мы наблюдали полностью развитый фенотип мышечного истощения через 28 дней после операции (Рисунки 1A – D). Сразу после операции у животных наблюдались признаки снижения иннервации пораженной задней конечности, как и ожидалось после повреждения периферического нерва (Gigo-Benato et al., 2010). У животных не было симптомов снижения бдительности или повседневной активности.Мышцы, иннервируемые седалищным нервом, потеряли значительную массу: через 28 дней масса ТА уменьшилась на 66%, с 946 до 350 мг (Рисунок 1B), EDL на 50% с 264 до 132 мг (Рисунок 1C). В районе м. soleus (SOL) потеря массы была менее выраженной. Масса мышц снизилась с 252 до 156 мг, что составляет примерно 38% потери мышечной массы (рис. 1D). Поскольку SOL почти полностью состоит из волокон типа 1 (Gregory et al., 2001), это может указывать на преобладающую атрофию волокон типа 2 в связи с неиспользованием, а не на нейрогенную атрофию.Мы проверили это с помощью гистологического анализа.
РИСУНОК 1. (A) Мозаичное изображение крысы tibialis anterior , окрашенной GLUT4. (B) Повреждение нерва вызывает значительную потерю мышечной массы на м. tibialis anterior (TA) ( n = 10), (C) m. длинный разгибатель пальцев (EDL) ( n, = 10) и (D) m. soleus (SOL) ( n = 9). ∗ p <0.05, ∗∗ p <0,01, ∗∗∗ p <0,001.
Атрофия волокон и ухудшение состава тела
Гистологический анализ на 28 день после начала повреждения нерва выявил признаки некротической миопатии с регенерирующими волокнами, волокнами с центрально расположенными ядрами, некротическими и атрофическими волокнами (рис. 2А). Диаметр Feret колеблется от 43–51 мкм в здоровых волокнах типа 1 и от 30–37 мкм в поврежденных волокнах типа 1 (рис. 2B).В волокнах типа 2а диаметр Ферета колеблется от 43–53 мкм в здоровой мышце и от 28–47 мкм в поврежденной мышце (рис. 2В). Волокна типа 2b варьировались от 52 до 63 мкм в здоровой и от 29 до 43 мкм в поврежденной мышце (рис. 2В). В целом, повреждение нерва вызвало уменьшение диаметра волокна во всех трех типах волокон (рис. 2В). В нашем исследовании волокна типа 2b были затронуты больше всего, их диаметр уменьшился на 41% (± 13%) (рис. 2B). Когда волокна типа 2a и -b были сгруппированы, потеря диаметра волокна была больше, чем у волокон типа 1 (дополнительный рисунок 3).Это подтверждает, что потеря мышечной массы в основном происходит из-за атрофии волокон 2-го типа, и объясняет, почему SOL продемонстрировал наименьшее снижение мышечной массы, состоящий почти исключительно из волокон 1-го типа (Gregory et al., 2001). Подсчитывали общее количество волокон в полном поперечном сечении ТА от контрольной мышцы и мышцы с повреждением нерва. В здоровой мышце мы обнаружили 13980 ± 999 по сравнению с 13270 ± 652 волокнами в поврежденной мышце (рис. 2С). Эти данные указывают на то, что мышечная атрофия была вызвана потерей массы отдельных волокон, а не уменьшением общего количества волокон, и все это соответствовало мышечной атрофии, а не дистрофии.
РИСУНОК 2. (A) Гистохимический анализ с помощью окрашивания трихромом по Гомори выявляет регенерирующие волокна, центрально расположенные ядра и некроз (верхняя панель). Окрашивание толуидиновым синим показывает специфичность типа волокна (нижняя панель). (B) Количественная оценка диаметра Ферета выявляет выраженную атрофию волокон типа 2b ( n = 5). (C) Нет значимой разницы в количестве мышечных волокон между поврежденной и контрольной мышцами ( n = 3). (D) Снижение безжировой массы тела, увеличение массы жира и повышение содержания воды в организме через 28 дней после операции ( n = 8). ∗ p <0,05, ∗∗ p <0,01, ∗∗∗ p <0,001.
Мы спросили, приводит ли атрофия, вызванная седалищным нервом, к общим изменениям в составе тела. С 0 по 28 день после операции мы обнаружили снижение мышечной массы на 3,7% (± 1,3%) с 75,4% (± 2,3%) до 71.7% (± 2,9%) (Рисунок 2D). Снижение процента безжировой массы тела произошло, несмотря на тенденцию к увеличению массы тела ( p = 0,61; дополнительный рисунок 7). Уменьшение безжировой массы тела сопровождалось небольшим увеличением процентного содержания жира в организме (рис. 2D).
Повышенный синтез миофибриллярного белка в атрофической мышце
Оксид дейтерия был введен, а затем добавлен в обычную воду для анализа скорости фракционного синтеза миофибрилл (рис. 3А). Мы подтвердили нашу способность надежно обнаруживать аланин, меченный 2 H, в огромном количестве различных образцов мышц крыс, полученных в результате нескольких вмешательств, в которых использовался D 2 O (рис. 3B).Скорость фракционного синтеза миофибрилл увеличилась в 1,6 раза в поврежденной ноге по сравнению с контрольной ногой после 2 недель лечения D 2 O (от 3,23 ± 0,72 до 2,09 ± 0,26% * день -1 , соответственно) (рис. ). Каждое животное ( n = 10) показало повышенную скорость синтеза мышечного белка в поврежденной ноге по сравнению с контрольной ногой (дополнительный рисунок 4). Насколько нам известно, это первое исследование, показывающее комплексное увеличение MPS в течение длительного периода потери мышечной массы.
РИСУНОК 3. (A) Принципиальная схема протокола маркировки D 2 O у крыс (слева) и мышц (справа). (B) Количественная оценка включения 2 H в m + 1 фракции миофибриллярного аланина в немеченой фоновой мышце ( n = 4) по сравнению с D 2 O меченой мышцы ( n = 40). (C) Схематическое изображение протокола исследования. Хирургия в день 0, начало эксперимента по мечению D 2 O на 14 день и оценка синтеза миофибриллярного белка между 14 и 28 днями. ∗∗∗ p <0,001.
РИСУНОК 4. Скорость фракционного синтеза миофибриллярного белка в ТА с повреждением нерва и контрлатеральном контроле ( n = 10). ∗∗∗ p <0,001.
Экспрессия ключевых сигнальных белков, регулирующих размер мышц
Протеолиз скелетных мышц частично регулируется убиквитиновым протеасомным путем E3 и его мышечно-специфическими лигазами MAFbx и MuRF1 (Bodine et al., 2001). Чтобы исследовать, как ключевые сигнальные белки протеасомного пути регулируются в нашей модели, мы исследовали MAFbx и MuRF1 с помощью вестерн-блоттинга. Экспрессия MAFbx была увеличена в четыре раза в поврежденной ноге по сравнению с контрольной ногой (от 5,3 ± 1,2 до 1,4 ± 0,4 AU, соответственно) (рис. 5A, верхняя панель). Экспрессия MuRF1 следовала аналогичной схеме ( p <0,0001) (дополнительная фигура 5). Экспрессия белка p70s6k1 увеличилась в 1,4 раза в поврежденной ноге (с 2,4 ± 0,3 до 1,8 ± 0.2 AU) (Рисунок 5A, нижняя панель). Фосфорилированный p70s6k1 не может быть обнаружен (дополнительный рисунок 6). Мы обнаружили корреляцию между экспрессией p70s6k1 и скоростью фракционного синтеза миофибрилл ( r 2 = 0,57) (рис. 6А). Корреляция для p70s6k1 и FSR не зависит от эффекта вмешательства и все еще присутствует, если анализ ограничен контрольной ногой ( r 2 = 0,65) (дополнительный рисунок 8).
РИСУНОК 5. (A) Экспрессия белка MAFbx и p70s6k1 в контралатеральном (ctrl) и поврежденном (Dmg) ТА крысы; репрезентативные изображения клякс ( n = 6). ∗∗ p <0,01, ∗∗∗ p <0,001.
РИСУНОК 6. (A) Корреляция между экспрессией белка p70s6k1 и скоростями фракционного синтеза миофибрилл (FSR) в ТА крысы ( n = 6).
Обсуждение
Наиболее распространенное предположение состоит в том, что в большинстве случаев потери мышечной массы происходит снижение синтеза белка, а также увеличение его распада (McKinnell and Rudnicki, 2004).При атрофии неиспользования и иммобилизации у людей снижение MPS, по-видимому, является преобладающим механизмом, вызывающим потерю мышечной массы (Wall et al., 2013a; Phillips and McGlory, 2014). Снижение MPS также наблюдалось при атрофии мышц, вызванной диетой, у мужчин с ожирением, раковой кахексии, сепсисе и ожоговых пациентах (Emery et al., 1984; Sakurai et al., 1995; Lang et al., 2007; Hector et al. ., 2018). В нашем исследовании мы исследовали хронические изменения MPS в ответ на мышечную атрофию, вызванную повреждением нервов. В отличие от сценариев, упомянутых выше, мы обнаружили, что частота MPS увеличивается, а не снижается во время потери мышечной массы, вызванной повреждением нервов (Рисунок 4).Ранние исследования МПС после повреждения нервов дали разные результаты. Сообщалось, что MPS временно увеличивался in vitro и in vivo Бузом, Голдспинком и другими (Buse et al., 1965; Goldspink, 1976, 1978). Более поздние исследования показали снижение MPS в мышцах, которые подверглись компенсаторному росту с последующей перерезкой нерва (Goldspink et al., 1983). Однако значение этих исследований сильно отличается от наших результатов. Одна из причин заключается в различиях между моделями повреждения нервов: несмотря на то, что было проделано много работы по перерезке нерва, меньше известно о хронических повреждениях нерва сужения, которые использовались в качестве модели в этом исследовании.Фактически, до сих пор ни одно исследование не изучало, как на оборот мышечного белка и MPS влияет повреждение нервного сужения. Кроме того, исследования, обнаружившие увеличение включения индикатора в EDL и SOL после перерезки нерва, были выполнены на особенно молодых крысах (Goldspink, 1976, 1978). Подвергаясь возрастному росту, эти животные все же увеличивали абсолютную массу денервированной мышцы в ходе эксперимента (Goldspink, 1976, 1978). Результатом был замедленный рост и относительная атрофия пораженных мышц по сравнению с контрольными животными, а не абсолютная атрофия.В условиях системной анаболической среды повышенная частота MPS может быть менее удивительной. Мы выбрали взрослых взрослых крыс (21–22 недель) и контролировали их потребление пищи, чтобы избежать избыточной массы тела и связанного с этим увеличения мышечной массы (дополнительный рисунок 7). В течение 4 недель после операции наши животные потеряли 66% TA по сравнению с контрлатеральной контрольной ногой и 50% массы EDL, соответственно (рисунки 1B, C). Несмотря на это значительное уменьшение мышечной массы, мы обнаружили увеличение MPS в TA в 1,6 раза (Рисунок 4).Насколько нам известно, это первое исследование, в котором было обнаружено столь выраженное увеличение интегрированного MPS, несмотря на абсолютную атрофию мышцы. Это подтверждает мнение о том, что частота MPS может быть более показательной для ремоделирования мышц и продолжающейся регенерации, чем рост мышц как таковой (Ochala et al., 2011; Mitchell et al., 2014; Damas et al., 2016).
Выбор времени для оценки оборота мышечного белка имеет решающее значение для понимания изменений мышечной массы. Хорошо известно, что изменение оборота мышечного белка в ответ на атрофический стимул динамично и зависит от множества параметров.Например, при атрофии неиспользования мышц большинство изменений в обмене мышечного белка происходит в течение первой недели после начала действия стимула (Wall et al., 2016). Считается, что MPS быстро снижается, что сопровождается быстрой потерей мышечной массы, которая постепенно уменьшается на второй и третьей неделе неиспользования (Wall et al., 2013a, b). Следовательно, оценка синтеза мышечного протеина на более позднем этапе может пропустить важные изменения. Что касается повреждения нервов, то в литературе предполагается довольно стабильная скорость потери мышечной массы (Goldspink, 1976; al-Amood et al., 1991; Ma et al., 2007). Важно отметить, что мышца продолжает терять массу до 3–12 месяцев после повреждения нерва (Wu et al., 2014). Чтобы избежать каких-либо артефактов из-за начальной воспалительной реакции, вызванной операцией, мы решили проанализировать MPS во второй половине нашего вмешательства. Мы использовали D 2 O в качестве индикатора для измерения интегрированного синтеза белка в течение 2 недель (рис. 3C). В отличие от краткосрочного эксперимента с методом постоянной инфузии или заливки, это позволило нам оценить хронические изменения МПС.
Чтобы исследовать изменения в экспрессии белка, которые могут лежать в основе наблюдаемых изменений в обмене белков, мы проанализировали ключевые сигнальные белки для синтеза и распада мышечного белка. Для синтеза мышечного белка мы сосредоточились на p70s6k1, белке, расположенном ниже mTORC1, который, как известно, увеличивает синтез белка при фосфорилировании и играет регулирующую роль в росте мышц (Baar and Esser, 1999; Saxton and Sabatini, 2017). Чтобы получить представление о передаче сигналов, лежащих в основе распада белка, мы проанализировали E3 ubiquitine ligases MAFbx и MuRF1.Это специфические для мышц белки, расположенные ниже FOXO, которые, как было показано, активируются в большинстве атрофических состояний и являются решающими регуляторами потери мышечной массы (Bodine et al., 2001; Gomes et al., 2001; Bodine and Baehr, 2014). В нашей модели экспрессия белка p70s6k1 значительно увеличена в ноге с повреждением нерва по сравнению с контрольной ногой (рис. 5А, нижняя панель). Экспрессия p70s6k1 коррелирует со скоростью фракционного синтеза миофибриллярного белка (рис. 6А). Интересно, что это все еще имеет место, когда уровни экспрессии и синтеза анализируются исключительно в контрольной ветви (дополнительный рисунок 8).Мы попытались проанализировать фосфорилированный p70s6k1, но не смогли обнаружить его ни в поврежденной, ни в контрольной ногах. Мы подтвердили отсутствие фосфорилированного p70s6k1 в наших образцах путем добавления положительных контролей (дополнительный рисунок 6). Отсутствие фосфорилированного p70s6k1 неудивительно, поскольку паттерн экспрессии, по-видимому, является временным, и отбор мышечной ткани должен происходить близко к инициированию раннего стимула, чего не было в нашем исследовании (Ogasawara et al., 2013; West et al., 2016). В конце концов, в случае нашей модели атрофии данные по экспрессии белка, кажется, совпадают с данными об обмене белка из экспериментов с индикаторами.
Заключение
Таким образом, мы обнаружили, что потеря мышечной массы, вызванная повреждением нервов, в первую очередь основана на атрофии мышечных волокон, а не на потере мышечных волокон. С помощью комбинации интеграции метода индикатора D 2 O с анализом абсолютных изменений мышечной массы мы смогли обнаружить, что в нашей модели мышечной атрофии потеря мышечной массы сопровождается увеличением, а не снижением MPS. ставки.Эти результаты подтверждают мнение о том, что синтез мышечного белка может отражать ремоделирование мышц и не должен использоваться в качестве косвенного показателя для прогнозирования изменений мышечной массы. В заключение, мышечная атрофия, вызванная хроническим повреждением нерва, не связана со снижением показателей MPS.
Авторские взносы
HL отвечал за дизайн исследования, эксперименты на животных, анализ образцов, интерпретацию данных и написание рукописи.JS, HL и AG подготовили образцы для анализа методом ГХ-МС. LvL участвовал в разработке исследования, интерпретации данных и написании рукописи. SK принимал участие в интерпретации данных. С.С. участвовал в разработке исследования, интерпретации данных и написании рукописи.
Финансирование
Исследование было поддержано Немецким исследовательским фондом (DFG) через Международную исследовательскую группу по обучению мышечным наукам (MyoGrad IGK1631) и грантом SS и HL.Французско-немецкий университет (УФА) поддержал HL посредством финансовой и образовательной поддержки. Взносы стали возможными благодаря финансированию DFG через Берлинско-Бранденбургскую школу регенеративной терапии (BSRT) GSC 203. Анализ состава тела был проведен в Центре фенотипирования Центра молекулярной медицины Макса Дельбрюка.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы благодарим Адриен Роте, Моник Бергеманн, Шоаиб Афзал и Кристин Засаду за техническую помощь. Мы хотели бы поблагодарить Энди Холверда за полезное обсуждение проекта и разработки протокола маркировки. Мы также благодарим Аннет Шюрманн за предоставление нам антитела GLUT4.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fphys.2018.01220 / полный # дополнительный материал
Список литературы
аль-Амуд, В. С., Льюис, Д. М., и Шмальбрух, Х. (1991). Влияние хронической электростимуляции на сократительные свойства длительно денервированных скелетных мышц крыс. J. Physiol. 441, 243–256. DOI: 10.1113 / jphysiol.1991.sp018749
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баар К., Эссер К. (1999). Фосфорилирование p70S6k коррелирует с увеличением массы скелетных мышц после упражнений с отягощениями. Am. J. Physiol. Cell Physiol. 276, C120 – C127. DOI: 10.1152 / ajpcell.1999.276.1.C120
CrossRef Полный текст | Google Scholar
Баптиста, А. Ф., Гомеш, Дж. Р., Оливейра, Дж. Т., Сантос, С. М., Ванье-Сантос, М. А., и Мартинес, А. (2008). Высокочастотная и низкочастотная чрескожная электрическая стимуляция нервов задерживает регенерацию седалищного нерва у мышей после травм. Дж. Перифер. Nerv. Syst. 13, 71–80. DOI: 10.1111 / j.1529-8027.2008.00160.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Беннетт, Г.Дж., Се, Ю.-К. (1988). Периферическая мононевропатия у крыс, вызывающая нарушения болевых ощущений, подобные тем, которые наблюдаются у человека. Боль 33, 87–107. DOI: 10.1016 / 0304-3959 (88)
-6
CrossRef Полный текст | Google Scholar
Бодин, С. К., Баер, Л. М. (2014). Атрофия скелетных мышц и убиквитин-лигазы E3 MuRF1 и MAFbx / атрогин-1. Am. J. Physiol. Эндокринол. Метаб. 307, E469 – E484. DOI: 10.1152 / ajpendo.00204.2014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бодин, С.C., Latres, E., Baumhueter, S., Lai, V.K., Nunez, L., Clarke, B.A., et al. (2001). Идентификация убиквитинлигаз, необходимых для атрофии скелетных мышц. Наука 294, 1704–1708. DOI: 10.1126 / science.1065874
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бурд Н. А., Эндрюс Р. Дж., Уэст Д. У., Литтл Дж. П., Кокран А. Дж., Гектор А. Дж. И др. (2012). Время, проведенное мышцами при напряжении во время упражнений с отягощениями, стимулирует дифференциальные субфракционные синтетические реакции мышечного белка у мужчин. J. Physiol. 590, 351–362. DOI: 10.1113 / jphysiol.2011.221200
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Busch, R., Kim, Y.K, Neese, R.A., Schade-Serin, V., Collins, M., Awada, M., et al. (2006). Измерение скорости белкового обмена с помощью тяжелой воды мечения заменимых аминокислот. Biochim. Биофиз. Acta 1760, 730–744. DOI: 10.1016 / j.bbagen.2005.12.023
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бусе, м.Дж., Макмастер Дж. И Бьюз Дж. (1965). Влияние денервации и инсулина на синтез белка в изолированной диафрагме крысы. Metab. Clin. Exp. 14, 1220–1232. DOI: 10.1016 / 0026-0495 (65)
-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дамас, Ф., Филлипс, С. М., Либарди, К. А., Вечин, Ф. К., Ликсандрао, М. Е., Джанниг, П. Р. и др. (2016). Вызванные тренировкой с отягощением изменения в синтезе интегрированного миофибриллярного белка связаны с гипертрофией только после ослабления повреждения мышц. J. Physiol. 594, 5209–5222. DOI: 10.1113 / JP272472
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дайк, П. (2005). Периферическая невропатия. Нью-Йорк, Нью-Йорк: Elsevier Inc.
Google Scholar
Эмери П., Эдвардс Р., Ренни М., Сухами Р. и Халлидей Д. (1984). Синтез белка в мышцах измеряется in vivo у кахектических больных раком. Br. Med. J. 289, 584–586. DOI: 10.1136 / bmj.289.6445.584
CrossRef Полный текст | Google Scholar
Энгель, В.К. и Каннингем Г. Г. (1963). Экспресс-исследование мышечной ткани Усовершенствованный метод трихрома для свежезамороженных срезов биопсии. Неврология 13, 919–923. DOI: 10.1212 / WNL.13.11.919
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гарбер, К. (2016). Больше не пропадать. Лондон: Издательская группа Nature.
Google Scholar
Гасье, Х. Г., Рихман, С. Э., Виггс, М. П., Превис, С. Ф. и Флуки, Дж. Д. (2009).Сравнение затопляющей дозы 2h3O и фенилаланина для исследования синтеза мышечного белка при острой физической нагрузке у крыс. Am. J. Physiol. Эндокринол. Метаб. 297, E252 – E259. DOI: 10.1152 / ajpendo..2008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джиго-Бенато Д., Руссо Т. Л., Геуна С., Домингес Н. Р., Сальвини Т. Ф. и Паризотто Н. А. (2010). Электростимуляция ухудшает раннее функциональное восстановление и усиливает атрофию скелетных мышц после повреждения седалищного нерва у крыс. Мышечный нерв 41, 685–693. DOI: 10.1002 / mus.21549
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Голдспинк, Д. (1976). Влияние денервации на белковый обмен в скелетных мышцах крыс. Biochem. J. 156, 71–80. DOI: 10.1042 / bj1560071
CrossRef Полный текст | Google Scholar
Голдспинк, Д. Ф. (1978). Изменения размера и белкового обмена в подошвенной мышце в ответ на иммобилизацию или денервацию. Лондон: Портленд Пресс Лимитед.
Google Scholar
Голдспинк, Д. Ф., Гарлик, П. Дж., И МакНурлан, М. (1983). Оборот белков измеряется in vivo и in vitro в мышцах, подвергающихся компенсаторному росту и последующей атрофии денервации. Biochem. J. 210, 89–98. DOI: 10.1042 / bj2100089
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гомес, М. Д., Лекер, С. Х., Джаго, Р. Т., Навон, А., и Голдберг, А. Л. (2001). Атрогин-1, мышечно-специфический белок F-бокса, высоко экспрессируемый во время мышечной атрофии. Proc. Nat. Акад. Sci. 98, 14440–14445. DOI: 10.1073 / pnas.251541198
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Грегори К. М., Ванденборн К. и Дадли Г. А. (2001). Метаболические ферменты и фенотипическое выражение среди опорно-двигательных мышц человека. Мышечный нерв 24, 387–393. DOI: 10.1002 / 1097-4598 (200103) 24: 3 <387 :: AID-MUS1010> 3.0.CO; 2-M
CrossRef Полный текст | Google Scholar
Гектор, А.Дж., МакГлори, К., Дамас, Ф., Мазара, Н., Бейкер, С. К., и Филлипс, С. М. (2018). Выраженное ограничение энергии с повышенным потреблением белка не приводит к изменению протеолиза и снижению синтеза белка скелетных мышц, что смягчается упражнениями с отягощениями. FASEB J. 32, 265–275. DOI: 10.1096 / fj.201700158RR
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ланг, К. Х., Фрост, Р. А., и Вэри, Т. К. (2007). Регуляция синтеза мышечного белка при сепсисе и воспалении. Am. J. Physiol. Эндокринол. Метаб. 293, E453 – E459. DOI: 10.1152 / ajpendo.00204.2007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ма, Дж., Шен, Дж., Гарретт, Дж. П., Ли, К. А., Ли, З., Эльзаиди, Г. А. и др. (2007). Экспрессия генов миогенных регуляторных факторов, субъединиц никотинового ацетилхолинового рецептора и GAP-43 в скелетных мышцах после денервации на модели крыс. J. Orthop. Res. 25, 1498–1505. DOI: 10.1002 / jor.20414
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Маркиз, К., Debigaré, R., Lacasse, Y., LeBlanc, P., Jobin, J., Carrier, G., et al. (2002). Площадь поперечного сечения мышц с высокой мышечной массой является лучшим показателем смертности, чем индекс массы тела у пациентов с хронической обструктивной болезнью легких. Am. J. Respir. Крит. Care Med. 166, 809–813. DOI: 10.1164 / rccm.2107031
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Меттер, Э. Дж., Талбот, Л. А., Шрагер, М., и Конвит, Р. (2002). Сила скелетных мышц как предиктор общей смертности у здоровых мужчин. J. Gerontol. Биол. Sci. Med. Sci. 57, B359 – B365. DOI: 10.1093 / gerona / 57.10.B359
CrossRef Полный текст | Google Scholar
Митчелл, К. Дж., Черчвард-Венн, Т. А., Париз, Г., Беллами, Л., Бейкер, С. К., Смит, К., и др. (2014). Острый посттренировочный синтез миофибриллярного белка не коррелирует с гипертрофией мышц, вызванной силовыми тренировками, у молодых мужчин. PLoS One 9: e89431. DOI: 10.1371 / journal.pone.0089431
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Очала, Дж., Gustafson, A.M, Diez, M.L., Renaud, G., Li, M., Aare, S., et al. (2011). Предпочтительная потеря миозина в скелетных мышцах в ответ на механическое молчание в новой модели отделения интенсивной терапии крыс: основные механизмы. J. Physiol. 589, 2007–2026. DOI: 10.1113 / jphysiol.2010.202044
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Огасавара Р., Кобаяши К., Цутаки А., Ли К., Абэ Т., Фудзита С. и др. (2013). Сигнальный ответ mTOR на упражнения с отягощениями изменяется хроническими тренировками с отягощениями и ослаблением скелетных мышц. J. Appl. Physiol. 114, 934–940. DOI: 10.1152 / japplphysiol.01161.2012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Огилви Р. и Фибак Д. (1990). Метахроматический краситель АТФазный метод для одновременной идентификации волокон скелетных мышц типов I, II A, II B и II C. Stain Technol. 65, 231–241. DOI: 10.3109 / 1052029
05613
CrossRef Полный текст | Google Scholar
Филлипс, С. М., и МакГлори, К. (2014).Предложение о перекрестных помехах: доминирующим механизмом, вызывающим атрофию неиспользуемых мышц, является снижение синтеза белка. J. Physiol. 592, 5341–5343. DOI: 10.1113 / jphysiol.2014.273615
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рейд М.Б., судья А.Р. и Бодин С.С. (2014). Противоположная точка зрения: доминирующим механизмом, вызывающим атрофию неиспользуемых мышц, является протеолиз. J. Physiol. 592, 5345–5347. DOI: 10.1113 / jphysiol.2014.279406
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сакурай, Ю., Aarsland, A., Herndon, D. N., Chinkes, D. L., Pierre, E., Nguyen, T. T., et al. (1995). Стимуляция синтеза мышечного белка длительной инфузией инсулина у сильно обгоревших пациентов. Ann. Surg. 222, 283–294. DOI: 10.1097 / 00000658-199509000-00007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Зоммер К. (2013). «Модель нейропатической боли, хроническое сжатие», в энциклопедии боли , , редакторы Г. Ф. Гебхарт и Р. Ф. Шмидт (Гейдельберг: Springer).DOI: 10.1007 / 2F978-3-642-28753-4_2678
CrossRef Полный текст | Google Scholar
Томас, Д. Р. (2007). Потеря массы скелетных мышц при старении: изучение взаимосвязи голодания, саркопении и кахексии. Clin. Nutr. 26, 389–399. DOI: 10.1016 / j.clnu.2007.03.008
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Троммелен, Дж., Холверда, А. М., Коув, И. У., Лангер, Х., Халсон, С. Л., Ролло, И., и др. (2016). Упражнения с отягощениями увеличивают скорость синтеза мышечного белка в течение ночи. Med. Sci. Спортивные упражнения. 48, 2517–2525. DOI: 10.1249 / MSS.0000000000001045
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уолл, Б. Т., Диркс, М. Л., Снейдерс, Т., ван, Дейк Дж. В., Фрич, М., Вердейк, Л. Б. и др. (2016). Кратковременное неиспользование мышц снижает скорость синтеза миофибриллярного белка и вызывает анаболическую устойчивость к потреблению белка. Am. J. Physiol. Эндокринол. Метаб. 310, E137 – E147. DOI: 10.1152 / ajpendo.00227.2015
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Стена, Б.Т., Диркс, М. Л., и ван Лун, Л. Дж. (2013a). Атрофия скелетных мышц при кратковременном неиспользовании: последствия для возрастной саркопении. Aging Res. Ред. 12, 898–906. DOI: 10.1016 / j.arr.2013.07.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уолл, Б. Т., Снейдерс, Т., Зенден, Дж. М., Оттенброс, К. Л., Гийсен, А. П., Вердейк, Л. Б. и др. (2013b). Неиспользование нарушает синтетический ответ мышечного белка на потребление белка у здоровых мужчин. Дж.Clin. Эндокринол. Метаб. 98, 4872–4881. DOI: 10.1210 / jc.2013-2098
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ваннамэти, С. Г., Шейпер, А. Г., Леннон, Л., и Уинкап, П. Х. (2007). Снижение мышечной массы и повышенное центральное ожирение независимо связаны со смертностью пожилых мужчин. Am. J. Clin. Nutr. 86, 1339–1346. DOI: 10.1093 / ajcn / 86.5.1339
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вест, Д.W., Baehr, L.M., Marcotte, G.R., Chason, C.M., Tolento, L., Gomes, A.V. и др. (2016). Острые упражнения с отягощениями активируют чувствительные и нечувствительные к рапамицину механизмы, которые контролируют трансляционную активность и емкость скелетных мышц. J. Physiol. 594, 453–468. DOI: 10.1113 / JP271365
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Уилкинсон, Д. Дж., Франчи, М. В., Брук, М. С., Наричи, М. В., Уильямс, Дж. П., Митчелл, В. К. и др. (2014).Подтверждение применения методов индикатора стабильного изотопа D (2) O для мониторинга ежедневных изменений в синтезе субфракций мышечного белка у людей. Am. J. Physiol. Эндокринол. Метаб. 306, E571 – E579. DOI: 10.1152 / ajpendo.00650.2013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wu, P., Chawla, A., Spinner, R.J., Yu, C., Yaszemski, M.J., Windebank, A.J., et al. (2014). Ключевые изменения денервированных мышц и их влияние на регенерацию и реиннервацию. Neural Regen. Res. 9, 1796–1809. DOI: 10.4103 / 1673-5374.143424
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ярашески К. Э., Захвейя Дж. Дж. И Бир Д. М. (1993). Острое влияние упражнений с отягощениями на скорость синтеза мышечного белка у молодых и пожилых мужчин и женщин. Am. J. Physiol. 265, E210 – E214. DOI: 10.1152 / ajpendo.1993.265.2.E210
PubMed Аннотация | CrossRef Полный текст | Google Scholar
.