Сократительная функция мышц — Справочник химика 21
Миозин и актин являются, по всей вероятности, белками, обеспечивающими сократительную функцию мышц. Тропомиозин представляет собой индивидуальный белок с молекулярным весом 130 ООО или 65 ООО, а миозин — по-видимому, полимер тропомиозина. Актин образует с миозином соединение, играющее, вероятно, существенную роль в сокращении мышц. [c.445]
Объясните регуляторное воздействие нервной системы на сократительную функцию мышц. [c.284]
Для понимания биохимических процессов, обеспечивающих сократительную функцию мышц, необходимо рассмотреть структурную организацию и химический состав мышечных волокон. [c.286]
Сократительная функция мышц обусловлена возм ожностью превращения в мышечных волокнах химической энергии определенных биохимических процессов в механическую работу. [c.413]
Чем сложнее организм, тем более разнообразны функции, выполняемые белкО М. Белки составляют основу опорных тканей животных (костей, хрящей, сухожилий), выполняют покровные и защитные функции (волос, шерсть, рога, копыта), откладываются в виде питательных запасных веществ в семенах и в яйце. Некоторые белки являются переносчиками кислорода (гемоглобин крови), другие выполняют сократительные функции мышц (миозин). Все известные в настоящее время энзимы являются белками. Многие гормоны, антибиотики, многие яды змей и бактериальные токсины также относятся к белкам. [c.697]
Белки составляют основу опорных тканей животных (костей, хрящей, сухожилий), выполняют покровные и защитные функции (волос, шерсть, рога, копыта), откладываются в виде питательных запасных веществ в семенах и в яйце. Некоторые белки являются переносчиками кислорода (гемоглобин крови), другие выполняют сократительные функции мышц (миозин). Все известные в настоящее время энзимы являются белками. Многие гормоны, антибиотики, многие яды змей и бактериальные токсины также относятся к белкам. [c.697]
В процессе обмена веществ происходят конформационные изменения макромолекул, синтез и распад различных веществ, образование и потребление энергии, которые обеспечивают проявление физиологических функций организма. Изменение конформации основных белков мышц — актина и миозина, а также использование химической энергии АТФ лежат в основе сократительной функции мышц. Эти процессы наряду с механизмами энергообразования, биосинтеза белка, транспорта веществ и другими биохимическими реакциями существенно изменяются при воздействии различных физических нагрузок и в ходе адаптации к ним, что влияет на физическую работоспособность и состояние здоровья спортсмена. [c.24]
[c.24]
Для поддержания сократительной функции мышцы концентрация АТФ в ней должна находиться на постоянном уровне в пределах от 2 до 5 ммоль кг . Поэтому при мышечной деятельности АТФ должна восстанавливаться со скоростью, с которой расщепляется в процессе сокращения, что осуществляется отдельными биохимическими механизмами ее ресинтеза. [c.305]
Функции белков в организме и в клетках весьма разнообразны. Белки образуют такой инертный материал, как волос, рог или кость, и из белков же состоит сократимое вещество мышечного волокна. Белки поперечнополосатой и гладкой мускулатуры, на долю которых приходится около 42% веса тела, по массе являются важнейшей тканью организма человека и животных. Скелетная мускулатура и мышцы внутренних органов обеспечивают возможность выполнения чрезвычайно важных физиологических функций движения, кровообращения, дыхания, передвижения пищевой кашицы в пищеварительных органах, поддержания тонуса сосудов и т. д. Сократительная функция мышц обусловлена возможностью превращения в мышечных волокнах химической энергии определенных биохимических процессов в механическую работу. Если в состоянии полного покоя организм взрослого человека расходует в течение суток 1700 ккал, то при тяжелом физическом труде расход энергии может превышать 5000 ккал. Таким образом, ири увеличенной физической нагрузке в мышечной ткани расходуется значительно больше энергии, чем во всех остальных органах, вместе взятых. Необходимо подчеркнуть, что любой вид труда (физического и умственного) всегда связан с деятельностью центральной нервной системы. Ведущая роль нервной системы в физиологических и патологических процессах, на основании работ И. П. Павлова и его школы, является бесспорно установленным фактом. Общее содержание белковых веществ в сухом остатке нервной ткани характеризуется следующими данными в коре полушарий— 33%, в спинном мозгу — 3I% ив седалищном нерве —29% белка. Среди белков нервной системы имеются как простые, так и сложные белки.
д. Сократительная функция мышц обусловлена возможностью превращения в мышечных волокнах химической энергии определенных биохимических процессов в механическую работу. Если в состоянии полного покоя организм взрослого человека расходует в течение суток 1700 ккал, то при тяжелом физическом труде расход энергии может превышать 5000 ккал. Таким образом, ири увеличенной физической нагрузке в мышечной ткани расходуется значительно больше энергии, чем во всех остальных органах, вместе взятых. Необходимо подчеркнуть, что любой вид труда (физического и умственного) всегда связан с деятельностью центральной нервной системы. Ведущая роль нервной системы в физиологических и патологических процессах, на основании работ И. П. Павлова и его школы, является бесспорно установленным фактом. Общее содержание белковых веществ в сухом остатке нервной ткани характеризуется следующими данными в коре полушарий— 33%, в спинном мозгу — 3I% ив седалищном нерве —29% белка. Среди белков нервной системы имеются как простые, так и сложные белки. [c.60]
[c.60]
Сократительная функция мышц связана с превраш,ением химической энергии в механическую. Работа мышц сопровождается резким усилением п1)оцессов обмена веществ, усиленным использованием энергетических ресурсов организма. [c.541]
Итак, в неработающей мышце, где нет больших энергетических затрат, нет и митохондриального ретикулума. Он появляется после включения основной, сократительной, функции мышцы. Такая ситуация вполне разумна, если принять, что митохондриальный ретикулум — электропроводка. Но как это доказать прямым экспериментом [c.177]
К группе миофибриллярных белков относятся миозин, актин и актомиозин—белки, растворимые в солевых средах с высокой ионной силой, и так называемые регуляторные белки тропомиозин, тропонин, а- и 3-актинин, образующие в мышце с актомиозином единый комплекс. Перечисленные миофибриллярные белки тесно связаны с сократительной функцией мышц. [c.648]
Миофибриллярные белки включают сократительные белки миозин, актин и актомиозин, а также регуляторные белки тропомиозин, тропонин, а- и р-актинины.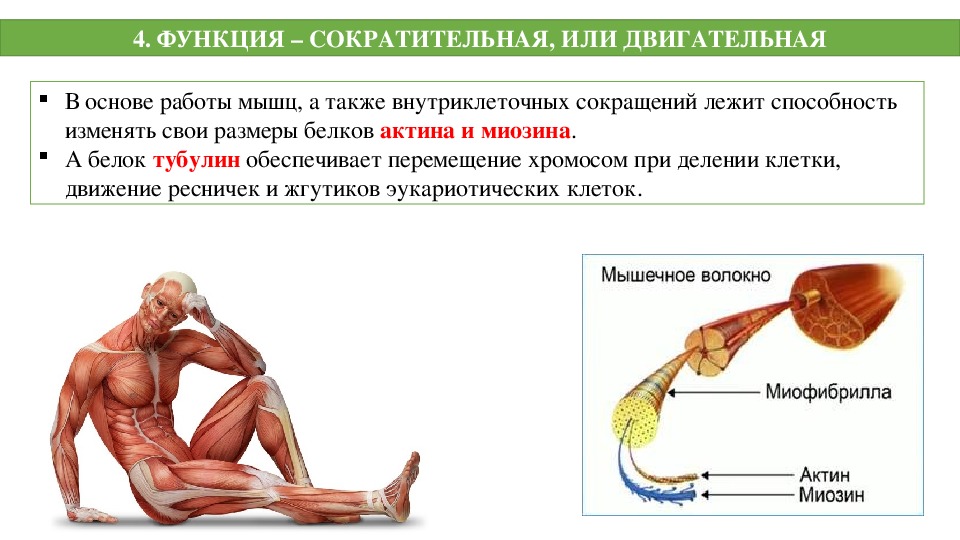 Миофибриллярные белки обеспечивают сократительную функцию мышц. [c.296]
Миофибриллярные белки обеспечивают сократительную функцию мышц. [c.296]
Белки сократительные и структурные — Справочник химика 21
Фибриллярные белки являются структурным или сократительным материалом организма. Например, коллаген входит в состав сухожилий, хрящей, кожи и принимает участие в образовании скелета, а миозин является сократительным белком мышц. Эти белки не растворяются в воде. [c.238]
В клетке белки выполняют структурные, сократительную и ферментативные функции. [c.45]
Вторая попытка сводится к классификации белков в соответствии с выполняемыми ими функциями. По этой классификации среди белков выделяют следующие группы 1) каталитически активные белки 2) белки-гормоны 3) регуляторные белки 4) защитные белки 5) токсические белки 6) транспортные белки 7) структурные белки 8) сократительные белки 9) рецепторные белки 10) белки-ингибиторы ферментов 11) белки вирусных оболочек 12) белки с иными функциями. [c.82]
[c.82]
Структурная и функциональная организация сократительных белков [c.284]
Структурные и сократительные белки 572 [c.9]
СТРУКТУРНЫЕ И СОКРАТИТЕЛЬНЫЕ БЕЛКИ [c.572]
В заключение этой главы остановимся на строении и свойствах фибриллярных белков — структурных и сократительных. Первые играют роль опорных и защитных компонент, входя в состав сухожилий, хрящей, костей, связок и т. д. (коллагены), а также кожи, волос, шерсти, рогов и т. д. (кератины). Вторые [c.126]
Пластический обмен — это комплекс химических реакций, которые обеспечивают синтез специфических для организма веществ структурных компонентов, сократительных белков, ферментов, гормонов, жиров, сложных углеводов и многих других. В пластических процессах используется энергия, которая затем извлекается при распаде питательных веществ. [c.31]
При систематических физических нагрузках в мышцах и других тканях активируется адаптивный синтез белка, увеличивается содержание структурных и сократительных белков, а также миоглобина и многих ферментов. Это приводит к увеличению мышечной массы, поперечного сечения мышечных волокон, что рассматривается как гипертрофия мышц. Увеличение количества ферментов создает благоприятные условия для расширения энергетического потенциала в работающих мышцах, что, в свою очередь, усиливает биосинтез мышечных белков после физических нагрузок и улучшает двигательные способности человека. [c.261]
Это приводит к увеличению мышечной массы, поперечного сечения мышечных волокон, что рассматривается как гипертрофия мышц. Увеличение количества ферментов создает благоприятные условия для расширения энергетического потенциала в работающих мышцах, что, в свою очередь, усиливает биосинтез мышечных белков после физических нагрузок и улучшает двигательные способности человека. [c.261]
Мышечная ткань является очень показательным объектом биохимического контроля мышечной деятельности, однако используется редко, так как образец мышечной ткани необходимо брать методом игольчатой биопсии. Для этого над исследуемой мышцей делается небольшой разрез кожи и с помощью специальной иглы берется кусочек (проба) мышечной ткани (2—3 мг), которая сразу замораживается в жидком азоте и в дальнейшем подвергается структурному и биохимическому анализу. В пробах определяют количество сократительных белков (актина и миозина), АТФ-азную активность миозина, показатели энергетического потенциала (содержание АТФ, гликогена, креатинфосфата), продукты энергетического обмена, электролиты и другие вещества.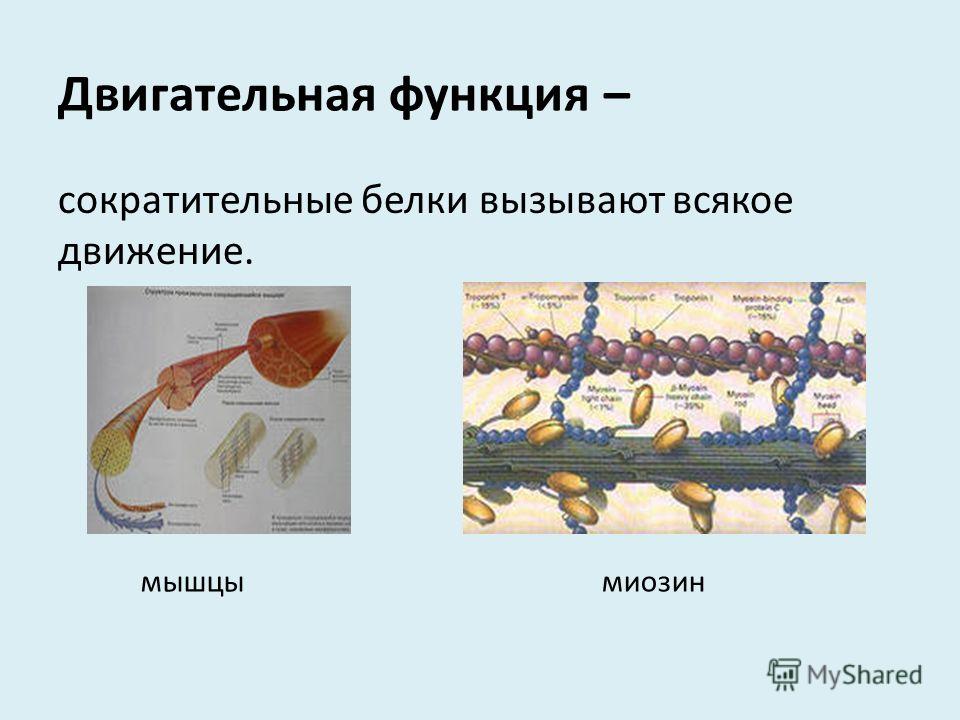 По их содержанию судят о составе и функциональной активности мышц, ее энергетическом потенциале, а также изменениях, которые происходят при воздействии однократной физической нагрузки или долговременной тренировки. [c.466]
По их содержанию судят о составе и функциональной активности мышц, ее энергетическом потенциале, а также изменениях, которые происходят при воздействии однократной физической нагрузки или долговременной тренировки. [c.466]
Сократительные и структурные белки [c.332]
По функциям ферменты, структурные белки, транспортные белки, защитные белки, сократительные белки мышц, гормоны (гормон роста, пролактин, паратгормон), токсины (ботулиновый, столбнячный, холерный), рецепторы (зрительный, ацетилхолиновый), запасные белки в семенах растений и др. [c.23]
Однократные физические нагрузки вызывают угнетение синтеза белка и усиление их катаболизма. Так, например, при беге на тредмиле в течение часа скорость синтеза белка в печени снижалась на 20 %, а при предельной работе — на 65 %. Такая закономерность наблюдается и в скелетных мышцах. Под воздействием физических нагрузок усиливается распад мышечных белков (преимущественно структурных), хотя отдельные виды нагрузок усиливают распад и сократительных белков. [c.261]
[c.261]
Белкам присущи регуляторные, защитные, токсические, транспортные, сократительные, структурные, рецепторные, модуляторные, морфогенные, запасные и многие другие функхщи. [c.23]
Монография построена как вводный курс по пространственной организации и функционированию белков. В ней кратко излагаются основные сведения об аминокислотных остатках, природе межостаточных и гидрофобных взаимодействий, структурной иерархии и т. д. вплоть до взаимодействия белков с другими молекулами, а также проблемы ферментативного катализа и механохимнческая функция сократительных белков. Книга написана логично, простым, ясным языком, хорошо иллюстрирована и снабжена обширным библиографическим списком. Знакомство с этим материалом подготовит читателя к углубленному усвоению специализированной литературы о пространственном строении наиболее сложных из известных современной науке молекул. [c.6]
Многие белки in situ присутствуют в значительно более высоких концентрациях, чем обычно бывает необходимо для реализации их специфических функций, например катализа определенных химических реакций. Это указывает на то, что белки возможно используются в качестве формы хранения аминокислот и (или) что они выполняют некие еще не известные нам функции. Например, высокая концентрация креатинкиназы в мышце (20 мг на 1 г ткани [751]) оставалась непонятной до тех пор, пока не установили, что этот белок функционирует не только как фермент, но также в форме, составляющей М-диск, как структурная опора сократительного аппарата [752]. [c.282]
Это указывает на то, что белки возможно используются в качестве формы хранения аминокислот и (или) что они выполняют некие еще не известные нам функции. Например, высокая концентрация креатинкиназы в мышце (20 мг на 1 г ткани [751]) оставалась непонятной до тех пор, пока не установили, что этот белок функционирует не только как фермент, но также в форме, составляющей М-диск, как структурная опора сократительного аппарата [752]. [c.282]
Все рассказанное в этой главе втносилось к глобулярным белкам со свойственным им многообразием структур и функций. Гораздо менее разнообразные фибриллярные белки характеризуются специфическими особенностями строения и выполняют специальные функции. Это — структурные и сократительные белки. Первые играют роль опорных и защитных компонент, входя в состав сухожилий, хрящей, костей, связок и т. д. (коллагены), а также эпидермиса, волос, шерсти, рогов и т. д. (кератины). Вторые входят в состав рабочих веществ механохими-ческих систем, в частности мышц (миозин). [c.254]
[c.254]
Жидковристаллическое состояние весьма распространено в живой природе. Возможно, что оно является необходимым условием функционирования всех без исключения живых систем. Причина этого состоит в том, что процессы метаболизма требуют наличия векторных потоков как нейтральных, так и заряженных частиц. Строгая направленность потоков молекул и зарядов, которая приводит к появлению электрических полей, необходимость разделения разноименных зарядов в ходе различных реакций — все это может быть реализовано только при помощи упорядоченных структур. Однако в живых организмах, в отличие от устройств, создаваемых человеком, необходимые структурные элементы не могут быть построены из любого мыслимого мате)риала. Самым необходимым свойствам такого материала должна быть его способность к самосборке [1]. Кроме того, материал должен сочетать в себе достаточно устойчивую упорядоченность с возможностью полиморфизма, т. е. со способностью структуры к изменению при изменении некоторых параметров окружающей среды. Обе эти особенности присущи жидкокристалличеокому состоянию. Наглядным примером такой структуры являются сократительные белки мышечной ткани [2]. Известно также, что синтез оптичеоки активных димеров [c.249]
Обе эти особенности присущи жидкокристалличеокому состоянию. Наглядным примером такой структуры являются сократительные белки мышечной ткани [2]. Известно также, что синтез оптичеоки активных димеров [c.249]
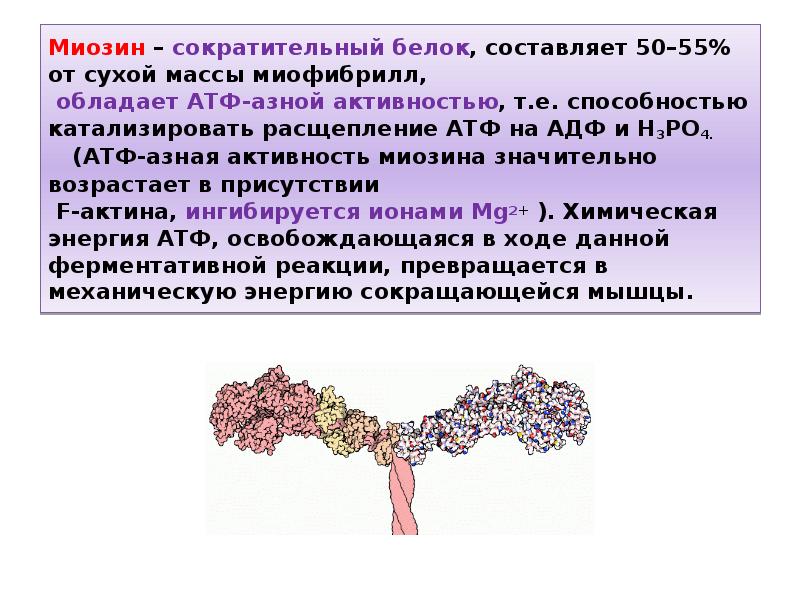
И структурные белки. Несомненно, что их роль не только механическая. Доказано, что структурным белкам присущи и каталитические функции. Эти функции особенно ярко проявляются у мышечного сократительного белка миозина. Исследования В. В. Эн-гельгардта и Н. А. Любимовой показали, что миозин ускоряет взаимодействие с водой (т. е. гидролиз) важнейшего аккумулятора энергии — аденозинтрифосфорной кислоты (АТФ). При этом получается аденозиндифосфорная кислота и фосфат. Энергия реакции используется мышцей, во время работы которой нити белка миозина сокращаются. Следовательно, этот белок выполняет двойную нагрузку он регулирует освобождение энергии и он же потребляет энергию, сокращаясь в процессе работы мышцы. Молекула миозина представляет собой длинную цепь — ее длина равна примерно 160 нм, а молекулярная масса достигает 600000, Кроме миозина, известны и другие мышечные белки (актин, тро-помиозин), Для того чтобы эти белки могли осуществлять обратимое сокращение, необходимо присутствие катионов металлов, вообще активно поглощаемых мышечными белками. Для работы мышцы требуются ионы калия, кальция, магния, нужен также запас фосфатов, используемых для синтеза АТФ, Связывание ионов металлов и водорода с ионными группами белков сильно влияет на взаимодействие участков цепи и приводит к изменению ее длины. Однако механизм мышечного сокращения более сложен и, по-видимому, связан с особым расположением нитей миозина и актина в мышце, позволяющих частицам актина при работе мышцы скользить вдоль нитей миозина. Из числа растворимых белков особенно важны альбумины и глобулины. [c.62]
Для работы мышцы требуются ионы калия, кальция, магния, нужен также запас фосфатов, используемых для синтеза АТФ, Связывание ионов металлов и водорода с ионными группами белков сильно влияет на взаимодействие участков цепи и приводит к изменению ее длины. Однако механизм мышечного сокращения более сложен и, по-видимому, связан с особым расположением нитей миозина и актина в мышце, позволяющих частицам актина при работе мышцы скользить вдоль нитей миозина. Из числа растворимых белков особенно важны альбумины и глобулины. [c.62]
Проницаемость в живых клетках представляет собой активный процесс и имеет мало общего с молекулярной диффузией или осмотическим потоком. Наоборот, активный транспорт осуществляется чаще всего против градиента концентрации, т. е. в направлении от мепьшей концентрации к большей. Ясно, что это — сложное явление, в котором обязательно должна потребляться энергия, так как движение веществ в направлении, обратном диффузии, связано с уменьшением энтропии. Активный перенос веществ как внутрь клетки из внешней среды, так и внутрь различных структурных элементов из заполяющей клетку гиалоплазмы осуществляется особыми нерастворимыми белками и белковыми комплексами, образующими наружную клеточную мембрану и различные структурные образования внутри клеток. Активный транспорт через мембраны и внутрь клеточных органелл связан с протеканием химических реакций, конечно, ферментативных. Поэтому проблема проницаемости и соответствующая функция белков тесно связана с их ферментативной функцией. С другой стороны, с помощью активного транспорта осуществляется один из механизмов автоматического регулирования. Как мы увидим дальше, регулирование проницаемости митохондрий осуществляется путем их сокращения пли расслабления. Причиной этого движения яляется сократительная реакция в особом белке, т. е. это явление вполне аналогично сокращению мышцы. [c.139]
Активный перенос веществ как внутрь клетки из внешней среды, так и внутрь различных структурных элементов из заполяющей клетку гиалоплазмы осуществляется особыми нерастворимыми белками и белковыми комплексами, образующими наружную клеточную мембрану и различные структурные образования внутри клеток. Активный транспорт через мембраны и внутрь клеточных органелл связан с протеканием химических реакций, конечно, ферментативных. Поэтому проблема проницаемости и соответствующая функция белков тесно связана с их ферментативной функцией. С другой стороны, с помощью активного транспорта осуществляется один из механизмов автоматического регулирования. Как мы увидим дальше, регулирование проницаемости митохондрий осуществляется путем их сокращения пли расслабления. Причиной этого движения яляется сократительная реакция в особом белке, т. е. это явление вполне аналогично сокращению мышцы. [c.139]
Белки, функции. По функциональному признаку белки можно раздедйть на ферменты (РНК-азы, цитохромы, трипсин и др. ), запасные белки (казеиноген, зеин, глиадин и др.), транспортные (гемоглобин, церулоплазмин и др.), сократительные (миозин, актин и др.), защитные (антитела, фибриноген и др.), токсины (дифтерийный токсин, змеиные яды и др.), гормоны (инсулин, адренокортикотропный гормон и др.), структурные белки (гликопротеиды, а-керотин, фиброин, мукопротеиды и др.). [c.17]
), запасные белки (казеиноген, зеин, глиадин и др.), транспортные (гемоглобин, церулоплазмин и др.), сократительные (миозин, актин и др.), защитные (антитела, фибриноген и др.), токсины (дифтерийный токсин, змеиные яды и др.), гормоны (инсулин, адренокортикотропный гормон и др.), структурные белки (гликопротеиды, а-керотин, фиброин, мукопротеиды и др.). [c.17]
Регуляция скорости синтеза белков. Такое действие оказывают стероидные и тиреоидные гормоны они проникают в клетку и взаимодействуют со специфическими рецепторами. Гормонрецепторный комплекс проникает в ядро, связывается с хроматином и увеличивает скорость синтеза белков на уровне генов (рис. 51). Активные гены усиливают синтез определенной РНК, которая выходит из ядра, поступает к рибосомам и запускает синтез новых белков, которые могут быть структурными или сократительными белками мышц и других тканей, а также ферментами или гормонами. В этом состоит их анаболическое действие. Однако скорость белкового синтеза в клетках — относительно медленный процесс, так как требует большого количества энергии и пластического материала.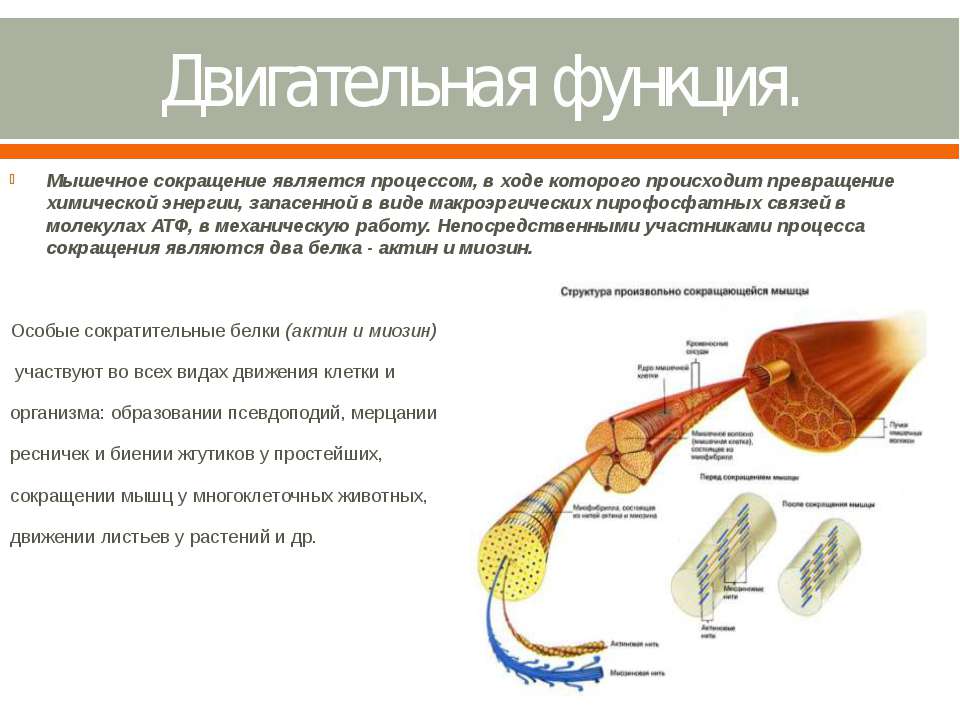 Поэтому такие гормоны не могут осуществлять быстрый контроль процессов метаболизма. Основная их функция сводится к регуляции процессов роста, развития и дифференцировки клеток организма. [c.138]
Поэтому такие гормоны не могут осуществлять быстрый контроль процессов метаболизма. Основная их функция сводится к регуляции процессов роста, развития и дифференцировки клеток организма. [c.138]
В проявлениях мышечной силы и мощности (в теории и практике спорта эти физические качества обычно объединяются в понятии скоростно-силовой подготовленности спортсмена) определяющее значение имеют структурная организация и ферментативные свойства сократительных белков мышц. Величина усилия, развиваемого мышцей в процессе сокраще-.ния, пропорциональна числу поперечных соединений (спаек) между актиновыми и миозиновыми нитями в миофибриллах. Потенциально возможное число этих соединений, а следовательно, и величина максимального проявления мышечной силы зависят от содержания актина и длины миозиновых нитей в пределах каждого саркомера, входящего в состав миофибрилл. [c.371]
Структурные факторы скоростно-силовых способностей человека (длина саркомеров в миофибриллах, содержание быстро- и медленносокращающихся волокон в мышцах) генетически обусловлены, поэтому основным методическим путем улучшения скоростно-силовых качеств спортсменов является подбор средств и методов, которые могли бы улучшить АТФ-аз-ную активность миозина и усилить синтез сократительных белков в мышцах.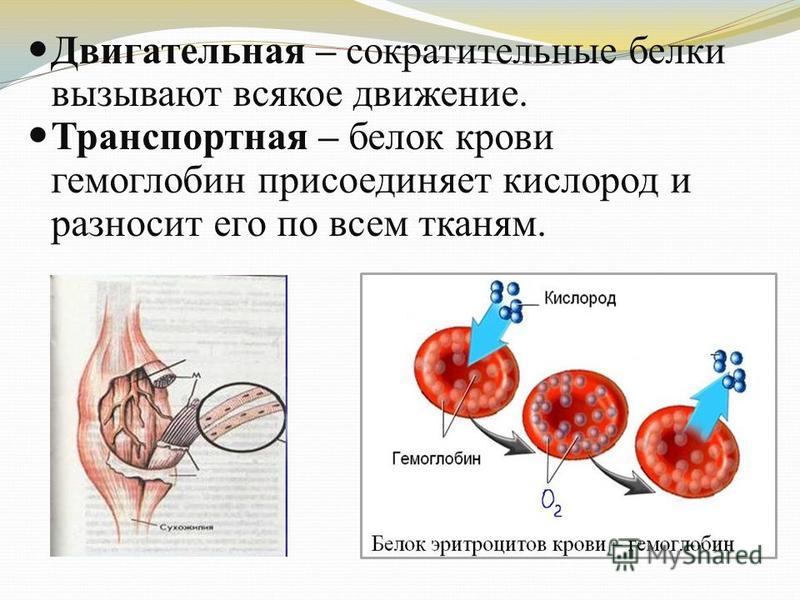 В скоростно-силовых видах спорта для решения этих задач в настоящее время используются два основных методических приема — метод максимальных усилий и метод повторных предельных упражнений. [c.386]
В скоростно-силовых видах спорта для решения этих задач в настоящее время используются два основных методических приема — метод максимальных усилий и метод повторных предельных упражнений. [c.386]
Актин. Содержание актина в скелетных мышцах в качестве структурного и сократительного белка существенно увеличивается в процессе тренировки. По его содержанию в мышцах можно было бы контролировать развитие скоростно-силовых качеств спортсмена при тренировке, однако определение его содержания в мышцах связано с большими методическими затруднениями. Тем не менее после выполненных физических нагрузок отмечается появление актина в крови, что свидетельствует о разрушении либо обновлении миофибриллярных структур скелетных мышц. В крови содержание актина определяют радиоиммуннологическим методом и по его изменению судят о переносимости физических нагрузок, интенсивности восстановления миофибрилл после мышечной работы. [c.471]
Белки вьшолняют в организме очень важные функции. К ним в первую очередь следует отнести структурную, каталитическую, сократительную, транспортную, регуляторную, защитную, а также энергетическую. На долю бежов в среднем приходится 1/6 часть от массы тела человека. [c.5]
К ним в первую очередь следует отнести структурную, каталитическую, сократительную, транспортную, регуляторную, защитную, а также энергетическую. На долю бежов в среднем приходится 1/6 часть от массы тела человека. [c.5]
Структурная единица скелетной мышцы — мышечное волокно—много ядерная клетка длиною в несколько сантиметров, диаметром в 0,2—0,1 мм. Внутри волокна, в саркоплазме, расположены в виде пучков нитей миофиб-риллы —сократительные элементы мышечного волокна. Л1иофибриллы обладают видимой под микроскопом попереч1юй исчерченностью, зависяш,ей от оптической неоднородности входящих в их состав белковых веществ. Мышечное волокно покрыто соединительнотканной оболочкой — сарколеммой. Из мышечных волокон состоят мышечные пучки, содержащие некоторое количество соединительной ткани. Обычно химический состав мышцы изучается не в отдельно взятых ее микроскопических элементах, а в общей массе. Для полного представления о составных частях мышечных волокон учитывают содержание в мышце белков соединительной ткаии.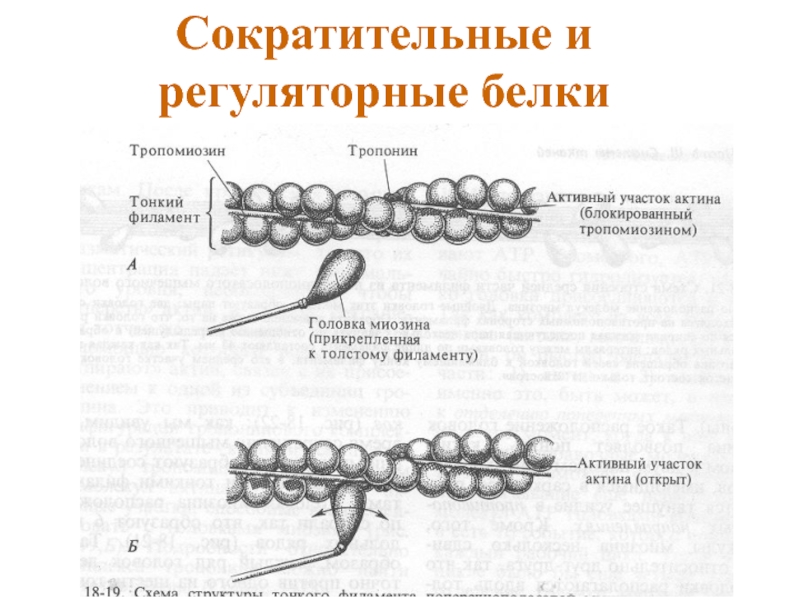 [c.542]
[c.542]
Миозин является белком многих качеств. В сокращении скелетных, сердечных и гладких мышц и во внутриклеточных движениях он одновременно выполняет, по крайней мере, три ключевых функции — структурную, аллостерическую и ферментативную. Наиболее полезная информация о функциях миозина была получена при исследовании поперечнополосатых скелетных мышц, сокращающихся произвольно, а также аналогичных тканей беспозвоночных, прежде всего летательных мышц насекомых. Электронно-микроскопическое изучение продольных и поперечных тонких срезов скелетных мышц, впервые проведенное в 1953 г. X. Хаксли, выявило высокий уровень их структурной организации [439]. Уже в следующем году X. Хаксли вместе с Дж. Хенсоном предложили так называемую модель скользящих нитей, которая имела основополагающее значение для понимания природы и молекулярного механизма мышечных сокращений [440]. Скелетные мышцы — это пучки мышечных волокон, наиболее крупным повторяющимся структурным элементом которых является миофибрилла — цилиндрическая нить диаметра 1-2 мкм (1000-2000 А), идущая от одного конца клетки до другого.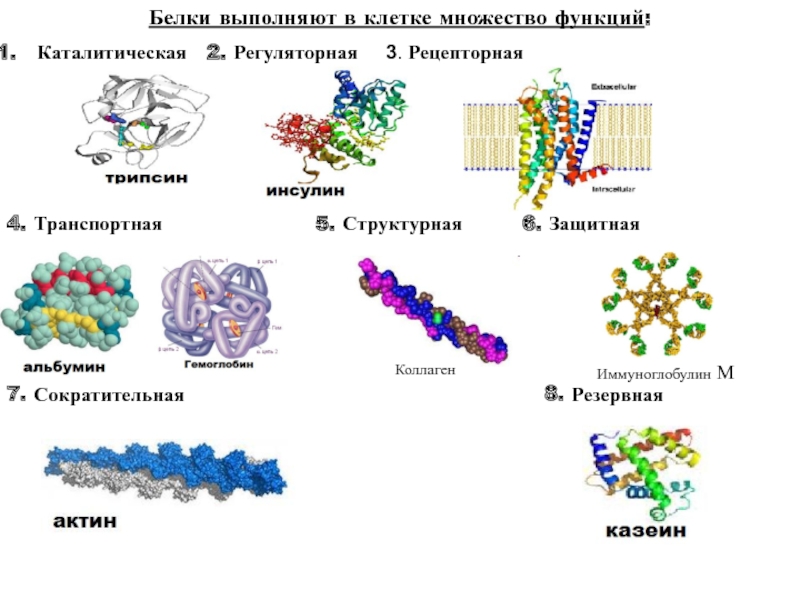 Миофибрилла, в свою очередь, содержит белковые филамен-ты двух типов толстые и тонкие. Основной белок толстых нитей — миозин, тонких — актин. Миозиновые и актиновые филаменты в миофиб-рилле строго упорядочены. Функциональной сократительной единицей миофибриллы является саркомера, имеющая длину около 2,5 мкм и разделяющаяся на I- и А-диски (рис. 1.31). Толстые филаменты (длина 1,6 мкм и толщина 0,015 мкм) тянутся от одного края А-диска до другого, а тонкие (длина 1,0 мкм и толщина 0,008 мкм) идут от [c.120]
Миофибрилла, в свою очередь, содержит белковые филамен-ты двух типов толстые и тонкие. Основной белок толстых нитей — миозин, тонких — актин. Миозиновые и актиновые филаменты в миофиб-рилле строго упорядочены. Функциональной сократительной единицей миофибриллы является саркомера, имеющая длину около 2,5 мкм и разделяющаяся на I- и А-диски (рис. 1.31). Толстые филаменты (длина 1,6 мкм и толщина 0,015 мкм) тянутся от одного края А-диска до другого, а тонкие (длина 1,0 мкм и толщина 0,008 мкм) идут от [c.120]
ФУНКЦИИ БЕЛКОВ. «БИОЛОГИЧЕСКАЯ ХИМИЯ», Березов Т.Т., Коровкин Б.Ф.
Белки
выполняют множество самых разнообразных функций, характерных для живых
организмов, с некоторыми из которых мы познакомимся более подробно при
дальнейшем изучении курса. Ниже рассматриваются главные и в некотором смысле
уникальные биологические функции белков, несвойственные или лишь частично
присущие другим классам биополимеров.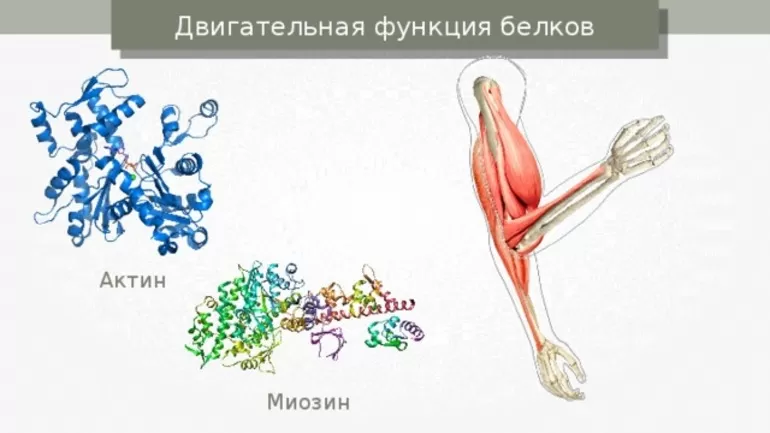
Каталитическая функция. К 1995 г. было идентифицировано более 3400 ферментов.
Большинство известных в настоящее время ферментов, называемых
биологическими катализаторами, является белками. Эта функция белков, хотя и не
оказалась уникальной, определяет скорость химических реакций в биологических
системах.
Транспортная функция. Дыхательная функция крови, в частности перенос кислорода,
осуществляется молекулами гемоглобина – белка эритроцитов. В транспорте липидов
принимают участие альбумины сыворотки крови. Ряд других сывороточных белков
образует комплексы с жирами, медью, железом, тироксином, витамином А и другими
соединениями, обеспечивая их доставку в соответствующие органы-мишени.
Защитная функция. Основную функцию защиты в организме выполняет иммунная
система, которая обеспечивает синтез специфических защитных белков-антител в
ответ на поступление в организм бактерий, токсинов, вирусов или чужеродных
белков. Высокая специфичность взаимодействия антител с антигенами (чужеродными
Высокая специфичность взаимодействия антител с антигенами (чужеродными
веществами) по типу белок-белковое взаимодействие способствует узнаванию и нейтрализации
биологического действия антигенов. Защитная функция белков проявляется и в
способности ряда белков плазмы крови, в частности фибриногена, к свертыванию. В
результате свертывания фибриногена образуется сгусток крови, предохраняющий от
потери крови при ранениях.
Сократительная функция. В акте мышечного сокращения и расслабления участвует
множество белковых веществ. Однако главную роль в этих жизненно важных
процессах играют актин и миозин – специфические белки мышечной ткани.
Сократительная функция присуща не только мышечным белкам, но и белкам
цитоскелета, что обеспечивает тончайшие процессы жизнедеятельности клеток
(расхождение хромосом в процессе митоза).
Структурная функция. Белки, выполняющие структурную (опорную) функцию, занимают
по количеству первое место среди других белков тела человека. Среди них
Среди них
важнейшую роль играют фибриллярные белки, в частности коллаген в соединительной
ткани, кератин в волосах, ногтях, коже, эластин в сосудистой стенке и др.
Большое значение имеют комплексы белков с углеводами в формировании ряда
секретов: мукоидов, муцина и т.д. В комплексе с липидами (в частности, с
фосфолипидами) белки участвуют в образовании биомембран клеток.
Гормональная функция. Обмен веществ в организме регулируется разнообразными
механизмами. В этой регуляции важное место занимают гормоны, синтезируемые не
только в железах внутренней секреции, но и во многих других клетках организма
(см. далее). Ряд гормонов представлен белками или полипептидами, например
гормоны гипофиза, поджелудочной железы и др. Некоторые гормоны являются
производными аминокислот.
Питательная (резервная) функция. Эту функцию выполняют так называемые резервные белки,
являющиеся источниками питания для плода, например белки яйца (овальбумины).
Основной белок молока (казеин) также выполняет главным образом питательную
функцию. Ряд других белков используется в организме в качестве источника
аминокислот, которые в свою очередь являются предшественниками биологически
активных веществ, регулирующих процессы метаболизма.
Можно назвать
еще некоторые другие жизненно важные функции белков. Это, в частности,
экспрессия генетической информации, генерирование и передача нервных импульсов,
способность поддерживать онкотическое давление в
клетках и крови, буферные свойства, поддерживающие физиологическое значение рН
внутренней среды, и др.
Таким
образом, из этого далеко не полного перечня основных функций белков видно, что
указанным биополимерам принадлежит исключительная и разносторонняя роль в живом
организме. Если попытаться выделить главное, решающее свойство, которое
обеспечивает многогранность биологических функций белков, то следовало бы
назвать способность белков строго избирательно, специфически соединяться с
широким кругом разнообразных веществ. В частности, эта высокая специфичность
В частности, эта высокая специфичность
белков (сродство) обеспечивает взаимодействие ферментов с субстратами, антител
с антигенами, транспортных белков крови с переносимыми молекулами других
веществ и т.д. Это взаимодействие основано на принципе биоспецифического
узнавания, завершающегося связыванием фермента с соответствующей молекулой
субстрата, что содействует протеканию химической реакции. Высокой
специфичностью действия наделены также белки, которые участвуют в таких
процессах, как дифференцировка и деление клеток, развитие живых организмов,
определяя их биологическую индивидуальность.
Предыдущая страница |
Следующая страница
СОДЕРЖАНИЕ
Функции белков | Параграф 1.5.
«Введение в общую биологию и экологию. 9 класс». А.А. Каменский (гдз)
Вопрос 1. Чем объясняется многообразие функций белков?
Уникальные свойства белков заложены в колоссальном разнообразии пространственного строения их молекул. Это разнообразие белков определяется огромным числом возможных сочетаний аминокислотных остатков в длинных, состоящих, как правило, из нескольких сотен остатков, полипептидных цепях белков. Как известно, в состав белков может входить 20 видов аминокислот. Белки образуют различные соединения с различными веществами. Кроме того, белки могут иметь пространственную структуру молекулы. Установлено, что белки могут иметь различные размеры и форму. Многие белки содержат в своём составе такие металлы, как железо, цинк, медь и др. Все это способствует тому, что белки выполняют множество функций.
Это разнообразие белков определяется огромным числом возможных сочетаний аминокислотных остатков в длинных, состоящих, как правило, из нескольких сотен остатков, полипептидных цепях белков. Как известно, в состав белков может входить 20 видов аминокислот. Белки образуют различные соединения с различными веществами. Кроме того, белки могут иметь пространственную структуру молекулы. Установлено, что белки могут иметь различные размеры и форму. Многие белки содержат в своём составе такие металлы, как железо, цинк, медь и др. Все это способствует тому, что белки выполняют множество функций.
Вопрос 2. Какие функции белков вам известны?
1. Строительная (пластическая) функция. Белки являются непременным компонентом всех биологических мембран, составляют основу цитоскелета, входят в состав соединительных тканей, волосяного покрова, т.е. обеспечивают «строительную» функцию.
2. Ферментативная функция. Обладая, прежде всего, ярко выраженной каталитической способностью, они в качестве ферментов детерминируют интенсивность всех метаболических процессов в клетке и организме в целом. Белки служат ферментами, т. е. биологическими катализаторами. Примером может служить амилаза, расщепляющая крахмал до моносахаридов; пепсин, расщепляющий белки на пептиды.
Белки служат ферментами, т. е. биологическими катализаторами. Примером может служить амилаза, расщепляющая крахмал до моносахаридов; пепсин, расщепляющий белки на пептиды.
3. Сократительная (двигательная) функция). Все виды движения, начиная с движений жгутиков бактерий и кончая движениями пальцев пианиста, обеспечиваются работой «белковых моторов» (сократительные белки). Сократительные свойства белков актина и миозина лежат в основе работы мышц.
4. Транспортная функция. Белки участвуют в транспорте молекул и ионов в пределах организма (гемоглобин переносит кислород из легких к органам и тканям, альбумин сыворотки крови участвует в транспорте жирных кислот).
5. Защитная функция. Она заключается в предохранении организма от повреждений и вторжения чужеродных белков и бактерий. Белки-антитела, вырабатываемые лимфоцитами, создают защиту организма от чужеродной инфекции, тромбин и фибрин участвуют в образовании тромба, тем самым, помогая организму избежать больших потерь крови.
6. Регуляторная функция. Белки-гормоны участвуют в регуляции активности клетки и всех жизненных процессов организма. Так, инсулин регулирует уровень сахара в крови и поддерживает его на определенном уровне.
7. Сигнальная функция. Белки формируют ионные каналы и осуществляют восприятие, трансформацию и передачу разнообразных внешних сигналов (белки-рецепторы).
8. Энергетическая функция. Она реализуется белками крайне редко. При полном расщеплении 1г белка способно выделиться 17,6кДж энергии. Однако белки для организма — очень ценное соединение. Поэтому расщепление белка происходит обычно до аминокислот, из которых строятся новые полипептидные цепочки. Они же осуществляют иммунологическую защиту от чужеродных соединений и патогенных микроорганизмов (защитные белки-иммуноглобулины).
Вопрос 3. Какую роль играют белки-гормоны?
Белки-гормоны контролирует физиологическую активность тканей и органов и всех жизненных процессов всего организма. Так, в организме человека соматотропин участвует в регуляции роста тела, инсулин поддерживает на постоянном уровне содержание глюкозы в крови.
Так, в организме человека соматотропин участвует в регуляции роста тела, инсулин поддерживает на постоянном уровне содержание глюкозы в крови.
Вопрос 4. Какую функцию выполняют белки-ферменты?
Белки-ферменты играют роль катализаторов, т. е. ускоряют химические реакции в сотни миллионов раз. Ферменты обладают строгой специфичностью по отношению к веществу, вступающему в реакцию. Каждая реакция катализируется своим ферментом.
Вопрос 5. Почему белки редко используются в качестве источника энергии?
Мономеры белков аминокислоты — ценное сырье для построения новых белковых молекул. По-этому полное расщепление полипептидов до неорганических веществ происходит редко. Следовательно, энергетическая функция, заключающаяся в выделении энергии при полном расщеплении, выполняется белками только в исключительных случаях, когда организм испытывает недостаток жиров или углеводов.
Основные биологические функции белков
Белки входят в состав каждой клетки и составляют около 50% ее сухой массы. Они играют ключевую роль в обмене веществ, реализуют важнейшие биологические функции, лежащие в основе жизнедеятельности всех организмов.
Они играют ключевую роль в обмене веществ, реализуют важнейшие биологические функции, лежащие в основе жизнедеятельности всех организмов.
Среди большого разнообразия функций, выполняемых белками, первостепенное значение имеют структурная, или пластическая, и каталитическая. Это универсальные функции, поскольку они присущи всем живым организмам.
Структурные белки формируют каркас внутриклеточных органелл и внеклеточных структур, а также участвуют в стабилизации клеточных мембран. Такие структурные белки, как коллаген и эластин составляют основу соединительной и костной тканей высших животных и человека. Структурными белками, в частности, являются кератины кожи, волос, ногтей, шерсти, когтей, рогов, копыт, перьев, клювов, а также фиброин шелка, паутины.
Каталитически активными белками являются ферменты. Они ускоряют химические реакции, обеспечивая тем самым необходимые скорости протекания обменных процессов в клетке.
Многие белки, присущие отдельным живым организмам, выполняют специфические функции, среди которых наиболее важными являются транспортная, регуляторная, защитная, рецепторная, сократительная, запасная и некоторые др.
Транспортные белки переносят различные молекулы и ионы внутри организма. Например: гемоглобин — кислород от легких к тканям; миоглобин — кислород внутри клеток; сывороточный альбумин с током крови — жирные кислоты, а также ионы некоторых металлов. Ту же функцию выполняют специфические белки, транспортирующие различные вещества через клеточные мембраны.
Регуляторные белки участвуют в регуляции обмена веществ как внутри клеток, так и в целом организме. Например, такие сложные процессы, как биосинтез белков и нуклеиновых кислот, протекают под строгим «контролем» множества регуляторных белков. Специфические белковые ингибиторы регулируют активность многих ферментов.
Защитные белки формируют защитную систему живых организмов. Например, иммуноглобулины (антитела) и интерфероны предохраняют организм от проникновения в его внутреннюю среду вирусов, бактерий, чужеродных соединений, клеток и тканей. Белки свертывающей системы крови — фибриноген, тромбин — препятствуют потере крови при повреждениях кровеносных сосудов.
Рецепторные белки воспринимают сигналы, поступающие из внешней среды, и воздействуют на внутриклеточные процессы. Например, белки-рецепторы, сосредоточенные на поверхности клеточных мембран, избирательно взаимодействуют с регуляторными молекулами (например, гормонами).
Рецепторными белками являются родопсин, участвующий в зрительном акте, вкусовой сладкочувствительный и обонятельный белки.
Сократительные белки способны преобразовывать свободную химическую энергию в механическую работу. Например, белки мышц миозин и актин обеспечивают мышечное сокращение.
Запасные белки представляют собой резервный материал, предназначенный для питания развивающихся клеток. Запасными белками являются яичный альбумин, глиадин пшеницы,
Казеин кукурузы, казеин молока и многие другие. Запасные белки — существенный источник пищевого белка для человека.
Некоторые организмы вырабатывают токсические белки. Таковы яды змей, дифтерийный токсин, рицин семян клещевины, лектины семян бобовых и др.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Тесты для подготовки к ЕГЭ по биологии по теме «Химическая организация клетки» Пояснительная записка — Тесты
Тесты
для подготовки к ЕГЭ по биологии по теме
«Химическая организация клетки»
Пояснительная записка
Анализ результатов ЕГЭ показал, что тема « Химическая организация клетки» для выпускников является проблемной. Для решения этой проблемы необходимо вырабатывать стойкие навыки выполнения заданий, используемых на экзамене. Предлагаемые тесты содержат задания, которые учителя биологии могут использовать для отработки этих навыков, как на уроках, так и на индивидуальных консультациях по подготовке к ЕГЭ.
Тесты составлены по материалам КИМов (они отмечены звездочкой) и из дополнительной литературы. Задания из дополнительной литературы отличаются своей информативностью, поэтому могут быть использованы в качестве дополнительного источника знаний.
Тема 1: «Неорганические вещества клетки»
Задания части А.
Выберите один правильный ответ.
1.* Тела живой и неживой природы сходны набором
1) белков
2) химических элементов
3) нуклеиновых кислот
4) ферментов
2.* Магний – обязательный компонент молекул
1) ДНК
2) хлорофилла
3) гемоглобина
4) РНК
3.* Какую роль играют в клетке ионы калия и натрия?
1) являются биокатализаторами
2) участвуют в проведении возбуждения
3) обеспечивают транспорт газов
4) способствуют перемещению веществ через мембрану
4. Каково соотношение ионов натрия и калия в клетках животных и в окружающей их среде — межклеточной жидкости и крови?
Каково соотношение ионов натрия и калия в клетках животных и в окружающей их среде — межклеточной жидкости и крови?
1) натрия в клетке больше, чем снаружи, калия, наоборот, больше снаружи, чем в клетке
2) натрия снаружи столько же, сколько калия внутри клетки
3) натрия в клетке меньше, чем снаружи, а калия, наоборот, больше в клетке, чем снаружи
5. Назовите химический элемент, который в виде иона в больших количествах входит в состав цитоплазмы клеток, где его существенно больше, чем в межклеточной жидкости и принимает непосредственное участие в формировании постоянной разности электрических потенциалов, по разные стороны наружной плазматической мембраны
1) Н 4) С 7)Са 10) Na
2) О 5)S 8)Mg 11) Zn
3) N 6) Fe 9) К 12) Р
6. Назовите химический элемент, который входит в состав неорганического компонента костной ткани и раковин моллюсков, принимает участие в мышечном сокращении и свертывании крови, является посредником в передаче информационного сигнала от наружной плазматической мембраны в цитоплазму клетки
1) Н 4) С 7) Са 10) Na
2) О 5) S 8) Mg 11) Zn
3) N 6) Fe 9) К 12) Р
7. Назовите химический элемент, который входит в состав хлорофилла и является необходимым для сборки малой и большой субъединиц рибосомы в единую структуру, активирует некоторые ферменты
Назовите химический элемент, который входит в состав хлорофилла и является необходимым для сборки малой и большой субъединиц рибосомы в единую структуру, активирует некоторые ферменты
1) Н 4) С 7) Са 10) Na
2) О 5) S 8) Mg 11) Zn
3) N 6) Fe 9) К 12) Р
8. Назовите химический элемент, который входит в состав гемоглобина и миоглобина, где участвует в присоединении кислорода, а также входит в состав одного из митохондриальных белков дыхательной цепочки, переносящей электроны в ходе клеточного дыхания.
1) Н 4) С 7) Са 10) Na
2) О 5) S 8) Mg 11) Zn
3) N 6) Fe 9) К 12) Р
9.Укажите группу химических элементов, содержание которых в клетке составляет в сумме 98%,
1) H,O,S,P
2) H,C,O,N
3) N,P,H,O
4) C,H,K,Fe
10. Назовите жидкость, которая по солевому составу наиболее близка к плазме крови наземных позвоночных животных
Назовите жидкость, которая по солевому составу наиболее близка к плазме крови наземных позвоночных животных
1) 0.9% раствор NaCl
2) морская вода
3) вода пресных водоемов
11.Назовите органические соединения, которые содержатся в клетке в наибольшем количестве (в % на сырую массу)
1) углеводы
2) липиды
3) белки
4) нуклеиновые кислоты
12. Назовите органические соединения, которые содержатся в клетке в наименьшем количестве (в % на сырую массу)
1) углеводы
2) липиды
3) белки
4) нуклеиновые кислоты
13.*Значительную часть клетки составляет вода, которая
1) образует веретено деления
2) образует глобулы белка
3) растворяет жиры
4) придаёт клетке упругость
14. Назовите основную особенность строения молекулы воды, которая определяет специфические свойства и биологическую роль воды
Назовите основную особенность строения молекулы воды, которая определяет специфические свойства и биологическую роль воды
1) небольшой размер
2) полярность молекулы
3) высокая подвижность
15.*Вода — хороший растворитель, так как
1) ее молекулы имеют взаимное притяжение
2) ее молекулы полярны
3) она медленно нагревается и остывает
4) она является катализатором
16.* Вода в клетке выполняет функцию
1) каталитическую
2) растворителя
3) структурную
4) информационную
17.* От содержания молекул воды в клетке зависит ее
1) связь с соседними клетками
2) рост и развитие
3) способность делиться
4) объем и упругость
18. Все выше перечисленные анионы , кроме одного, входят в состав солей и являются наиболее важными для жизнедеятельности клетки анионами . Укажите «лишний» среди них анион.
Все выше перечисленные анионы , кроме одного, входят в состав солей и являются наиболее важными для жизнедеятельности клетки анионами . Укажите «лишний» среди них анион.
1) НСО—3
2) SO42-
3) Cl—
4) Н2РО4—
5) НРО42-
Правильные ответы
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
2 |
2 |
4 |
3 |
9 |
7 |
8 |
6 |
2 |
2 |
3 |
4 |
4 |
2 |
2 |
2 |
4 |
2 |
Задания части Б.
Выберите три правильных ответа из шести.
1)Каковы функции воды в клетке?
А) выполняет энергетическую функцию
Б) обеспечивает упругость клетки
В) защищает содержимое клетки
Г) участвует в теплорегуляции
Д) участвует в гидролизе веществ
Е) обеспечивает движение органоидов.
Ответ: Б, Г, Д
2)*Вода в клетке выполняет роль
А) внутренней среды
Б) структурную
В) регуляторную
Г) гуморальную
Д) универсального источника энергии
Е) универсального растворителя
Ответ: А, Б, Е.
Тема 2: « Биологические полимеры – белки».
Задания части А.
Выберите один правильный ответ.
1*. Белки относят к группе биополимеров, так как они:
1) отличаются большим разнообразием
2) играют большую роль в клетке
3) состоят из многократно повторяющихся звеньев
4) имеют большую молекулярную массу
2*. Мономерами молекул белка являются
Мономерами молекул белка являются
1) нуклеотиды
2) аминокислоты
3) моносахариды
4) липиды
3*. Полипептиды образуются в результате взаимодействия
-
1) азотистых оснований
-
2) липидов
-
3) углеводов
-
4) аминокислот
4*. От вида числа и порядка расположения аминокислот зависит
-
1) последовательность триплетов РНК
-
2) первичная структура белков
-
3) гидрофобность молекул жиров
-
4) гидрофильность моносахаридов
5*. В составе клеток всех живых организмов входит
-
1) гемоглобин
-
2) белок
-
3) хитин
-
4) клетчатка
6*. Последовательность расположения аминокислот в молекул белка определяется
-
1) расположением триплетов в молекуле ДНК
-
2) особенностью строения рибосомы
-
3) набором рибосом в полисоме
-
4) особенностью строения Т-РНК
7*.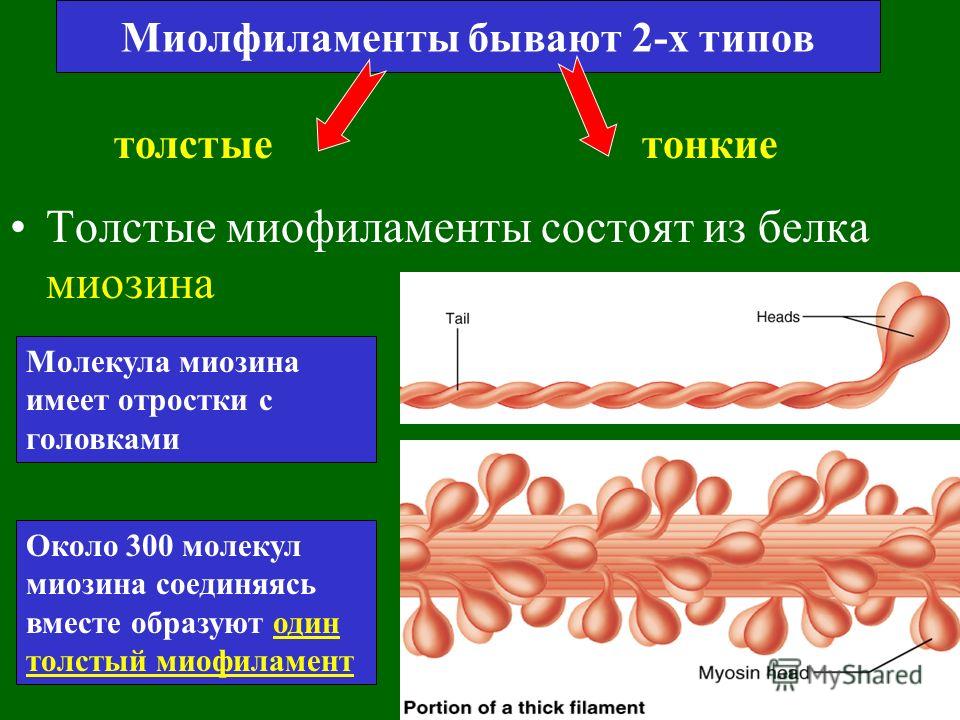 При обратимой денатурации молекул белка происходит
При обратимой денатурации молекул белка происходит
-
1) нарушение его первичной структуры
-
2) образование водородных связей
-
3) нарушение его третичной структуры
-
4) образование пептидных связей
8*. Способность молекул белка образовать соединения с другими веществами определяет их функцию
-
1) транспортную
-
2) энергетическую
-
3) сократительную
-
4) выделительную
9*. Какую функцию в организме животных выполняют сократительные белки?
1) транспортную
2) сигнальную
3) двигательную
4) каталитическую
10*. Органические вещества, ускоряющие процессы обмена веществ,-
1) аминокислотные
2) моносахариды
3) ферменты
4) липиды
11*. Какую функцию не выполняют в клетке белки?
1) защитную
2) ферментативную
3) информационную
4) сократительную
Ответы:
Задания части В.
Выберите три правильных ответа из шести.
1*. Каковы особенности строения и свойств молекул белков?
А) имеет первичную, вторичную, третичную, четвертичную структуры.
Б) имеют вид одиночной спирали
В) мономеры-аминокислоты
Г) мономеры-нуклеотиды
Д) способны к репликации
Е) способны к денатурации
Ответы: А, В, Е.
Задания части С.
Дайте полный развернутый ответ.
1*. Ферменты теряют свою активность при повышении уровня радиации.
Объясните, почему.
Ответ: Все ферменты – белки. Под действием радиации изменяется структура
белка-фермента, происходит его денатурация.
Задания из дополнительной литературы по теме « Белки».
Выберите один правильный ответ:
-
1.
 Определите признак, по которому все нижеперечисленные соединения, кроме одного, объединены в одну группу. Укажите «лишние» среди них химическое соединение.
Определите признак, по которому все нижеперечисленные соединения, кроме одного, объединены в одну группу. Укажите «лишние» среди них химическое соединение.
1) пепсин 5) каталаза
2) коллаген 6) мальтаза
3) кератин 7) гемоглобин
4) хитин
2. Соли тяжелых металлов (ртути, мышьяка, свинца) являются ядами для организма. Они связываются с сульфидными группировками белков. Назовите структуру белков, которая разрушается под действием солей тяжелых металлов.
1) первичная 3) третичная
2) вторичная
3. Назовите белок, выполняющий ферментативную функцию.
1) гормон роста 4) актин
2) фибрин 5) трипсин
3) инсулин
4. В каком ответе все названные химические соединения относятся к
аминокислотам?
1) тубулин, коллаген, лизоцим
2) лизин, триптофан, аланин
3) холестерин, прогестерон, стеариновая кислота
4) валин, мальтаза, кератин
5) сахароза, лактоза, глицин
6) аденин, тимин, гуанин
5. Белки как полимеры имеют особенности, по которым существенно отличаются от
Белки как полимеры имеют особенности, по которым существенно отличаются от
каких полисахаридов, как гликоген и крахмал. Найдите эти особенности среди
ответов
и укажите признак, который такой особенностью НЕ является.
1) очень большое число мономеров
2) являются линейными полимерами
3) иная структура мономеров
4) мономеры белка отличаются друг от друга
6. Первичные структуры разных белков отличаются друг от друга по ряду признаков. Найдите эти признаки среди ответов и укажите особенность строения, по которой разные белки, наоборот, похожи друг на друга.
1) количество аминокислот
2) количественное соотношение аминокислот разных видов
3) последовательность соединения аминокислот друг с другом
4) структура химических связей, участвующих в формировании
последовательности аминокислот
7. Назовите органические соединения, которые содержатся в клетке в наибольшем
количестве (в % на сырую массу).
-
1) углеводы
-
2) липиды
-
3) белки
-
4) нуклеиновые кислоты
-
5) низкомолекулярные органические вещества
8. Назовите функциональные группы соседних аминокислот в белке, между
которыми образуется пептидная связь.
-
1) радикалы 4) карбоксильные группы
-
2) карбоксильная группа и аминогруппа 5) карбоксильная группа и радикал
-
3) радикал и ион водорода 6) аминогруппа и радикал
9. Назовите белок, выполняющий рецепторную функцию.
1) лизоцим 3) протромбин
2) пепсин 4) родопсин
10. Назовите белок, выполняющий рецепторную функцию.
1) коллаген 3) гемоглобин
3) фибрин 4) инсулин
11. Назовите белок, выполняющий в основном структурную функцию.
1) кератин 4) липаза
2) каталаза 5) гормон роста
3) нуклеаза
12. Назовите белок, выполняющий в основном транспортную функцию.
Назовите белок, выполняющий в основном транспортную функцию.
1) коллаген 4)гемоглобин
2) кератин 5) миоглобин
3) фибрин
13. Назовите основную функцию, которую выполняют такие белки, кератин,
коллаген, тубулин.
1) двигательная 4) транспортная
2) защитная 5) строительная
3) ферментативная
14. Назовите белок, выполняющий в основном двигательную функцию.
1) актин 4) каталаза
2) фибрин 5) липаза
3) тромбин 6) миоглобин
15. Назовите функцию, которую выполняет основная масса белков семян растений и
яйцеклеток животных.
1) защитная 4) двигательная
2) строительная 5) ферментативная
3) запасающая
16. В каком ответе все названные химические соединения являются белками?
1) сахароза, инсулин, урацил
2) фенилаланин, глюкагон, пепсин
3) глюкоза, фруктоза, гликоген
4) каталаза, глюкагон, кератин 5) рибоза, тимин, актин
17. Определите признак, по которому все нижеперечисленные химические
Определите признак, по которому все нижеперечисленные химические
соединения, кроме одного, объединены в одну группу. Укажите это «лишнее»
среди них химическое соединение.
1) аланин 5) актин
2) валин 6) лейцин
3) глицин 7) цистеин
4) триптофан
18. Назовите белок, выполняющий ферментативную функцию.
1) каталаза 4) глюкагон
2) протромбин 5) кератин
3) тубулин
19. Назовите белок, входящий в состав микротрубочек жгутиков и ресничек,
центриолей и веретина движения.
1) кератин 3) миозин
2) тубулин 4) коллаген
20. Назовите белок волос.
1) кератин 3) миозин 5) актин
2) тубулин 4) коллаген 6) фибрин
21. Что является мономером белков?
1) глюкоза 4) нуклеиновая кислота
2) нуклеотид 5) азотистое основание
3) аминокислота
22. Сколько видов аминокислот входит в состав природных белков?
1) 10 3) 20 5) 46
2) 15 4) 25 6) 64
ГДЗ таблицы по биологии 9 класс ответы и решения онлайн.
 Задание: Функции белков
Задание: Функции белков
Изображения обложек учебников приведены на страницах данного сайта исключительно в качестве иллюстративного материала (ст. 1274 п. 1 части четвертой Гражданского кодекса Российской Федерации)
На данной странице представлено детальное решение задания Функции белков по биологии для учеников 9 классa автор(ы)
Функции белков
| Строительная | Одна из важнейших функций белковых молекул. Белки входят в состав всех клеточных мембран и органоидов клетки. Преимущественно из белка состоят стенки кровеносных сосудов, хрящи, сухожилия, волосы и ногти |
| Защитная | Специфические белки выполняют эту функцию. Они предохраняют организм от вторжения чужеродных белков и микроорганизмов, а также от повреждений. Антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки, фибрин и тромбин предохраняют организм от кровопотери |
| Двигательная | Выполняют особые сократительные белки. Благодаря им двигаются реснички и жгутики у простейших, перемещаются хромосомы при делении клетки, сокращаются мышцы у многоклеточных, совершенствуются другие виды движения у живых организмов Благодаря им двигаются реснички и жгутики у простейших, перемещаются хромосомы при делении клетки, сокращаются мышцы у многоклеточных, совершенствуются другие виды движения у живых организмов |
| Регуляторная | Присуща белкам-гормонам. Они поддерживают постоянные концентрации веществ в крови и клетках, участвующих в росте, размножении и других важных процессах. Например, инсулин регулирует содержание сахара в крови |
| Транспортная | Гемоглобин переносит кислород из лёгких к клеткам других тканей и органов. В мышцах эту функцию выполняет белок миоглобин. Белки сыворотки крови способствуют переносу липидов и жирных кислот, различных биологически активных веществ. Белки в наружной мембране клетки переносят различные вещества из окружающей среды в цитоплазму |
| Ферментативная | Белки-ферменты способны ускорять биохимические реакции в клетке в десятки и сотни миллионов раз |
| Энергетическая | Являются одним из источников энергии в клетке. При полном расщеплении 1 г белка до конечного продукта выделяется 17,6 кДж энергии. Аминокислоты, высвобождаемые при расщеплении белковых молекул, используются при построении новых белков При полном расщеплении 1 г белка до конечного продукта выделяется 17,6 кДж энергии. Аминокислоты, высвобождаемые при расщеплении белковых молекул, используются при построении новых белков |
Add
© 2021Copyright. Все права защищены. Правообладатель SIA Ksenokss.
Адрес: 1069, Курземес проспект 106/45, Рига, Латвия.
Тел.: +371 29-851-888 E-mail: [email protected]
Contractile Protein — обзор
Характеристика гладкомышечных клеток
Цитоскелетные и сократительные белки экспрессируются в дифференцированных популяциях гладких мышц и других типах клеток. Эти белки обычно используются для характеристики этих типов клеток и для идентификации SMC в урологических тканях. Эти маркеры SMC включают альфа-актин гладких мышц (α-SM-актин), смоотелин, десмин, тяжелую цепь миозина, кальпонин, кальдесомон и виментин.
актин α-SM экспрессируется в SMC в актине гладких мышц и миофибриллах, что указывает на образование внутриклеточных «стрессовых волокон». Актин α-SM также экспрессируется в других типах клеток, таких как активированные фибробласты или миофибробласты в ранах или трансплантированном сердце, или в пролиферирующих мезангиальных клетках при гломерулярной болезни почек. Таким образом, белок актина α-SM не является SMC-специфичным. Хотя его нельзя использовать в качестве окончательного маркера для линии SMC, α-SM-актин по-прежнему полезен в качестве маркера дифференцировки для SMC, поскольку он является первым селективным по типу клеточным белком, экспрессируемым SMC во время дифференцировки, и одним из последних белков. подавляется в процессе фенотипической модуляции.Смуотелин — еще один белок сокращения гладких мышц, который присутствует в мышцах детрузора мочевого пузыря человека и свиньи. 41 Smoothelin представляет собой цитоскелетный белок, специфически экспрессируемый в дифференцированных SMC, и было показано, что он локализуется совместно с актином α-SM.
Актин α-SM также экспрессируется в других типах клеток, таких как активированные фибробласты или миофибробласты в ранах или трансплантированном сердце, или в пролиферирующих мезангиальных клетках при гломерулярной болезни почек. Таким образом, белок актина α-SM не является SMC-специфичным. Хотя его нельзя использовать в качестве окончательного маркера для линии SMC, α-SM-актин по-прежнему полезен в качестве маркера дифференцировки для SMC, поскольку он является первым селективным по типу клеточным белком, экспрессируемым SMC во время дифференцировки, и одним из последних белков. подавляется в процессе фенотипической модуляции.Смуотелин — еще один белок сокращения гладких мышц, который присутствует в мышцах детрузора мочевого пузыря человека и свиньи. 41 Smoothelin представляет собой цитоскелетный белок, специфически экспрессируемый в дифференцированных SMC, и было показано, что он локализуется совместно с актином α-SM.
Тяжелые цепи миозина гладких мышц (SMHC) — это моторные белки, которые обеспечивают сокращение гладких мышц. SMHC имеют две основные изоформы: SM1 и SM2. SM1 экспрессируется в SMCs на протяжении всего эмбрионального развития до зрелой стадии, тогда как SM2 выполняет особую функцию для сокращения гладких мышц и является специфическим маркером зрелых SMCs.Отношение SM1 / SM2 составляет примерно 1: 1 42 в нормальной мышечной ткани мочевого пузыря, но уменьшается в гиперактивном мочевом пузыре. 43 Изоформы SM1 и SM2 молекул SMHC являются специфическими маркерами при иммуноокрашивании дифференцировки SMC. SMC содержат меньше белка, чем типичная поперечно-полосатая мышечная клетка, и гораздо меньше миозина. Содержание актина аналогично, поэтому отношение актина к миозину составляет ∼6: 1 в поперечнополосатых мышцах и ∼15: 1 в гладких мышцах.
SMHC имеют две основные изоформы: SM1 и SM2. SM1 экспрессируется в SMCs на протяжении всего эмбрионального развития до зрелой стадии, тогда как SM2 выполняет особую функцию для сокращения гладких мышц и является специфическим маркером зрелых SMCs.Отношение SM1 / SM2 составляет примерно 1: 1 42 в нормальной мышечной ткани мочевого пузыря, но уменьшается в гиперактивном мочевом пузыре. 43 Изоформы SM1 и SM2 молекул SMHC являются специфическими маркерами при иммуноокрашивании дифференцировки SMC. SMC содержат меньше белка, чем типичная поперечно-полосатая мышечная клетка, и гораздо меньше миозина. Содержание актина аналогично, поэтому отношение актина к миозину составляет ∼6: 1 в поперечнополосатых мышцах и ∼15: 1 в гладких мышцах.
Десмин вступает в реакцию с частями белка промежуточных филаментов мышечных клеток.В гладких мышцах десмин располагается в цитоскелетной области в плотных телах и плотных бляшках. В статической культуральной среде SMC постепенно теряют сократительный фенотип, поскольку экспрессия генов, таких как десмин и миозин, снижается в долгосрочной культуре. 22, 44–46 Однако было показано, что присутствие инсулиноподобного фактора роста, ламинина 47 или трансформирующего фактора роста β (TGF-β) и механического штамма 48 может предотвратить спонтанная потеря сократительного фенотипа SMC in vitro.
22, 44–46 Однако было показано, что присутствие инсулиноподобного фактора роста, ламинина 47 или трансформирующего фактора роста β (TGF-β) и механического штамма 48 может предотвратить спонтанная потеря сократительного фенотипа SMC in vitro.
Кальпонин действует как один регуляторный сократительный белок и имеет три изоформы: основную (h2 или α), нейтральную (h3) и кислотную. h2-кальпонин экспрессируется только в дифференцированных SMC. 49 Вариант кальпонина с более низкой молекулярной массой часто наблюдается в ГМК урогенитального тракта человека. 50 Кальдесмон, имеющий две изоформы, (H) и (L), расположен в тонких филаментах SMC и является регуляторным белком, связывающимся с кальмодулином и актином. H-кальдесмон преимущественно экспрессируется в дифференцированных SMC, тогда как L-кальдесмон экспрессируется в дедифференцированных мышечных клетках.Обе изоформы могут быть взаимно преобразованы при модуляции клеточных фенотипов. 51
51
Виментин экспрессируется в SMC плодного пузыря, и его экспрессия заметно снижается в послеродовой период и во время физиологической гипертрофии SMC, которая происходит одновременно со снижением синтеза ДНК. Виментин также присутствует в цитоплазме миофибробластов. Существует организованный цитоскелет, состоящий из белков промежуточных филаментов виментина и десмина, а также филаментов актина.
Цитоплазматические сократительные белки | SpringerLink
Часть
Монографии по клеточной биологии
серия книг (CELLBIOL, том 13)
Abstract
Цитоплазматические сократительные белки широко изучаются с конца 1960-х годов, когда они были признаны основными компонентами цитоплазмы практически всех эукариотических клеток. Однако сократимость цитоплазмы считалась важным свойством живых клеток еще 150 лет назад, когда впервые возникла концепция клетки как единицы жизни.В 1835 году Dujardin предположил, что цитоплазма структурирована и обладает эластичными сократительными свойствами и . Он описал липкий материал, который появляется из раздавленных клеток, как однородное, hyahne, живое вещество («gelée vivante») и назвал его «саркодом». Идея Дурджадина об однородном саркоде была заменена на рубеже веков новой концепцией, в которой цитоплазма рассматривалась как гетерогенная и высокоструктурированная субстанция. Наблюдения в течение первой половины этого столетия добавили представление о том, что цитоплазма имеет характерную «вязкость» (Heilbrunn 1926).Однако, как только были осознаны сложности взаимосвязи между механическими и сократительными свойствами цитоплазмы и ее супрамолекулярной архитектурой, идея о том, что цитоплазма может быть охарактеризована одним физическим параметром, ее вязкостью, была оставлена. В 1939 году Льюис разработал удивительно точную точку зрения, согласно которой цитоплазма заполнена «чрезвычайно большими и асимметричными молекулами, которые предположительно образуют длинные волокна при гелеобразовании», а также могут оказывать «сократительное напряжение».
Он описал липкий материал, который появляется из раздавленных клеток, как однородное, hyahne, живое вещество («gelée vivante») и назвал его «саркодом». Идея Дурджадина об однородном саркоде была заменена на рубеже веков новой концепцией, в которой цитоплазма рассматривалась как гетерогенная и высокоструктурированная субстанция. Наблюдения в течение первой половины этого столетия добавили представление о том, что цитоплазма имеет характерную «вязкость» (Heilbrunn 1926).Однако, как только были осознаны сложности взаимосвязи между механическими и сократительными свойствами цитоплазмы и ее супрамолекулярной архитектурой, идея о том, что цитоплазма может быть охарактеризована одним физическим параметром, ее вязкостью, была оставлена. В 1939 году Льюис разработал удивительно точную точку зрения, согласно которой цитоплазма заполнена «чрезвычайно большими и асимметричными молекулами, которые предположительно образуют длинные волокна при гелеобразовании», а также могут оказывать «сократительное напряжение».
Ключевые слова
Легкая цепь Актиновая нить Контрактильный белок Миозин Голова Актиновый мономер
Эти ключевые слова были добавлены машиной, а не авторами. Это экспериментальный процесс, и ключевые слова могут обновляться по мере улучшения алгоритма обучения.
Это предварительный просмотр содержимого подписки,
войдите в
, чтобы проверить доступ.
Предварительный просмотр
Невозможно отобразить предварительный просмотр. Скачать превью PDF.
Информация об авторских правах
© Springer-Verlag / Wien 1986
Авторы и аффилированные лица
- 1.Кафедра зоологии Калифорнийского университета, Беркли, США,
Взаимосвязи между структурой и функцией сократительных и сигнальных белков в сердце
Krenz M, Sadayappan S, Osinska HE, Henry JA, Beck S, Warshaw DM, Robbins J. Распределение и взаимосвязь между структурой и функцией изоформ тяжелой цепи миозина в сердце взрослой мыши. J Biol. Chem. 2007; 282: 24057-24064.
Распределение и взаимосвязь между структурой и функцией изоформ тяжелой цепи миозина в сердце взрослой мыши. J Biol. Chem. 2007; 282: 24057-24064.
Hambleton M, York A, Sargent MA, Kaiser RA, Lorenz JN, Robbins J, Molkentin JD. Индуцируемое и специфичное для миоцитов ингибирование PKCalpha усиливает сердечную сократимость и защищает от сердечной недостаточности, вызванной инфарктом. Am J Physiol Heart Circ Physiol. 2007; 293: h4768-h4771.
Нагьяма Т., Такимото Е., Садаяппан С., Мадд Дж.О., Сейдман Дж. Г., Роббинс Дж., Касс Д.А. Контроль in vivo кинетики [коррекции] сокращения / релаксации левого желудочка с помощью миозин-связывающего протеина C: протеинкиназы A, зависимого от фосфорилирования и независимого регулирования. Тираж. 2007; 116: 2399-2408.
Диван А., Кренц М., Сайед Ф.М., Ванасапура Дж., Рен Х, Маткович С.Дж., Кестерс А.Г., Ли Х., Киршенбаум Л.А., Роббинс Дж., Джонс В. К., Дорн Г.В. 2 и . Ингибирование апоптоза ишемических кардиомиоцитов посредством целенаправленного удаления bnip3 сдерживает постинфарктное ремоделирование. J Clin Invest. 2007; 117: 2825-2833.
К., Дорн Г.В. 2 и . Ингибирование апоптоза ишемических кардиомиоцитов посредством целенаправленного удаления bnip3 сдерживает постинфарктное ремоделирование. J Clin Invest. 2007; 117: 2825-2833.
Oka T, Xu J, Kaiser RA, Melendez J, Hambleton M, Sargent MA, Lorts A, Brunskill EW, Dorn GW 2nd, Conway SJ, Aronow BJ, Robbins J, Molkentin JD. Генетическая манипуляция экспрессией периостина выявляет роль в гипертрофии сердца и ремоделировании желудочков. Circ Res . 2007; 101: 313-321.
Накамура Т., Колберт М., Кренц М., Молькентин Д.Д., Хан Х.С., Дорн Г.В. 2-й, Роббинс Дж. Посредничество передачи сигналов ERK1 / 2 спасает врожденные пороки сердца на мышиной модели синдрома Нунана. J Clin Invest. 2007; 117: 2123-2132.
Hsieh PCH, Дэвис М.Э., МакГилливрей К., Гэннон Дж., Молькентин Дж. Д., Роббинс Дж., Ли Р. Т.. Данные исследования генетического картирования судеб, свидетельствующие о том, что стволовые клетки обновляют кардиомиоциты взрослых млекопитающих после повреждения. Nature Med. 2007; 13, 970-974.
Nature Med. 2007; 13, 970-974.
Yasuda S-I, Coutu P, Sadayappan S, Robbins J, Metzger JM. Кардиальные трансгенные стратегии и стратегии переноса генов сходятся, чтобы поддерживать важную роль тропонина I в регуляции релаксации сердечных миоцитов. Circ Res. 2007; 101: 377-386.
Перселл Н.Х., Уилкинс Б.Дж., Йорк А., Роббинс Дж., Молькентин Дж. Генетическое ингибирование сердечной ERK1 / 2 способствует индуцированному стрессом апоптозу и сердечной недостаточности, но не влияет на гипертрофию в vivo . Proc. Natl Acad Sci U S. A. 2007; 104, 14074-14079.
Galvez AS, Diwan A, Odley AM, Hahn HS, Osinska H, Melendez JG, Robbins J, Lynch RA, Marreez Y, Dorn GW. Дегенерация кардиомиоцитов с дефицитом кальпаина показывает критическую роль в гомеостазе белка. Circ Res. 2007; 100, 1071-1078.
Nishizawa T, Shen Y-T, Rossi F, Hong C, Robbins J, Ishikawa J, Sadoshima J, Vatner D, Vatner S. Измененный вегетативный контроль у трансгенных кроликов в сознании с гиперэкспрессией сердечного Gsa. Am J Physiol. 2007; 292, H971-975.
Хойер К., Кренц М., Роббинс Дж., Ингуолл Дж. С.. Сдвиги изоферментов тяжелой цепи миозина в сердце мыши приводят к повышению энергоэффективности. J Mol Cell Cardiol. 2007; 42, 214-221.
Ютзи К.Э., Роббинс Дж. Принципы генетических моделей сердечных заболеваний на мышах. Тираж. 2007; 115: 792-799.
2.5: Структура и функция — функция белка II
Источник: BiochemFFA_2_4.pdf. Весь учебник доступен бесплатно у авторов по адресу http://biochem.science.oregonstate.edu/content/biochemistry-free-and-easy
.
До сих пор белки, которые мы обсуждали, не были катализаторами (ферментами). Однако большинство белков в клетках катализируют реакции.В этом разделе мы начинаем обсуждение подкласса белков, которые катализируют реакции, высвобождая энергию и преобразуя ее в механическую силу. Они действуют на клеточном и организменном уровне и известны как моторные белки. Моторные белки полагаются на глобулярные структурные белки, поэтому важно описать, как собираются эти клеточные «железные дороги», прежде чем обсуждать сами моторные белки. Есть две соответствующие волокнистые структуры, служащие рельсами для моторных белков. Их:
Они действуют на клеточном и организменном уровне и известны как моторные белки. Моторные белки полагаются на глобулярные структурные белки, поэтому важно описать, как собираются эти клеточные «железные дороги», прежде чем обсуждать сами моторные белки. Есть две соответствующие волокнистые структуры, служащие рельсами для моторных белков. Их:
- микрофиламенты (состоящие из актинового полимера) и
- микротрубочек (состоит из полимера тубулина.
Актин
Мономерная единица актина называется G-актин (глобулярный актин), а полимер известен как F-актин (нитчатый актин). Нити фактина состоят из мельчайших нитей клеток, известных как микрофиламенты (рис. 2.101). Актин необходим для сокращения мышц, а также играет разнообразную роль в передаче сигналов и поддержании соединений между клетками. Вместе с другими белками актин имеет множество взаимодействий с клеточной мембраной. Β- и γ-формы актина являются компонентами цитоскелета и способствуют подвижности внутри клеток. α-актин важен в мышечных тканях, где он используется миозином в механическом процессе сокращения (см. ЗДЕСЬ).
α-актин важен в мышечных тканях, где он используется миозином в механическом процессе сокращения (см. ЗДЕСЬ).
Рисунок 2.101 — Модель актиновых филаментов. Изображение используется с разрешения (CC BY-SA 3.0; Thomas Splettstoesser).
Мономерные и полимерные формы актина играют роль в клеточной активности, связанной с движением. Две параллельные нити F-актина могут спариваться друг с другом и создавать двойную спиральную структуру с 2,17 субъединицей на виток спирали. Спиральный F-актин в мышцах содержит тропомиозин, который покрывает участки связывания актина для миозина в мышцах покоя, чтобы предотвратить сокращение.Другие белки, связанные с актиновыми мышечными филаментами, включают тропонины (I, T и C).
Актин клеточного действия
Примеры действия актина на клеточном уровне включают подвижность клеток, цитокинез, внутриклеточный транспорт везикул и органелл, а также форму клеток. Каждый мономер актина связан с молекулой АТФ или АДФ, и присутствие одного из них необходимо для правильного функционирования G-актина.
Рисунок 2.102 — Присоединение актина к комплексу клеточной мембраны, известному как адгезивный переход, Wikipedia
Роль АТФ
В мономере актин чаще связан с АТФ, тогда как в филаментах он обычно связан с АДФ.Актин — неэффективная АТФаза, медленно разрушающая молекулу, но катализ ускоряется в 40 000 раз, когда мономер начинает полимеризоваться. Актин также имеет сайт связывания двухвалентных катионов — кальция или магния. F-
Актин связывается со структурными белками на стыке адгезивов (рис. 2.102). К ним относятся α-актинин, винкулин (обеспечивает мембранную связь и связи с катенинами и кадгерином).
Полимеризация
Фигура 2.103 — Полимеризация мономеров G-актина в полимеры фактина
Полимеризация актина начинается с момента зародышеобразования (рис. 2.103). Один фактор, который, как известно, влияет на процесс, известен как комплекс Arp 2/3. Он делает это, имитируя димер актина, запуская автокаталитический процесс сборки актина. Комплекс Arp 2/3 играет роль как в инициации полимеризации новых актиновых филаментов, так и в образовании разветвлений в филаментах.
Комплекс Arp 2/3 играет роль как в инициации полимеризации новых актиновых филаментов, так и в образовании разветвлений в филаментах.
Два белка играют роль в модуляции роста полимера.Тимозин действует на концах актиновых нитей, контролируя рост. Профилин работает с мономерами G-актина, обменивая АДФ на АТФ, способствуя присоединению мономеров к растущей цепи.
филаментов F-актина удерживаются вместе относительно слабыми связями по сравнению с ковалентными связями мономеров нуклеиновых кислот, что позволяет при желании облегчить разборку. Аминокислотная последовательность актина оптимизирована, разница лишь в относительно небольшом количестве (20%) между водорослями и людьми. Мутации в гене актина приводят к мышечным заболеваниям и / или глухоте.
Тубулин
Рис. 2.104. Структура микротрубочек. Wikipedia
. Белки тубулина являются мономерными строительными блоками эукариотических микротрубочек (рис. 2.104 и 2.105). Бактериальные (TubZ) и архейные (FtsZ) эквиваленты известны. Белки α-тубулина и β-тубулина полимеризуются, образуя структуры микротрубочек в цитоплазме клеток. Микротрубочки являются основными компонентами цитоскелета эукариотических клеток, обеспечивая структурную поддержку, транспорт внутри клетки и функции, необходимые для разделения ДНК во время деления клетки.
Белки α-тубулина и β-тубулина полимеризуются, образуя структуры микротрубочек в цитоплазме клеток. Микротрубочки являются основными компонентами цитоскелета эукариотических клеток, обеспечивая структурную поддержку, транспорт внутри клетки и функции, необходимые для разделения ДНК во время деления клетки.
Димеризация белков α-тубулина и β-тубулина необходима для полимеризации и требует, чтобы субъединицы связывались с GTP. Микротрубочки растут только в одном направлении. β-тубулин находится на положительном конце канальца (конец роста = положительный конец), а α-тубулин обнажается на другом конце (конец без роста = отрицательный конец). В этой ориентации димеры α-тубулина / β-тубулина встраиваются в растущие микротрубочки. Если димер связан с GDP вместо GTP, он имеет тенденцию быть нестабильным и распадаться, тогда как те, которые связаны с GTP, стабильно собираются в микротрубочки.
Рисунок 2.105 — Анатомия микротрубочек Википедия
Микротрубочки
Микротрубочки вместе с микрофиламентами и промежуточными филаментами (см. ЗДЕСЬ) составляют цитоскелет клеток. Находясь в цитоплазме, они обнаруживаются в эукариотических клетках, а также в некоторых бактериях. Микротрубочки помогают придать клеткам структуру. Они составляют внутреннюю структуру жгутиков и ресничек и обеспечивают рельсовидные поверхности для транспортировки материалов внутри клеток.
ЗДЕСЬ) составляют цитоскелет клеток. Находясь в цитоплазме, они обнаруживаются в эукариотических клетках, а также в некоторых бактериях. Микротрубочки помогают придать клеткам структуру. Они составляют внутреннюю структуру жгутиков и ресничек и обеспечивают рельсовидные поверхности для транспортировки материалов внутри клеток.
Рисунок 2.106 — Кинезин и динеин «ходят» по микротрубочкам, но движутся в противоположных направлениях Изображение Алейи Ким
Полимеризация α-тубулина и β-тубулина с образованием микротрубочек происходит после события нуклеации.Отдельные единицы располагаются в центрах организации микротрубочек (MTOC), примером которых является центросома. Центросомы — это узловые точки соединения микротрубочек. Базальные тела ресничек и жгутиков также помогают организовывать микротрубочки.
Моторные белки
От транспорта материалов внутри клетки до процесса цитокинеза, когда одна клетка делится на две в митозе, клетке необходимо движение на молекулярном уровне. Секреторные везикулы и органеллы необходимо транспортировать.Хромосомы должны быть разделены в митозе и мейозе.
Белки динеин и кинезин (рис. 2.106) необходимы для внутриклеточного движения. Эти моторные белки способствуют перемещению материалов внутри клеток по «рельсам» микротрубочек. Эти моторные белки способны перемещаться вдоль части цитоскелета, преобразовывая химическую энергию в движение при гидролизе АТФ. Исключением является вращение жгутиков, при котором используется энергия градиента, создаваемого протонным насосом.
Кинезины и динеины
Как уже отмечалось, кинезины и динеины перемещаются в клетках по трекам микротрубочек (рис. 2.108 и ролик 2.4). Большинство кинезинов движется в направлении синтеза микротрубочек (движение + конца), которое, как правило, находится от центра клетки и в противоположном направлении движения динеинов, которые, как говорят, осуществляют ретроградный транспорт к центру клетки. Оба белка обеспечивают двигательные функции, необходимые для процессов митоза и мейоза.К ним относятся формирование веретена, разделение хромосом и перемещение органелл, таких как митохондрии, аппараты Гольджи и везикулы.
Рисунок 2.107 — Кинезин. «Ноги» наверху.
Кинезины состоят из двух тяжелых цепей и двух легких цепей. Головные моторные домены тяжелых цепей (в стопах) используют энергию гидролиза АТФ для выполнения механической работы по движению вдоль микротрубочек. Существует по крайней мере четырнадцать различных семейств кинезинов и, возможно, еще много родственных.
На рис. 2.105 показаны стержень и шаровидная головка структуры. Wikipedia
Динеины разделены на две группы — цитоплазматические и аксонемные (также называемые цилиарными или жгутиковыми динеинами — рис. 2.109). Динеины имеют более сложную структуру, чем кинезины с большим количеством мелких полипептидных единиц. Примечательно, что у растений нет моторных белков динеина, но они содержат кинезины.
Movie 2.4 Моторный белок кинезин, идущий по микротрубочке. Изображение используется с разрешения (Public Domain; zp706).
Миозин
Важной группой моторных белков в клетке являются миозины. Как кинезины и динеины, миозины используют энергию гидролиза АТФ для движения. В этом случае движение происходит в основном не по микротрубочкам, а скорее по микрофиламентам, состоящим из полимера актина (F-актина). Движение миозина на актин наиболее известно как движущая сила сокращения мышц. Миозины — это огромное семейство белков, все из которых связываются с актином и все связаны с движением.Известно восемнадцать различных классов белков миозина.
Рисунок 2.109 — Динеин в аксонеме Wikipedia
Миозин II — это форма, ответственная за сокращение мышц. Это удлиненный белок, образованный двумя тяжелыми цепями с моторными головками и двумя легкими цепями. Каждая моторная головка миозина связывает актин и имеет сайт связывания АТФ. Головки миозина связывают и гидролизуют АТФ. Этот гидролиз производит энергию, необходимую миозину для движения к положительному концу актиновой нити.
Фигура 2.110 — Анатомия актиновых волокон Википедия
Немышечные миозины II обеспечивают сокращение, необходимое для обеспечения действия цитокинеза. Другие белки миозина участвуют в движении немышечных клеток. Миозин I участвует во внутриклеточной организации. Миозин V осуществляет транспорт везикул и органелл. Миозин XI обеспечивает движение по сетям клеточных микрофиламентов для облегчения движения органелл и цитоплазмы в определенном направлении.
Структура
Миозины имеют шесть субъединиц, две тяжелые цепи и четыре легкие цепи.Белки миозина имеют домены, часто описываемые как голова и хвост (рис. 2.111). Некоторые также описывают промежуточный шарнир как шею. Головная часть миозина — это часть, которая связывается с актином. Он использует энергию гидролиза АТФ для движения по актиновым филаментам. В мышцах белки миозина образуют агрегированные структуры, называемые толстыми филаментами. Движения имеют направленный характер.
Рисунок 2.111 — Анатомия миозинового белка Википедия
Структурные аспекты мышечного сокращения
Прежде чем мы обсудим этапы процесса мышечного сокращения, важно описать анатомические аспекты мышц и номенклатуру.
Существует три типа мышечной ткани — скелетная (поперечнополосатая), гладкая и (у позвоночных) сердечная. Здесь мы будем больше интересоваться тканью скелетных мышц. Мышцы могут активироваться центральной нервной системой или, в случае гладких и сердечных мышц, могут непроизвольно сокращаться. Скелетные мышцы могут сокращаться медленно или быстро.
Рисунок 2.112 — Структурные компоненты мышцы. Википедия
Саркомеры
Саркомеры описываются как основные единицы, состоящие из поперечно-полосатых мышц и состоящие из толстых (миозин) и тонких (актин) нитей и белка, называемого тайтином.Нити скользят друг мимо друга при мышечном сокращении, а затем назад при мышечном расслаблении. Их нет в гладких мышцах.
Под микроскопом саркомер — это область между двумя Z-линиями поперечно-полосатой мышечной ткани (рис. 2.112). Z-линия — это отчетливая узкая темная область в середине I-полосы. Внутри саркомера находится весь Абанд с его центральной H-зоной. Внутри Hzone расположены хвосты миозиновых волокон, голова которых направлена наружу оттуда, полностью выступая в I-полосу.Внешняя сторона Aband самая темная, и она становится светлее по направлению к центру.
Внутри Iband расположены тонкие филаменты, которые не заняты толстыми миозиновыми филаментами. Aband содержит неповрежденные толстые нити, перекрывающие тонкие нити, за исключением центральной зоны H, которая содержит только толстые нити. В центре H-зоны проходит линия, известная как M-линия. Он содержит соединительные элементы клеточного цитоскелета. При мышечном сокращении миозиновые головки ходят, натягивая свои хвосты на тонкие нити актина, используя энергию гидролиза АТФ и притягивая их к центру саркомера.
Рисунок 2.113 — Продольный разрез скелетной мышцы. Википедия
Сарколемма
Сарколемма (также известная как миолемма) для мышечных клеток то же самое, что плазматическая мембрана для других эукариотических клеток — барьер между внутренним и внешним миром. Он содержит липидный бислой и гликокаликс снаружи. Глиокаликс содержит полисахариды и соединяется с базальной мембраной. Базальная мембрана служит каркасом для соединения мышечных волокон. Эта связь осуществляется трансмембранными белками, соединяющими актиновый цитоскелет внутри клетки с базальной мембраной снаружи.На концах мышечных волокон каждая сарколемма сливается с сухожильным волокном, а они, в свою очередь, прикрепляются к костям.
Саркоплазматическая сеть
Саркоплазматический ретикулум (рис. 2.114) — это название структуры внутри мышечных клеток, которая похожа на гладкую эндоплазматическую сеть, обнаруженную в других клетках. Он содержит специальный набор белков для удовлетворения потребностей, уникальных для мышечных клеток. Органелла в значительной степени служит кальциевой «батареей», высвобождая накопленный кальций для инициирования мышечного сокращения при стимуляции и поглощая кальций при получении сигнала в конце цикла сокращения.Он выполняет эти задачи, используя ионные каналы кальция для высвобождения иона и специальные насосы для ионов кальция, которые его принимают.
Направление движения
Все миозины, кроме миозина VI, движутся к +-концу (растущему концу) микрофиламента. Часть шеи служит для соединения головы и хвоста. Это также сайт связывания белков легкой цепи миозина, которые образуют часть макромолекулярного комплекса с регуляторными функциями. Хвост — это точка прикрепления молекул или другого перемещаемого «груза».Он также может соединяться с другими субъединицами миозина и может играть роль в управлении движением.
Рисунок 2.114 — Анатомия мышечного волокна Википедия
Мышечное сокращение
Модель скользящей нити была предложена для описания процесса мышечного напряжения / сокращения. В этом процессе повторяющийся набор действий скользит тонкой актиновой нитью по толстой миозиновой нити как средство создания напряжения / укорочения мышечного волокна.
Этапы процесса следующие:
А.Сигнал от центральной нервной системы (потенциал действия) поступает в двигательный нейрон, который он передает к нервно-мышечному соединению (подробнее о нейротрансмиссионной части процесса ЗДЕСЬ)
Рисунок 2.115 — 1. Активация мышечной клетки высвобождением кальция (шаг H) Wikipedia
B. На конце аксона нервный сигнал стимулирует открытие кальциевых каналов на конце аксона, заставляя кальций поступать в терминал.
C. Движение кальция в аксон нерва заставляет ацетилхолин (нейромедиатор) в синаптических пузырьках сливаться с плазматической мембраной.Это вызывает выброс ацетилхолина в синаптическую щель между аксоном и соседним волокном скелетных мышц.
Рис. 2.116 — 2. Связывание кальция тропонином позволяет миозину получать доступ к сайтам актина (I). Wikipedia
D. Ацетилхолин диффундирует через синапс, а затем связывается с никотиновыми рецепторами ацетилхолина в нервно-мышечном соединении, активируя их.
E. Активация рецептора стимулирует открытие ворот натриевых и калиевых каналов, позволяя натрию перемещаться в клетку, а калию — выходить.Полярность мембраны мышечной клетки (называемая сарколеммой — рис. 2.111) быстро меняется (это называется потенциалом концевой пластинки).
Рисунок 2.117 — 3. Расщепление АТФ миозином позволяет присоединиться к актину (J) Wikipedia
F. Изменение потенциала концевой пластинки приводит к открытию чувствительных к напряжению ионных каналов, специфичных только для натрия или калия, как показано на рисунке 2.117 — 3. Расщепление АТФ миозином позволяет приложение актина (J) Wikipediaopen, создавая потенциал действия (изменение напряжения), который распространяется по клетке во всех направлениях.
G. Распространяющийся потенциал действия деполяризует внутреннее мышечное волокно и открывает кальциевые каналы в саркоплазматической сети (рис. 2.115).
H. Кальций, высвобождаемый из саркоплазматической сети, связывается с тропонином на актиновых филаментах (рис. 2.115).
I. Тропонин изменяет структуру тропомиозина, с которым он связан. Это заставляет тропомиозин немного перемещаться, обеспечивая доступ к участкам связывания миозина на микрофиламенте (также называемом тонкой нитью), который он покрывает (Рисунок 2.116).
J. Миозин (связанный с АТФ) расщепляет АТФ до АДФ и Pi, которые он удерживает в своей области головы, а затем прикрепляется к открытым участкам связывания на тонких нитях, вызывая высвобождение неорганического фосфата из миозина, а затем АДФ (Рисунок 2.117).
Рис. 2.118 — 4. Высвобождение Pi вызывает изгиб миозинового шарнира. Тонкая нить потянута влево (K). Wikipedia
K. Высвобождение ADP и Pi тесно связано с изгибом миозинового шарнира, что приводит к так называемому силовому удару.Это заставляет тонкую нить двигаться относительно толстых волокон миозина (рис. 2.118 и 2.119).
Рисунок 2.119 — 5. Высвобождение ADP способствует дальнейшему изгибу шарнира и перемещению тонкой нити влево (K). Wikipedia
L. Такое движение тонких нитей приводит к тому, что линии Z сближаются. Это приводит к укорачиванию саркомера в целом (рис. 2.122) и сужению полосы I и зоны H (рис. 2.123). М. Если АТФ доступен, он связывается с миозином, позволяя ему уйти от актина (рисунки 2.120 и 2.121). Если АТФ недоступен, мышца останется заблокированной в этом состоянии. Это причина смертельного окоченения — сокращения без расслабления мышц
.
Рисунок 2.120 — Когда присутствует АТФ, он связывается с миозином (M). Википедия
N. После того, как миозин связал АТФ, он гидролизует его, производя АДФ и Pi, которые удерживаются головой. Гидролиз АТФ возвращает шарнирную область в исходное состояние, разгибая ее. Это несогнутое состояние также называется взведенным положением.
O. Если тропомиозин все еще разрешает доступ к сайтам связывания на актине, процесс повторяется до тех пор, пока доступен АТФ, а концентрация кальция остается достаточно высокой, чтобы позволить ему связываться с тропонином.
Рисунок 2.121 — Связывание АТФ способствует высвобождению миозина из актинового участка (N) Wikipedia
Расслабление мышечного напряжения происходит, когда потенциал действия в мышечной клетке рассеивается. Это происходит потому, что происходит все следующее: 1) прекращается нервный сигнал; 2) нейромедиатор разрушается ферментом ацетилхолинэстеразой; и 3) концентрация кальция снижается, потому что он поглощается саркоплазматической сетью.
Рисунок 2.122 — Анатомия саркомера Wikipedia
Следует отметить, что саркоплазматический ретикулум всегда поглощает кальций. Только когда его кальциевые ворота открываются под действием потенциала действия, он не может снизить концентрацию кальция в клетках. По мере снижения потенциала действия кальциевые ворота закрываются, и саркоплазматический ретикулум «догоняет», и концентрация кальция в клетках падает. В этот момент тропонин высвобождает кальций, тропомиозин снова покрывает участки связывания миозина на актине, миозин теряет связь с актином, и тонкие волокна возвращаются в исходное положение относительно толстых волокон миозина.
Рисунок 2.123 — Модель мышечного сокращения скользящей нитью Wikipedia
Tropomyosin
Рисунок 2.124 — Тропомиозин и тропонин в анатомии мышц Wikipedia
Тропомиозины — это белки, которые взаимодействуют с тонкими нитями актина, чтобы помочь регулировать их роль в движении, как в мышечных, так и в немышечных клетках (рис. 2.124). Тропомиозины взаимодействуют, образуя димеры с ног до головы и располагаясь вдоль α-спиральной бороздки актинового филамента. Изоформы тропомиозина, которые находятся в мышечных клетках, контролируют взаимодействия между миозином и актиновой нитью внутри саркомера и помогают регулировать сокращение мышцы.В других клетках немышечные тропомиозины помогают регулировать функции цитоскелета.
Взаимодействие тропомиозина с цитоскелетом значительно сложнее, чем то, что происходит в мышечных клетках. Мышечные клетки имеют пять изоформ тропомиозина, но в цитоскелете немышечных клеток насчитывается более 40 тропомиозинов.
Тропонин
Рисунок 2.125 — Тропониновый комплекс мышцы. Синий = тропонин C, пурпурный = тропонин T, зеленый = тропонин I
Тропонины, участвующие в сокращении мышц, на самом деле представляют собой комплекс из трех белков, известных как тропонин I, тропонин C и тропонин T (Рисунок 2.125). Они связываются друг с другом и с тропомиозином на актиновых филаментах, помогая регулировать процесс мышечного сокращения. Тропонин I предотвращает связывание головки миозина с актином и, таким образом, предотвращает наиболее важный этап сокращения.
Тропонин С — это единица, связывающаяся с ионами кальция. Тропонин Т отвечает за связывание всех трех белков с тропомиозином. Тропонины в кровотоке указывают на сердечные заболевания. Повышение уровня тропонинов в крови происходит после инфаркта миокарда и может оставаться высоким до двух недель.
Актинин
Актинин — это белок скелетных мышц, который прикрепляет нити актина к Z-линиям клеток скелетных мышц. В гладкомышечных клетках он также соединяет актин с плотными телами.
Титин
Титин (также известный как коннектин) является молекулярным эквивалентом пружины, которая придает эластичность поперечно-полосатым мышечным клеткам. Это третий по содержанию белок в мышечных клетках. Белок огромен, с 244 сложенными отдельными доменами белка, распределенными по 363 экзонам (наибольшее известное число), с наибольшим известным экзоном (длиной 17 106 пар оснований), и это самый большой известный белок (от 27 000 до 33 000 аминокислот, в зависимости от сплайсинга) ).
Неструктурированные последовательности
Сложенные белковые домены связаны неструктурированными последовательностями. Неструктурированные области белка допускают разворачивание при растяжении и повторное сворачивание при релаксации. Титин соединяет линии M и Z в саркомере (рис. 2.123). Напряжение, создаваемое тайтином, ограничивает диапазон движений саркомера, вызывая так называемую пассивную жесткость.
Скелетные и сердечные мышцы имеют небольшие вариации аминокислотной последовательности в своих титановых белках, и это, по-видимому, связано с различиями в механических характеристиках каждой мышцы.
Резервная энергия для мышечной энергии
Миоглобин был описан как молекулярное тесто для кислорода. Мышечные клетки лучше усваивают АТФ. Это важно для животных, но не для растений, потому что потребность растений в энергии отличается от потребности животных. Растениям не нужно так быстро получать доступ к источникам энергии, как животным, и им не нужно поддерживать постоянную внутреннюю температуру. Растения не могут ни убежать от хищников, ни преследовать добычу. Эти потребности животных гораздо более насущны и требуют, чтобы запасы энергии были доступны по запросу.Мышцы, конечно, обеспечивают движение животных, а энергия, необходимая для сокращения мышц, — это АТФ. Чтобы запасы энергии были легко доступны, в мышцах, помимо АТФ, есть креатинфосфат для энергии и гликоген для быстрого высвобождения глюкозы для выработки большего количества энергии. Синтез креатинфосфата является ярким примером влияния концентрации на синтез высокоэнергетических молекул. Например, креатинфосфат имеет энергию гидролиза -43,1 кДж / моль, тогда как АТФ имеет энергию гидролиза -30.5 кДж / моль. Однако креатинфосфат образуется из креатина и АТФ в реакции, показанной на рис. 2.126. Как это возможно?
Рисунок 2.126 — Фосфорилирование креатина (фосфокреатина) — изготовление креатинфосфатной батареи Изображение Алейи Ким
∆G ° ’этой реакции составляет +12,6 кДж / моль, что соответствует энергии, указанной выше. В покоящейся мышечной клетке АТФ в изобилии, а АДФ низкий, что приводит к снижению реакции и образованию креатинфосфата. Когда начинается сокращение мышц, уровень АТФ падает, а уровень АДФ повышается.Вышеупомянутая реакция затем меняет направление и немедленно переходит к синтезу АТФ. Таким образом, креатинфосфат действует как батарея, накапливая энергию при высоком уровне АТФ и почти мгновенно высвобождая ее для создания АТФ, когда его уровень падает.
белков | Определение, структура и классификация
Белок , очень сложное вещество, которое присутствует во всех живых организмах. Белки имеют большую питательную ценность и непосредственно участвуют в химических процессах, необходимых для жизни.Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел в обращение термин белок , слово, производное от греческого prōteios , что означает «удерживать первое место». Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Популярные вопросы
Что такое белок?
Белок — это встречающееся в природе чрезвычайно сложное вещество, состоящее из аминокислотных остатков, соединенных пептидными связями.Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Где происходит синтез белка?
Где хранится белок?
Белки не хранятся для дальнейшего использования в животных. Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов. Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Что делают белки?
Белки необходимы для жизни и необходимы для широкого спектра клеточной деятельности. Белковые ферменты катализируют подавляющее большинство химических реакций, происходящих в клетке. Белки обеспечивают многие структурные элементы клетки и помогают связывать клетки вместе в ткани. Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Белковая молекула очень велика по сравнению с молекулами сахара или соли и состоит из множества аминокислот, соединенных вместе, образуя длинные цепи, подобно тому, как бусинки расположены на нити. Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
пептид
Молекулярная структура пептида (небольшого белка) состоит из последовательности аминокислот.
© raimund14 / Fotolia
Растения могут синтезировать все аминокислоты; животные не могут, хотя все они необходимы для жизни. Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. В процессе фотосинтеза они используют углекислый газ, содержащийся в воздухе, для образования органических соединений, таких как углеводы.Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, очень большое количество растительного материала требуется животным, таким как жвачные животные (например, коровы), которые едят только растительный материал для удовлетворения своих потребностей в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
бобовые; amino acid
Бобовые, такие как фасоль, чечевица и горох, богаты белком и содержат много незаменимых аминокислот.
© Elenathewise / Fotolia
Содержание белка в органах животных обычно намного выше, чем в плазме крови. Например, в мышцах содержится около 30 процентов белка, в печени — от 20 до 30 процентов, а в красных кровяных тельцах — 30 процентов. Более высокий процент белка содержится в волосах, костях и других органах и тканях с низким содержанием воды.Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы продуцируются в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишитесь сейчас
Высокое содержание белка в некоторых органах не означает, что важность белков связана с их количеством в организме или ткани; напротив, некоторые из наиболее важных белков, таких как ферменты и гормоны, присутствуют в очень малых количествах.Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни, — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их. Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела.Большая группа структурных белков поддерживает и защищает структуру тела животного.
гемоглобин
Гемоглобин — это белок, состоящий из четырех полипептидных цепей (α 1 , α 2 , β 1 и β 2 ). Каждая цепь присоединена к группе гема, состоящей из порфирина (органическое кольцеобразное соединение), присоединенного к атому железа. Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.
Британская энциклопедия, Inc.
Роль белка для спортсмена на выносливость / Блог «Наука в спорте»
Функции белков
Когда мы слышим слово «белок», мы часто просто думаем о пищевых продуктах, содержащих белок. На самом деле, однако, белки намного интереснее этого! Скорее, мы должны рассматривать белки как «маленькие машины с большими структурами», каждая из которых выполняет уникальные повседневные функции.
Действительно, наши мышцы содержат сотни белков, каждый из которых выполняет множество функций, которые необходимы для повседневной жизни и, конечно же, для выполнения упражнений.Например, «сократительные» белки отвечают за выработку силы в наших мышцах, «структурные» белки обеспечивают структуру наших мышц, а «ферментативные» белки помогают обеспечивать молекулы действия, которые могут расщеплять углеводы и жир для производства энергии.
Эта энергия затем используется структурными белками для движения. Таким образом, все наши мышечные белки работают вместе, чтобы выполнить поставленную задачу, то есть двигаться как можно быстрее!
Белок и тренировочная адаптация
Белок часто считается незаменимым для спортсменов, занимающихся силовыми тренировками, чтобы способствовать росту мышц.В этой ситуации сочетание подъема тяжестей и кормления белками используется для создания новых белков (особенно сократительных белков), и, следовательно, наши мышцы становятся больше.
Однако для спортсмена на выносливость потребление белка не менее важно. В этой ситуации стресс от упражнений на выносливость создает метаболический сигнал, который инструктирует наши мышцы производить новые белки, участвующие в аэробном метаболизме, например. митохондриальные ферменты. Упражнения также заставляют многие из наших мышечных белков фактически разрушаться (это называется деградацией белка), процесс, который, конечно, может быть вредным для адаптации к тренировкам.
К счастью, в присутствии адекватного кормления протеином комбинированные эффекты упражнений и приема протеина приводят к образованию новых протеинов (называемых синтезом протеина), так что мы можем лучше выдерживать физические нагрузки, связанные со следующей тренировкой. . Именно эти повторяющиеся изменения в синтезе белка в ответ на каждую тренировку формируют основу того, как наши мышцы адаптируются и восстанавливаются к требованиям тренировки. Поэтому для того, чтобы произошла такая оптимальная тренировочная адаптация, важно, чтобы белок поступал в непосредственной близости от физической нагрузки, учитывая, что богатые белком продукты и добавки содержат ключевые аминокислоты, которые используются в качестве строительных блоков для производства новых белков в нашем организме. мышцы.
В контексте спортсменов, занимающихся выносливостью, эти аминокислоты используются для выработки многих сотен ферментов, необходимых для обеспечения энергии от расщепления углеводов и жиров. В результате наши мышцы теперь содержат больше митохондрий (фабрик, на которых мы производим энергию во время упражнений на выносливость), и наша производительность при выполнении упражнений значительно улучшилась!
Потребность в белке для спортсмена на выносливость
Научный консенсус относительно оптимальных суточных потребностей в белке для выносливых спортсменов еще не достигнут, хотя большинство ученых согласятся, что это где-то в районе 1.4-1,8 грамма на килограмм массы тела спортсмена. Таким образом, атлету 75 кг потребуется от 105 до 135 граммов в день, а во время тренировок, предназначенных для уменьшения жировых отложений, но для сохранения мышечной массы, может потребоваться больше. В последнем случае спортсменам часто советуют увеличить суточное потребление белка до 2–2,5 г / кг, количества, которое, как было показано, поддерживает мышечную массу в течение целевого времени набора веса и потери жира.
Возможно, более важным, чем общее суточное потребление белка, является характер потребления белка в течение дня, когда рекомендуется потреблять белок в виде болюсов по 20-30 граммов каждые 3-4 часа.В контексте упражнений также рекомендуется употреблять белок в течение 60 минут до тренировки и сразу после тренировки (снова при приеме пищи по 20-30 граммов), хотя новые данные свидетельствуют о том, что спортсменам, работающим на выносливость, также следует потреблять белок во время упражнений. чтобы предотвратить деградацию белка (и, следовательно, способствовать лучшей адаптации к тренировкам), которая происходит во время продолжительных упражнений средней или высокой интенсивности.
Наконец, важное время для потребления белка — это перед сном, когда в этом случае аминокислоты могут быть доставлены в ваши мышцы, чтобы поддерживать синтез белка в течение ночи.
Источники белка для спортсменов на выносливость
В дополнение к высококачественной белковой пище (например, рыба / птица / молочные продукты / красное мясо / яйца / греческий йогурт и т. Д.), Белковые добавки являются чрезвычайно полезным дополнением к инструментарию спортсмена на выносливость. Действительно, белковые добавки содержат большое количество незаменимой аминокислоты лейцина (ключевой триггер для активации процесса синтеза белка) и часто перевариваются быстрее, чем цельные продукты, что обеспечивает эффективную стратегию восстановления.
Линия протеина Science in Sport может быть использована для удовлетворения ваших ежедневных потребностей в протеине, доказав варианты протеина, которые можно употреблять в качестве закуски (протеиновый батончик), до, во время и после тренировки (Advanced Isolate / Whey / REGO), а также перед сном. (Ночной протеин).
Написано
Наука в спорте
Белок может играть роль в реакции «бей или беги»
Сонг говорит, что продвижение знаний о быстром связывании миозина протеина С может когда-нибудь помочь в лечении скелетно-мышечных заболеваний.
«Люди теряют способность генерировать мышечную силу по разным причинам», — говорит Сонг.«Они могут быть крайне малоподвижными или находиться в больнице в течение длительных периодов времени. Причиной некоторых может быть старение. Мы также думаем, что если мы сможем манипулировать работой быстрого миозинсвязывающего протеина С в скелетных мышцах, мы сможем предотвратить или, по крайней мере, замедлить потерю мышечной функции при генетическом заболевании мышц, таком как дистальный артрогрипоз. Наше исследование пытается решить эту проблему в отношении здоровья человека ».
Среди других соавторов исследования из Калифорнийского университета Лиза Мартин, старший научный сотрудник отдела сердечно-сосудистых заболеваний и болезней; Джудит Хейни, доктор философии, профессор фармакологии и системной физиологии; и Джон Лоренц, доктор философии, профессор фармакологии и системной физиологии.
Дополнительные соавторы: Джеймс Макнамара, доктор философии, Детский научно-исследовательский институт Мердока; Вэйкан Ма, доктор философии, Технологический институт Иллинойса; Майкон Ландим Виейра из Университета штата Флорида; Кёнхван Ли, доктор философии, Медицинская школа Массачусетского университета; Роджер Крейг, доктор философии, Медицинская школа Массачусетского университета; Хосе Ренато Пинто, доктор философии, Государственный университет Флориды; и Томас Ирвинг, доктор философии, Технологический институт Иллинойса.
Садаяппан получил поддержку различных грантов Национальных институтов здравоохранения, включая Национальный институт артрита, скелетно-мышечных и кожных заболеваний, а также Американскую кардиологическую ассоциацию.Сонг и Макнамара были поддержаны стипендией Американской кардиологической ассоциации, а Крейг получил грант от Национального института здоровья. В исследовании использовались ресурсы Advanced Photon Source, пользовательского объекта Управления науки Министерства энергетики США.
Садаяппан предоставил консультации и совместные исследования фонда Leducq Foundation, Red Saree Inc., Greater Cincinnati Tamil Sangam, AstraZeneca, MyoKardia, Merck и Amgen.Эта работа не имела отношения к содержанию опубликованного исследования.
Показанное изображение вверху: Тэджон Сон, доктор философии / Коллин Келли / UC Creative + Brand.
.