из растительных или животных продуктов?
О пользе растительного рациона не говорит только ленивый. Как результат, все чаще растительный белок занимает своё почётное место на столе рядом со своими мясными конкурентами. Может возникнуть закономерный вопрос: какой белок всё-таки полезнее – из мяса или из растений?
Как часто случается с наукой о питании, ответ намного сложнее и, к счастью, намного интереснее, чем мы можем предположить. Что же нам следует знать о растительном и мясном белках?
Что такое белок?
Давайте для начала рассмотрим, что собой представляет белок на базовом уровне. Белок — это важнейший макроэлемент клеток человеческого организма. Макроэлемент — это одно из трех питательных веществ (наравне с углеводами и жирами), которые нужны организму в больших количествах. Как объясняет Управление по контролю за качеством пищевых продуктов и медикаментов (FDA), белок играет решающую роль в росте и развитии организма, создавая и восстанавливая различные клетки и ткани (мышцы, кости, органы, кожу и др. ). Он также необходим для выполнения таких важных функций в организме, как свертывание крови, выработка гормонов, нормальная работа иммунной системы. Так что да, белок – штука серьезная.
). Он также необходим для выполнения таких важных функций в организме, как свертывание крови, выработка гормонов, нормальная работа иммунной системы. Так что да, белок – штука серьезная.
Весь белок, который мы получаем из пищи, на молекулярном уровне состоит из крошечных органических соединений – аминокислот. Всего их насчитывается 20 видов. Когда белок попадает в организм, он разбивается на отдельные аминокислотные “строительные блоки”, которые затем перестраиваются в нужный “конструктор” и отправляются на выполнение различных функций в организме. Так что хотя куриная грудка и миска с чечевицей на вид и вкус очень разные, они состоят из одних и тех же базовых блоков белка.
“Если говорить о процессах на химическом уровне, то к тому времени, когда одна из аминокислот попадает в желудок, впитывается и утилизируется, была она растительного или животного происхождения…не имеет никакого значения”, – говорит Кристофер Гарднер, доктор философии, профессор медицины в Стэнфордском центре профилактических исследований.
Тут такое дело: белки бывают полноценными и неполноценными
20 аминокислот можно разделить на две группы: незаменимые и заменимые. Незаменимые аминокислоты (их 9) организм не способен синтезировать самостоятельно, вот почему так важно получать их с пищей. Заменимые аминокислоты организм способен выработать сам.
Гордый титул полноценного белок получает, если в нём присутствуют все 9 основных аминокислот. Когда аминокислот мало или какой-то из них не хватает, белок – как бы обидно ему от этого не было – начинают относить к неполноценным.
Полноценными считаются только белки животного происхождения – вот главная разница по сравнению с растительным белком. К источникам полноценного белка относится мясо животных (говядина, бекон и ветчина, куриные грудки, филе рыбы и др.) и продукты животного происхождения (яйца, молочные продукты). Из растений посчастливилось только двум категориям: производимым из сои (эдамаме, тофу, соевое молоко) и киноа – лишь они гордо носят звание полноценных белков.
Уитни Линсенмайер, доктор философии и диетологии, инструктор по питанию и диетологии в Колледже наук о здоровье Doisy при Университете Сент-Луиса и пресс-секретарь Академии питания и диетологии говорит: “Если рассуждать только о питательной ценности, то если вы будете употреблять животный белок, легче гарантировать, что вы получите все необходимые аминокислоты”.
Ну что, вы сделали выводы? Внимание, спойлер: подождите! Академия питания и диетологии в официальном документе о вегетарианской диете от 2016 года выражает сомнение, что определение “полноценный” и “неполноценный” имеет место быть, так как в самом названии заложен искаженный смысл.
“Прежде всего,- указывает Гарднер – в большинстве растительных белков не хватает всего одной или двух основных аминокислот”. Поскольку в растительных продуктах отсутствуют разные аминокислоты, они дополняют друг друга и вместе создают полноценный аминокислотный комплекс. Мило, не правда ли? Согласно Управлению по контролю за продуктами и лекарствами США, в зернах мало лизина, а в бобах и орехах мало метионина. Однако, классический тост из цельной пшеницы с арахисовой пастой и джемом содержит все 9 незаменимых аминокислот. Так что можно сказать, что тост снабжает организм всем необходимым “за один присест”.
Однако, классический тост из цельной пшеницы с арахисовой пастой и джемом содержит все 9 незаменимых аминокислот. Так что можно сказать, что тост снабжает организм всем необходимым “за один присест”.
Кстати, раньше считалось, что взаимодополняемые белки нужно употреблять в паре за один прием пищи, например, рис есть с фасолью. Однако последние исследования показали, что следует учитывать рацион за весь день. “Что важно, так это получать достаточно качественного белка, а не то, что с чем вы едите”- говорит Линсенмейер. “Вот почему люди, которые получают протеин из растений (т.е. веганы и вегетарианцы), как правило, могут получить все необходимые аминокислоты без труда – конечно, при условии разнообразного и сбалансированного питания” – добавляет Гарднер. Так что садиться на “фасолевую”, “соевую” или другую моно-диету – это плохая идея!
Сколько белка организм действительно способен получить и использовать
Животная пища как правило (но не всегда) содержит большее количество белка, чем растительная. Возьмем среднюю порцию разных источников белка. В 100 г куриной грудки содержится 20 граммов белка; в 100 г яиц (это чуть больше двух яиц) – 13,6 г; в 100 г (½ стакана) черной фасоли – 22 г; в 100 г (½ стакана) чечевицы – 9 граммов белка.
Возьмем среднюю порцию разных источников белка. В 100 г куриной грудки содержится 20 граммов белка; в 100 г яиц (это чуть больше двух яиц) – 13,6 г; в 100 г (½ стакана) черной фасоли – 22 г; в 100 г (½ стакана) чечевицы – 9 граммов белка.
Также важно учитывать, какое количество этого белка используется для роста и восстановления организма. “Похоже, по сравнению с животным белком, синтез белка в организме ниже, когда в него поступает растительный белок – говорит Линсенмейер – это означает, что для роста мышечной массы организм переваривает, всасывает и утилизирует меньшее количество аминокислот из растительной пищи, чем из животной”.
“Когда мы смотрим на качество белка с точки зрения его усвояемости, способности снабжать тело всеми необходимыми аминокислотами, а также того, насколько хорошо он участвует в восстановлении мышц, мы делаем вывод, что животный белок в целом справляется с этой задачей несколько лучше”, – объясняет Китчин. В животном белке также содержится одна аминокислота, которой нет в растительном – лейцин. Именно она считается крайне важной для роста мышц.
Именно она считается крайне важной для роста мышц.
Однако, ученые признают, что синтез белка из растительной пищи недостаточно изучен и делать однозначный выбор в пользу животного белка рано. Кроме этого, исследования проводятся в основном с использованием не готовых продуктов, а на белковых порошках, что дает противоречивые данные. Так, результаты одних исследований показывают, что на рост мышц лучше влияет употребление животного белка в порошке, другие исследования не обнаруживают разницы.
Вот еще кое-что: неясно, действительно ли скорость синтеза белка так важна. По данным Академии питания и диетологии, при нормальном количестве калорий вегетарианцы и веганы получают достаточно, а иногда и более чем достаточно белка. (Обращение к тем, кто все еще спрашивает: “ОТКУДА веганы получают свой белок?!”. Хм, возможно, вы получаете белка меньше, чем они). “И даже если чисто технически животный белок используется в организме лучше, чем растительный, для обычного человека, который регулярно тренируется, но не является ни профессиональным спортсменом, ни тренером, колоссального значения это не имеет”, – отмечает Китчин.
В 2017 году в Американском журнале клинического питания была опубликована статья, в которой анализируются данные о рационе питания и строении тела 2986 белых мужчин и женщин в возрасте от 19 до 72 лет, исследуемых на протяжении трех лет. Участники были разделены на 6 групп в зависимости от того, получают ли они белок из животных источников (рыба, курица, красное мясо и т.д.) или растений (бобовые, орехи и семена, фрукты и овощи, а также каши и злаки). Результат исследования показал, что для роста мышечной массы и квадрицепса в целом неважно, был это белок животного или растительного происхождения.
Что еще содержится в источниках растительного и животного белков
Что ещё, кроме протеина, дают нам продукты, содержащие белок?. У растительных и животных источников белков есть свои плюсы и минусы.
Продукты животного происхождения являются богатейшими природными источниками некоторых жизненно важных микроэлементов. Одним из них является витамин D – он содержится в яйцах, сыре и океанской рыбе, такой как лосось и тунец. Такие растительные продукты как злаки, апельсиновый сок и соевое молоко часто также обогащены витамином D. А если говорить о витамине В12, то, согласно данным Национальной Медицинской библиотеки США, его единственным натуральным источником являются животные белки (хотя B12 также содержится в обогащенных злаках и неактивных дрожжах).
Такие растительные продукты как злаки, апельсиновый сок и соевое молоко часто также обогащены витамином D. А если говорить о витамине В12, то, согласно данным Национальной Медицинской библиотеки США, его единственным натуральным источником являются животные белки (хотя B12 также содержится в обогащенных злаках и неактивных дрожжах).
По утверждению Гарднера, растительный белок обладает уникальными преимуществами, возможно, главное из которых — клетчатка, которую можно найти только в растениях. Бобы и цельные злаки наносят в этом плане двойной удар, ведь они содержат в себе убойную дозу клетчатки и белка. Растения также содержат различные биологически активные соединения, включая флавоноиды, каротиноиды и полифенолы. Их употребление рекомендуют в качестве профилактики рака и сердечно-сосудистых заболеваний.
Растительная пища также содержит углеводы — где-то их всего несколько грамм, например, в миндале (6 г в порции из 28 г), где-то много, как в консервированном нуте (19 г в стандартной порции ½ стакана). Что касается еды животного происхождения — углеводы содержатся только в виде лактозы или молочных сахаров в молочных продуктах.
Что касается еды животного происхождения — углеводы содержатся только в виде лактозы или молочных сахаров в молочных продуктах.
Если говорить о жирах, то почти все животные белки содержат насыщенные жиры, хотя их количество варьируется от продукта к продукту. Так, молочные продукты могут быть обезжирены, морепродукты содержат низкое количество жиров, а сочные куски красного мяса содержат огромное количество насыщенных жиров.
Делаем выводы
Какой бы рацион вы не выбрали, сам по себе тип питания — будь вы мясоед, веган или совмещаете разные продукты — ни о чём не говорит. Можно питаться хорошо или плохо независимо от этого. “Питаться правильно можно по-разному: совмещать животные и растительные продукты или придерживаться разнообразного растительного питания — говорит Китчин — Есть множество источников белка”. Растительное и животное питание не взаимоисключают друг друга, а следование только одному типу рациона не гарантирует вам жизнь в здоровом теле.
В реальной жизни важна не только пищевая ценность продуктов. В определенных местностях или для конкретных людей найти животные продукты проще (например, покупать те же дешевые консервы), чем сою, тофу или киноа. Не стоит также забывать о кулинарных традициях, связанных с определенной культурой. Например, в каких-то странах не принято есть мясо или определенное животное, где-то, наоборот, принято наделять мясо какого-то животного необычной силой.
В определенных местностях или для конкретных людей найти животные продукты проще (например, покупать те же дешевые консервы), чем сою, тофу или киноа. Не стоит также забывать о кулинарных традициях, связанных с определенной культурой. Например, в каких-то странах не принято есть мясо или определенное животное, где-то, наоборот, принято наделять мясо какого-то животного необычной силой.
Также необходимо учитывать предпочтения в еде или ограничения. Очевидно, что для тех, кто против негуманного отношения к животным в мясной индустрии или беспокоится об окружающей среде, единственный выбор — это вегетарианство или веганство. А если человек страдает аллергией на сою или целиакией, или же если ему не нравится вкус бобов или чечевицы, — таким людям проще получать необходимые организму вещества из животных продуктов.
Перевод с английского: Виктория Запольская
Оригинал с источниками: https://www.self.com/story/plant-vs-animal-protein
Растительные белки для вегетарианцев
09. 08.2017
08.2017
Растительный белок (или растительный протеин) – это альфа-аминокислотное соединение не животного происхождения. Этот вид белка добывается из растений (соя, рис, горох, овес, подсолнечник) и других не животных источников (к примеру, зеленая водоросль спирулина – популярный высокобелковый элемент рациона вегетарианцев).
Животный белок не имеет концептуальных преимуществ перед белком растительного происхождения, что доказано рядом исследований, например, работой доктора Дж. Гамильтона-Ривза «Сравнение молочного и соевого протеина в контексте синтеза мышечного белка у молодых и пожилых людей». В рамках исследования 36 здоровых мужчин различного возраста регулярно тренировались в одинаковых условиях, но были разбиты на группы по рациону – одни принимали соевый белок, другие – молочный. Результат не выявил концептуальной разницы в рамках выбранной статистической модели.
Популярен миф о том, что некоторые виды растительных белков (к примеру, соевый белок) из-за высокого содержания изофлавонов могут негативно сказываться на мужской гормональной системе. Это заблуждение, которое наглядно развеяно в исследовании доктора С. Филлипса «Клиническое изучение влияния соевого белка и изофлавонов на репродуктивные гормоны мужчин: результаты мета-анализа».
Это заблуждение, которое наглядно развеяно в исследовании доктора С. Филлипса «Клиническое изучение влияния соевого белка и изофлавонов на репродуктивные гормоны мужчин: результаты мета-анализа».
Конопляный протеин, изолят соевого белка, белок овса, рисовый белок – это натуральные растительные продукты, которые могут заменять традиционные животные протеины. Растительный протеин оптимален для диетического питания, но вопрос о том, какие растительные белки лучше для конкретной ситуации, решается в индивидуальном порядке, исходя из особенностей того или иного продукта.
Гороховый белок
Гороховый протеин изготавливается из натурального сырья – чистого посевного гороха. В нашей продуктовой линии это изолят горохового белка с содержанием протеина не менее 85%. В состав белка входят все заменимые и незаменимые аминокислоты, по содержанию BCAA соответствует казеиновому и сывороточному протеину.
Польза горохового протеина заключается в полноценном аминокислотном профиле (22 аминокислоты) и отсутствии антинутриентов, он содержит минимальное количество жиров и клетчатки, что обеспечивает уровень усвоения 98%. Этот растительный протеин популярен среди спортсменов, целью которых является увеличение сухой мышечной массы. Точный аминокислотный профиль предлагаемого продукта (гр на 100 гр) выглядит следующим образом:
Этот растительный протеин популярен среди спортсменов, целью которых является увеличение сухой мышечной массы. Точный аминокислотный профиль предлагаемого продукта (гр на 100 гр) выглядит следующим образом:
- аспаргиновая кислота 9,89;
-
треонин 2,55; -
серин 4,7; -
глутаминовая кислота 13,27; -
пролин 3,25; -
глицин 1,45; -
аланин 3,74; -
валин 3,71; -
цистин 1,18; -
метионин 0,2; -
изолейцин 1,32; -
лейцин 6,24; -
тирозин 2,14; -
фенилаланин 4,79; -
гистидин 2,80; -
триптофан 0,92; -
лизин 5,3; -
аргинин 8,3.
Соевый белок
Соевый изолят белка на 90% состоит из протеина. Изолированный соевый протеин способствует воспроизводству тироксина, гормона щитовидной железы, без которого невозможно функционирование организма человека.
Соевый белок содержит минимум жиров и углеводов, в его состав входит небольшое количество клетчатки, которая способствует сбалансированной работе кишечника и стимулирует выведение шлаков. Аминокислотный состав изолята соевого белка выглядит так (гр на 100 гр):
аспаргиновая кислота 13;
- треонин 4,3;
-
серин >0,1; -
пролин 5,7; -
глицин 4,7; -
аланин 4,9; -
валин 5,3; -
изолейцин 5,5; -
лейцин 9,1; -
тирозин 4,3; -
фенилаланин >0,1; -
лизин 7; -
гистидин 3,3; -
аргинин 8,5; -
цистин 1,4; -
метионин 1,4; -
триптофан 1,3.
Овсяной белок
Углеводную часть белка овса представляет мальтодекстрин, быстроусвояемый растительный углевод с высоким гликемическим индексом (105), не относится к сахарам. Входящая в состав белка клетчатка представлена бета-глюканом, это растворимые волокна, стимулирующие пищеварение и выведение шлаков.
Входящая в состав белка клетчатка представлена бета-глюканом, это растворимые волокна, стимулирующие пищеварение и выведение шлаков.
Овес, содержание белка в котором довольно высоко, включает в себя все незаменимые кислоты. Концентрат овсяного белка с содержанием протеина 55% изготовлен из экологически чистого шведского овса, не содержащего ГМО. Помимо клетчатки и мальтодекстрина в углеводной части белок овса отличается сбалансированным соотношением протеинов, жиров и углеводов, а также синергичным витаминно-минеральным составом (витамины А, Е, К, группа В, кальций, калий, магний, железо и фосфор). Его аминокислотный профиль выглядит так (мг на 1 гр белка):
- аспаргиновая кислота 62,155;
-
треонин 25,182; -
серин 31, 796; -
глютаминовая кислота 185,452; -
пролин 43,400; -
глицин 29,510; -
аланин 32,934; -
валин 45,840; -
изолейцин 34,424; -
лейцин 66,736; -
тирозин 33,657; -
фенилаланин 49,201; -
лизин 28,801; -
гистидин 19,152; -
аргинин 60,710; -
цистин 17,526; -
метионин 15,997; -
триптофан 10,809.
Подсолнечный белок
Подсолнечный протеин получают способом нехимической мембранной ультрафильтрации белковых молекул очищенного подсолнечного шрота, соответствующего ГОСТ 11246. У нас представлен концентрат подсолнечного белка отечественного производства с содержанием собственно белка не менее 82%. Не содержит лактозы, он очищен от антинутриентов.
Подсолнечный протеин (как принимать его – смотрите в описании соответствующего продукта) усваивается на 95%, так как в нем нет сырой клетчатки, а объем зол составляет не больше 6%. Обладает полноценным аминокислотным профилем (22 аминокислоты), включает в себя хлорогеновую кислоту (она тормозит высвобождение гликогена, в результате, организм активнее расходует подкожные жировые запасы). Аминокислотный состав подсолнечного белка (гр на 100 гр):
- треонин 2,95;
-
валин 4,58; -
метионин 1,71; -
изолейцин 3,76; -
лейцин 5,55; -
фениланин 4,67; -
лизин 6,53; -
триптофан 1,43; -
аспаргин 8,61; -
серин 3,63; -
глютамин 24,72; -
пролин 3,51; -
глицин 4,73; -
аланин 2,92; -
тирозин 2,29; -
аргинин 7,84.
Рисовый белок
Рисовый протеин отличается быстрым усвоением и не влияет на усвоение остальной пищи. Этот белок оптимален для безглютеновых диет. У нас можно купить концентрат рисового белка бельгийского производства с содержание протеина 80%.
Особенности рисового белка – богатый аминокислотный состав (то есть он снабжает организм полным комплексом заменимых и незаменимых аминокислот), отсутствие клетчатки и минимум антинутриентов (не более 3,5 гр на 100 гр продукта), поэтому он усваивается быстро и практически на 100%. Оптимален для прироста мышечных объемов, не может вызывать аллергические реакции. Аминокислотный состав на 100 гр выглядит следующим образом (мг на 1 гр белка):
- аланин 54;
-
аргинин 83; -
аспаргиновая кислота 91; -
цистин 18; -
глютаминовая кислота 179; -
глицин 43; -
гистидин 24; -
изолейцин 43; -
лейцин 85; -
лизин 36; -
метионин 37; -
фенилаланин 55; -
пролин 44; -
серин 49; -
треонин 37; -
триптофан 9; -
тирозин 54; -
валин 61.
Спирулина как источник белка
Зеленая водоросль спирулина, содержание белка в которой составляет 50-70%, имеет полноценный аминокислотный состав (то есть в ней есть все заменимые и незаменимые кислоты), а по объемам цистеина, метионина и лизина она превосходит любой белок растительного типа.
В 100% состава водоросли примерно 7% липидов, большую часть объема которых составляет гамма-линоленовая кислота, иммуномодулятор и антиоксидант, стимулирующий работу ЖКТ и функции восстановления. Прием спирулины полезен для иммунитета, сердечнососудистой системы, глаз и памяти, так как в ее состав входят витамины А, С, D, Е, группа B, тиамин, рибофлавин, микроэлементы и минералы – кальций, калий, железо, цинк, магний, фосфор.
Спирулина содержит липоевую и стеариновую кислоты, которые относятся к группе Омега-3. Она снижает холестерин, стабилизирует АД, способствует выведению токсинов, улучшает состояние кожи. В сочетании с обширным перечнем дополнительных функций белок спирулины является одним из лучших растительных протеинов. Спирулина популярна в сфере спорта, так как подавляет иммуносупрессию (снижение иммунитета), вызванную регулярными физическими нагрузками. Аминокислотный профиль (в % от общей массы белка):
В сочетании с обширным перечнем дополнительных функций белок спирулины является одним из лучших растительных протеинов. Спирулина популярна в сфере спорта, так как подавляет иммуносупрессию (снижение иммунитета), вызванную регулярными физическими нагрузками. Аминокислотный профиль (в % от общей массы белка):
- изолейцин 4,13;
-
лейцин 5,80; -
лизин 4,00; -
метионин 2,17; -
фенилаланин 3,95; -
треонин 4,17; -
триптофан 1,13; -
валин 6,00; -
аланин 5,82; -
аргинин 5,98; -
аспарагиновая кислота 6,43; -
цистин 0,67; -
глютаминовая кислота 8,94; -
глицин 3,46; -
гистидин 1,08; -
пролин 2,97; -
серин 4,00; -
тирозин 4,60.
Все представленные растительные белки оптимальны для веганов, вегетарианцев и людей, которые не могут употреблять животный белок по физиологическим, этическим или религиозным причинам. Они могут употребляться спортсменами и обычными людьми.
Схема приема вариативна, она зависит от вашей цели и особенностей вашего рациона. Предлагаемые виды растительного белка могут комбинироваться с другими белками (как растительными, так и животными) и спортивными добавками, исходя из принципов целесообразности.
Растительные протеины для вегетарианцев отлично заменяют белки животного типа, они питательны и безопасны. Тем не менее, перед тем, как добавить в свой рацион тот или иной белок, рекомендуется проконсультироваться со специалистом, так как возможны случаи индивидуальной непереносимости.
Животные белки
Животные белки в детском рационе
Важность белков как составляющей части детского питания переоценить невозможно. Подробно об их ведущей роли в меню ребенка мы уже говорили. Необходимо прояснить вопрос – почему родители обязательно должны включать в меню ребенка белки именно животного происхождения и какие из них – лучшие.
Подробно об их ведущей роли в меню ребенка мы уже говорили. Необходимо прояснить вопрос – почему родители обязательно должны включать в меню ребенка белки именно животного происхождения и какие из них – лучшие.
Продукты животного происхождения – это источник полноценных, легкоусвояемых белков, витаминов и минеральных веществ. Однако не все они подходят детям. Некоторые виды мяса и рыбы до поры до времени ребенку тяжело переварить, так как пищеварительные функции желудка, кишечника, печени и поджелудочной железы еще не достигли полной зрелости.
Яйца
Это один из значимых продуктов в детском меню, так как яйца содержат целый комплекс питательных веществ в легкой для усвоения форме (они усваиваются на 97-98%). Желток содержит комплекс жирорастворимых витаминов А, D, Е, фосфатиды, различные минеральные вещества и микроэлементы, а белок яйца имеет самую высокую пищевую ценность из всех белков животного происхождения. Можно сказать, что яйца – природный концентрат питательных веществ.
Как и любым другим концентратом, яйцами увлекаться нельзя. В детском рационе они должны быть ограничены: 1 яйцо через день для детей дошкольного и школьного возраста — вполне достаточно.
Мясо и рыба
Для детского питания подходят нежирные сорта мяса и рыбы.
Крольчатина — ценнейший диетический продукт, содержит мало соединительной ткани и сухожилий, легко переваривается. По сравнению с мясом других животных, в нем меньше холестерина, больше фосфолипидов и железа.
Индейка — низкокалорийное, но очень питательно мясо, содержит минеральные вещества, витамины (В2, В6, В12, РР), аминокислоты.
Курица — легкое и нежное, прекрасно усваивается организмом.
Телятина — нежное светлое мясо, считается диетическим.
Говядина — содержит много железа, поэтому полезна при железодефицитной анемии, но слишком старую говядину детям лучше не давать: она жирнее и хуже усваивается.
Баранина — содержит мало холестерина, но в бараньем жире – больше насыщенных жиров (по сравнению с другими).
Печень — содержит белки, а также является концентратом кроветворных микроэлементов – витаминов А, В2, В12, РР, холина, минеральных веществ. В печени много холестерина (в 3-4 раза больше, чем в мясе). Детям до двух лет лучше давать ее в виде паштета, старшим — тушить.
Рыба — различные сорта морских и речных рыб (судак, треска, хек, морской окунь). Белок рыб полноценный и легко усваивается, белки рыбы усваиваются на 93-98%, в то время как белки мяса – на 87-89%. Кроме того, рыба содержит необходимые организму омега-3 и омега-6 жирные кислоты.
Икра рыб – продукт с высокой питательной ценностью. Все ее виды богаты белком, жиром и жирорастворимыми витаминами А и D, Е. Не стоит кормить ребенка икрой слишком часто: она может вызвать аллергию.
Специалисты рекомендуют давать детям продукты, содержащие животный белок, каждый день. Не забывайте, что источником белка также являются молочные продукты – творог, сыры.
Растительные белки тоже важны, и должны составлять 40% от всех белков. Богаты белком бобовые, орехи, цельные злаки, об этих продуктах мы поговорим подробнее в статье, посвященной растительным белкам.
Богаты белком бобовые, орехи, цельные злаки, об этих продуктах мы поговорим подробнее в статье, посвященной растительным белкам.
Мясо и рыба не для детей
Колбаса и колбасные изделия — по большому счету, это не детские продукты, но обычно детьми очень любимые. Необходимо ограничивать колбасы и сосиски в детском рационе, так как они не имеют почти никакой питательной ценности, зато часто содержат чрезмерное количество жиров и соли. Детям до трех лет вообще не рекомендуется давать сосиски и колбасу, а в более старшем возрасте нужно ограничивать их потребление до 1-2 раз в неделю, выбирая при этом изделия с пометкой «для детского питания»: они содержат меньше жира, нитратов и соли и проверяются на наличие токсических элементов, антибиотиков и пестицидов.
Сырую рыбу давать маленьким детям нельзя, так как она тяжела для переваривания и может содержать паразитов. Дети 12-15 лет могут есть сырую рыбу, но в небольших количествах, проверенную и под строгим контролем родителей.
Сырые яйца не полезны детям. Белок сырых яиц гораздо хуже усваивается организмом, чем белок вареных, а кроме того, может содержать опасные для здоровья микроорганизмы, которые погибают при термической обработке.
Как готовить животные продукты для детей?
• выбирайте филейную часть мяса или рыбы;
• предпочитайте обжарке отваривание или запекание;
• перед приготовлением обрезайте с мяса видимый жир и снимайте кожу с птицы;
• рекомендуется охлаждать супы на мясном или рыбном бульоне, а затем удалять затвердевший на поверхности жир; • ограничивайте в рационе детей копченые продукты;
• варите яйца для детского питания не меньше 10 минут после закипания.
Может ли ребенок обойтись без животного белка?
Итак, организм ребенок нуждается в ежедневном поступлении белков, которые обеспечат его строительным материалом и энергией. Дефицит белка резко снижает устойчивость ребенка к инфекциям, страдают процессы кроветворения, нарушаются функции многих ферментов, принимающих участие в белковом обмене, и выработка гормонов. Доля животных белков в рационе детей дошкольного возраста должна составлять не менее 65% от общей потребности в белках, а у детей 7-14 лет – 60%, потому что животные продукты – источник самых полноценных белков, содержащих незаменимые аминокислоты.
Доля животных белков в рационе детей дошкольного возраста должна составлять не менее 65% от общей потребности в белках, а у детей 7-14 лет – 60%, потому что животные продукты – источник самых полноценных белков, содержащих незаменимые аминокислоты.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вот почему для ребенка может быть опасным увлечение родителей вегетарианством. Ему не навредят 1-2 вегетарианских дня в неделю, но полный отказ от мяса специалисты по питанию и педиатры не поддерживают.
Ему не навредят 1-2 вегетарианских дня в неделю, но полный отказ от мяса специалисты по питанию и педиатры не поддерживают.
Исследование белка S100 (S100 protein), правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Белок S100: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показания для назначения исследования
Белок S100 представляет собой вещество (белок), которое присутствует во многих органах (в коже, печени, почках, сердце и др. ). Его основная особенность заключается в способности связывать кальций и за счет этого влиять на многие процессы, происходящие в организме. Этот белок необходим для нормальной работы клеток органов и тканей, но самое большое содержание S100 выявлено в клетках головного мозга.
). Его основная особенность заключается в способности связывать кальций и за счет этого влиять на многие процессы, происходящие в организме. Этот белок необходим для нормальной работы клеток органов и тканей, но самое большое содержание S100 выявлено в клетках головного мозга.
Уровень белка S100 в крови позволяет оценить степень повреждения мозга при инсульте, черепно-мозговой травме и других состояниях, приводящих к неврологическим заболеваниям. Концентрация белка S100 повышается при онкологических заболеваниях. Огромное значение имеет исследование уровня белка S100 для оценки и контроля лечения рака кожи.
Подготовка к процедуре
- Предпочтительно выдержать 4 часа после последнего приема пищи.
- Рекомендуется сдавать кровь утром, в период с 8 до 11 часов, накануне избегать пищевых перегрузок.
- Исключить прием алкоголя накануне исследования.
- Не курить минимально в течение 1 часа до исследования.
- Исключить физические и эмоциональные перегрузки накануне исследования.
- При исследовании концентрации белка S100 в динамике рекомендуется проводить повторные исследования в одной и той же лаборатории.
Срок исполнения
1 рабочий день, исключая день взятия биоматериала.
Что может повлиять на результаты
Обычно результат оказывается корректным, если соблюдены все правила подготовки к исследованию. Важно помнить, что физиологическое повышение уровня белка S100 фиксируется после интенсивных занятий спортом.
Белок S100
Для исследования берется кровь из вены.
Референсные значения
В норме концентрация белка S100 в крови менее 0,105 мкг/л. Интерпретация результата проводится с целью комплексной оценки состояния при различных заболеваниях головного мозга, прогноза и контроля лечения при онкологии, а также при воспалительных процессах, например, при ревматоидном артрите.
Существуют несколько разных видов белка S100. Для указания вида белка S100 к названию прибавляют буквенно-цифровое обозначение, например, S100А1. Разные виды белка S100 характерны для различных органов. Определение конкретного вида белка S100 имеет значение в кардиологии, онкологии, при травмах и патологиях головного мозга.
Разные виды белка S100 характерны для различных органов. Определение конкретного вида белка S100 имеет значение в кардиологии, онкологии, при травмах и патологиях головного мозга.
В кардиологии повышенные концентрации таких видов как S100A1, S100A2 и S100A4 позволяют судить об остром повреждении клеток сердца (инфаркте миокарда) и инфекционном эндокардите (поражении сердца, особенно его клапанов, различными бактериями). Уровень S100 используют в дополнение к «классическим» биомаркерам: креатинкиназе (СК), креатинкиназе-МВ (СК-МВ) и тропонину-I.
Исследование группы белков S100 является ценным у пациентов с воспалительными заболеваниями и аллергией. При остром воспалении, как правило, повышаются уровни S100A8, S100A9 и / или S100A12. Эти белки считаются неспецифическими маркерами активации фагоцитов (клеток, уничтожающих бактерии и вирусы), поэтому определение значений S100A8 / A9 и S100A12 с другими маркерами того или иного заболевания повышает диагностическую точность. В таблице представлена связь белка S100 с некоторыми заболеваниями.
|
Показатель (белок S100) |
Болезни, при которых S100 играет роль дополнительного биомаркера воспаления и аллергии |
|
S100В |
Витилиго (нарушение пигментации кожи) |
|
S100А4 |
Связь между воспалением и прогрессированием опухоли Аллергия Сезонный аллергический ринит (аллергический насморк) |
|
S100А7 |
Псориаз (воспалительное заболевание кожи) |
|
S100А8 |
Ревматоидный артрит (хроническое воспаление суставов) Болезнь Крона (хроническое заболевание кишечника) Воспаление желудочно-кишечного тракта Воспалительные заболевания легких |
|
S100А12 |
Болезнь Кавасаки (повреждение мелких сосудов собственной иммунной системой) Воспаление сосудов и атеросклероз |
Представляемый Независимой лабораторией ИНВИТРО тест количественного определения S100 направлен на выявление таких видов белка как S100A1B и S100BB.
Компонентная диагностика аллергии на молоко
Количественное определение в крови специфических иммуноглобулинов класса E к казеину и цельному коровьему молоку, которое позволяет дифференцировать сенсибилизацию к термостабильной и термолабильной фракциям белков молока и решить вопрос о возможности употребления в пищу некоторых молочных и кисломолочных продуктов пациентами с аллергией на молоко.
Синонимы русские
Специфические иммуноглобулины класса Е к казеину и цельному коровьему молоку.
Синонимы английские
Component diagnostics of milk allergy, Cow’s Milk and Casein, IgE (ImmunoCAP).
Метод исследования
Иммунофлюоресценция на твердой фазе (ImmunoCAP).
Единицы измерения
kU/l (килоединица на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.

Общая информация об исследовании
Молоко – важный компонент детского питания. Молоко и молочные продукты являются ценным источником белка, калорий, витаминов и микроэлементов, особенно кальция. В то же время молоко — один из наиболее распространенных пищевых аллергенов. В развитых странах, по разным данным, частота сенсибилизации к нему составляет 0,5-7,5 %. Пищевая аллергия на молоко чаще наблюдается у детей первых лет жизни, преимущественно до 5-6-летнего возраста.
У людей, сенсибилизированных к коровьему молоку, аллергия может проявляться кожными симптомами в виде крапивницы, ангиоотеков и обострений атопического дерматита, поражением пищеварительного тракта (боль в животе, тошнота, рвота, диарея), ринитом, обострением бронхиальной астмы, анафилактическими реакциями. Аллергические реакции могут возникать и при употреблении продуктов, которые не считаются молочными, но содержат некоторые молочные белки или их следы, попавшие на производстве. Поэтому при аллергии очень важно внимательно читать состав продуктов перед употреблением в пищу. Гиперчувствительность к коровьему молоку не всегда исчезает в детстве и может сохраняться на многие годы во взрослом возрасте или на всю жизнь, что в некоторой степени зависит от вида белков, к которым возникла сенсибилизация.
Поэтому при аллергии очень важно внимательно читать состав продуктов перед употреблением в пищу. Гиперчувствительность к коровьему молоку не всегда исчезает в детстве и может сохраняться на многие годы во взрослом возрасте или на всю жизнь, что в некоторой степени зависит от вида белков, к которым возникла сенсибилизация.
В коровьем молоке содержится около 40 белков, которые могут выступать аллергенами. С учетом физико-химических свойств их разделяют на казеины (80 % белков молока) и сывороточные белки (20 %).
Казеин является термостабильным белком и сохраняет свои аллергенные свойства после термической обработки молока. Он в большом количестве содержится в сыре, твороге, а в пищевой промышленности применяется в качестве добавок в колбасные и кондитерские изделия, соусы, супы, рагу, напитки, мороженое, глазури. Данный белок нередко является скрытым аллергеном, а реакции на него обычно ассоциированы с более тяжелым течением аллергии и длительной персистенцией сенсибилизации к молоку и молочным продуктам в любом виде.
Сыворотка коровьего молока содержит преимущественно глобулярные белки, бета-лактоглобулин и альфа-лактальбумин и в меньшем количестве бычий сывороточный протеин, лактоферрин, иммуноглобулины. Сывороточные белки снижают или утрачивают аллергенность после термической обработки, например в процессе выпечки, при кипячении, а также в процессе брожения, ферментации. Поэтому пациенты, сенсибилизированные только к цельному молоку и нечувствительные к казеину, могут в большинстве случаев употреблять кисломолочные продукты (творог, кефир, ряженку, простоквашу, йогурт), топленое масло, а также содержащую молоко выпечку без развития аллергических реакций.
Белки коровьего молока на 80 % схожи по структуре с белками козьего и овечьего молока, что обуславливает их перекрестную аллергическую реактивность. Поэтому замена коровьего молока козьим возможна далеко не у всех пациентов с аллергией на коровье молоко, а только приблизительно у трети сенсибилизированных.
Однако полное исключение молочных продуктов без адекватной их замены другими видами молока или специальными смесями может отрицательно отразиться на росте и развитии детского организма. Подбор смесей для детей раннего возраста должен осуществляться под наблюдением врача с учетом индивидуального профиля сенсибилизации пациента. Среди возможных смесей рассматриваются частичные или полные гидролизаты молочного белка, смеси на козьем молоке, соевые или рисовые формулы, а в случаях тяжелой аллергии – аминокислотные смеси. Пациентам могут быть рекомендованы дополнительные лекарственные препараты и добавки с витаминами и минералами.
Подбор смесей для детей раннего возраста должен осуществляться под наблюдением врача с учетом индивидуального профиля сенсибилизации пациента. Среди возможных смесей рассматриваются частичные или полные гидролизаты молочного белка, смеси на козьем молоке, соевые или рисовые формулы, а в случаях тяжелой аллергии – аминокислотные смеси. Пациентам могут быть рекомендованы дополнительные лекарственные препараты и добавки с витаминами и минералами.
С возрастом многие дети становятся толерантны к аллергенам молока. Однако, если уровень специфических IgE-антител к молоку превышает 60 МЕ/мл (КЕ/л), то высока вероятность персистирующей аллергии – сохранение реакций до подросткового или взрослого возраста, а в некоторых случаях и на всю жизнь.
Основным лечебным мероприятием при аллергии на белки коровьего молока является полное исключение данного продукта из рациона, а при сенсибилизации только к сывороточным белкам – исключение цельного термически необработанного молока. В настоящее время ведется изучение возможности сублингвальной и пероральной иммунотерапии для лечения аллергии на белки коровьего молока.
Для чего используется исследование?
- Диагностика аллергии на белки коровьего молока;
- решение вопроса о возможности включения в питание термически обработанных молочных и кисломолочных продуктов;
- подбор гидролизированных или альтернативных смесей для питания детей раннего возраста.
Когда назначается исследование?
- При подозрении на сенсибилизацию к коровьему молоку;
- при выявлении реакции на молоко по результатам кожных тестов;
- при подборе смеси для детей раннего возраста;
- при обследовании детей с атопическим дерматитом, крапивницей, ангиоотеками, бронхиальной астмой, аллергическим ринитом/конъюнктивитом, желудочно-кишечными расстройствами, анафилактическим шоком и другими проявлениями аллергических заболеваний.
Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
|
IgE к цельному кровьему молоку +
|
IgE к казеину +
|
Сенсибилизация к казеину c или без сенсибилизации к сывороточным белкам (возможны реакции на любые виды молочных продуктов, следы молочного белка)
|
|
IgE к цельному кровьему молоку +
|
IgE к казеину —
|
Сенсибилизация только к белкам сыворотки (возможно употребление кисломолочных продуктов, а также выпечки, содержащей молоко)
|
|
IgE к цельному кровьему молоку —
|
IgE к казеину —
|
Отсутствие IgE-сенсибилизации к коровьему молоку
|
Скачать пример результата
Важные замечания
- Результаты анализа не должны применяться для составления диеты больного без рекомендаций врача.
Отсутствие антител к белкам коровьего молока не исключает другие возможные реакции желудочно-кишечного тракта на употребление молока, например при лактазной недостаточности, не-IgE-связанных механизмах гиперчувствительности при эозинофильном эзофагите.
- Выполнение данного исследования безопасно для пациента по сравнению с кожными тестами (in vivo), так как исключает контакт пациента с аллергеном. Прием антигистаминных препаратов и возрастные особенности не влияют на качество и точность исследования.
Также рекомендуется
[02-029] Клинический анализ крови с лейкоцитарной формулой и СОЭ
[08-017] Суммарные иммуноглобулины E (IgE) в сыворотке
[21-673] Аллергочип ImmunoCAP ISAC (112 аллергокомпонентов)
[40-443] Экзема
[21-713] Аллергокомпонент f77 — Бета-лактоглобулин nBos d 5, IgE (ImmunoCAP)
[21-712] Аллергокомпонент e204 — Бычий сывороточный альбумин nBos d6, IgE (ImmunoCAP)
[21-636] Аллерген f79 — глютен (клейковина), IgE (ImmunoCAP)
[21-622] Аллерген f245 – яйцо, IgE (ImmunoCAP)
[42-018] Лактозная непереносимость (взрослые и дети старше 3 лет)
+ определение специфических иммуноглобулинов класса E к прочим аллергенам
Кто назначает исследование?
Аллерголог, гастроэнтеролог, педиатр, дерматолог, терапевт, врач общей практики.
Литература
- Matricardi P.M. et al. EAACI Molecular Allergology User’s Guide. Pediatr Allergy Immunol. 2016 May;27 Suppl 23:1-250. doi: 10.1111/pai.12563.
- Monaci L, Tregoat V, van Hengel AJ, Elke Anklam. Milk allergens, their characteristics and their detection in food: A review. Eur Food Research Tech 2006;223(2):149-79
- Martorell-Aragonés A., Echeverría-Zudaire L. et al. Food allergy committee of SEICAP (Spanish Society of Pediatric Allergy, Asthma and Clinical Immunology). Position document: IgE-mediated cow’s milk allergy. Allergol Immunopathol (Madr). 2015 Sep-Oct;43(5):507-26
- Wal JM. Cow’s milk proteins/allergens. Ann Allergy Asthma lmmunol 2002;89(Suppl 1):3-10.
- Fiocchi A, Dahdah L, Albarini M, Martelli A. Cow’s Milk Allergy in Children and Adults. Chem Immunol Allergy 2015;101:114-123.
Виды растительного белка и их польза
Мы привыкли, что основным источником белка в рационе веганов служат бобы, орехи и зерновые. Их используют и в промышленных целях, но в производство они попадают не в своем изначальном виде, а в очищенном, как изолят растительного белка. Давайте разберемся, какие изоляты белка наиболее распространены, как их получают и в чем их преимущества.
Их используют и в промышленных целях, но в производство они попадают не в своем изначальном виде, а в очищенном, как изолят растительного белка. Давайте разберемся, какие изоляты белка наиболее распространены, как их получают и в чем их преимущества.
Изолят белка – это белковый продукт, очищенный от жира, углеводов и клетчатки, с содержанием белка 90-95%. Наиболее распространенные растительные изоляты – пшеничный, соевый, гороховый. Как правило, это порошки от кремового до светло-коричневого оттенка с характерным для исходного сырья запахом и вкусом.
Изолят горохового белка (вы его наверняка встречали в составе наших сыров) получают при переработке желтого гороха. Это распространенный ингредиент продуктов для веганов и вегетарианцев, спортивного питания, для людей с непереносимостью молочных белков. Кроме того, он обладает гелеобразующей и эмульгирующей способностью, благодаря чему его используют в выпечке, в частности безглютеновой.
В отличие от соевого белка, гороховый не содержит генетически модифицированных ингредиентов. При этом по аминокислотному составу он максимально к нему близок. Изолят горохового белка усваивается на 98%, он очищен от веществ, вызывающих газообразование, характерное для бобовых, и гипоаллергенен. Единственный его минус – специфический вкус и запах в чистом виде.
При этом по аминокислотному составу он максимально к нему близок. Изолят горохового белка усваивается на 98%, он очищен от веществ, вызывающих газообразование, характерное для бобовых, и гипоаллергенен. Единственный его минус – специфический вкус и запах в чистом виде.
Изолят соевого белка, который получают из бобов сои, очень близок по аминокислотному профилю к белкам животного происхождения, несмотря на немного пониженное содержание серосодеражащих аминокислот (цистеин, метионин). Уникальным компонентом соевых белков являются изофлавоны – это растительные антиоксиданты, которые защищают организм человека от сердечно-сосудистых заболеваний, злокачественных опухолей, климактерических состояний.
В пищевой промышленности изолят соевого белка используют в кондитерских изделиях, соевом молоке, тофу, диетическом и детском питании в качестве замены животного белка, эмульгатора, улучшителя консистенции, а также для имитации мясных продуктов.
Единственный серьезный минус соевого белка – это содержание ингибиторов протеиназ – веществ, снижающее усвояемость белка. Однако эта проблема легко устраняется дополнительной очисткой соевых бобов от оболочек. На сегодняшний день очень распространена генетически модифицированная соя импортного производства, которая в принципе лишена этого недостатка.
Однако эта проблема легко устраняется дополнительной очисткой соевых бобов от оболочек. На сегодняшний день очень распространена генетически модифицированная соя импортного производства, которая в принципе лишена этого недостатка.
Наименее известен изолят пшеничного белка. Это результат переработки зерна пшеницы в муку. Другое название – пшеничная клейковина. Благодаря клейковине из муки выпекается хлеб, она дает пористость тесту и изделиям из него.
Изолят пшеничного белка хорошо связывает воду, образует прочные гели. Он беден аминокислотами, по сравнению с другими изолятами, но благодаря связывающим свойствам его активно применяют при производстве веганской колбасы, паштетов, сейтана. Изолят пшеничного белка, как и гороховый, имеет специфический привкус.
Верблюды, белки и питоны: самые агрессивные животные-захватчики
Некоторые обитающие на планете живые существа зачастую появляются в районах, которые не являются естественной средой их обитания. Преднамеренно или случайно, но чаще всего их туда приводит человек.
Преднамеренно или случайно, но чаще всего их туда приводит человек.
Эти инвазивные виды могут отрицательно влиять на местную экосистему и создавать проблемы животным, которые считают это место своим домом.
От млекопитающих до моллюсков — мы выбрали семь наиболее агрессивных захватчиков чужих территорий.
1. Верблюды, переполошившие австралийскую глубинку
Автор фото, Getty Images
Подпись к фото,
Верблюды, завезенные европейцами, поселились в австралийской пустыне
Выживание в Австралии — непростая задача для растений, животных и даже людей.
Еды и пищи не хватает, поэтому если кто-то или что-то начнет забирать себе слишком много, это вызовет природную катастрофу.
К сожалению, именно этим занимаются верблюды.
Эти одногорбые травоядные были завезены сюда европейцами в середине 1800-х годов для использования в качестве рабочего скота.
Однако к 1930-м годам поезда и грузовики освободили верблюдов от работы. Зверей отпустили на волю, где жилось очень хорошо.
В настоящее время около 400-600 тысяч верблюдов бороздят австралийские просторы.
В числе прочего они присвоили себе источники воды, которые помогают выживать местным птицам и животным, таким как динго и валлаби.
Учитывая, что верблюды пьют в 2 тысячи раз больше, чем самые крупные австралийские млекопитающие — рыжие кенгуру, — можно представить, как быстро они осушают водоемы.
В Австралии возводят новые, искусственные источники воды в надежде, что верблюды оставят естественные водоемы. Кроме того, действуют программы по отстрелу верблюдов для последующей продажи мяса.
Однако верблюдов настолько много, что никуда исчезать они, похоже, не собираются.
2. Серые белки-разносчики болезней в лесах Британии
Автор фото, Getty Images
Подпись к фото,
Серые белки почти полностью вытеснили обыкновенных (рыжих) белок на большей части Британии
Серые белки из Северной Америки в свое время считались модным украшением элегантных британских усадеб.
Однако в итоге они стали господствующим в Британии видом, после того как их выпустили на волю в 1876 году.
Их ассимиляция оказала разрушительное воздействие на местных рыжих белок.
Их серые родственники не только оказались больше и сильнее (а значит, с более высокими шансами на выживание зимой и размножение), они еще и переносили вирус чумки, к которому у рыжих белок не было иммунитета.
Это привело к тому, что рыжие белки практически вымерли на Британских островах — в дикой природе осталось лишь 150 тысяч особей.
К счастью, рыжие белки до сих пор держат оборону в Шотландии, где есть крупные проекты по сохранению этого вида.
3. Тропические длиннохвостые попугаи, захватившие Лондон
Автор фото, Getty Images
Подпись к фото,
Длиннохвостые попугаи из Западной Африки и Индии теперь считают своим домом Лондон
Прогуляйтесь по любому лондонскому парку, и вы непременно встретите громко кричащих зеленых птиц.
Это ожереловые попугаи, которых в городе часто называют «модными голубями».
Но как эти тропические птицы из Западной Африки и Индии поселились в Британии?
По одной из легенд, они происходят от попугаев, улетевших из киностудии во время съемок фильма «Африканская королева».
Некоторые считают, что птицы улетели из вольера в парке Сайон, который был поврежден обломком, выпавшим из самолета.
Есть и третье объяснение — такое же красочное, как и сами птицы: якобы это Джими Хендрикс выпустил попугаев на лондонской улице Карнаби в 1970-е годы.
Хотя тропические птицы хорошо смотрятся в сером городе, они могут оказывать отрицательное воздействие на местных пернатых.
Недавние исследования показали, что шумные стаи попугаев отпугивают маленьких птиц, мешают им есть и строить гнезда.
4. Тигровые питоны в парке Эверглейдс во Флориде
Автор фото, Getty Images
Подпись к фото,
Бирманские тигровые питоны выстесняют коренных жителей заповедника
Бирманские питоны расползаются по национальному парку Эверглейдс во Флориде.
Считалось, что змеи — просто кучка сбежавших рептилий, однако их количество стало расти в геометрической прогрессии.
Это неудивительно, учитывая, что одна женская особь откладывает до 100 яиц.
Эти огромные змеи, обладающие большим аппетитом, готовы потеснить аллигаторов в борьбе за звание главного хищника этой местности.
В результате в некоторых районах заповедника число оленей, енотов, кроликов, рысей и опоссумов заметно сокращается.
К сожалению, эти вредители умело маскируются, и даже эксперты не в силах обнаружить змею в траве.
Это значит, что никто толком не знает, сколько питонов прячется в лесах Флориды.
5. Рыба-лев в Карибском бассейне
Автор фото, Getty Images
Подпись к фото,
Рыба-лев появилась на коралловых рифах на побережье Кубы
Красная рыба-лев обычно обитает в водах Тихого океана.
Но, начиная с 1990-х годов, эта очень красивая и крайне ядовитая рыба, у которой почти нет врагов, начала размножаться в западных районах Атлантики.
К настоящему времени она распространилась по всему Карибскому бассейну и в Мексиканском заливе.
Никто толком не знает, как эта рыба добралась до этих вод; возможно, она случайно вырвалась на свободу, когда ураган Эндрю разрушил аквариум в штате Флорида, а может быть, кто-то держал эту рыбу дома.
Как бы то ни было, стаи этих хищных рыб уничтожают экосистему Карибских островов.
За несколько недель эта рыба в состоянии съесть до 80% запасов мелкой рифовой рыбы на небольшом острове.
На некоторых рифах у побережья Флориды и Южной Каролины сейчас можно встретить до 4 тысяч особей на 4 тысячи квадратных метров площади, а охота на эту рыбу стала популярным спортом.
Проводятся настоящие родео, когда за день нужно насадить на пику и выбросить на берег максимальное число этих рыб с целью защиты хрупкой местной морской экосистемы.
6. Американская норка вытесняет британскую водяную крысу
Автор фото, Getty Images
Подпись к фото,
Американская норка практически вытеснила британских водяных крыс
В конце 1920-х годов в Британии стали культивировать американскую норку с целью получения ценного меха.
Но некоторым из этих животных удавалось удрать из клеток на фермах, и они стали размножаться на воле.
Норка является агрессивным и ловким хищником, в Британии у нее не было врагов, и она чрезвычайно размножилась.
К сожалению, это происходит за счет местных водяных крыс, которые практически исчезли на территориях, где они когда-то процветали.
7. Полосатая мидия покоряет Великие озера
Автор фото, Getty Images
Подпись к фото,
Полосатые мидии, обитающие в водах Черного моря, сейчас часто встречаются на пляжах озера Мичиган
Полосатые мидии обитают в Черном и Каспийском морях, но уже в течение многих лет они наблюдаются в водах Великих озер на границе США и Канады.
Они мигрировали в Северную Америку в балластной воде торговых судов. Эти мидии относятся к числу одного из самых агрессивных пресноводных видов на планете.
Они живут огромными колониями, интенсивно фильтруют воду и не оставляют после себя планктон и водоросли, необходимые для питания местных рыб и устриц.
Теперь многие суда осматриваются перед выходом из порта, а полосатые мидии, обычно обитающие на днищах и гребных винтах судов, уничтожаются.
Виды белков и белки-подработки: очень небольшие изменения ковалентной структуры белка могут изменить его биохимическую функцию.
Основные моменты
- •
-
Белки-подработки выполняют две или более физиологически значимых биохимических или биофизических функций.
- •
-
Посттрансляционные модификации могут переключать подрабатывающий белок между двумя функциями.
- •
-
Небольшие различия между видами белка могут привести к тому, что гомолог «подрабатывающего» белка будет выполнять только одну из функций.
- •
-
Разница в одной аминокислоте может вызвать усиление «неоморфной функции подработки».
Abstract
За последние несколько десятилетий были идентифицированы сотни подрабатывающих белков, которые выполняют две или более различных и физиологически значимых биохимических или биофизических функций, которые не связаны с слиянием генов, множественными вариантами сплайсинга РНК или плейотропными эффектами. В этом специальном выпуске о видах белков в этой статье обсуждаются три темы, связанные с белками-подработками, которые иллюстрируют, как небольшие изменения или различия в ковалентных структурах белков могут приводить к различным функциям.Приведены примеры подрабатывающих белков, которые переключаются между функциями после прохождения посттрансляционных модификаций (ПТМ), белков, которые имеют высокий уровень идентичности аминокислотной последовательности с подрабатывающим белком, но разделяют только одну из его функций, и несколько «неоморфных подрабатывающих белков» в мутация одной аминокислоты приводит к добавлению новой функции.
В этом специальном выпуске о видах белков в этой статье обсуждаются три темы, связанные с белками-подработками, которые иллюстрируют, как небольшие изменения или различия в ковалентных структурах белков могут приводить к различным функциям.Приведены примеры подрабатывающих белков, которые переключаются между функциями после прохождения посттрансляционных модификаций (ПТМ), белков, которые имеют высокий уровень идентичности аминокислотной последовательности с подрабатывающим белком, но разделяют только одну из его функций, и несколько «неоморфных подрабатывающих белков» в мутация одной аминокислоты приводит к добавлению новой функции.
Биологическое значение
В этом специальном выпуске, посвященном видам белков, в этой статье обсуждаются три темы, связанные с подрабатывающими белками: посттрансляционные модификации (ПТМ), которые могут вызывать переключение между функциями, гомологи, которые имеют только одну из множества функций, и белки. в котором мутация одной аминокислоты приводит к созданию новой функции. Приведенные примеры показывают, что даже в среднем белке, состоящем из сотен аминокислот, относительно небольшое различие в последовательности или PTM может привести к большому различию в функции, что может быть важным для прогнозирования функций белка, регуляции функций белка и эволюция новых функций.
Приведенные примеры показывают, что даже в среднем белке, состоящем из сотен аминокислот, относительно небольшое различие в последовательности или PTM может привести к большому различию в функции, что может быть важным для прогнозирования функций белка, регуляции функций белка и эволюция новых функций.
Ключевые слова
Белки лунного света
Многофункциональные
Гомологические белки
Виды белков
Неоморфный белок лунного света
Структура и функция белка
Функция фермента
Рекомендуемые статьи
Рекомендуемые статьи
© 2015 Else (Полный текст) Б.V. Все права защищены.
Рекомендуемые статьи
Цитирующие статьи
На пути к анализу видов белка: обзор стратегий и методов
Abstract
Расшифровка взаимосвязи между функцией и точным химическим составом определенных видов белка в контексте протеома является одной из основных задач протеомики и молекулярной физиологии клетки. В специальном выпуске Amino Acids об анализе видов белков рассматриваются современные подходы и описываются новые методы с упором на изучение видов белков.На основании статей в этом специальном выпуске можно резюмировать, что первые важные и многообещающие шаги к всестороннему анализу видов белков были сделаны. Уже возможно получить полное (100%) покрытие последовательности белков с помощью масс-спектрометрии, если количество белков, доступных для их анализа, позволяет их протеолитическую деградацию более чем одной протеазой и последующий масс-спектрометрический анализ полученных пептидов. Использование аффинной хроматографии помогает анализировать белки с определенными посттрансляционными модификациями, что открывает целенаправленный взгляд на e.грамм. фосфопротеом. В будущем цель определения точного химического состава, включая не одну, а каждую посттрансляционную модификацию и полное покрытие последовательности на уровне видов белка, должна быть достижима с дальнейшим прогрессом в методах подготовки образцов, особенно в отношении методов разделения на уровне белка, масс-спектрометрии и алгоритмы обработки масс-спектрометрических данных.
В специальном выпуске Amino Acids об анализе видов белков рассматриваются современные подходы и описываются новые методы с упором на изучение видов белков.На основании статей в этом специальном выпуске можно резюмировать, что первые важные и многообещающие шаги к всестороннему анализу видов белков были сделаны. Уже возможно получить полное (100%) покрытие последовательности белков с помощью масс-спектрометрии, если количество белков, доступных для их анализа, позволяет их протеолитическую деградацию более чем одной протеазой и последующий масс-спектрометрический анализ полученных пептидов. Использование аффинной хроматографии помогает анализировать белки с определенными посттрансляционными модификациями, что открывает целенаправленный взгляд на e.грамм. фосфопротеом. В будущем цель определения точного химического состава, включая не одну, а каждую посттрансляционную модификацию и полное покрытие последовательности на уровне видов белка, должна быть достижима с дальнейшим прогрессом в методах подготовки образцов, особенно в отношении методов разделения на уровне белка, масс-спектрометрии и алгоритмы обработки масс-спектрометрических данных. Для определения функции определенных видов белков желательно более тесное сотрудничество между клеточными биологами и экспертами в области протеомики.
Для определения функции определенных видов белков желательно более тесное сотрудничество между клеточными биологами и экспертами в области протеомики.
Термин «разновидности белка» был введен Jungblut et al. (1996) для описания наименьшей единицы в протеоме (Jungblut et al. 2008; Schlüter et al. 2009) и для избежания двусмысленности в отношении термина изоформы, который уже используется для описания генетических вариаций, таких как аллельные формы в соответствии с правилами IUPAC (Объединенная комиссия по биохимической номенклатуре IUPAC-IUBMB 1992). Почему термин «виды белков» так важен для раскрытия молекулярных механизмов в науках о жизни? Этот специальный выпуск предназначен для того, чтобы дать некоторые ответы, а также поднять новые вопросы для улучшения доступа к молекулам, которые определяют множество различных процессов в жизни: виды белков.
В то время как геном определяет структуру и функции организма, молекулярный фенотип в определенный момент жизненного цикла организма лучше описывается протеомом и метаболомом. В рамках расшифровки геномов сотен микроорганизмов, растений и животных за последние 20 лет были сделаны снимки протеомов многих биологических ситуаций. Большинство этих исследований было сосредоточено на обнаружении белков, которые показывают изменения в количестве между двумя или более биологическими ситуациями, такими как болезнь и контроль.Важность посттрансляционных модификаций стала очевидной задолго до того, как протеомика стала новой дисциплиной биохимического анализа. Между тем, с помощью классических биохимических подходов многочисленные результаты демонстрируют важность посттрансляционных модификаций для определения функции белка. Прекрасный пример приведен в обзоре Deribe et al. (2010), который фокусируется на влиянии полиубиквитинирования на передачу сигналов в клетках. В течение многих лет биохимики подчеркивали важность посттрансляционных модификаций, и детектирование сайтов модификации, таких как фосфорилирование, было улучшено, что привело к обнаружению 10000 сайтов фосфорилирования в фосфопротеоме клеток Drosophila Schneider (Hilger et al.
В рамках расшифровки геномов сотен микроорганизмов, растений и животных за последние 20 лет были сделаны снимки протеомов многих биологических ситуаций. Большинство этих исследований было сосредоточено на обнаружении белков, которые показывают изменения в количестве между двумя или более биологическими ситуациями, такими как болезнь и контроль.Важность посттрансляционных модификаций стала очевидной задолго до того, как протеомика стала новой дисциплиной биохимического анализа. Между тем, с помощью классических биохимических подходов многочисленные результаты демонстрируют важность посттрансляционных модификаций для определения функции белка. Прекрасный пример приведен в обзоре Deribe et al. (2010), который фокусируется на влиянии полиубиквитинирования на передачу сигналов в клетках. В течение многих лет биохимики подчеркивали важность посттрансляционных модификаций, и детектирование сайтов модификации, таких как фосфорилирование, было улучшено, что привело к обнаружению 10000 сайтов фосфорилирования в фосфопротеоме клеток Drosophila Schneider (Hilger et al. 2009 г.). Редакторы этого специального выпуска сформулировали концепцию видов белков в 2008 и 2009 годах (Jungblut et al. 2008; Schlüter et al. 2009) и выяснили, что комбинация посттрансляционных модификаций определенного белка определяет его функцию в организме. Если необходимо выяснить функциональные аспекты, необходимо исследовать протеом на уровне видов белка. Спустя 2 года редакция пригласила 15 авторов написать обзор или представить свои оригинальные исследования в рамках концепции видов белка.
2009 г.). Редакторы этого специального выпуска сформулировали концепцию видов белков в 2008 и 2009 годах (Jungblut et al. 2008; Schlüter et al. 2009) и выяснили, что комбинация посттрансляционных модификаций определенного белка определяет его функцию в организме. Если необходимо выяснить функциональные аспекты, необходимо исследовать протеом на уровне видов белка. Спустя 2 года редакция пригласила 15 авторов написать обзор или представить свои оригинальные исследования в рамках концепции видов белка.
Одна из основных предпосылок для достижения уровня видов белков, 100% охват последовательностей, была выбрана в качестве центральной темы Бьорном Мейером и др., Которые согласились с тем, что необходимо достичь уровня видов белков, но из-за сложность эта кажется довольно «сюрреалистической». Тем не менее, они рассматривают такие решения, как подходы «сверху вниз» или «посередине», которые разделяют на первом этапе виды белка, а на втором этапе анализируются более или менее очищенные виды белка. Этот обзор будет интересно прочитать через 10 лет, и изменится ли нынешний сюрреализм на реализм. В обзоре Wolfgang Hoehenwarter et al. сюрреализм, кажется, стал реальностью уже сегодня: виды белков функционально анализируются с помощью протеомики дробовика в сочетании с линейной математикой. Действительно ли возможно получить информацию о виде белка из пептида (охват белковой последовательности до 1%)? Особенно трудно анализировать мембранные белки. Яцек Вишневски сделал обзор современного состояния фосфо- и гликопротеомики плазматических мембран.Сегодня с помощью методов ЖХ-МС можно получить доступ ко многим тысячам мембранных белков и даже их посттрансляционным модификациям, но не на уровне видов белков. Доступ к модифицированным пептидам возможен, но не к видам белков с их особой комбинацией посттрансляционных модификаций.
Этот обзор будет интересно прочитать через 10 лет, и изменится ли нынешний сюрреализм на реализм. В обзоре Wolfgang Hoehenwarter et al. сюрреализм, кажется, стал реальностью уже сегодня: виды белков функционально анализируются с помощью протеомики дробовика в сочетании с линейной математикой. Действительно ли возможно получить информацию о виде белка из пептида (охват белковой последовательности до 1%)? Особенно трудно анализировать мембранные белки. Яцек Вишневски сделал обзор современного состояния фосфо- и гликопротеомики плазматических мембран.Сегодня с помощью методов ЖХ-МС можно получить доступ ко многим тысячам мембранных белков и даже их посттрансляционным модификациям, но не на уровне видов белков. Доступ к модифицированным пептидам возможен, но не к видам белков с их особой комбинацией посттрансляционных модификаций.
Три обзора содержат информацию об определенных посттрансляционных модификациях: гликозаминогликаны хондроитина и дерматансульфата, АДФ-рибозилирование и металлопротеиназы. Первый и второй обзоры являются типичными примерами по теме различных классов строительных блоков, которые используются для классификации белков.Eugen Sisu et al. подробно остановимся на масс-спектрометрическом анализе хондроитинсульфата и дерматансульфата, которые изначально были связаны с белками. Методы, описанные в обзоре, особенно полезны для анализа состава гликозаминогликанов после удаления олигосахаридов из основных белков. Следовательно, отнесение олигосахаридной композиции к одному виду белка возможно только в том случае, если вид белка был очищен до анализа состава его гликозаминогликана.Высокопроизводительный анализ с применением описанных стратегий к белковым смесям даст данные о гликозаминогликановом статусе белковой смеси, который может быть характерным для развития заболеваний. Обзор Sabrina Laing et al. об аргинин-специфическом АДФ-рибозилировании дает целостный и впечатляющий обзор его физиологического воздействия, включая ферменты, ответственные за эту модификацию и ее обращение, а также последствия для функций белков.
Первый и второй обзоры являются типичными примерами по теме различных классов строительных блоков, которые используются для классификации белков.Eugen Sisu et al. подробно остановимся на масс-спектрометрическом анализе хондроитинсульфата и дерматансульфата, которые изначально были связаны с белками. Методы, описанные в обзоре, особенно полезны для анализа состава гликозаминогликанов после удаления олигосахаридов из основных белков. Следовательно, отнесение олигосахаридной композиции к одному виду белка возможно только в том случае, если вид белка был очищен до анализа состава его гликозаминогликана.Высокопроизводительный анализ с применением описанных стратегий к белковым смесям даст данные о гликозаминогликановом статусе белковой смеси, который может быть характерным для развития заболеваний. Обзор Sabrina Laing et al. об аргинин-специфическом АДФ-рибозилировании дает целостный и впечатляющий обзор его физиологического воздействия, включая ферменты, ответственные за эту модификацию и ее обращение, а также последствия для функций белков. Кроме того, авторы обсуждают методы обнаружения аргинин-специфичного ADP-рибозилирования.Тема АДФ-рибозилирование белков отображает текущие расхождения между исследованиями биохимии белков, сфокусированными на функциях белков, и областью протеомики, целью которой является исследование комплемента генома и, таким образом, наделение генов функциями. Хотя важность АДФ-рибозилирования белков для живых организмов сегодня полностью установлена, как описано в обзоре Laing et al. Эта тема более или менее игнорируется сообществом исследователей протеомики, что становится очевидным с точки зрения PubMed.Поиск с использованием термина «АДФ-рибозилирование» в сочетании с «протеомикой» дал только 31 результат. Для сравнения, термин «фосфорилирование» в сочетании с «протеомикой» дал 1,611 совпадений. Это также ясно показывает, что протеомика все еще далека от цели дать исчерпывающий функциональный статус исследуемого протеома. Эта проблема также становится очевидной при чтении обзора Тео Кляйна и Райнера Бишоффа.
Кроме того, авторы обсуждают методы обнаружения аргинин-специфичного ADP-рибозилирования.Тема АДФ-рибозилирование белков отображает текущие расхождения между исследованиями биохимии белков, сфокусированными на функциях белков, и областью протеомики, целью которой является исследование комплемента генома и, таким образом, наделение генов функциями. Хотя важность АДФ-рибозилирования белков для живых организмов сегодня полностью установлена, как описано в обзоре Laing et al. Эта тема более или менее игнорируется сообществом исследователей протеомики, что становится очевидным с точки зрения PubMed.Поиск с использованием термина «АДФ-рибозилирование» в сочетании с «протеомикой» дал только 31 результат. Для сравнения, термин «фосфорилирование» в сочетании с «протеомикой» дал 1,611 совпадений. Это также ясно показывает, что протеомика все еще далека от цели дать исчерпывающий функциональный статус исследуемого протеома. Эта проблема также становится очевидной при чтении обзора Тео Кляйна и Райнера Бишоффа. Авторы раскрыли аспект мира протеаз — матриксные металлопротеиназы.Они ясно и подробно резюмируют физиологическое и патофизиологическое значение этих протеаз, тем самым подчеркивая важность видов белков. Многочисленные различные протеазы, которые присутствуют, например, у людей оказывают огромное влияние на регуляцию функций белков только за счет укорачивания их белков-мишеней. Опять же, многие современные протеомные подходы игнорируют вопрос о точной аминокислотной последовательности белков, тем самым не имея возможности предоставить информацию о функциональном статусе отдельных белков.
Авторы раскрыли аспект мира протеаз — матриксные металлопротеиназы.Они ясно и подробно резюмируют физиологическое и патофизиологическое значение этих протеаз, тем самым подчеркивая важность видов белков. Многочисленные различные протеазы, которые присутствуют, например, у людей оказывают огромное влияние на регуляцию функций белков только за счет укорачивания их белков-мишеней. Опять же, многие современные протеомные подходы игнорируют вопрос о точной аминокислотной последовательности белков, тем самым не имея возможности предоставить информацию о функциональном статусе отдельных белков.
Jörg Seidler et al. обращаются в своем исследовании к проблеме низкой эффективности обнаружения фосфопептидов в ЖХ – МС. Хотя эта область уже была исследована многими другими коллегами, результаты их исследования показывают, что улучшение аналитических методов анализа фосфопептидов все еще возможно и необходимо. Таким образом, этот обзор должен побудить всех продолжать разработку метода.
Алессандро Куомо и др. сообщают об исследовании PTM на гистонах h4 и h5 из четырех клеточных линий рака груди человека в сравнении с нормальными эпителиальными клетками груди.Применяя метку стабильных изотопов с аминокислотами в культуре клеток (SILAC) для количественной оценки модификационных изменений в раковых клетках, авторы наблюдали «эпигенетическую подпись, специфичную для рака груди». Это исследование убедительно показывает, что сегодня можно применять «омический» подход не только на уровне триптических пептидов, но и на уровне определенных посттрансляционных модификаций, в данном случае ацетилирования и метилирования лизина по четырнадцати различным сайтам в h4 и h5. Конечно, этот подход очень сфокусирован и не включает все аспекты концепции видов белка, особенно в соответствии с общим точным химическим составом.Тем не менее, это правильный шаг вперед к анализу видов белков.
сообщают об исследовании PTM на гистонах h4 и h5 из четырех клеточных линий рака груди человека в сравнении с нормальными эпителиальными клетками груди.Применяя метку стабильных изотопов с аминокислотами в культуре клеток (SILAC) для количественной оценки модификационных изменений в раковых клетках, авторы наблюдали «эпигенетическую подпись, специфичную для рака груди». Это исследование убедительно показывает, что сегодня можно применять «омический» подход не только на уровне триптических пептидов, но и на уровне определенных посттрансляционных модификаций, в данном случае ацетилирования и метилирования лизина по четырнадцати различным сайтам в h4 и h5. Конечно, этот подход очень сфокусирован и не включает все аспекты концепции видов белка, особенно в соответствии с общим точным химическим составом.Тем не менее, это правильный шаг вперед к анализу видов белков.
Рукопись Zsuzsanna Darula et al. описывает повторный опрос данных MSMS диссоциации с переносом электрона (ETD) сложной смеси O-связанных гликопептидов с помощью недавно разработанных инструментов анализа. Подход повторного допроса — обработка и интерпретация «старых» масс-спектрометрических данных с использованием новых алгоритмов — вызвал некоторые важные дискуссии между редакторами, поскольку один рецензент предложил отклонить эту рукопись, аргументируя это тем, что старые данные (обработанные с использованием «старых» программное обеспечение) уже были опубликованы в другом месте.В отличие от рецензента, наше мнение состоит в том, что повторный опрос «старых» масс-спектрометрических данных должен быть поддержан, так как это открывает возможность получить лучшие и более высокие результаты из исходного масс-спектрометрического эксперимента. Особенно в связи с темой видов белков рекомендуется повторный опрос масс-спектрометрических данных, потому что фактические базы данных последовательностей неполны относительно посттрансляционных модификаций, а доступное в настоящее время программное обеспечение еще не способно учесть все возможные посттрансляционные модификации, но в будущем программное обеспечение будет улучшаться в этом направлении, поскольку рукопись Zsuzsanna Darula et al.
Подход повторного допроса — обработка и интерпретация «старых» масс-спектрометрических данных с использованием новых алгоритмов — вызвал некоторые важные дискуссии между редакторами, поскольку один рецензент предложил отклонить эту рукопись, аргументируя это тем, что старые данные (обработанные с использованием «старых» программное обеспечение) уже были опубликованы в другом месте.В отличие от рецензента, наше мнение состоит в том, что повторный опрос «старых» масс-спектрометрических данных должен быть поддержан, так как это открывает возможность получить лучшие и более высокие результаты из исходного масс-спектрометрического эксперимента. Особенно в связи с темой видов белков рекомендуется повторный опрос масс-спектрометрических данных, потому что фактические базы данных последовательностей неполны относительно посттрансляционных модификаций, а доступное в настоящее время программное обеспечение еще не способно учесть все возможные посттрансляционные модификации, но в будущем программное обеспечение будет улучшаться в этом направлении, поскольку рукопись Zsuzsanna Darula et al. показывает. Поскольку протеомические исследования дороги, повторный опрос старых масс-спектрометрических данных дополнительно снижает затраты и позволяет устойчиво использовать эти данные. Более того, поскольку сложность протеомов чрезвычайно велика, необходимо собрать как можно больше информации в базах данных, доступных через www, по каждому отдельному эксперименту.
показывает. Поскольку протеомические исследования дороги, повторный опрос старых масс-спектрометрических данных дополнительно снижает затраты и позволяет устойчиво использовать эти данные. Более того, поскольку сложность протеомов чрезвычайно велика, необходимо собрать как можно больше информации в базах данных, доступных через www, по каждому отдельному эксперименту.
Стефани Хеннинг и др. описывают метод прямого анализа альфа- и бета-цепей гемоглобинов из разбавленных образцов крови путем одновременного внутрикапиллярного протеолитического расщепления и нано-ESI – MS и MS / MS.С помощью своего недавно разработанного метода авторы достигли высокого охвата последовательностей обеих цепей гемоглобина, и поэтому это замечательное исследование также является шагом вперед к всестороннему анализу видов белков.
Восемь оригинальных статей проанализировали протеомы клеток, крови и тканей. Во всех исследованиях с использованием 2-DE признавалась встречаемость белков. 100% покрытие последовательности не было достигнуто ни в одном из этих исследований. Только Франк Шмидт и др. описывают отличительные посттрансляционные модификации между двумя видами белков.Одно из двух пятен протеасомного белка альфа-7 было фосфорилировано, и один из его цистеинов был окислен до цистеинсульфоновой кислоты, тогда как другой вид белка не был модифицирован. Эти два белка по-разному регулируются при апоптозе. Четкая дифференциация на виды белков была также обнаружена для супероксиддисмутазы типа 1 Alexandra Scholze et al. Один из видов белка был подавлен в контроле по сравнению с пациентами, находящимися на гемодиализе и с хроническим заболеванием почек.Все другие виды белков были подавлены в образцах болезни, несмотря на повышенную регуляцию гена супероксиддисмутазы типа 1 на уровне транскриптомики, что снова показывает, что корреляции между транскриптомикой и протеомикой нельзя ожидать как таковой, и необходимость анализа протеом на уровне видов белков. Эвелин Зейндл-Эберхарт и др. начал с протеомного исследования папиллярных карцином щитовидной железы и обнаружил видообразование нескольких белков цитоскелета и дифференциальную регуляцию различных видов белков одного и того же белка во время развития карциномы.
 Карима Шваб и др. выяснили несколько белков, встречающихся с несколькими видами белков, в протеомном анализе 2-DE на влияние генистеина фитогормона на нормальный протеом сердца мыши. Посредством мультипротеиназного переваривания и идентификации FTICR-MS удалось найти некоторых кандидатов для посттрансляционных модификаций, но 100% покрытие последовательности не было достигнуто. Исследование Фрэнка Козельски и соавт. показывает высокую разрешающую способность ЖХ – МС. Связанные с микротрубочками белки и их партнеры по взаимодействию из мозга млекопитающих были разделены на 573 белка.Они смогли выявить множество посттрансляционных модификаций в проанализированных пептидах, предсказывая множество различных видов белков, недоступных с помощью этого подхода.
Карима Шваб и др. выяснили несколько белков, встречающихся с несколькими видами белков, в протеомном анализе 2-DE на влияние генистеина фитогормона на нормальный протеом сердца мыши. Посредством мультипротеиназного переваривания и идентификации FTICR-MS удалось найти некоторых кандидатов для посттрансляционных модификаций, но 100% покрытие последовательности не было достигнуто. Исследование Фрэнка Козельски и соавт. показывает высокую разрешающую способность ЖХ – МС. Связанные с микротрубочками белки и их партнеры по взаимодействию из мозга млекопитающих были разделены на 573 белка.Они смогли выявить множество посттрансляционных модификаций в проанализированных пептидах, предсказывая множество различных видов белков, недоступных с помощью этого подхода.
Даже через 6 лет исследование Okkels et al. (2004) остается одним из редких примеров, когда с помощью протеомики один белок (ESAT-6) был разделен на восемь видов белков и четыре из них были проанализированы со 100% охватом последовательностей, что позволило дифференцировать реальные виды белков и корреляцию с разные функции. Только неацетилированные белковые разновидности были способны взаимодействовать с CFP-10. Это взаимодействие важно для переноса ESAT-6 из бактериальной клетки. Можно предположить, что в секретоме, который был проанализирован, следует избегать повторного связывания ESAT-6 с CFP-10 и, следовательно, ESAT-6 ацетилируется для выполнения своей задачи без конкуренции с взаимодействием с CFP-10.
Только неацетилированные белковые разновидности были способны взаимодействовать с CFP-10. Это взаимодействие важно для переноса ESAT-6 из бактериальной клетки. Можно предположить, что в секретоме, который был проанализирован, следует избегать повторного связывания ESAT-6 с CFP-10 и, следовательно, ESAT-6 ацетилируется для выполнения своей задачи без конкуренции с взаимодействием с CFP-10.
Статьи этого специального выпуска дают репрезентативный обзор современного состояния белковой науки с упором на тему видов белков и ясно показывают видообразование многих белков и в некоторых случаях различное поведение видов белков одного белка. касательно различных биологических ситуаций.Последствиями этих наблюдений должны быть: (1) Будьте осторожны с результатами протеомных исследований, касающихся корреляции идентифицированных белков из пептидов с их функцией. (2) Разработать новые стратегии и инструменты в ближайшие годы для исследования протеома на уровне видов белков, а также установить более высокую степень сотрудничества между клеточными биологами и специалистами по протеомике, хотя протеомика достигла высокой производительности для анализ белков и полный доступ к протеомам на уровне белка уже заявлены (Nilsson et al. 2010). Анализ на уровне белков, необходимый для достижения функционального уровня протеомики, все еще находится в зачаточном состоянии. (3) Добавить записи для каждого вида белков в базы данных последовательностей белков, позволяющие идентифицировать белки на уровне видов белков с помощью поисковых систем. До настоящего времени идентификация белков с помощью масс-спектрометрии основана на поиске в базах данных последовательностей белков, в которых есть записи для каждого белка. В этих записях аннотируются посттрансляционные модификации.После признания важности комбинации посттрансляционных модификаций для функции полипептида необходимо идентифицировать белки на уровне видов белков, а это означает, что нельзя избежать адаптации базы данных последовательностей белков к требованиям однозначного описания. видов белка. (4) Прийти к соглашению относительно однозначного описания видов белков, как это предлагается в Schlüter et al. (2009).
Редакция благодарит авторов за отличный вклад, рецензентов за их участие и Springer Wien New York за их поддержку в выпуске этого специального выпуска по видам белков. Надеюсь, этот специальный выпуск будет способствовать лучшему пониманию здоровья и болезней на молекулярном уровне и будет способствовать поиску более эффективных диагностических и терапевтически значимых биомаркеров в будущем.
Надеюсь, этот специальный выпуск будет способствовать лучшему пониманию здоровья и болезней на молекулярном уровне и будет способствовать поиску более эффективных диагностических и терапевтически значимых биомаркеров в будущем.
Ссылки
-
Deribe YL, Pawson T, Dikic I (2010) Посттрансляционные модификации в интеграции сигналов. Nat Struct Mol Biol 17 (6): 666–672
PubMed
Статья
CASGoogle ученый
-
Hilger M, Bonaldi T, Gnad F, Mann M (2009) Общесистемный анализ нокдауна фосфатазы с помощью количественной протеомики и фосфопротеомики.Протеомика клеток Mol 8: 1908–1920
PubMed
Статья
CASGoogle ученый
-
Jungblut P, Thiede B, Zimny-Arndt U, Muller EC, Scheler C, Wittmann-Liebold B, Otto A (1996) Разрешающая способность двумерного электрофореза и идентификация белков из гелей.Электрофорез 17: 839–847
PubMed
Статья
CASGoogle ученый
-
Jungblut PR, Holzhütter HG, Apweiler R, Schlüter H (2008) Видообразование протеома. Chem Cent J 18 (2): 16
Артикул
Google ученый
-
Okkels LM, Müller EC, Schmid M, Rosenkrands I, Kaufmann SHE, Andersen P, Jungblut PR (2004) CFP10 различает неацетилированный и ацетилированный ESAT-6 Mycobacterium tuberculosis путем дифференциального взаимодействия. Протеомика 4: 2954–2960
PubMed
Статья
CASGoogle ученый
-
Schlüter H, Apweiler R, Holzhütter HG, Jungblut PR (2009) В поисках своего пути в протеомике: номенклатура видов белков.Chem Cent J 9 (3): 11
Артикул
Google ученый
Скачать ссылки
Информация об авторе
Принадлежность
-
Core Facility Protein Analysis, Институт биологии инфекций им.
 Макса Планка, Charitéplatz 1, 10117, Берлин, Германия
Макса Планка, Charitéplatz 1, 10117, Берлин, Германия Peter R. клинической химии — масс-спектрометрическая протеомика, Медицинский университет Гамбург-Эппендорф, Martinistr.52, 20246, Гамбург, Германия
Hartmut Schlüter
Авторы, отвечающие за корреспонденцию
Для корреспонденции
Питер Р. Юнгблут или Хартмут Шлютер.
Об этой статье
Цитируйте эту статью
Jungblut, P.R., Schlüter, H. На пути к анализу видов белка: обзор стратегий и методов.
Аминокислоты 41, 219–222 (2011). https://doi.org/10.1007/s00726-010-0828-4
Скачать цитату
(PDF) В поисках пути в протеомике: номенклатура видов белка
Chemistry Central Journal 2009, 3:11 http: // журнал.Chemistrycentral.com/content/3/1/11
Страница 9 из 10
(номер страницы не для цитирования)
только с трипсином, но с несколькими другими протеазами параллельно, что обеспечивает более высокий охват последовательностей. За короткий срок
За короткий срок
во многих случаях может оказаться невозможным достичь
100% охвата последовательностей и / или идентификации
каждой PTM отдельных видов белка. Тем не менее,
, даже в этих случаях, использование номенклатуры видов белка
будет полезным, указывая на текущий уровень знания точной химической структуры и давая подсказки относительно
направления дальнейших исследований. .
Таким образом, мы предлагаем инструмент для хранения информации о видах белков, который делает доступным четкое
химическое описание белковых молекул.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Вклад авторов
HS разработал номенклатуру, написал текст и приложил
рисунки 2-4. Части текста и рисунка 1 были
подготовлены PRJ, который внес свой вклад вместе с HGH
и РА — к понятию номенклатуры и критически
переработанный текст.
Благодарности
Анна Вальдак и Питер Жермен благодарим за редакционную поддержку.
Ссылки
1. Jungblut P, Thiede B, Zimny-Arndt U, Muller EC, Scheler C, Witt-
Mann-Liebold B, Otto A: Разрешающая способность двумерного электрофореза
и идентификация белков из гели. Elec-
трофорез 1996, 17: 839-47.
2. Jungblut PR, Holzhütter HG, Apweiler R, Schlüter H: Спецификация
протеома.Chem Cent J 2008, 2:16.
3. Blanchard JM, Brissac C, Jeanteur P: Характеристика белков
, выделенных из цитоплазмы клеток HeLa, методом аффинной хроматографии
на полиаденилат-сефарозе. Proc Natl Acad Sci
USA 1974, 71: 1882-6.
4. O’Farrell PH: Двумерный электрофорез высокого разрешения —
sis белков. J. Biol Chem. 1975, 250: 4007-21.
5. Совместная комиссия по биохимической номенклатуре IUPAC-IUBMB:
Номенклатура множественных форм ферментов.В биохимическом
Номенклатура и связанные документы 2-е издание. Под редакцией: Liébecq
C. Колчестер: Portland Press; 1992.
6. UNIMOD — модификации белков для масс-спектрометрии: [http: //
www.unimod.org/modifications_list.php].
7. Creasy DM, Cottrell JS: Модификации белков для масс-спектрометрии
. Протеомика 2004, 4: 1534-6.
8. Нильсен М.Л., Савицкий М.М., Зубарев Р.А.: Степень модификаций в образцах протеома человека
и их влияние на динамический диапазон
анализа в протеомике дробовика.Mol Cell Proteomics 2006,
5: 2384-91.
9. Sun SC: Деубиквитилирование и регуляция иммунного ответа
. Нат Рев Иммунол 2008, 8: 501-11.
10. Клозе Дж., Кобальз У.: Двумерный электрофорез про-
теинов: обновленный протокол и значение для функционального анализа генома
. Электрофорез 1995, 16: 1034-59.
11. Jungblut P, Thiede B: Идентификация белков из гелей 2-DE с помощью масс-спектрометрии
MALDI.Mass Spectrom Rev 1997, 16: 145-62.
12. McCormack AL, Schieltz DM, Goode B, Yang S, Barnes G, Drubin D,
Yates JR 3rd: Прямой анализ и идентификация белков в смесях
с помощью ЖХ / МС / МС и поиск в базе данных на низком уровне —
фемтомолей уровень.![]() Anal Chem 1997, 69: 767-76.
Anal Chem 1997, 69: 767-76.
13. Келлехер Н: Нисходящая протеомика. Anal Chem 2004,
76: 197A-203A.
14. Хан Х, Джин М., Брейкер К., Маклафферти Ф. В.: Распространение масс-спектрометрии сверху вниз
на белки с массой более 200
килодальтон.Наука 2006, 314 (5796): 109-12.
15. Roth M, Forbes A, Boyne M, Kim Y, Robin son D., Kell eher N: Точная
и параллельная характеристика кодирующих полиморфизмов, альтернативный сплайсинг
и модификации белков человека с помощью масс-спектрометрии
. Mol Cell Proteomics 2005, 4: 1002-8.
16. Schmidt F, Donahoe S, Hagens K, Mattow J, Schaible U, Kaufmann S,
Aebersold R, Jungblut PR: Дополнительный анализ протеома бактерии Myco-
туберкулеза с помощью двумерного электрофореза
trop. и технология аффинных тегов с изотопным кодированием.Мол
Cell Proteomics 2004, 3 (1): 24-42.
17. Wu S, Lourette NM, Tolic N, Zhao R, Robinson EW, Толмачев А. В.,
В.,
Smith RD, Pasa-Tolic L: интегрированная стратегия сверху вниз и снизу вверх
для широкой характеристики изоформ белков и
модификаций. J. Proteome Res 2009, 8 (3): 1347-57.
18. Scheler C, Muller E, Stahl J, Muller-Werdan U, Salnikow J, Jungblut P:
Идентификация и характеристика белка теплового шока 27
видов белков в двумерном электрофорезе миокарда человека
паттерны трофореза .Электрофорез 1997, 18: 2823-31.
19. Клозе Дж., Нок К., Херрманн М., Штулер К., Маркус К., Блюггель М., Краузе
Е, Шалквик Л.С., Растан С.Д., Браун С.Д., Буссоу К., Химмельбауэр Х.,
Лехрах Х .: Генетический анализ протеом мозга мыши. Nat
Genet 2002, 30 (4): 385-93.
20. Mattow J, Jungblut PR, Muller E, Kaufmann S: Идентификация
кислых низкомолекулярных белков Mycobacterium
туберкулезного штамма h47Rv с помощью матричной лазерной десорбции.
масс-спектрометрия с ионизацией и электрораспылением. —
—
попробовать.Протеомика 2001, 1: 494-507.
21. Strahl B, Allis C: язык ковалентных модификаций гистонов —
вариантов. Nature 2000, 403: 41-5.
22. Брамбо Дж., Фанстиэль Д., Кун Дж. Дж.: Раскрытие потенциала гистона
: перспектива протеомики. Эпигенетика 2008, 3: 254-7.
23. Sims RJ 3rd, Reinberg D: Есть ли код, встроенный в белки
, который основан на посттрансляционных модификациях? Нат Рев Мол
Cell Biol 2008, 9: 815-20.
24. Майер М.П., Букау Б. Шапероны Hsp70: клеточные функции и молекулярный механизм
. Cell Mol Life Sci 2005, 62 (6): 670-84.
25. Моришима N: Контроль клеточной судьбы с помощью Hsp70: больше, чем новая встреча eva-
. Дж. Биохим (Токио) 2005, 137 (4): 449-53.
26. Okkels L, Muller E, Schmid M, Rosenkrands I, Kaufmann S, Andersen
P, Jungblut PR: CFP10 различает неацетилированный
и ацетилированный ESAT-6 Mycobacterium tuberculosis по дифференциальному взаимодействию
. Протеомика 2004, 4: 2954-60.
Протеомика 2004, 4: 2954-60.
27. Уоррен Э.Х., Виньерон, штат Нью-Джерси, Гэвин М.А., Кули П.Г., Стробант В., Далет
А, Тайкоди СС, Сюереб С.М., Мито Дж. К., Ридделл С.Р., Эйнде Б.Дж. пептиды
в обратном порядке. Science 2006, 313: 1444-7.
28. Кумар Р.С., Теккумкара Т.Дж., Сен GC: мРНК, кодирующие два ангиотензин-превращающих изофермента
, транскрибируются с
того же гена путем тканеспецифичного выбора альтернативных сайтов инициации транскрипции
.J Biol Chem, 1991, 266: 3854-62.
29. Рамчандран Р., Сен I: Процессинг расщепления ангиотензин-кон-
проверяющего фермента мембрано-ассоциированной металлопро-
тизиной. Биохимия 1995, 34: 12645-52.
30.Ramchandran R, Kasturi S, Douglas JG, Sen I: Metalloprotease-medi-
приводило к расщеплению секреции легочного АПФ сосудистыми
эндотелиальными и эпителиальными клетками почек. Am J Physiol 1996, 271 (2
Pt 2): H744-51.
31.Sadhukhan R, Santhamma KR, Reddy P, Peschon JJ, Black RA, Sen I:
Неизмененное расщепление и секреция ангиотензин-превращающего фермента
фермента, превращающего альфа-фактор некроза опухоли,
мышей с дефицитом. J. Biol Chem., 1999, 274: 10511-6.
J. Biol Chem., 1999, 274: 10511-6.
32. Chattopadhyay S, Santhamma KR, Sengupta S, McCue B, Kinter M,
Sen GC, Sen I. Кальмодулин связывается с цитоплазматическим доменом
ангиотензин-превращающего фермента и регулирует его расщепление и расщепление фосфора-
. секреция.J Biol Chem 2005,
280 (40): 33847-55.
33. Сировер М.А.: Новые взгляды на старый белок: функциональное
разнообразия глицеральдегид-3-фосфатдегидрогеназы у млекопитающих. Biochim Biophys Acta 1999, 1432: 159-184.
34. Хара М.Р., Снайдер SH: Оксид азота-ГАФД-Сиа: новая клетка
Каскад смерти. Cell Mol Neurobiol 2006, 26: 527-38.
35. Консорциум UniProt: универсальный протеиновый ресурс
(UniProt). Nucleic Acids Res 2009, 37: D169-D174.
белков | Определение, структура и классификация
Белок , очень сложное вещество, которое присутствует во всех живых организмах. Белки имеют большую питательную ценность и непосредственно участвуют в химических процессах, необходимых для жизни. Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел в обращение термин белок , слово, происходящее от греческого слова prōteios , что означает «удерживать первое место».”Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел в обращение термин белок , слово, происходящее от греческого слова prōteios , что означает «удерживать первое место».”Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Популярные вопросы
Что такое белок?
Белок — это встречающееся в природе чрезвычайно сложное вещество, состоящее из аминокислотных остатков, соединенных пептидными связями. Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Где происходит синтез белка?
Где хранится белок?
Белки не хранятся для дальнейшего использования в животных. Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов. Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов. Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Что делают белки?
Белки необходимы для жизни и необходимы для широкого спектра клеточной деятельности.Белковые ферменты катализируют подавляющее большинство химических реакций, происходящих в клетке. Белки обеспечивают многие структурные элементы клетки и помогают связывать клетки вместе в ткани. Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Молекула белка очень велика по сравнению с молекулами сахара или соли и состоит из множества аминокислот, соединенных вместе, чтобы образовать длинные цепи, подобно тому, как бусинки расположены на нити. Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
пептид
Молекулярная структура пептида (небольшого белка) состоит из последовательности аминокислот.
© raimund14 / Fotolia
Растения могут синтезировать все аминокислоты; животные не могут, хотя все они необходимы для жизни. Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. Они используют углекислый газ, содержащийся в воздухе, в процессе фотосинтеза для образования органических соединений, таких как углеводы. Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, животные, например, жвачные, требуют очень большие количества растительного материала (например,g., коровы), которые едят только растительный материал, чтобы удовлетворить свои потребности в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
Поскольку содержание белка в большинстве растений низкое, животные, например, жвачные, требуют очень большие количества растительного материала (например,g., коровы), которые едят только растительный материал, чтобы удовлетворить свои потребности в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
бобовые; аминокислота
Бобовые, такие как фасоль, чечевица и горох, богаты белком и содержат много незаменимых аминокислот.
© Elenathewise / Fotolia
Содержание белка в органах животных обычно намного выше, чем в плазме крови.Например, в мышцах содержится около 30 процентов белка, в печени — от 20 до 30 процентов, а в красных кровяных тельцах — 30 процентов. Более высокий процент белка содержится в волосах, костях и других органах и тканях с низким содержанием воды. Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы производятся в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы производятся в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.Подпишись сейчас
Высокое содержание белка в некоторых органах не означает, что важность белков связана с их количеством в организме или ткани; напротив, некоторые из наиболее важных белков, таких как ферменты и гормоны, присутствуют в очень малых количествах. Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их.Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела. Большая группа структурных белков поддерживает и защищает структуру тела животного.
У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела. Большая группа структурных белков поддерживает и защищает структуру тела животного.
гемоглобин
Гемоглобин — это белок, состоящий из четырех полипептидных цепей (α 1 , α 2 , β 1 и β 2 ).Каждая цепь присоединена к группе гема, состоящей из порфирина (органическое кольцеобразное соединение), присоединенного к атому железа. Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.
Британская энциклопедия, Inc.
белков | Определение, структура и классификация
Белок , очень сложное вещество, которое присутствует во всех живых организмах. Белки имеют большую питательную ценность и непосредственно участвуют в химических процессах, необходимых для жизни. Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел термин белок , слово, производное от греческого prōteios , что означает «удерживать первое место». Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел термин белок , слово, производное от греческого prōteios , что означает «удерживать первое место». Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Популярные вопросы
Что такое белок?
Белок — это встречающееся в природе чрезвычайно сложное вещество, состоящее из аминокислотных остатков, соединенных пептидными связями.Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Где происходит синтез белка?
Где хранится белок?
Белки не хранятся для дальнейшего использования в животных. Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов.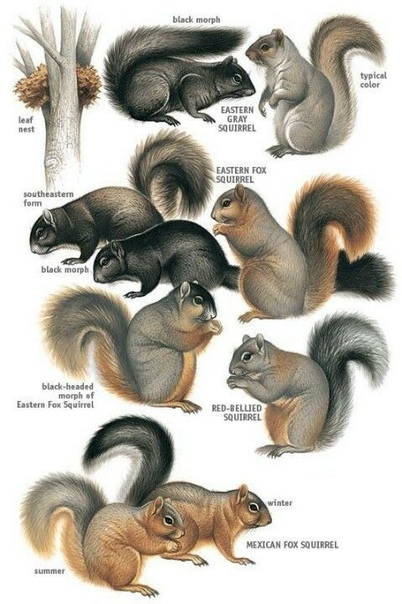 Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Что делают белки?
Белки необходимы для жизни и необходимы для широкого спектра клеточной деятельности. Белковые ферменты катализируют подавляющее большинство химических реакций, происходящих в клетке. Белки обеспечивают многие структурные элементы клетки и помогают связывать клетки вместе в ткани. Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Молекула белка очень велика по сравнению с молекулами сахара или соли и состоит из множества аминокислот, соединенных вместе, чтобы образовать длинные цепи, подобно тому, как бусинки расположены на нити. Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
пептид
Молекулярная структура пептида (небольшого белка) состоит из последовательности аминокислот.
© raimund14 / Fotolia
Растения могут синтезировать все аминокислоты; животные не могут, хотя все они необходимы для жизни. Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. Они используют углекислый газ, содержащийся в воздухе, в процессе фотосинтеза для образования органических соединений, таких как углеводы.Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, очень большое количество растительного материала требуется животным, таким как жвачные животные (например, коровы), которые едят только растительный материал для удовлетворения своих потребностей в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
бобовые; аминокислота
Бобовые, такие как фасоль, чечевица и горох, богаты белком и содержат много незаменимых аминокислот.
© Elenathewise / Fotolia
Содержание белка в органах животных обычно намного выше, чем в плазме крови. Например, в мышцах содержится около 30 процентов белка, в печени — от 20 до 30 процентов, а в красных кровяных тельцах — 30 процентов. Более высокий процент белка содержится в волосах, костях и других органах и тканях с низким содержанием воды.Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы производятся в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишись сейчас
Высокое содержание белка в некоторых органах не означает, что важность белков связана с их количеством в организме или ткани; напротив, некоторые из наиболее важных белков, таких как ферменты и гормоны, присутствуют в очень малых количествах.Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их. Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела.Большая группа структурных белков поддерживает и защищает структуру тела животного.
гемоглобин
Гемоглобин — это белок, состоящий из четырех полипептидных цепей (α 1 , α 2 , β 1 и β 2 ). Каждая цепь присоединена к группе гема, состоящей из порфирина (органическое кольцеобразное соединение), присоединенного к атому железа. Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.
Британская энциклопедия, Inc.
белков | Определение, структура и классификация
Белок , очень сложное вещество, которое присутствует во всех живых организмах. Белки имеют большую питательную ценность и непосредственно участвуют в химических процессах, необходимых для жизни. Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел в обращение термин белок , слово, происходящее от греческого слова prōteios , что означает «удерживать первое место». ”Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
”Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Популярные вопросы
Что такое белок?
Белок — это встречающееся в природе чрезвычайно сложное вещество, состоящее из аминокислотных остатков, соединенных пептидными связями. Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Где происходит синтез белка?
Где хранится белок?
Белки не хранятся для дальнейшего использования в животных. Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов. Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Что делают белки?
Белки необходимы для жизни и необходимы для широкого спектра клеточной деятельности.Белковые ферменты катализируют подавляющее большинство химических реакций, происходящих в клетке. Белки обеспечивают многие структурные элементы клетки и помогают связывать клетки вместе в ткани. Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Молекула белка очень велика по сравнению с молекулами сахара или соли и состоит из множества аминокислот, соединенных вместе, чтобы образовать длинные цепи, подобно тому, как бусинки расположены на нити.Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
пептид
Молекулярная структура пептида (небольшого белка) состоит из последовательности аминокислот.
© raimund14 / Fotolia
Растения могут синтезировать все аминокислоты; животные не могут, хотя все они необходимы для жизни. Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. Они используют углекислый газ, содержащийся в воздухе, в процессе фотосинтеза для образования органических соединений, таких как углеводы. Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, животные, например, жвачные, требуют очень большие количества растительного материала (например,g., коровы), которые едят только растительный материал, чтобы удовлетворить свои потребности в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
бобовые; аминокислота
Бобовые, такие как фасоль, чечевица и горох, богаты белком и содержат много незаменимых аминокислот.
© Elenathewise / Fotolia
Содержание белка в органах животных обычно намного выше, чем в плазме крови.Например, в мышцах содержится около 30 процентов белка, в печени — от 20 до 30 процентов, а в красных кровяных тельцах — 30 процентов. Более высокий процент белка содержится в волосах, костях и других органах и тканях с низким содержанием воды. Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы производятся в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.Подпишись сейчас
Высокое содержание белка в некоторых органах не означает, что важность белков связана с их количеством в организме или ткани; напротив, некоторые из наиболее важных белков, таких как ферменты и гормоны, присутствуют в очень малых количествах. Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их.Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела. Большая группа структурных белков поддерживает и защищает структуру тела животного.
Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их.Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела. Большая группа структурных белков поддерживает и защищает структуру тела животного.
гемоглобин
Гемоглобин — это белок, состоящий из четырех полипептидных цепей (α 1 , α 2 , β 1 и β 2 ).Каждая цепь присоединена к группе гема, состоящей из порфирина (органическое кольцеобразное соединение), присоединенного к атому железа. Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.
Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.
Британская энциклопедия, Inc.
белков | Определение, структура и классификация
Белок , очень сложное вещество, которое присутствует во всех живых организмах. Белки имеют большую питательную ценность и непосредственно участвуют в химических процессах, необходимых для жизни.Важность белков была признана химиками в начале 19 века, в том числе шведским химиком Йенсом Якобом Берцелиусом, который в 1838 году ввел термин белок , слово, производное от греческого prōteios , что означает «удерживать первое место». Белки видоспецифичны; то есть белки одного вида отличаются от белков другого вида. Они также специфичны для органов; например, в пределах одного организма мышечные белки отличаются от белков мозга и печени.
Популярные вопросы
Что такое белок?
Белок — это встречающееся в природе чрезвычайно сложное вещество, состоящее из аминокислотных остатков, соединенных пептидными связями. Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Белки присутствуют во всех живых организмах и включают многие важные биологические соединения, такие как ферменты, гормоны и антитела.
Где происходит синтез белка?
Где хранится белок?
Белки не хранятся для дальнейшего использования в животных. Когда животное потребляет избыток белков, они превращаются в жиры (глюкозу или триглицериды) и используются для снабжения энергией или создания энергетических запасов. Если животное не потребляет достаточное количество белка, организм начинает расщеплять богатые белком ткани, такие как мышцы, что приводит к истощению мышц и, в конечном итоге, к смерти, если дефицит является серьезным.
Что делают белки?
Белки необходимы для жизни и необходимы для широкого спектра клеточной деятельности. Белковые ферменты катализируют подавляющее большинство химических реакций, происходящих в клетке. Белки обеспечивают многие структурные элементы клетки и помогают связывать клетки вместе в ткани. Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Белки в форме антител защищают животных от болезней, и многие гормоны являются белками. Белки контролируют активность генов и регулируют экспрессию генов.
Молекула белка очень велика по сравнению с молекулами сахара или соли и состоит из множества аминокислот, соединенных вместе, чтобы образовать длинные цепи, подобно тому, как бусинки расположены на нити. Существует около 20 различных аминокислот, которые естественным образом встречаются в белках. Белки с аналогичной функцией имеют сходный аминокислотный состав и последовательность. Хотя пока невозможно объяснить все функции белка на основе его аминокислотной последовательности, установленные корреляции между структурой и функцией можно отнести к свойствам аминокислот, из которых состоят белки.
пептид
Молекулярная структура пептида (небольшого белка) состоит из последовательности аминокислот.
© raimund14 / Fotolia
Растения могут синтезировать все аминокислоты; животные не могут, хотя все они необходимы для жизни. Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. Они используют углекислый газ, содержащийся в воздухе, в процессе фотосинтеза для образования органических соединений, таких как углеводы.Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, очень большое количество растительного материала требуется животным, таким как жвачные животные (например, коровы), которые едят только растительный материал для удовлетворения своих потребностей в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
Растения могут расти в среде, содержащей неорганические питательные вещества, обеспечивающие азот, калий и другие вещества, необходимые для роста. Они используют углекислый газ, содержащийся в воздухе, в процессе фотосинтеза для образования органических соединений, таких как углеводы.Однако животные должны получать органические питательные вещества из внешних источников. Поскольку содержание белка в большинстве растений низкое, очень большое количество растительного материала требуется животным, таким как жвачные животные (например, коровы), которые едят только растительный материал для удовлетворения своих потребностей в аминокислотах. Нежвачные животные, в том числе люди, получают белки в основном от животных и их продуктов, например мяса, молока и яиц. Семена бобовых все чаще используются для приготовления недорогой, богатой белком пищи ( см. питание человека).
бобовые; аминокислота
Бобовые, такие как фасоль, чечевица и горох, богаты белком и содержат много незаменимых аминокислот.
© Elenathewise / Fotolia
Содержание белка в органах животных обычно намного выше, чем в плазме крови. Например, в мышцах содержится около 30 процентов белка, в печени — от 20 до 30 процентов, а в красных кровяных тельцах — 30 процентов. Более высокий процент белка содержится в волосах, костях и других органах и тканях с низким содержанием воды.Количество свободных аминокислот и пептидов у животных намного меньше количества белка; Белковые молекулы производятся в клетках путем поэтапного выравнивания аминокислот и попадают в жидкости организма только после завершения синтеза.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишись сейчас
Высокое содержание белка в некоторых органах не означает, что важность белков связана с их количеством в организме или ткани; напротив, некоторые из наиболее важных белков, таких как ферменты и гормоны, присутствуют в очень малых количествах.Важность белков в основном связана с их функцией. Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их. Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела.Большая группа структурных белков поддерживает и защищает структуру тела животного.
Все идентифицированные ферменты являются белками. Ферменты, которые являются катализаторами всех метаболических реакций, позволяют организму накапливать химические вещества, необходимые для жизни — белки, нуклеиновые кислоты, углеводы и липиды, — превращать их в другие вещества и разлагать их. Жизнь без ферментов невозможна. Есть несколько белковых гормонов с важными регуляторными функциями. У всех позвоночных респираторный белок гемоглобин действует как переносчик кислорода в крови, транспортируя кислород от легких к органам и тканям тела.Большая группа структурных белков поддерживает и защищает структуру тела животного.
гемоглобин
Гемоглобин — это белок, состоящий из четырех полипептидных цепей (α 1 , α 2 , β 1 и β 2 ). Каждая цепь присоединена к группе гема, состоящей из порфирина (органическое кольцеобразное соединение), присоединенного к атому железа. Эти комплексы железо-порфирин обратимо координируют молекулы кислорода, что напрямую связано с ролью гемоглобина в переносе кислорода в крови.