Функции белков в организме | Химия онлайн
Функции белков в природе универсальны. Белки входят в состав всех живых организмов. Мышцы, кости, покровные ткани, внутренние органы, хрящи, шерсть, кровь — все это белковые вещества.
Растения синтезируют белки из углекислого газа и воды за счет фотосинтеза. Животные организмы получают, в основном, готовые аминокислоты с пищей и на их базе строят белки своего организма.
Ни один из известных нам живых организмов не обходится без белков. Белки служат питательными веществами, они регулируют обмен веществ, исполняя роль ферментов – катализаторов обмена веществ, способствуют переносу кислорода по всему организму и его поглощению, играют важную роль в функционировании нервной системы, являются механической основой мышечного сокращения, участвуют в передаче генетической информации и т.д.
Видеофильм «Функции белков»
Разнообразные функции белков определяются a-аминокислотным составом и строением их высокоорганизованных макромолекул.

1. Каталитическая (ферментативная) функция
Каталитическая функция — одна из основных функций белков. Абсолютно все биохимические процессы в организме протекают в присутствии катализаторов – ферментов. Все известные ферменты представляют собой белковые молекулы.
Белки – это очень мощные катализаторы. Они ускоряют реакции в миллионы раз, причем для каждой реакции существует свой фермент.
В настоящее время известно свыше 2000 различных ферментов, которые являются биологическими катализаторами.
Например, фермент пепсин расщепляет белки в процессе пищеварения.
Даже такая простая реакция как гидратация углекислого газа катализируется ферментом карбоангидразой.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК.
2. Транспортная функция
Некоторые белки способны присоединять и переносить (транспортировать) различные вещества по крови от одного органа к другому и в пределах клетки.
Белки транспортируют липиды (липопротеиды), углеводы (гликопротеиды), ионы металлов (глобулины), кислород и углекислый газ (гемоглобин), некоторые витамины, гормоны и др.
Например, альбумины крови транспортируют липиды и высшие жирные кислоты (ВЖК), лекарственные вещества, билирубин.
Белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин. Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
Белок миоглобин запасает кислород в мышцах.
Специфические белки-переносчики обеспечивают проникновение минеральных веществ и витаминов через мембраны клеток и субклеточных структур.
3. Защитная функция
Защитную функцию выполняют специфические белки (антитела — иммуноглобулины), которые вырабатываются иммунной системой организма. Они обеспечивают физическую, химическую и иммунную защиту организма путем связывания и обезвреживания веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Например, белок плазмы крови фибриноген участвует в свертывании крови (образовывает сгусток). Это защищает организм от потери крови при ранениях.
Альбумины обезвреживают ядовитые вещества (ВЖК и билирубин) в крови.
Антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки. Интерфероны — универсальные противовирусные белки.
Многие живые существа для обеспечения защиты выделяют белки, называемые токсинами, которые в большинстве случаев являются сильными ядами. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
4. Сократительная (двигательная) функция
Важным признаком жизни является подвижность, в основе которой лежит данная функция белков, таких как актин и миозин – белки мышц. Кроме мышечных сокращений к этой функции относят изменение форм клеток и субклеточных частиц.
B результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
5. Структурная функция
Структурная функция — одна из важнейших функций белков. Белки играют большую роль в формировании всех клеточных структур.
Белки – это строительный материал клеток. Из них построены опорные, мышечные, покровные ткани.
Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей, эластин стенок кровеносных сосудов, фиброин шелка и др.) выполняют почти исключительно структурную функцию.
Кератин синтезируется кожей. Волосы и ногти – это производные кожи.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
6. Гормональная (регуляторная) функция
Регуляторная функция присуща белкам-гормонам (регуляторам). Они регулируют различные физиологические процессы.
Например, наиболее известным гормоном является инсулин, регулирующий содержание глюкозы в крови. При недостатке инсулина в организме возникает заболевание, известное как сахарный диабет.
Интересно знать!
В плазме некоторых антарктических рыб содержатся белки со свойствами антифриза, предохраняющие рыб от замерзания, а у ряда насекомых в местах прикрепления крыльев находится белок резилин, обладающий почти идеальной эластичностью. В одном из африканских растений синтезируется белок монеллин с очень сладким вкусом.
7. Питательная (запасная) функция
Питательная функция осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
8. Рецепторная (сигнальная) функция
Некоторые белки (белки-рецепторы), встроенные в клеточную мембрану, способны изменять свою структуру под воздействием внешней среды. Так происходит прием сигналов извне и передача информации в клетку.
Например, действие света на сетчатку глаза воспринимается фоторецептором родопсином.
Рецепторы, активизируемые низкомолекулярными веществами типа ацетилхолина, передают нервные импульсы в местах соединения нервных клеток.
9. Энергетическая функция
Белки могут выполнять энергетическую функцию, являясь одним из источников энергии в клетке (после их гидролиза). Обычно белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Но в качестве источника энергии белки используются крайне редко. Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Белки
функции, синтез, строение, свойства, продукты богатые белком, виды, состав и норма в день
Содержание статьи:
- Что такое белок
- Виды белков
- Синтез белка
- Состав белков
- Свойства
- Функции белков
- Строение
- Переваривание белков
- Обмен белков в организме
- Продукты богатые белком
- Норма в день для организма
- Усваиваемость белка
- Вред белков
Белки – это важные компоненты, которые имеют большое значение для нормальной работы организма. Источниками этих веществ являются животные и растительные продукты. Чтобы белковые элементы полноценно усваивались организмом, необходимо правильно употреблять их.

Что такое белок
Белок — это органическое соединение, которое включает альфа-аминокислоты. Они соединяются в цепь пептидной связью. В живых организмах белковый состав определяется генетическим кодом. В процессе выработки этих веществ обычно принимает участие 20 аминокислот. Их сочетания создают белковые молекулы, которые отличатся своими свойствами.
Виды белков

Виды белков бывают следующие:
- Белки куриных яиц. Они усваиваются лучше всего и считаются эталонными. Всем известно, что яйца включают белок, который почти на 100 % состоит из альбумина, и желток.
- Казеин. При попадании в желудок вещество превращается в сгусток, который долгое время переваривается. Это обеспечивает невысокую скорость расщепления белка, что провоцирует стабильное снабжение организма аминокислотами.
- Белки молочной сыворотки. Такие компоненты расщепляются быстрее всего. Уровень аминокислот и пептидов в крови увеличивается уже в течение 1 часа после употребления таких продуктов. При этом кислотообразующая функция желудка остается неизменной.
- Соевые белки. Такие вещества имеют сбалансированный состав важных аминокислот. После употребления подобных продуктов снижается содержание холестерина. Потому такую пищу стоит есть людям с лишним весом. При этом главным минусом соевых белков считается наличие ингибитора пищеварительного фермента трипсина.
- Растительные белки. Такие вещества усваиваются человеческим организмом достаточно плохо. Их клетки обладают толстыми оболочками, которые не поддаются влиянию пищеварительного сока. Также проблемы с усвоением обусловлены наличием ингибиторов пищеварительных ферментов в отдельных растениях.
- Рыбный белок. Изолят рыбного белка достаточно медленно расщепляется до состояния аминокислот.
Синтез белка

Синтез белка осуществляется в особых частицах – рибосомах.
Этот процесс происходит в несколько стадий:
- активация аминокислот;
- инициация белковой цепи;
- элонгация;
- терминация;
- сворачивание и процессинг.
Состав белков

Состав белков представляет собой линейные полимеры, которые включают остатки α-L-аминокислот. Также в белковых молекулах могут присутствовать модифицированные аминокислотные остатки и составляющие неаминокислотной природы.
Аминокислоты обозначают сокращениями, включающими 1 или 3 буквы. Белки, которые имеют длину от 2 до нескольких десятков аминокислотных остатков, называют пептидами. Если наблюдается высокая степень полимеризации, их именуют белками. Однако такое деление считается достаточно условным.
Свойства белков

Для белков характерны следующие свойства:
- Различная растворимость в воде. Белковые элементы, которые растворяются, приводят к формированию коллоидных растворов.
- Гидролиз. Под влиянием ферментов или растворов минеральных кислот разрушается первичное строение белка и формируется смесь аминокислот.
- Денатурация. Под этим термином понимают частичное или полное разрушение структуры белковой молекулы. Этот процесс может происходить под воздействием разных факторов – повышенных температур, растворов солей тяжелых металлов, кислот или щелочей, радиоактивного излучения, отдельных органических веществ.
Функции белков
Рассмотрим детальнее ряд важных функций белков:
- Строительная. Такие вещества принимают участие в формировании клеток и внеклеточных элементов. Они присутствуют в составе мембранклеток, сухожилий, волос.
- Транспортная. Белковый компонент крови, который называется гемоглобином, присоединяет кислород и распространяет его в разные ткани и органы. После чего обратно переносит углекислый газ.
- Регуляторная. Гормоны белкового характера участвуют в обменных процессах. Инсулин отвечает за регуляцию содержания глюкозы в крови, обеспечивает выработку гликогена, повышает трансформацию углеводов в жиры.
- Защитная. При попадании в организм инородных объектов или микроорганизмов вырабатываются особенные белки – антитела. Они помогают связать и нейтрализовать антигены. Фибрин, который вырабатывается из фибриногена, останавливает кровотечения.
- Двигательная. Существуют особые сократительные белковые элементы. К ним относят актин и миозин. Эти веществаобеспечивают сокращение мышечных тканей.
- Сигнальная. В поверхностной клеточной мембране присутствуют белковые молекулы, которые могут менять третичную структуру под влиянием внешних факторов. Это помогает принимать сигналы извне и передавать в клетку команды.
- Запасающая. У животных белковые вещества обычно не запасаются. К исключениям относят яичный альбумин и казеин, который присутствует в молоке. При этом белки способствуют скоплению определенных веществ. Распад гемоглобина приводит к тому, что железо не выводится, а сохраняется. Благодаря этому формируется комплекс с ферритином.
- Энергетическая. Распад 1 г белка сопровождается синтезом 17,6 кДж энергии. Вначале белковые элементы распадаются до аминокислот, а затем – до конечных продуктов. В результате вырабатывается вода, аммиак и углекислый газ. При этом белки применяются в качестве источника энергии лишь в том случае, если остальные – израсходованы.
- Каталитическая. Это одна из наиболее важных функций белковых элементов. За нее отвечают ферменты, которые активизируют биохимические процессы в клеточных структурах.
Строение белков

Среди органических веществ белки, которые называются биополимерами, считаются самыми многочисленными. Они отличаются разнообразием. На долю этих веществ приходится 50-80 % сухой массы клетки.
Белковые молекулы отличаются большими размерами. Потому их нередко именуют макромолекулами. В строение белков входят углерод, водород, азот, кислород. Помимо этого, в них могут присутствовать сера, железо, фосфор.
Белки отличаются числом – от 100 до нескольких тысяч, составом, последовательностью мономеров. В качестве мономеров выступают аминокислоты.
Переваривание белков

Белки усваиваются в желудке и тонком кишечнике. Процесс переваривания представляет собой гидролитическое расщепление белков до аминокислот.
Он имеет определенные особенности:
- протеолитические ферменты продуцируются в неактивном состоянии;
- активирование наблюдается в просвете пищеварительного тракта за счет частичного протеолиза;
- протеазы пищеварительного тракта характеризуются субстратной специфичностью – они могут относиться к эндопептидам или экзопептидазам.
Основным ферментом желудка, который расщепляет белки, считается пепси. Он синтезируется в неактивном состоянии и представляет собой профермент пепсиноген. Под воздействием соляной кислоты наблюдается частичный протеолиз пепсиногена. В результате появляется активная форма – пепсин.
Обмен белков в организме

Обмен белков в организме значительно сложнее, чем метаболизм липидов или углеводов. Жирные кислоты попадают в клетки почти в исходном виде, а углеводы – служат источником энергии. При этом основной строитель мышц претерпевает немало изменений в организме. На отдельных этапах белок преобразуется в углеводы. Как следствие, вырабатывается энергия.
Существует несколько этапов белкового обмена, для каждого из которых характерны определенные особенности:
- Попадание белков в организм. Под действием слюны происходит расщепление связей гликогена. Как следствие, формируется глюкоза, доступная для усвоения. Оставшиеся ферменты запечатываются. На этой стадии белки, которые присутствуют в продуктах, распадаютсяна отдельные элементы.Впоследствии они будут перевариваться.
- Переваривание. Под действием панкреатина и остальных ферментов наблюдается последующая денатурация до белков первого порядка. Организм способен получать аминокислоты исключительно из простейших белковых цепей. Для этого он вырабатывает кислоту. Это облегчает расщепление веществ.
- Расщепление на аминокислоты. Под действием клеток слизистых оболочек кишечника денатурированные белки попадают в кровь. Простой белок преобразуется организмом в аминокислоты.
- Расщепление до энергии. Под действием большого количества заменителей инсулина и ферментов для усваивания углеводов белок трансформируется в глюкозу. При нехватке энергии организм не выполняет денатурацию белка, а сразуегорасщепляет. В результате вырабатывается чистая энергия.
- Перераспределение аминокислот. Белковые элементы циркулируют в системном кровотоке и под действием инсулина попадают во все клетки. Как следствие, образуются требуемые аминокислотные связи. По мере распространения белков по организму происходит восстановление фрагментов мышечных элементов и структур, которые связаны со стимуляцией выработки, работой мозга, дальнейшей ферментацией.
- Образование новых белковых структур. Аминокислоты связываются с микроразрывами в мышцах и приводят к созданию новых тканей. Как следствие, наблюдается гипертрофия мышц. Аминокислоты в требуемом составе трансформируются в мышечно-белковую ткань.
- Обмен белков. При избытке таких структур под влиянием инсулина они снова проникают в систему кровообращения. Это приводит к формированию новых структур. При существенном напряжении в мышцах, длительном голодании или в период заболевания организм использует белки для компенсации недостатка аминокислот в остальных тканях.
- Перемещение липидных структур. Белки, которые соединяются в фермент липазу, способствуют перемещению и перевариванию с желчью полинасыщенных жирных кислот. Эти элементы принимают участие в перемещении жиров и выработке холестерина. С учетом состава аминокислот белки могут синтезироваться в полезный или вредный холестерин.
- Выведение окисленных продуктов. Использованные аминокислоты покидают организм с продуктами обмена. Мышцы, которые повреждаются вследствие нагрузок, тоже выводятся из организма.
Продукты богатые белком

Существует довольно много источников таких элементов. Животные продукты богатые белком, бывают следующие:
- Куриное мясо. 100 г продукта включает около 20 г белков. При этом такое мясо почти не содержит жира. Это актуально для людей, которые контролируют свой вес или занимаются спортом.
- Рыба. Самыми ценными источниками белка считаются тунец и лосось. Помимо этого, в продуктах имеются ценные кислоты омега-3, которые обеспечивают стабилизацию функций сердца и улучшают настроение.
- Свинина. В зависимости от жирности мяса в 100 г продукта может присутствовать 11-16 г белков. Также свинина включает витамины группы В.
- Яйца. В 1 яйце присутствует 6 г белка. Также продукт включает витамин В12 и холин.
- Говядина. На 100 г продукта приходится 19 г белков. Также говядина включает железо, карнитин и креатин
К растительным источникам белков стоит отнести следующее:
- Бобовые. Эти продукты включают большое количество белков. 100 г гороха содержит 23 г этих компонентов, а в сое присутствует 34 г белков.
- Орехи. Они представляют собой ценные источники белков и включают ненасыщенные жирные кислоты.
- Грибы. Эти продукты включают 2-5 % белков от общего количества. При этом есть сведения, что пищевые компоненты из грибов усваиваются с большим трудом.
- Гречка. В 100 г продукта присутствует 13 г белков. В гречке нет глютена, потому она вызывает аллергических реакций. При этом крупа включает фитонутриенты, которые сказываются на выработке инсулина и восстанавливают метаболизм.
Норма белка в день для организма

Норма белка в день для организма взрослого человека составляет минимум 50 г в чистом виде, что соответствует 150 г белого мяса или рыбы. Люди, которые активно занимаются спортом и нацелены на развитие мышечных тканей, должны употреблять большее количество белков.
Для профилактики распада мышечной ткани женщины должны употреблять минимум 1 г белка на 1 кг веса. Однако оптимальным количеством считается 2 г. Для мужчин этот параметр увеличивается до 3 г. Это означает, что представитель сильного пола весом 90 кг должен съедать в день 270 г чистого белка.
Усваиваемость белка

При употреблении таких веществ, стоит помнить о чувстве меры. Избыточное количество белков представляет определенную опасность. Они с трудом перевариваются и могут вызвать нарушения пищеварительных функций.
Проблемы с усвоением белков могут возникать в следующих ситуациях:
- Избыточное количество белка за 1 прием пищи. За 1 прием организм не может усвоить больше 35 г белков. Помимо этого, избыток таких веществ отрицательно влияет на пищеварительные функции. Организм не способен переварить большое количество протеинов. Как следствие, неусвоенная часть начинает гнить в пищеварительных органах. Это провоцирует запоры, увеличение ацетона и нарушения в работе поджелудочной железы.
- Систематическое переедание. Диетологи советуют придерживаться принципов дробного питания – 4-5 раз в день. Это помогает лучше переваривать пищу, в том числе и белки.
- Употребление большого количества трудноперевариваемых белков. Протеины могут усваиваться в разном объеме. Есть белки, которые легко перевариваются. Однако существуют и трудноперевариваемые продукты. Эталоном белковой пищи считаются куриные яйца. Также к легким белкам относят нежирные кисломолочные продукты, куриное филе, кролика.
- Исключение жиров. Безусловно, жирные продукты содержат большое количество калорий и с трудом усваиваются. Однако полностью отказываться от них не следует. Это чревато гормональными нарушениями, ухудшением состояния волос и кожи. Также исключение жиров провоцирует нарушение процесса переваривания белков. Чтобы обеспечить эффективную работу печени и выведение продуктов синтеза белка, стоит включать в рацион желчегонные жиры. Они присутствуют в оливковом и кунжутном маслах.
- Дефицит жидкости. Нарушение питьевого режима провоцирует разные проблемы, включая ухудшение усвоения белка. В сутки человек должен пить 30-40 мл воды на 1 кг массы тела. В жаркую погоду или при серьезных физических нагрузках норма дополнительно повышается на 500-800 мл.
- Неправильные дополнения к белкам. Чтобы протеины усваивались максимально хорошо, их рекомендуется сочетать с овощами. В такой пище присутствуют ферменты и клетчатка. Это облегчает переваривание белков.
Вред белков

Нарушения белкового обмена представляют большой вред для организма. Эти вещества принимают участие почти во всех физиологических процессах. При нарушении обмена белков есть риск развития опасных нарушений.
При этом для здоровых людей белки представляют опасность лишь при избыточном потреблении в течение долгого периода времени. При соблюдении белковых диет, которые базируются на употреблении большого количества протеинов, нужно помнить о чувстве меры. Такие системы питания должны быть кратковременными и плавными.
Избыточное количество белков в рационе провоцирует поражение почек и печени. Это связано со сложным процессом выведения веществ. В этом случае вырабатываются кетоновые тела, которые провоцируют отравление организма.
При некоторых патологиях есть противопоказания к употреблению белков. К ним относят подагру, недостаточность почек и печени, хроническую форму панкреатита.
Белки представляют собой ценные вещества, которые принимают участие во всех физиологических процессах. Потому каждый человек должен употреблять достаточное количество протеинов. При этом необходимо помнить о чувстве меры и соблюдать рекомендации врачей.
Белки как молекулы. Состав, структура и функции белков
Белки выполняют ведущую роль в жизни организмов, преобладая в них и количественно. В теле животных они составляют 40-50% сухой массы, в растениях – 20-35%. Это самая разнообразная группа молекул – как химически, так и функционально. Состав и структура белков определяет огромное разнообразие их функций в клетке: их так много, что невозможно перечислить и описать их все. Однако можно сгруппировать эти функции в следующие восемь категорий. Но этот список также будет неполным.

-
- Ферментативная (каталитическая). Ферменты имеют белковое происхождение. Это трёхмерные глобулярные (свёрнутые) белки, плотно прилегающие к молекуле для её расщепления или сборки. Такая подгонка ускоряет специфические химические реакции в клетке.
- Защитная. Другие глобулярные белки используют свою форму для распознавания чужеродных микроорганизмов и раковых клеток. Эти приёмные устройства формируются эндокринной и иммунной системами. Многие живые организмы выделяют белки, ядовитые для других. Токсины синтезируют ряд животных, грибов, растений, микроорганизмов. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
- Транспортная. Глобулярные белки присоединяют и транспортируют мелкие молекулы и ионы. Например, транспортный белок гемоглобин переносит кислород и углекислоту с потоком крови. Мембранные транспортные белки помогают молекулам и ионам двигаться через плазмалемму. Альбумины крови транспортируют жирные кислоты, глобулины – ионы металлов и гормоны.
- Структурная. Белковые молекулы входят в состав всех клеточных мембран и органоидов. Из белков построены элементы цитоскелета, сократительные структуры мышечных волокон. Структурными являются кератин в волосах, фибрин в сгустках крови, коллаген в коже, связках, сухожилиях и костях. В состав связок, стенок артерий и лёгких входит также структурный белок эластин.
- Двигательная. Сократительные белки обеспечивают способность клеток, тканей, органов и целых организмов изменять форму, двигаться. Мышцы сокращаются за счёт движения двух видов белковых нитей: актина и миозина. Контрактильные (лат. contraho, contractum – стягивать, сокращать) протеины играют ключевую роль в цитоскелете и передвижении веществ внутри клетки. Белок тубулин также входит в состав микротрубочек веретена деления, ресничек и жгутиков эукариотических клеток.
- Регуляторная. Крошечные белки, называемые гормонами, служат межклеточными посланниками в теле животных. Другие белки регулируют синтез РНК на ДНК, включая и выключая гены. Кроме того белки получают информацию, действуя в качестве рецепторов клеточной поверхности (эту функцию иногда считают отдельной, называя рецепторной).
- Запасающая. Кальций и железо хранятся в организме в виде ионов, связанных с белками хранения. В семенах растений запасаются резервные белки, которые используются зародышем при прорастании, а затем и проростком как источник азота.
- Энергетическая. После расщепления до аминокислот белки могут служить источником энергии в клетке. При полном окислении 1 г белка выделяется 17,6 кДж энергии. Однако белки расходуются на энергетические нужды лишь в крайних случаях, когда исчерпаны запасы углеводов и липидов.
 Сравнительный размер молекул белков. Слева направо: антитело (IgG) (150 кДа), гемоглобин (66,8 кДа), гормон инсулин, фермент аденилаткиназа и фермент глютаминсинтетаза.
Сравнительный размер молекул белков. Слева направо: антитело (IgG) (150 кДа), гемоглобин (66,8 кДа), гормон инсулин, фермент аденилаткиназа и фермент глютаминсинтетаза.
Автор: en:User:Gareth White, CC BY-SA 2.0
|
Функции белков
|
|||
| Функция | Класс белка | Образцы | Примеры использования |
| Каталитическая | Ферменты | Карбогидразы | Расщепляют полисахариды |
| Протеазы | Разрушают белки | ||
| Полимеразы | Синтезируют нуклеиновые кислоты | ||
| Киназы | Фосфорилируют сахара и белки | ||
| Защитная | Иммуноглобулины | Антитела | Маркируют чужеродные белки для элиминации (удаления) |
| Токсины | Змеиный яд | Блокирует нервные импульсы | |
| Клеточные белки-антигены | МНС-белки (главный комплекс гистосовместимости) | Опознание чужеродных белков | |
| Транспортная | Циркуляционные транспортёры | Гемоглобин | Переносит кислород и углекислый газ крови |
| Миоглобин | Переносит кислород и углекислый газ в скелетных мышцах и мышце сердца | ||
| Цитохромы | Транспортируют электроны | ||
| Мембранные транспортные белки | Натриево-калиевый насос | Возбуждение мембраны | |
| Протонный насос | Хемиосмос | ||
| Транспортёр глюкозы | Транспортирует глюкозу в клетки | ||
| Структурная | Волокна | Коллаген | Образует хрящ |
| Кератин | Формирует волосы, ногти, перья и др. | ||
| Фибрин | Образует сгустки крови | ||
| Двигательная | Мускулы | Актин | Сокращение мышечных волокон |
| Миозин | Сокращение мышечных волокон | ||
| Регуляционная | Осмотические белки | Сывороточный альбумин | Поддерживает осмотическую концентрацию крови |
| Регуляторы генов | Репрессор | Регулирует транскрипцию | |
| Гормоны | Инсулин | Контролирует уровень глюкозы в крови | |
| Вазопрессин | Увеличивает задержку воды почками | ||
| Окситоцин | Регулирует сокращение матки и выделение молока | ||
| Запасающая | Ион-связывание | Ферритин | Хранит железо, особенно в селезёнке |
| Казеин | Хранит ионы в молоке | ||
| Кальмодулин | Связывает ионы кальция | ||
Белки – это полимеры
Белки, или протеины – это нерегулярные (не имеющие определённой закономерности в последовательности мономеров) полимеры, состоящие из мономеров, называемые аминокислотами. Протеины, в состав молекул которых входит от пятидесяти до нескольких тысяч остатков аминокислот, называются белками. Молекулы с меньшим количеством мономеров именуются пептидами.
 Общие сведения о пептидах и белках
Общие сведения о пептидах и белках
Белок состоит из одной или нескольких длинных неразветвлённых цепей. Каждая цепь называется полипептидом и состоит из аминокислот, скреплённых пептидными связями. Термины «белок» и «полипептид» часто используются свободно, что может вызывать путаницу. Для белка, который включает только одну полипептидную цепь, оба термина являются синонимами.
В природе существуют около 500 аминокислот. В образовании белков обычно (но не всегда) участвуют только 20 из них – их называют белокобразующими. Порядок соединения мономеров в белке определяет его структуру и функции. Многие учёные считают, что аминокислоты были первыми органическими молекулами, появившимися на Земле. Возможно, океаны, которые существовали в начале истории нашей планеты, содержали большое их разнообразие.
 Белокобразующие аминокислоты
Белокобразующие аминокислоты
Автотрофные организмы синтезируют все необходимые им аминокислоты из продуктов фотосинтеза и азотсодержащих неорганических соединений. Для гетеротрофов источником аминокислот являются продукты питания. В организме человека и животных некоторые аминокислоты могут синтезироваться из продуктов обмена веществ (в первую очередь — из других аминокислот). Такие аминокислоты называются заменимыми.
Другие же, так называемые незаменимые аминокислоты, не могут быть собраны в организме и поэтому должны постоянно поступать в него в составе белков пищи. Протеины, содержащие остатки всех незаменимых аминокислот, называются полноценными. Неполноценные белки – это те, в составе которых отсутствуют остатки тех или иных незаменимых аминокислот.
Незаменимыми аминокислотами для человека являются: триптофан, лизин, валин, изолейцин, треонин, фенилаланин, метионин и лейцин. Для детей незаменимыми являются также аргинин и гистидин.
Полипептидные цепи могут быть очень длинными и включать самые разные комбинации аминокислотных остатков. Каждый конкретный белок характеризуется строго постоянным составом и последовательностью аминокислот.
 Димер мембранного белка кальсеквестрина.
Димер мембранного белка кальсеквестрина.
Deposition authors: Wang, S., Trumble, W.R., Liao, H., Wesson, C.R., Dunker, A.K., Kang, C., CC BY 3.0
Белки, образованные только остатками аминокислот, называются простыми. Сложными являются протеины, имеющие в своём составе компонент неаминокислотной природы. Это могут быть ионы металлов (Fe2+, Zn2+, Mg2+, Mn2+), липиды, нуклеотиды, сахара и др. Простыми белками являются альбумины крови, фибрин, некоторые ферменты (трипсин) и др. Сложные белки – это большинство ферментов, иммуноглобулины (антитела).
Состав аминокислот
Аминокислоты, как следует из их названия, содержат основную аминогруппу (— NH2), а также кислотную карбоксильную группу (—COOH), обе они связаны с центральным атомом углерода. Углерод дополнительно скреплен с водородом и функциональной белковой группой, называемой радикалом (R). Эти компоненты полностью заполняют все связи центрального атома углерода.
 Общая структура α-аминокислот, составляющих белки (кроме пролина).
Общая структура α-аминокислот, составляющих белки (кроме пролина).
Автор: User:X-romix
Уникальный характер каждой аминокислоты определяется природой группы радикала. Обратите внимание, что если группа радикала не содержит атома водорода (Н), как в глицине, то аминокислота хиральна и может существовать в форме двух энантиомеров: d или L. В белках живых систем содержатся обычно α (L)-аминокислоты, а β (d)-аминокислоты встречаются крайне редко.
Группа радикала определяет химические свойства аминокислот – они могут быть полярными или неполярными, гидрофобными или гидрофильными. Серин с радикалом -CH2OH является полярной молекулой, Аланин, который имеет –CH3 как группу радикала – неполярен.
Существуют также основные аминокислоты (более чем с одной аминогруппой) и кислые аминокислоты (более чем с одной карбоксильной группой). Наличие дополнительной амино- или карбоксильной группы оказывает влияние на свойства аминокислоты, которые играют определяющую роль в формировании пространственной структуры белка.
В состав радикала некоторых аминокислот (например, цистеина) входят атомы серы. Все 20 аминокислот сгруппированы в пять химических классов, основанных на группе их радикала.
- Неполярные аминокислоты, такие как лейцин, часто имеют в качестве радикала —CH2 или —CH3.
- Полярные незаряженные аминокислоты, такие как треонин, с радикалом, содержащим кислород или гидроксильную группу (-OH).
- Заряженные аминокислоты, такие как глутаминовая кислота, с радикалом, имеющим кислоты или основания, способные к ионизации.
- Ароматические аминокислоты, такие как фенилаланин, имеющий группу радикала, содержащую органическое (углеродное) кольцо с чередованием одиночных и двойных связей. Они также неполярны.
- Аминокислоты, обладающие особыми функциями и свойствами. Например, метионин, который часто является первой аминокислотой в цепи белков, пролин, вызывающий перегибы в цепях, цистин, связывающий цепи вместе.
Каждая аминокислота влияет на форму белка по-разному, в зависимости от химической природы боковых групп. Например, части белковой цепи с многочисленными неполярными аминокислотами сворачиваются внутрь своей цепи путём гидрофобного исключения.
Белки и пептидные связи
В дополнении к группе радикала каждая аминокислота имеет положительно заряженную аминогруппу (NH3 +) на одном конце и отрицательно заряженную гидроксильную группу (COO -) на другом. Амино- и карбоксильные группы у пары аминокислот могут подвергаться реакции дегидрации (выделение молекулы воды) с образованием ковалентной связи. Ковалентная связь, скрепляющая две аминокислоты, называется пептидной. Скреплённые таким способом аминокислоты не могут свободно вращаться вокруг N-C связи. Этот факт является основным фактором образования конструкции белковых молекул.
 Пептидная связь
Пептидная связь
Наличие как основной, так и кислотной групп обусловливает амфотерность (проявление как кислотных, так и основных свойств) и высокую реакционную способность аминокислот.
При соединении двух аминокислот образуется дипептид. На одном конце молекулы дипептида находится свободная аминогруппа, на другом — свободная карбоксильная группа. Благодаря этому дипептид может присоединять к себе другие аминокислоты, образуя олигопептиды. Если таким образом соединяется более 10 остатков аминокислот, то образуется полипептид.
Новаторская работа Фредерика Сангера в начале 1950-х годов доказала, что каждый вид белка имеет определённую аминокислотную последовательность. Для отщепления аминокислот он использовал химические методы, после этого определял их. Сангер преуспел в расшифровке аминокислотной последовательности инсулина. Он продемонстрировал, что все молекулы инсулина имеют одинаковый состав аминокислот.
Уровни структурной организации белков
Форма белка определяет его функцию. Один из способов изучить что-то столь же маленькое как белок – посмотреть на него при помощи коротковолнового излучения, которое представлено рентгеновскими лучами. Рентгеновские лучи пропускают через белок для получения дифракции его узора. Эта картинка кропотливо анализируется и позволяет исследователю построить трёхмерное изображение молекулы с положением каждого её атома. Первым белком, проанализированным таким образом, был миоглобин; вскоре такому же анализу был подвергнут связанный с ним белок гемоглобин.
Когда было изучено достаточное количество протеинов, стал очевиден общий принцип их строения: в каждом исследованном белке все внутренние аминокислоты, такие как лейцин, валин и фенилаланин, неполярны. Тенденция воды к исключению неполярных молекул буквально толкает такие части цепи аминокислот внутрь протеина. Неполярные аминокислоты вынуждены тесно контактировать друг с другом, оставляя мало свободного места внутри молекулы. Полярные и заряженные аминокислоты концентрируются на поверхности белка, за исключением немногих, играющих ключевые функциональные роли.
Структура белков, как правило, описывается как иерархия четырёх уровней: первичного, вторичного, третичного и четвертичного. Мы рассмотрим эту точку зрения, а затем интегрируем её с более современным подходом, вытекающим из расширяющихся знаний о белковой структуре.
 Уровни организации молекул белка
Уровни организации молекул белка
Первичная структура белков
Первичная структура белка – это его аминокислотная последовательность, т. е. это цепочка из множества аминокислотных остатков, соединённых пептидными связями. Это наиболее важная структура, так как именно она определяет форму, свойства и функции белка. На основе первичной структуры создаются другие формы молекулы.
Группы радикалов, которыми отличаются аминокислоты, не играют роли в пептидной цепи белков и протеин может включать любую последовательность аминокислот. Так как любая из 20 аминокислот может появиться в любом месте, белок, содержащий 100 мономеров, может образовать любую из 20 100 различных аминокислотных последовательностей. Это важное свойство белков позволяет им быть разнообразными, но каждый из них функционирует только при определённой аминокислотной последовательности.

Вторичная структура белка
Боковые и пептидные группы полипептидных цепей могут образовывать водородные связи. Вторичная структура белка возникает в результате связывания атомов водорода NH-групп и кислорода CO-групп. Полипептидная цепь при этом спирально закручивается. Водородные связи слабые, но благодаря их большому числу они обеспечивают стабильность этой структуры. Спиральную конфигурацию имеют, например, молекулы кератина, миозина и коллагена.
Водородные связи пептидов могут образовываться с водой. Если связей с водой будет слишком много, белки не смогут приобрести глобулярной структуры. Лайнус Полинг предположил, что пептидные группы могут взаимодействовать друг с другом, если пептид свёрнут в спираль, которую он назвал α-спиралью. Этот вид регулярного взаимодействия в пептиде формирует его вторичную структуру.
 Вторичная структура инсулина
Вторичная структура инсулина
Другая форма вторичной структуры формируется между зонами пептида, расположенными в один ряд, в результате чего получается плоская молекула, собранная в складки, называемая β-листом. Части белка могут быть либо параллельными, либо антипараллельными – в зависимости от того, являются ли смежные участки пептида ориентированными в одном или в противоположном направлении.
Эти два вида вторичной структуры создают зоны белка – цилиндрические (α-спирали) и плоские (β-листы). Конечная структура белка может включать области каждого типа вторичной структуры. Например ДНК-связывающие белки обычно имеют области α-спирали, которые могут лежать поперёк ДНК и взаимодействовать непосредственно с основаниями ДНК. Белки порины, образующие отверстия в мембранах, состоят из β-листов. В гемоглобине α и β-структуры (глобины) имеют в молекуле свои зоны.
 Вторичная структура белков
Вторичная структура белков
Третичная структура белков
Окончательная структура химически связанных белков называется третичной. Третичная структура формируется за счет образования водородных, ионных и других связей, возникающих в водной среде между разными группами атомов белковой молекулы вторичной структуры.
У некоторых белков важную роль в образовании третичной структуры играют S – S связи (дисульфидные) между остатками цистеина (аминокислоты, содержащей серу). При этом полипептидная спираль укладывается в своеобразный клубок (глобулу) таким образом, что гидрофобные аминокислотные радикалы погружаются внутрь глобулы, а гидрофильные располагаются на поверхности и взаимодействуют с молекулами воды. Третичной структурой определяются специфичность белковых молекул, их биологическая активность. Её имеют многие белки, например миоглобин (белок, который участвует в создании запаса кислорода в мышцах) и трипсин (фермент, расщепляющий белки пищи в кишечнике).
Третичная структура стабилизируется рядом сил, в том числе:
- водородными связами между радикалами различных аминокислот;
- электростатическим притяжением радикалов с противоположными зарядами;
- гидрофобным исключением неполярных радикалов;
- ковалентными дисульфидными связами.
На стадии третичной структуры по форме молекул белки можно разделить на две группы:
- глобулярные – имеют округлую форму. Такую форму имеют глобулины и альбумины крови, фибриноген, гемоглобин;
- фибриллярные – характеризуются вытянутой, нитевидной формой молекул. Это кератин, коллаген, миозин, эластин и др.

Четвертичная структура белка
Когда два или более полипептида связываются с образованием функционального белка, отдельные его цепи называются субъединицами. Расположение этих субъединиц и есть четвертичная структура. Субъединицы в таких белках чаще всего неполярны, поэтому они не связаны химически и отвечают за отдельные виды деятельности. Прочность четвертичной структуры обеспечивается взаимодействием слабых межмолекулярных сил.
Четвертичная структура характерна для белка гемоглобина. Вспомните, что гемоглобин состоит из двух α-цепей и двух β-цепей, а ещё в его состав входит небелковый компонент – гем.
Субъединицы располагаются в их окончательной четвертичной структуре. Это конечная структура некоторых, но не всех белков. У протеинов, которые состоят только из одной полипептидной цепи, например у фермента лизоцима, конечной структурой является третичная.

Мотивы и домены – структурные элементы белков
Ручное определение последовательности аминокислот в белке – трудоёмкая работа. Эту ситуацию изменило открытие способности хранения информации о белке молекулой ДНК. Первоначально геном человека был расшифрован вручную. Появление технологий следующего поколения привело к заметному ускорению секвенирования.
Сегодня расшифрованы более 40 000 бактериальных геномов и почти 8 000 геномов эукариот, в том числе 80 последовательностей генов млекопитающих. Так как состав ДНК имеет непосредственное отношение к последовательности аминокислот в белках, у биологов теперь есть огромная база данных строения протеинов.
Новая информация заставила задуматься о логике генетического кода и основных закономерностях структуры белка. Исследователи до сих пор рассматривают иерархическую систему из четырёх уровней как важную, но в лексикон биологов вошли и новые термины: мотив укладки и белковый домен.
Мотив укладки белковых молекул
Когда биологи обнаружили третичную структуру белка (ещё более трудоёмкая работа, чем определение последовательности аминокислот в цепи), они заметили сходные элементы, расположенные в непохожих белках. Подобные структуры называются мотивами, а иногда «сверхсекундными структурами». Термин «мотив» заимствован из искусства и относится к тематическому повторяющемуся элементу в музыке или дизайне.
Один общий мотив β-α-β образует так называемую «складку Россмана» у большого количества протеинов. Вторым часто встречающимся мотивом является β-баррель, который представляет собой β-лист, сложенный по кругу, чтобы сформировать трубку. Третий тип мотива – спираль-поворот-спираль, состоит из двух α-спиралей, разделённых изгибом. Его используют белки для связывания с молекулой ДНК.
Логику структуры мотивов укладки исследователи до сих пор не могут понять. Вероятно, если аминокислоты являются буквами в языке белков, то мотивы представляют собой повторяющиеся слова или фразы. Мотивы укладки помогли определить неизвестные функции белков, а база данных белковых мотивов используется для поиска новых неизвестных протеинов.
Мотивы укладки являются довольно консервативными и встречаются в белках, которые не имеют ни функциональных, ни эволюционных связей. Определение мотивов укладки лежит в основе физической, или рациональной классификации белков.
Белковые домены
Домены – это функциональные единицы в виде глобулы внутри более крупной структуры белков. Их можно рассматривать как субструктуры внутри третичной структуры белка. В языке белков это «абзацы». Большинство белков состоит из нескольких доменов, которые выполняют различные части функций протеинов.
Во многих структурах эти домены могут быть физически разделены. Например, так устроены факторы транскрипции – белки, которые связываются с ДНК и инициируют построение РНК по комплементарной ей ДНК. Было выяснено, что если ДНК-связывающие области поменять местами с факторами транскрипции, специфичность фактора может быть изменена без изменения его способности стимулировать транскрипцию. Эксперименты по замене доменов были проведены со многими факторами транскрипции, и они указывают, что активационные и ДНК-связывающие домены действуют отдельно.
Эти образования также могут помогать протеинам складываться. По мере того, как полипептидная цепь приобретает свою структуру, домены принимают правильную форму. Это действие может быть продемонстрировано экспериментально. Искусственное продуцирование фрагмента полипептида, который образует домен в интактном белке, показывает, что фрагмент складывается, чтобы сформировать такую же структуру, как у прототипа.
Процесс складывания, белки-шапероны
Первоначально биохимики думали, что новоиспечённые белки сворачиваются спонтанно, пробуя различные конфигурации, как гидрофобные взаимодействия с водой толкают неполярные аминокислоты внутрь белков до тех пор, пока не будет достигнута их окончательная структура. Оказалось, что эта точка зрения слишком проста. Цепи протеинов могут быть сложены многими способами, поэтому пробы и ошибки заняли бы слишком много времени. По мере того как первичная цепь складывается, приобретая финальную структуру, неполярные «липкие» внутренние участки во время промежуточных стадий обнажаются. Если эти промежуточные формы поместить в пробирку со средой, идентичной той, что внутри клетки, они прилипают к другим, и нежелательные белки-партнёры образуют клейкую массу.
Как клетки избегают того, чтобы их белки слипались в массу? Ответ на вопрос появился во время изучения необычных мутаций, которые спасают бактериальные клетки от размножения внутри них вирусов. При этом белки вирусов, произведённые внутри клетки, не могут сложиться как следует. Дальнейшее исследование помогло выяснить, что клетки содержат белки-шапероны, помогающие другим белкам складываться правильно.
 Свёртывание белков
Свёртывание белков
В настоящее время молекулярные биологи выявили массу белков, действующих как шапероны. Это большой класс полимеров, который можно разделить на подклассы. Представители шаперонов были найдены в каждом исследуемом организме. Некоторые из них, называемые тепловыми шоковыми белками, вырабатывается в ответ на повышение температуры тела. Высокие температуры служат фактором денатурации белков, шоковые белки-шопероны помогают белкам правильно сворачиваться и в такой ситуации.
Один из хорошо изученных классов этих белков, названных шаперонинами, был изучен у кишечной палочки (Escherichia coli). У мутантов при инактивации шаперонинов 30% бактериального белка не складывались должным образом. Шаперонины собираются в комплекс, напоминающий цилиндрический контейнер. Белки могут заходить в этот контейнер, и даже неправильно сложенные молекулы складываются там заново.
Исследователи склонны думать о белках как о фиксированных структурах, но это не относится к шаперонинам. Их гибкость поразительна. Видимо, это нужно им для выполнения своих функций. Клетки используют эти белки для складывания некоторых молекул протеинов и восстановления их неправильной структуры.
Денатурация инактивирует белки
Еще одной важной особенностью белков является то, что они проявляют свою активность лишь в узких температурных рамках и в определённом диапазоне кислотности среды.
Если условия, окружающие белок, изменяются, то он может частично потерять свою структуру или полностью развернуться. Этот процесс называется денатурацией. Белки могут быть денатурированы, когда рН, температура или ионная концентрация окружающего раствора изменена. Денатурация происходит вследствие разрыва водородных, ионных, дисульфидных и других связей, стабилизирующих пространственную структуру белковых молекул. При этом может утрачиваться их четвертичная, третичная и даже вторичная структуры.
Денатурированные белки как правило биологически неактивны. Это особенно значимо в отношении ферментов: так как почти каждая химическая реакция происходит при их помощи, жизненно важно, чтобы они функционировали нормально.
До появления морозильников и холодильников единственным способом предохранения продуктов от размножения в них микроорганизмов было хранение их внутри раствора, содержащего высокую концентрацию соли или уксуса, которые денатурировали ферменты микроорганизмов и предотвращали их рост.
Большинство ферментов функционирует в очень узком диапазоне условий окружающей среды. У каждого энзима этот диапазон специфичен. Ферменты крови, которые работают при рН около 7,4, быстро денатурируют в кислой среде желудка. И наоборот, протеолитические ферменты желудка, работающие при рН=2 или менее, разбираются в основной среде крови. Аналогично у организмов, живущих вблизи океанических гидротермальных источников, есть ферменты, которые хорошо работают только в экстремальных температурах (до 100°С). Эти организмы не могут выжить в более прохладных водах, потому что их энзимы не функционируют должным образом при относительно низких температурах.
Если нормальные показатели окружающего раствора восстанавливаются, небольшой белок, не потерявший первичной структуры, может восстановиться. Этот процесс называется ренатурацией, он происходит благодаря взаимодействию неполярных аминокислот и воды. Первоначально этот процесс был установлен для энзима рибонуклеазы, его ренатурация привела к выводу, что первичная структура определяет третичную структуру белка. Более сложные белки редко складываются вновь из-за их сложной окончательной структуры. Их денатурация носит необратимый характер.

Важно отличать денатурацию от диссоциации. Субъединицы белков с четвертичной структурой могут быть диссоциированы (разделены) без потери своей индивидуальной третичной структуры. Например, молекула гемоглобина может диссоциировать на 4 молекулы (2 α-глобина и 2 β-глобина) без денатурации свёрнутых глобиновых белков. Они легко восстанавливают свою четвертичную структуру из четырёх субъединиц.
Вам будет интересно
что является основными ферментативными функциями рибосомы или углеводов в организме и таблица об этом
Функции белков в природе универсальны. Белки входят в состав всех живых организмов. Мышцы, кости, покровные ткани, внутренние органы, хрящи, шерсть, кровь — все это белковые вещества.
Растения синтезируют белки из углекислого газа и воды за счет фотосинтеза. Животные организмы получают, в основном, готовые аминокислоты с пищей и на их базе строят белки своего организма.
Функции белков в организме

Ни один из известных нам живых организмов не обходится без белков.
Белки служат питательными веществами, они регулируют обмен веществ, исполняя роль ферментов – катализаторов обмена веществ, способствуют переносу кислорода по всему организму и его поглощению, играют важную роль в функционировании нервной системы, являются механической основой мышечного сокращения, участвуют в передаче генетической информации и т.д.
Каталитическая (ферментативная) функция
Каталитическая функция — одна из основных функций белков. Абсолютно все биохимические процессы в организме протекают в присутствии катализаторов – ферментов. Все известные ферменты представляют собой белковые молекулы.
Белки – это очень мощные катализаторы. Они ускоряют реакции в миллионы раз, причем для каждой реакции существует свой фермент.
В настоящее время известно свыше 2000 различных ферментов, которые являются биологическими катализаторами.
Например, фермент пепсин расщепляет белки в процессе пищеварения.
Даже такая простая реакция как гидратация углекислого газа катализируется ферментом карбоангидразой.
Ферменты катализируют реакции расщепления сложных молекул (катаболизм) и их синтеза (анаболизм), а также репликации ДНК и матричного синтеза РНК.
Транспортная функция
Некоторые белки способны присоединять и переносить (транспортировать) различные вещества по крови от одного органа к другому и в пределах клетки.
Белки транспортируют липиды (липопротеиды), углеводы (гликопротеиды), ионы металлов (глобулины), кислород и углекислый газ (гемоглобин), некоторые витамины, гормоны и др. Например, альбумины крови транспортируют липиды и высшие жирные кислоты (ВЖК), лекарственные вещества, билирубин.
Белок эритроцитов крови гемоглобин соединяется в легких с кислородом, превращаясь в оксигемоглобин.
Достигая с током крови органов и тканей, оксигемоглобин расщепляется и отдает кислород, необходимый для обеспечения окислительных процессов в тканях.
Белок миоглобин запасает кислород в мышцах. Специфические белки-переносчики обеспечивают проникновение минеральных веществ и витаминов через мембраны клеток и субклеточных структур.
Защитная функция
Защитную функцию выполняют специфические белки (антитела — иммуноглобулины), которые вырабатываются иммунной системой организма. Они обеспечивают физическую, химическую и иммунную защиту организма путем связывания и обезвреживания веществ, поступающих в организм или появляющихся в результате жизнедеятельности бактерий и вирусов.
Например, белок плазмы крови фибриноген участвует в свертывании крови (образовывает сгусток). Это защищает организм от потери крови при ранениях. Альбумины обезвреживают ядовитые вещества (ВЖК и билирубин) в крови.
Антитела, вырабатываемые лимфоцитами, блокируют чужеродные белки. Интерфероны — универсальные противовирусные белки.
Многие живые существа для обеспечения защиты выделяют белки, называемые токсинами, которые в большинстве случаев являются сильными ядами. В свою очередь, некоторые организмы способны вырабатывать антитоксины, которые подавляют действие этих ядов.
Сократительная (двигательная) функция
Важным признаком жизни является подвижность, в основе которой лежит данная функция белков, таких как актин и миозин – белки мышц. Кроме мышечных сокращений к этой функции относят изменение форм клеток и субклеточных частиц.
B результате взаимодействия белков происходит передвижение в пространстве, сокращение и расслабление сердца, движение других внутренних органов.
Структурная функция
Структурная функция — одна из важнейших функций белков. Белки играют большую роль в формировании всех клеточных структур.
Белки – это строительный материал клеток. Из них построены опорные, мышечные, покровные ткани.
Некоторые из них (коллаген соединительной ткани, кератин волос, ногтей, эластин стенок кровеносных сосудов, фиброин шелка и др.) выполняют почти исключительно структурную функцию. Кератин синтезируется кожей. Волосы и ногти – это производные кожи.
В комплексе с липидами белки участвуют в построении мембран клеток и внутриклеточных образований.
Гормональная (регуляторная) функция
Регуляторная функция присуща белкам-гормонам (регуляторам). Они регулируют различные физиологические процессы.
Например, наиболее известным гормоном является инсулин, регулирующий содержание глюкозы в крови. При недостатке инсулина в организме возникает заболевание, известное как сахарный диабет.
Интересно знать! В плазме некоторых антарктических рыб содержатся белки со свойствами антифриза, предохраняющие рыб от замерзания, а у ряда насекомых в местах прикрепления крыльев находится белок резилин, обладающий почти идеальной эластичностью. В одном из африканских растений синтезируется белок монеллин с очень сладким вкусом.
Питательная (запасная) функция
Питательная функция осуществляется резервными белками, которые запасаются в качестве источника энергии и вещества.
Например: казеин, яичный альбумин, белки яйца обеспечивают рост и развитие плода, а белки молока служат источником питания для новорожденного.
Рецепторная (сигнальная) функция
Некоторые белки (белки-рецепторы), встроенные в клеточную мембрану, способны изменять свою структуру под воздействием внешней среды. Так происходит прием сигналов извне и передача информации в клетку.
Например, действие света на сетчатку глаза воспринимается фоторецептором родопсином.
Рецепторы, активизируемые низкомолекулярными веществами типа ацетилхолина, передают нервные импульсы в местах соединения нервных клеток.
Энергетическая функция
Белки могут выполнять энергетическую функцию, являясь одним из источников энергии в клетке (после их гидролиза). Обычно белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
При полном расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии. Но в качестве источника энергии белки используются крайне редко. Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.
Источник: https://himija-online.ru/organicheskaya-ximiya/belki/funkcii-belkov-v-organizme.html
Функции белков в клетке:
- Строительная – обусловлена наличием белка во всех клеточных структурах. (Форма всех органелл клетки зависит от структуры белков).
- Каталитическая – реакции в клетке без ферментов идут медленно, так как концентрации исходных веществ (субстратов) в клетке малы. Обычно размеры молекул ферментов больше, чем размеры субстратов. Например, молекулярная масса каталазы, разрушающей пероксид водорода Н2О2, равна 250000, а самого пероксида – 34. Активный центр фермента – лишь небольшой участок его молекулы, на котором и происходит сама реакция. Фермент сравнивают с замком, а субстрат – с ключом, так как они должны точно подходить друг другу. Каждая реакция катализируется своим ферментом, однако существуют ферменты, которые катализируют несколько реакций.
- Двигательная – все движения обусловлены работой двигательных (сократительных) белков. В мышечных клетках при сокращении нитей более активна внедрённая между волокнами миозина за счёт энергии АТФ.
- Транспортная – белок гемоглобин транспортирует кислород и углекислый газ в организме. Через мембраны происходит транспорт различных веществ (сахар, ионы и др.).
- Защитная – осуществляется с помощью антител и антигенов. Антитела – белковые структуры β-лимфоцитов избирательно связывающиеся с чужеродными белками и клетками. Антигены – белки на поверхности клетки или в растворе, по которым Т-лимфоциты различают свои клетки и чужеродные. Убитые или ослабленные бактерии и вирусы (вакцины) несут свои антигены. При введении их в организм иммунная система вырабатывает антитела, что препятствует заболеванию.
- Энергетическая – белки являются источниками энергии. 1г белка при окислении даёт 17,6 кДж. Белок при разрушении образует СО2, Н2О, Nh4. Аммиак Nh4 ядовит, поэтому в печени он превращается в мочевину и мочевую кислоту.
- Регуляторная – пептидные гормоны, выделяемые железами внутренней секреции, изменяют обмен веществ в клетках определенных тканей.
Инсулин активирует захват молекулы глюкозы клеткой и синтез из неё гликогена. Без инсулина клетки голодают, так как не поглощают глюкозу, в результате чего развивается сахарный диабет. Т-лимфоциты передают с помощью белков информацию о чужеродных клетках β-лимфоцитам.
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Свойства белков так же разнообразны, как и функции. Одни растворяются в воде и образуют коллоидные растворы, другие растворяются в разбавленных растворах солей. Некоторые нерастворимы, например, белки кожи.
ХИМИЧЕСКИЕ СВОЙСТВА
В радикалах АК-остатков белков содержатся различные функциональные группы, способные вступать в химические реакции:
- восстановления;
- этерификации;
- лкилирования;
- нитрования.
Будучи амфотерным соединением белок реагирует и с кислотами, и со щелочами.
Источник: https://megaobuchalka.ru/9/32081.html
Функции белков
Работа и функции белков лежат в основе структуры любого организма и всех протекающих в нем жизненных реакций. Любые нарушения этих белков приводят к изменению самочувствия и нашего здоровья. Необходимость изучения строения, свойств и видов белков кроется в многообразии их функций.
Первые слова из определения Ф.Энгельсом понятия жизни «Жизнь есть способ существования белковых тел, …. » до сих пор, по прошествии полутора веков, не потеряли своей правильности и актуальности.
Структурная функция
Вещество соединительной ткани и межклеточный матрикс формируют белки коллаген, эластин, кератин, протеогликаны.
Непосредственно участвуют в построении мембран и цитоскелета (интегральные, полуинтегральные и поверхностные белки) – спектрин (поверхностный, основной белок цитоскелета эритроцитов), гликофорин (интегральный, фиксирует спектрин на поверхности).
К данной функции можно отнести участие в создании органелл – рибосомы.
Ферментативная функция
Все ферменты являются белками. В то же время есть данные о существовании рибозимов, т.е. рибонуклеиновых кислот, обладающих каталитической активностью.
Гормональная функция
Регуляцию и согласование обмена веществ в разных клетках организма осуществляют гормоны. Такие гормоны как инсулин и глюкагон являются белками, все гормоны гипофиза являются пептидами или небольшими белками.
Рецепторная функция
Эта функция заключается в избирательном связывании гормонов, биологически активных веществ и медиаторов на поверхности мембран или внутри клеток.
Транспортная функция
Только белки осуществляют перенос веществ в крови, например, липопротеины (перенос жира), гемоглобин (связывание кислорода), гаптоглобин (транспорт гема), трансферрин (транспорт железа). Белки транспортируют в крови катионы кальция, магния, железа, меди и другие ионы.
Транспорт веществ через мембраны осуществляют белки — Na+,К+-АТФаза (антинаправленный трансмембранный перенос ионов натрия и калия), Са2+-АТФаза (выкачивание ионов кальция из клетки), глюкозные транспортеры.
Резервная функция
В качестве примера депонированного белка можно привести производство и накопление в яйце яичного альбумина. У животных и человека таких специализированных депо нет, но при длительном голодании используются белки мышц, лимфоидных органов, эпителиальных тканей и печени.
Сократительная функция
Существует ряд внутриклеточных белков, предназначенных для изменения формы клетки и движения самой клетки или ее органелл (тубулин, актин, миозин).
Защитная функция
Защитную функцию, предупреждая инфекционный процесс и сохраняя устойчивость организма, выполняют иммуноглобулины крови, факторы системы комплемента (пропердин), при повреждении тканей работают белки свертывающей системы крови — например, фибриноген, протромбин, антигемофильный глобулин. Механическую защиту в виде слизистых и кожи осуществляют коллаген и протеогликаны.
К данной функции также можно отнести поддержание постоянства коллоидно-осмотического давления крови, интерстиция и внутриклеточных пространств, а также иные функции белков крови.
Белковая буферная система участвует в поддержании кислотно-щелочного состояния.
Существуют белки, которые являются предметом особого изучения:
Монеллин – выделен из африканского растения, обладает очень сладким вкусом, не токсичен и не способствует ожирению.
Резилин – обладает почти идеальной эластичностью, составляет „шарниры» в местах прикрепления крыльев насекомых.
Белки со свойствами антифриза обнаружены у антарктических рыб, они предохраняют кровь от замерзания
Источник: https://biokhimija.ru/belki/belki.html
Функции белка в клетке: структура белковой молекулы, виды органического вещества
Каждая клетка живого организма функционирует за счет содержания необходимых компонентов. Они выполняют важную роль, стимулируют обменные процессы и способствуют обновлению.
Особенно важны функции белка в клетке. Органические компоненты могут иметь разный состав, строение, некоторые отличия в жизненном цикле. Сегодня специалисты используют различные методы для исследования молекул и выявления их особенностей.
Что такое белки
Белки представляют собой органические соединения, имеющие различный состав и выполняющие важные функции в организме всех живых существ. Существует несколько видов этих молекул, каждый из которых имеет значение в процессе жизнедеятельности.
Состав
Органические вещества являются высокомолекулярными, поэтому могут включать в свой состав различные аминокислоты и другие соединения. Набор важных компонентов в каждой молекуле закладывается генетическим кодом животного или человека.
Основные компоненты каждой молекулы:
- углерод;
- кислород;
- азот;
- водород;
- сера.
Первый компонент обнаруживается в белке в наибольшем количестве, последний — не более 5 % от состава.
История открытия
Первый белок был получен необычным способом. Его выделили из пшеничной муки в виде клейковины. Произошло открытие в 1728 году, сделал его Якопо Беккари, итальянец. В качестве отдельного биологического класса молекулы белка были выделены в XVIII веке после обнародования работ французского ученого и химика Антуана де Фуркруа.
Другие ученые одновременно с французом отметили, что молекулы имеют свойство коагулировать (объединяться) под воздействием некоторых кислот или в процессе нагревания.
На тот момент ученые смогли изучить только альбумин, фибрин и глютен.
Только через 100 лет, в XIX веке, другие исследователи, изучив состав простых белков, отметили, что при нагревании происходит выделение аминокислот. Это помогло сделать вывод, что молекулы включают в себя довольно большое количество важных и разных аминокислот, а состав каждой из них индивидуален.
В 1836 году Мульдер предложил первую структурную формулу белков, основанную на теории радикалов. Он и еще несколько ученых вывели формулу протеинов, что в переводе с греческого означает «первый».
Мульдер также определил почти точную молекулярную массу наиболее простого белка, равную 131 дальтону. Дальтон — единица измерения молекул, называемая еще атомной массой или углеродной единицей.
Позже ученые выявили, что молекулярная масса может быть различной и зависит от состава и структуры органического соединения. В 1880-х годах русский ученый Данилевский изучил пептидные группы и доказал их существование в белковой молекуле. К этому времени большинство аминокислот уже были изучены.
В 1894 году немецкий ученый и физиолог Альбрехт Коссель рассказал о своем предположении. Он считал, что именно аминокислоты являются основными структурными элементами белковой молекулы.
Его теория была подтверждена в начале ХХ века химиком из Германии Эмилем Фишером. Ученый в ходе своего эксперимента доказал, что каждая молекула содержит около 20 аминокислот.
Важность белка в живом организме была признана только в 1926 году благодаря эксперименту американца Джеймса Самнера. После этого начинается активное изучение структур молекулы, выделяются различные виды. В 60—80-ых годах ХХ века исследования продолжаются.
К 2012 году в базе данных насчитывалось около 87 тысяч структур. Сегодня методы изучения молекулы усовершенствованы, поэтому работа в этом направлении продолжается.
Строение
Белок считается макромолекулой, поскольку имеет большой размер и множество составляющих. В строении белков присутствуют разные аминокислоты или их остатки, они чередуются с полипептидными цепями.
В молекулу могут входить следующие аминокислоты:
- глицин;
- аланин;
- изолейцин;
- серин;
- лейцин;
- валин;
- треонин.
Эти встречаются в составе наиболее часто, сочетаются с пептидными цепями и аминокислотными остатками.
Классификация
Существуют несколько классификаций белков в зависимости от состава, строения, формы, растворимости в воде. Чаще всего молекулы делят на простые и сложные с учетом строения.
К простым относятся следующие:
- Альбумины — жизненно необходимы животным и человеку. Содержатся во многих продуктах, хорошо растворяются в воде, соленых жидкостях под воздействием кислот. Являются основной составляющей мышечных тканей в организме, формируют резерв на случай длительного голодания.
- Глобулины в воде слабо растворяются. Являются составляющими крови, мышечной ткани, оказывают влияние на свертываемость, выполняют защитную функцию.
- Протамины — низкомолекулярные белки, хорошо растворимые в воде. В организме выполняют структурную функцию, являются строительным материалом для мышц и других тканей.
- Гистоны — низкомолекулярные вещества, содержат большое количество лизина и аргинина. Принимают участие в формировании структуры молекул ДНК, предупреждают передачу генетической информации к РНК.
- Проламины — растительные белки с невысокой пищевой ценностью. Создают в организме резерв.
- Глютелины — растительные вещества, принимающие участие в формировании клеточной оболочки. Денатурация происходит в солевых растворах, в воде они не растворимы.
- Протеноиды — животные белки, богатые аминокислотами, не растворяются в воде, кислотах, щелочах, солевых жидкостях. Входят в состав костной, хрящевой ткани, связок, сухожилий.
Среди сложных белков выделяют фосфопротеины, гликопротеины, нуклеопротеины, липопротеины, хромопротеины, металлопротеины.
Каждый вид имеет свои особенности:
- Фосфопротеины — сложные белки, содержащие остатки фосфорной кислоты, связывающиеся с пептидными цепями. Выполняют в организме защитную, строительную, энергетическую функции.
- Гликопротеины — сложные органические компоненты, содержащие углеводный остаток. Принимают участие в выработке ферментов, выполняют защитную и секреторную функции, стимулируют образование важных для жизнедеятельности гормонов.
- Нуклеопротеины состоят из нуклеиновых кислот (нуклеотиды), наиболее распространенные РНК и ДНК. Содержатся в мембранах клетки, формируют генетический код человека.
- Липопротеины содержат липиды (жиры), присутствуют в лимфе и плазме крови, не растворяются в воде. Выполняют транспортировочную функцию, переносят липиды по всему организму.
- Хромопротеины называют «цветными белками». В составе содержат окрашивающий компонент. Участвуют в транспортировке кислорода. Яркий представитель вида — гемоглобин.
- Металлопротеины содержат ионы металла в составе. Транспортируют металл в организме, создают его резерв.
Любой из видов играет важную роль в метаболических процессах.
Функции
Различные виды белков выполняют в организме важные функции. При отсутствии основных типов нарушаются все жизненно важные процессы.
Каталитическая
Катализ реакций в организме осуществляется благодаря наличию ферментов, являющихся белками по своему составу и строению. Ферменты помогают расщеплять сложные вещества на простые, облегчают их переработку.
Благодаря этому возможно поступление полезных компонентов ко всем тканям, органам, регенерация клеток, осуществление нормального метаболизма.
Структурная
Осуществляется благодаря коллагену и эластину. Белки являются важным строительным элементом, стимулируют формирование костной ткани, мышц, хрящей, связок и сухожилий.
Выделяют 4 структуры белковой молекулы:
- Первичная структура представляет собой последовательность остатков аминокислот, чередующихся с полипептидной цепью. Встречается во многих тканях, на протяжении жизни организма не меняет строения.
- Вторичная структура — упорядочивание фрагментов полипептидной цепи, подверженное стабилизации за счет наличия водородных связей.
- Третичная структура — строение полипептидной цепи пространственного типа. При детальном рассмотрении можно увидеть, что строение напоминает вторичную структуру, но присутствуют гидрофобные взаимодействия.
- Четвертичная структура представляет собой белковое соединение, состоящее из нескольких пептидных цепей в одном комплексе.
Благодаря различной структуре белковых молекул осуществляется построение всех клеток и тканей в организме.
Защитная
Физическая защита осуществляется благодаря наличию в клетках и тканях коллагена, отвечающего за прочность и предотвращающего повреждения. Химическая защита осуществляется благодаря способности белков связывать токсины, выводить их из организма.
Иммунная защита возможна благодаря способности некоторых белков стимулировать образование лимфоцитов, уничтожать вирусы, патогенные микроорганизмы.
Сигнальная и регуляторная
Регуляция всех процессов в клетках осуществляется с участием белков, представленных ферментами. Часто компоненты связываются с другими веществами, стимулируют процессы регенерации, регулируют метаболизм.
Многие внутриклеточные белки осуществляют сигнальную функцию, помогают передавать информацию между тканями, клетками, органами. Обычно сигнальную функцию выполняют белки-гормоны.
Транспортная
Транспортная функция осуществляется в основном за счет белка-гемоглобина. Он доставляет кислород ко всем тканям и клеткам, переправляет в легкие углекислый газ для выведения его наружу. Ученые нашли во всех живых организмах молекулы, напоминающие по строению гемоглобин.
Запасная и моторная
Запасная или резервная функция возможна благодаря наличию в клетке белков, содержащих аминокислоты. Они служат источником питания и энергии при недостаточном поступлении подобных компонентов с пищей.
Моторная или двигательная функция играет важную роль. Разные виды белковых молекул принимают участие в сокращении мышечных волокон, передвижении лейкоцитов и других клеток для обеспечения иммунной защиты.
Свойства
Белковые соединения обладают физическими и химическими свойствами, отличающими их от других молекул.
Физические
Физические свойства позволяют выявить белок среди других соединений в живом организме.
Основными будут следующие:
- вес молекулы может достигать 1 млн дальтон;
- при попадании в водный раствор происходит формирование коллоидной системы;
- в зависимости от кислотности среды отличается заряд белкового соединения;
- самый крупный сегодня белок — титин.
Молекулярная масса у каждого соединения отличается, определяется разными способами.
Химические
При определенных условиях белковые соединения проявляют свои химические свойства.
Наиболее частыми реакциями будут следующие:
- Амфотерность — способность белков в зависимости от условий проявлять основные свойства и кислотные.
- Денатурация — изменение биологической активности соединения в результате потери вторичной, третичной или четвертичной структуры. Может быть механической, физической и химической, обратимой и необратимой, полной и неполной.
Химические свойства белков изучаются различными методами для выявления особенностей молекул.
Этапы синтеза белка
Биосинтез белка представляет собой процесс, состоящий из нескольких этапов, в ходе которых происходит созревание соединений. Протекает во всех живых организмах.
Основные этапы синтеза:
- Инициация. Образование аминоацеладинелата одновременно с активацией аминокислоты в присутствии АТФ и специфического фермента.
- Элонгация. Присоединение образовавшейся кислоты к специфичной тРНК с последующим освобождением аденозинмнофосфата.
- Терминация. Связывание соединения аминокислоты и тРНК с рибосомами.
- Трансляция. Включение аминокислоты в белковую молекулу с одновременным высвобождением тРНК.
У разных живых организмов процесс может проходить с разной скоростью, но последовательность этапов неизменна.
Методы изучения
Сегодня исследование белковых соединений продолжается в современных лабораториях.
Популярные методы изучения:
- Метод клеточной и молекулярной биологии используется с целью фиксирования локализации молекул в клетках, наблюдения за синтезом веществ. Для стимулирования реакции используются антитела. Наблюдение проводится посредством микроскопа. На предметное стекло помещается подготовленный белок и антитела, проводится эксперимент, результаты фиксируются.
- Биохимический метод предполагает изучение чистого белка, избавленного от дополнительных компонентов. Для дальнейшего изучения используют центрифугирование, высаливание, электрофокусирование.
- Протеомика — наука, изучающая совокупность белковых соединений в составе одной клетки. Для исследования используются специальные приборы, соединения, белковые микрочипы, позволяющие изучать сразу несколько молекул в клетке.
Благодаря новейшим современным методикам возможно прогрессирование науки в области исследования живых клеток и их составляющих.
Биологическое значение
Биологическое значение органических соединений объясняется множеством полезных функций. Компоненты принимают участие во всех жизненно важных процессах в организме, являются незаменимым строительным материалом, стимулируют выработку лимфоцитов, отвечающих за стойкость иммунной системы животного или человека.
При отсутствии сложных белков невозможно образование гормонов, новых клеток и регенерация тканей. Без белковых молекул в организме не осуществляется процесс дыхания, поскольку невозможен перенос кислорода и выведение углекислого газа.
Особенно важное значение имеют белки для человека, поскольку некоторые виды помогают связывать и выводить из организма токсины, вредные соединения. Длительное отсутствие в питании белка приводит к постепенному истощению и смерти организма.
Интересные факты
Некоторые интересные факты о белковых соединениях доказывают важность их в живых организмах.
Наиболее интересными считаются следующие:
- Около 50 % от сухого веса организма приходится на белки.
- Вирусы почти полностью состоят из этого компонента, некоторые на 95 %.
- Более 30 % органических веществ у человека концентрируется в мышцах.
- Клетки головного мозга состоят преимущественно из белковых молекул.
- Волосы на теле и голове человека представлены ороговевшими клетками, состоящими из белковых молекул.
- Недостаток вещества в пище отрицательно отражается на всех процессах.
- В более чем 50 % случаев аллергия на белок у человека проявляется в детском возрасте.
- Человеку одинаково необходим растительный и животный белок.
- Детям белковые соединения необходимы в больших количествах, чем взрослым.
- Яичный белок считается наиболее качественным и легко усваивается.
Белки в организме — незаменимый и необходимый ежедневно компонент, позволяющий обеспечивать здоровье и правильное функционирование клеток.
Источник: https://obrazovanie.guru/nauka/biologiya/funktsii-belka.html
Белки
Белок – это фундамент организма. Он целиком построен из маленьких строительных блоков, называемых аминокислотами. Аминокислоты являются основными составными частями и строительными элементами белковой молекулы.
Название «протеины» (от греч. protos – первый, важнейший) более точно отражает первостепенное биологическое значение этого класса веществ, хотя в отечественной литературе их принято называть белками или белковыми веществами по аналогии с белком куриного яйца, приобретающего при кипячении (денатурации) белый цвет.
Молекула белка построена из 100 или более остатков аминокислот, ковалентно связанных в полимерные цепи. В человеческом организме 5 миллионов белков, причем ни один из белков человека не идентичен с белком любого другого живого организма.

Несмотря на такое разнообразие белковых структур для их построения необходимы всего 22 аминокислоты, 9 из которых незаменимы, то есть должны поступать с пищей человека, они не синтезируются в организме человека, остальные аминокислоты могут образовываться в нашем организме из других аминокислот. Таким образом, необходимо обеспечить адекватную поставку организму этих аминокислот соответствующим питанием с хорошо сбалансированным составом животных и растительных белков.
Большинство растительных белков, даже очень важных, содержит лишь незначительное число незаменимых аминокислот – именно поэтому строгие вегетарианцы (не потребляющие даже яиц и молочных продуктов) могут испытывать дефицит данных аминокислот. Невозможно переоценить важность сбалансированного питания для обеспечения достаточного уровня всех незаменимых аминокислот. Это существенный фактор здоровья!
Биологические функции белков очень разнообразны. Они выполняют каталитические, регуляторные, структурные, двигательные, транспортные, защитные, запасные и другие функции. Белки составляют основу биомембран, важнейшей составной части клетки и клеточных компонентов.
Исключительное свойство белков – самоорганизация структуры, то есть способность самопроизвольно создавать определенную свойственную только данному белку структуру. Для того, чтобы организм мог эффективно использовать и синтезировать белок, должны присутствовать все незаменимые аминокислоты и в необходимой пропорции. Даже временное отсутствие одной незаменимой аминокислоты может отрицательно сказаться на синтезе белка. При уменьшении количества любой незаменимой аминокислоты или ее отсутствии пропорционально уменьшается эффективность всех остальных аминокислот.
Девять незаменимых аминокислот – гистидин (необходим для детей), изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Организм в состоянии строить белки только при наличии достаточных количеств их всех. При отсутствии хотя бы одной из этих кислот белки уже не синтезируются, а пища используется как источник энергии или сохраняется в жировых отложениях.
Остальные 13 аминокислот синтезируются в организме человека в реакциях трансаминации. Эти аминокислоты – аланин, аргинин, аспарагин, карнитин, цистеин, цистин, глутаминовая кислота, глутамин, глицин, гидроксипролин, пролин, серин, тирозин.
Помимо 22 аминокислот, входящих в состав белков, известно свыше 150 других, которые встречаются в различных клетках и тканях либо в свободном, либо в связанном виде, но никогда не встречаются в составе белков.
Значение аминокислот не ограничивается их ролью в синтезе тканевых белков. Каждая из них выполняет в организме свои особые функции, направленные на поддержание гомеостаза организма.
Лишение всех аминокислот приводит к совершенной потере белка организмом, истощению, полной потере энергии, потере веса, анемии, разрушению мышц, в самом тяжелом случае – к смерти.

ФУНКЦИИ БЕЛКОВ
- Белки выполняют множество самых разнообразных функций, характерных для живых организмов. Здесь будут перечислены главные и в некотором смысле уникальные для жизнедеятельности человека функции, не свойственные или лишь частично присущие другим классам биополимеров.
- Каталитическая функция белков. Все до сих пор открытые биологические катализаторы – ферменты являются белками. Эта функция белков является уникальной, не свойственной другим полимерным молекулам.
- Питательная (резервная) функция белков. К таким белкам относятся так называемые резервные белки, являющиеся источниками питания для развития плода; белки яйца (овальбумины) и основной белок молока (казеин) также выполняют главным образом питательную функцию. Ряд других белков несомненно используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессы обмена веществ.
- Транспортная функция белков. Дыхательная функция крови, в частности перенос кислорода, целиком осуществляется молекулами гемоглобина – белка эритроцитов. В транспорте липидов принимают участие альбумины сыворотки крови. Ряд других сывороточных белков образует комплексы с жирами, медью, железом, тироксином, витамином A и другими соединениями, обеспечивая их доставку в соответствующие органы-мишени.
- Защитная функция белков. Основную функцию защиты в организме выполняет иммунологическая система, которая обеспечивает синтез специфических защитных белков – антител в отвег на поступление в организм бактерий, токсинов или вирусов. Высокая специфичность взаимодействия антител с антигенами (чужеродными веществами) по типу белок – белковое взаимодействие способствует нейтрализации их биологического действия и сохранению нормального состояния. В качестве другого примера защитной роли можно привести способность ряда белков крови к свертыванию. Свертывание белка плазмы крови фибриногена приводит к образованию сгустка крови, что предохраняет от потери крови при ранениях.
- Сократительная функция белков. В акте мышечного сокращения и расслабления участвует множество белковых веществ тела. Однако главную роль в этих жизненно важных процессах играют актин и миозин – специфические белки мышечной ткани. Сократительная функция присуща не только мышечным белкам, но и белкам ряда субклеточных структур, что обеспечивает тончайшие процессы жизнедеятельности клеток.
- Структурная функция белков. Данная функция белков многопланова. Белки со структурными функциями занимают по количеству первое место среди других белков тела человека. Широко распространены такие важные структурные белки, как коллаген в соединительной ткани, кератин в волосах, ногтях, коже, эластин в сосудистой стенке и др. Не менее важную роль выполняют белки в комплексе с углеводами в формировании ряда секретов – мукоидов, муцинов и т. д. Наконец, в комплексе с липидами (в частности, фосфолипидами) белки участвуют в образовании биомембран клеток.
- Гормональная функция белков. Обмен веществ в организме регулируется разнообразными механизмами. В этой регуляции важное место занимают гормоны, вырабатываемые в железах внутренней секреции. Ряд гормонов представлен белками или полипептидами, например, гормоны гипофиза, поджелудочной железы и др.
Можно указать еще на некоторые другие жизненно важные функции белков, в частности, на способность белков к сохранению онкотического давления в клетках и в крови, на буферные свойства белков, регулирующие физиологическое значение pH внутренней среды, и др.
Функции белков в организме. — Студопедия
Общая характеристика белков.
Белки – это высокомолекулярные органические, азотсодержащие соединения, состоящие из аминокислот.
Белки – наиболее сложные соединения живых систем. Не только каждый вид живого, но и каждый орган, каждый тип клеток обладает своим специфическим набором белков.Наконец, каждый индивидуум отличается от подобных своего вида собственным набором белков (биохимическая индивидуальность). Эта индивидуальность поддерживается всеми живущими организмами. При внедрении в организм чужих белков образуются защитные вещества (антитела) и разрушают чужие белки. Однако имеется и общность между определенными белками одного и того же вида, которая позволяет проводить обмен белками (например, переливание крови).
В количественном отношении они занимают первое место среди всех содержащихся в живой клетке макромолекул. В организме человека белки составляют примерно 1/5 часть, или 20 % массы, а в пересчете на сухой вес — 45%. Содержание белков в разных тканях различно, так в мышцах и печени содержится до 22 % белка, в мозге – 11 %, в жировой ткани – 6 %.
Свое название белки получили от белого цвета куриного яйца, на примере которого изучались их свойства. В 1838 г. Н. Мульдер назвал белки протеинами (от греч. protos — первый, важный). Это же название принято в международной номенклатуре.
Белки занимают первое место среди макромолекул не случайно, ведь там где есть белки, отмечены признаки жизни и наоборот там где есть жизнь, обнаруживаются белки.
Функции белков в организме.
Белки, входящие в состав организма человека, отличаются большим разнообразием состава, структуры, местом расположения и соответственно функциями.
Белки выполняют следующие функции в организме:
1. Каталитическая или ферментативная функция. Одна из основных функций белков. В настоящее время известно свыше 2000 различных ферментов, которые являются биологическими катализаторами и ускоряют все биохимические процессы в организме. Практически все они являются по своей химической природе белками.
2. Структурная или пластическая функция. Еще одна из важнейших функций белков. Мембраны всех клеток и субклеточных единиц представляют собой бислой: белки и фосфолипиды, т.е. белки играют большую роль в формировании всех клеточных структур. Эту функцию выполняют, например следующие белки: кератин – составляет основу волос и ногтей, коллаген – главный белок соединительной ткани.
3. Сократительная функция. Важным признаком жизни является подвижность, в основе которой лежит данная функция белков, таких как актин и миозин – белки мышц. Кроме мышечных сокращений к этой функции относят и изменение форм клеток и субклеточных частиц.
4. Транспортная функция. Перенос различных веществ по крови и в пределах клетки. Например, альбумины переносят по крови ВЖК, лекарственные вещества, билирубин; гемоглобин переносит кислород и углекислый газ, другие белки транспортируют липиды, стероиды, витамины и т.д.
5. Защитная функция. В процессе эволюции в организме выработан механизм узнавания и связывания «чужих» молекул с помощью белков-антител, которые являются белковой фракцией гамма-глобулинов; кроме этого ряд белков, например, альбумины обезвреживают ядовитые вещества (ВЖК и билирубин) в крови; белки свертывающей (фибриноген, протромбин и др.) и противосвертывающей системы предотвращают свертывание крови в нормальных условиях и наоборот образуют сгустки крови при повреждениях сосудов.
6. Регуляторная функция. Среди молекул-регуляторов важное место принадлежит регуляторам белковой природы, таким как гормоны, 50% которых имеют белковую природу; белки-гистоны, кислые белки играют роль в регуляции процесса трансляции в биосинтезе белка; белки крови альбумины играют большую роль в создании и поддержании онкотического и осмотического давления крови; белки входя в состав белковой и гемоглобиновой буферных систем участвуют в поддержании рН крови и т.д.
7. Рецепторная функция. Избирательное связывание различных регуляторов-гормонов, биогенных аминов, простогландинов, медиаторов, циклических мононуклеотидов, протекает с помощью белков-рецепторов на мембранах клетки.
8. Опорная или механическая функция. Прочность соединительной, хрящевой и костной ткани за счет белков – коллагена, эластина, фибронектина.
9. Энергетическая функция. 1 г. белка, окисляясь до конечных продуктов – мочевины, углекислого газа и воды, дает 4,1 ккал энергии.
О функциях белков в организме человека: строительной, двигательной, сигнальной
Несмотря на сложное устройство живых организмов на нашей планете, структурных единиц всего три – это белки, жиры и углеводы. Каждый из них выполняет свою роль и по-своему важен. Но именно белки отвечают за нашу индивидуальность. Их набор сложен и никогда не повторяется.
Чем объясняется многообразие функций белков
Белки – это полипептиды, состоящие из альфа-аминокислот, которые соединены пептидной связью. На сегодняшний день открыто порядка 500 аминокислот, 10 из них незаменимые, то есть должны поступать с пищей. Особый состав белков заложен в генетическом коде. Его синтез происходит при помощи 20 стандартных аминокислот.
Многообразие функций белков
Биология человека такова, что белок может состоять всего из 20 аминокислот. Но не стоит забывать, что помимо различной последовательности аминокислотных остатков, образуются и пространственные изоформы, которые также кодируются генетически. Такое строение обуславливает разнообразие биологических видов.
Выделяют несколько уровней организации белка:
- первичная – это последовательность аминокислот;
- вторичная – образование спиралей из цепочки при помощи водородных связей;
- третичная – пространственная форма спирали, на этом этапе белок имеет собственную форму;
- четвертичная – доменная, при которой несколько третичных структур (доменов) соединяются в макроструктуру.
Обратите внимание! В зависимости от последовательности аминокислотных остатков и их пространственной конфигурации меняются свойства и функции белка.
Функции белков
Эти вещества можно сравнить с биологическими кирпичиками, потому что они участвуют в постройке всех структур организма. А так как все органы выполняют разные функции, то и функции белков разнообразны. Сложно сказать, какую функцию в клетке не выполняет белок.
Строительная функция
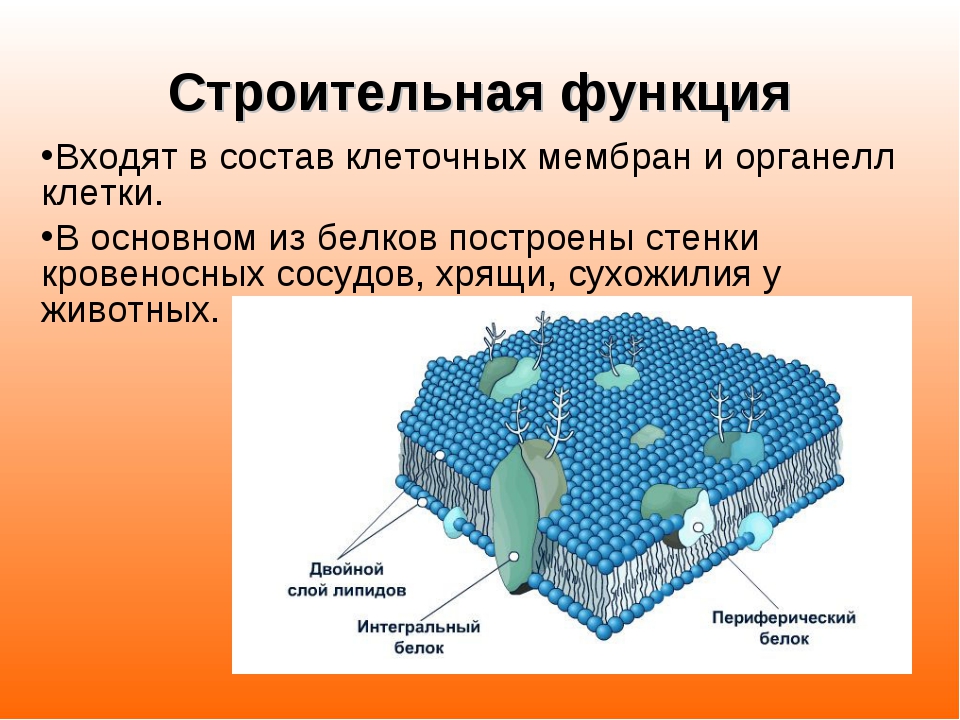
Строительная функция
Главная функция белка – пластическая, или строительная. Заключается она в том, что вещества участвуют в построении клеточных и неклеточных структур. По принципу работы напоминают арматурные прутья, т. к. отвечают за поддержание формы клетки или её изменения. Поэтому они называются структурными и являются основным классом белков. Например, в животной клетке цитоскелет состоит из белков. Также в качестве примера можно взять коллаген, который составляет основу межклеточного вещества соединительной ткани. Или кератин, из которого состоят волосы и ногти. Но самый известный структурный белок – это альбумин, в большом количестве он содержится в курином яйце и становится особенно заметен при жарке.
Двигательная или сократительная, функция
С помощью особых белков даже самые мелкие микроорганизмы могут передвигаться в пространстве. Например, реснички и жгутики одноклеточных состоят из белка флагеллина. При его сокращении жгутики совершают поступательные движения. Если объяснять кратко, то у многоклеточных организмов за мышечное сокращение отвечают актин и миозин. Для избирательного сокращения миоволокна миозин находится в активной форме не всегда, а лишь после воздействия киназы лёгких цепей миозина. После этого миозин фосфорилируется и взаимодействует с актином, образуя мышечное сокращение.
Важно! Кардиомиоциты работают по такому же принципу, благодаря этому сердце выполняет свою функцию.
Регуляторная и сигнальная функции

Регуляторная и сигнальная функции
Белки отвечают за регуляцию внутриклеточных процессов. Связано это с их способностью не только принимать поток информации, но и передавать следующим структурам. К регуляторным веществам относят:
- рецепторы;
- гормоны;
- белки, напрямую отвечающие за процессы внутри клеток.
Как правило, гормоны образуются железами внутренней секреции и циркулируют в крови. Затем они присоединяются к рецепторам. Специфическое строение этих функциональных единиц позволяет гормонам безошибочно присоединиться к нужному рецептору. Последние находятся в толще билипидного слоя клеточной мембраны, поэтому их ещё называют мембранными. После присоединения гормона рецептор меняет свою конформацию, и запускает каскад внутриклеточных реакций.
Обратите внимание! Очень часто сигнальную и регуляторную функции белков объединяют и отождествляют, потому что с физиологической точки зрения при передаче сигнала всегда изменяется внутренняя регуляция клеток. А значит невозможно провести чёткую линию между этими функциями.
Запасающая функция
Самая спорная функция – это запасающая. Для организма выгоднее сначала переварить углеводы, потом жиры, а затем белки. Последние требуют больших затрат энергии при переваривании, а энергии дают намного меньше, чем углеводы или жиры. Поэтому организм начинает переваривать белковые соединения только в самую последнюю очередь при отсутствии иных энергетических запасов. Некоторые учёные утверждают, что при переваривании белков энергии затрачивается столько же, сколько они в итоге выделяют, но точно установить так ли это не представляется возможным. Поэтому вопрос о запасающей функции остаётся открытым. Однако, белковые соединения могут выступать в качестве резервуара аминокислот, которые затем идут на построение других веществ, регулирующих метаболические пути. В этом их резервная функция.
Защитная функция

Защитная функция
Эту функцию можно разделить на несколько типов:
- иммунная;
- химическая;
- активная.
Иммунная система состоит практически полностью из белковых соединений. Это и антитела, которые атакуют заражённую клетку, а также интерфероны, участвующие в противовирусном иммунитете и белки компонента комплимента, без которых ни одна иммунная реакция не знала бы, в какой момент стоит начинаться и что атаковать. Также белки осуществляют основное звено иммунитета – образование мембраноатакующего комплекса, чтобы осуществить презентацию АГ следующим иммунным клеткам.
Химическая защитная функция проявляется в способности белков связываться с токсинами и нейтрализовать их. Особое место занимают ферменты печени, которые способствуют быстрому выведению опасных веществ из организма.
Обратите внимание! Многие бактерии и животные имеют ядовитый белковый секрет. Например, яд змеи, ботулотоксин или токсины холерного вибриона. Растения обычно не обладают белковыми ядами, но есть исключения – клещевина в своих семенах содержит рицин.
Функция дестабилизирующих белков
При размножении клеток необходимо копирование наследственного материала, находящегося в ДНК. При этом происходит процесс репликации ДНК, то есть, образование дочерней цепи на матричной. Перед этим нужно расплести двойную цепь. Помогают такому процессу дестабилизирующие белковые соединения. Кроме этого, присоединяясь к одноцепочечному фрагменту, они не позволяют закрывать основания цепи. Поэтому процесс репликации не останавливается.
Функция гистоновых белков
Не самая большая, но очень важная группа белков – это гистоны. Их функции напоминают шарниры при упаковке генетического материала. Дело в том, что длина цепочки ДНК очень большая, потому что в ней содержится вся информация о признаках, которые развились или могли развиться. Чтобы вся информация поместилась в ядро каждой клетки, её необходимо правильно упаковать. Упаковка ДНК на белковые «шарниры» образует нуклеосому.
После этого укладывать образовавшиеся пружины проще. Нуклеосомы закручиваются относительно друг друга с образованием фибриллы. Нитевидная фибрилла крепится на белковый тяж с образованием большого количества дезоксирибонуклеиновых петель (ДНП). Белковый тяж также образует петли, которые образуют хромонему. Последняя в свою очередь укладывается с образованием хромосомы.
Буферная функция
Буферная функция проявляется в способности некоторых белковых соединений поддерживать pH среду. Типичный пример – белки плазмы крови. Совокупность таких веществ образует буферные системы крови, которые поддерживают среду на уровне pH = 7,4. Почти 80% всех буферных веществ в крови – это глобулины и альбумины.
Гормональная функция
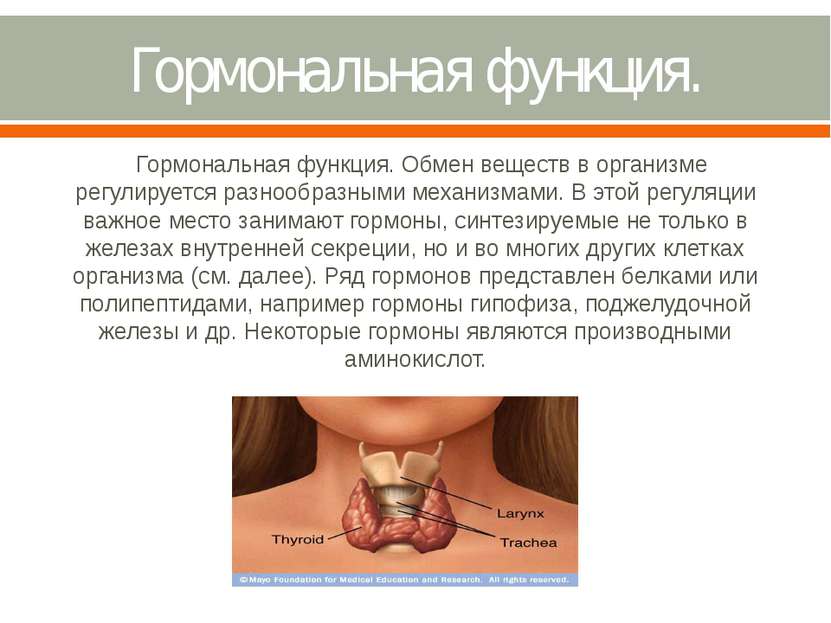
Гормональная функция
Гормоны напрямую регулируют обмен веществ. Они выделяются железами внутренней секреции в кровь, где они находят мишень в виде рецептора и присоединяются к нему. Не все гормоны являются белковыми субъединицами, но многие. Рассмотрим их действие на примере всем известного гормона инсулина, который выделяется бета-клетками островков поджелудочной железы.
По строению гормон инсулин представляет собой полипептид, состоящий из двух полипептидных цепочек, соединённых дисульфидными мостиками (связь между двумя атомами серы). Инсулин присоединяется к рецептору, который представляет из себя соединённые дисульфидными связями две альфа- и две бета-субъединицы. При присоединении к рецептору он меняет свою конформацию. Комплекс инсулин-рецептор проникает внутрь клетки, где инсулин высвобождается и образуется специальный переносчик – GLUT4. Последний отвечает за захват жировой тканью, мышцами и печенью. К слову, этиология сахарного диабета 2-го типа связана именно со снижением чувствительности рецептора к инсулину.
Белки – это универсальный строительный материал. Сложно точно сказать, каковы роли белков в организме. Ведь работа практически всех систем организма зависит от этих веществ, а значит, выбрать три функции, характерные только для белков, невозможно. Поэтому необходимо поддерживать нормальный уровень этих веществ с помощью полноценного питания.
9 Важные функции белка в организме
Белок важен для хорошего здоровья.
Фактически, название происходит от греческого слова proteos , что означает «первичный» или «первое место».
Белки состоят из аминокислот, которые соединяются в длинные цепи. Вы можете думать о белке как о нитке бусинок, каждая из которых представляет собой аминокислоту.
Есть 20 аминокислот, которые помогают формировать тысячи различных белков в вашем теле.
Белки выполняют большую часть своей работы в клетке и выполняют различные функции.
Вот 9 важных функций белка в вашем организме.
Белок необходим вашему организму для роста и поддержания тканей.
Тем не менее, белки вашего тела постоянно обновляются.
В нормальных условиях ваше тело расщепляет то же количество белка, которое оно использует для создания и восстановления тканей. В других случаях он расщепляет больше белка, чем может создать, что увеличивает потребности вашего организма.
Обычно это происходит в периоды болезни, во время беременности и кормления грудью (1, 2, 3).
Людям, выздоравливающим после травмы или операции, пожилым людям и спортсменам также требуется больше белка (4, 5, 6).
Резюме Белок необходим для роста и поддержания тканей. Потребности вашего организма в белке зависят от вашего здоровья и уровня активности.
Ферменты — это белки, которые помогают тысячам биохимических реакций, происходящих внутри и вне ваших клеток (7).
Структура ферментов позволяет им объединяться с другими молекулами внутри клетки, называемыми субстратами, которые катализируют реакции, необходимые для вашего метаболизма (8).
Ферменты могут также функционировать вне клетки, например, пищеварительные ферменты, такие как лактаза и сахароза, которые помогают переваривать сахар.
Некоторым ферментам для прохождения реакции требуются другие молекулы, например витамины или минералы.
Функции организма, зависящие от ферментов, включают (9):
- Пищеварение
- Производство энергии
- Свертывание крови
- Сокращение мышц
Отсутствие или неправильное функционирование этих ферментов может привести к болезни (10).
Резюме Ферменты — это белки, которые позволяют ключевым химическим реакциям происходить в вашем теле.
Некоторые белки представляют собой гормоны, которые являются химическими посредниками, которые помогают общаться между вашими клетками, тканями и органами.
Они производятся и секретируются эндокринными тканями или железами, а затем транспортируются с кровью к своим тканям или органам-мишеням, где они связываются с рецепторами белков на поверхности клеток.
Гормоны можно разделить на три основные категории (11):
- Белки и пептиды: Они состоят из цепочек аминокислот, от нескольких до нескольких сотен.
- Стероиды: Они сделаны из жирного холестерина. Половые гормоны, тестостерон и эстроген, основаны на стероидах.
- Амины: Они сделаны из отдельных аминокислот триптофана или тирозина, которые помогают вырабатывать гормоны, связанные со сном и обменом веществ.
Белки и полипептиды составляют большую часть гормонов вашего тела.
Некоторые примеры включают (12):
- Инсулин: Сигнализирует о поглощении глюкозы или сахара клеткой.
- Глюкагон: Сигнализирует о распаде хранимой глюкозы в печени.
- hGH (гормон роста человека): Стимулирует рост различных тканей, в том числе костей.
- АДГ (антидиуретический гормон): Сообщает почкам о реабсорбции воды.
- АКТГ (адренокортикотропный гормон): Стимулирует высвобождение кортизола, ключевого фактора метаболизма.
Резюме Аминокислотные цепи различной длины образуют белок и пептиды, которые составляют несколько гормонов вашего тела и передают информацию между клетками, тканями и органами.
Некоторые белки являются волокнистыми и придают клеткам и тканям жесткость и жесткость.
Эти белки включают кератин, коллаген и эластин, которые помогают формировать соединительный каркас определенных структур вашего тела (13).
Кератин — это структурный белок, который содержится в коже, волосах и ногтях.
Коллаген — самый распространенный белок в организме, структурный белок костей, сухожилий, связок и кожи (14).
Эластин в несколько сотен раз гибче коллагена.Его высокая эластичность позволяет многим тканям вашего тела возвращаться к своей первоначальной форме после растяжения или сокращения, например матке, легким и артериям (15).
Резюме Класс белков, известных как волокнистые белки, придает различным частям вашего тела структуру, прочность и эластичность.
Белок играет жизненно важную роль в регулировании концентрации кислот и оснований в крови и других жидкостях организма (16, 17).
Баланс между кислотами и основаниями измеряется с помощью шкалы pH.Он варьируется от 0 до 14, где 0 означает наиболее кислотный, 7 нейтральный и 14 наиболее щелочной.
Примеры значения pH обычных веществ включают (18):
- pH 2: Желудочная кислота
- pH 4: Томатный сок
- pH 5: Черный кофе
- pH 7,4: Кровь человека
- pH 10: Молоко магнезии
- pH 12: Мыльная вода
Различные буферные системы позволяют жидкостям вашего тела поддерживать нормальный диапазон pH.
Необходим постоянный pH, так как даже небольшое изменение pH может быть вредным или потенциально смертельным (19, 20).
Один из способов, которым ваш организм регулирует pH — это протеины. Примером является гемоглобин, белок, из которого состоят эритроциты.
Гемоглобин связывает небольшое количество кислоты, помогая поддерживать нормальный уровень pH в крови.
Другие буферные системы в вашем организме включают фосфат и бикарбонат (16).
Резюме Белки действуют как буферная система, помогая вашему организму поддерживать надлежащие значения pH крови и других жидкостей организма.
Белки регулируют процессы в организме, поддерживая баланс жидкости.
Альбумин и глобулин — это белки в крови, которые помогают поддерживать баланс жидкости в организме за счет привлечения и удержания воды (21, 22).
Если вы не едите достаточно белка, уровень альбумина и глобулина в конечном итоге снижается.
Следовательно, эти белки больше не могут удерживать кровь в ваших кровеносных сосудах, и жидкость вытесняется в промежутки между вашими клетками.
По мере того, как жидкость продолжает накапливаться в промежутках между клетками, возникает опухоль или отек, особенно в области желудка (23).
Это форма тяжелой белковой недостаточности, называемая квашиоркор, которая развивается, когда человек потребляет достаточно калорий, но не потребляет достаточное количество белка (24).
Квашиоркор редко встречается в развитых регионах мира и чаще встречается в районах голода.
Резюме Белки в крови поддерживают баланс жидкости между кровью и окружающими тканями.
Белки помогают формировать иммуноглобулины или антитела для борьбы с инфекцией (25, 26).
Антитела — это белки в вашей крови, которые помогают защитить ваше тело от вредных захватчиков, таких как бактерии и вирусы.
Когда эти чужеродные захватчики проникают в ваши клетки, ваше тело вырабатывает антитела, которые маркируют их для уничтожения (27).
Без этих антител бактерии и вирусы могли бы свободно размножаться и поражать ваше тело вызываемой ими болезнью.
Как только ваше тело вырабатывает антитела против определенных бактерий или вирусов, ваши клетки никогда не забывают, как их вырабатывать.
Это позволяет антителам быстро отреагировать в следующий раз, когда конкретный возбудитель болезни вторгнется в ваше тело (28).
В результате в вашем организме вырабатывается иммунитет против болезней, которым он подвержен (29).
Резюме Белки образуют антитела для защиты вашего тела от чужеродных захватчиков, таких как болезнетворные бактерии и вирусы.
Транспортные белки переносят вещества по кровотоку — в клетки, из клеток или внутри клеток.
Вещества, переносимые этими белками, включают питательные вещества, такие как витамины или минералы, сахар в крови, холестерин и кислород (30, 31, 32).
Например, гемоглобин — это белок, который переносит кислород из легких в ткани организма. Транспортеры глюкозы (GLUT) перемещают глюкозу к вашим клеткам, а липопротеины переносят холестерин и другие жиры в вашу кровь.
Белковые переносчики специфичны, то есть они связываются только с определенными веществами. Другими словами, переносчик белка, который перемещает глюкозу, не будет перемещать холестерин (33, 34).
Белки также выполняют роль хранилища. Ферритин — это запасной белок, в котором хранится железо (35).
Еще один запасной белок — казеин, который является основным белком молока, который помогает детям расти.
Резюме Некоторые белки переносят питательные вещества по всему телу, а другие накапливают их.
Белки могут снабжать ваш организм энергией.
Белок содержит четыре калории на грамм, то есть столько же энергии, что и углеводы. Наибольшее количество энергии обеспечивают жиры — девять калорий на грамм.
Однако последнее, что ваше тело хочет использовать для получения энергии, — это белок, так как это ценное питательное вещество широко используется в организме.
Углеводы и жиры намного лучше подходят для обеспечения энергией, поскольку ваше тело сохраняет резервы для использования в качестве топлива. Более того, они метаболизируются более эффективно по сравнению с белком (36).
На самом деле, в нормальных условиях белок обеспечивает организм очень малым количеством энергии.
Однако в состоянии голодания (18–48 часов без приема пищи) ваше тело разрушает скелетные мышцы, чтобы аминокислоты могли снабжать вас энергией (37, 38).
Ваше тело также использует аминокислоты из разрушенных скелетных мышц, если запасы углеводов недостаточны.Это может произойти после изнурительных упражнений или если вы в целом не потребляете достаточно калорий (39).
Резюме Белок может служить ценным источником энергии, но только в ситуациях голодания, изнурительных упражнений или недостаточного потребления калорий.
Белок играет в организме множество ролей.
Он помогает восстанавливать и укреплять ткани вашего тела, способствует метаболическим реакциям и координирует функции организма.
Помимо создания структурного каркаса для вашего тела, белки также поддерживают правильный pH и баланс жидкости.
Наконец, они укрепляют вашу иммунную систему, транспортируют и хранят питательные вещества и при необходимости могут действовать как источник энергии.
В совокупности эти функции делают белок одним из наиболее важных питательных веществ для вашего здоровья.
Вредно ли слишком много белка?
.
Что такое белки? Определение, функции, примеры белка

 Гемоглобин — это белок, состоящий из четырех полипептидных субъединиц. (Ричард Уиллер)
Гемоглобин — это белок, состоящий из четырех полипептидных субъединиц. (Ричард Уиллер)
Белки — это большой класс биологических молекул, состоящих из цепочек аминокислот, называемых полипептидами. Один полипептид может образовывать белок, хотя многие белки состоят из нескольких полипептидных субъединиц.
ФУНКЦИИ БЕЛКОВ
Белки выполняют важные функции в организмах. Фактически, этот класс молекул находится в каждой клетке и необходим для жизни.Вот несколько примеров функций, выполняемых белками:
- образуют каркас, который поддерживает форму клетки
- катализирует метаболические реакции
- необходим в рационе животных как источник определенных аминокислот
- транспортирует молекулы внутри клеток и по всему организму
- незаменим для репликации ДНК
- действуют в иммунном ответе
СТРУКТУРА БЕЛКА
Белок может состоять из одного полипептида или нескольких полипептидных субъединиц.Некоторые белки включают непептидные группы, называемые кофакторами. Кофактором может быть органическая группа (например, кофермент, простетическая группа) или неорганическая группа (например, ион металла или кластер железо-сера).
Каждый полипептид представляет собой линейную молекулу, состоящую из цепочки аминокислот, которые связаны в цепь пептидными связями. ДНК или РНК организма кодируют последовательность аминокислот, образующих белки. Построение каждой аминокислотной цепи из генетического кода называется трансляцией . После трансляции полипептид обычно претерпевает дополнительные химические изменения, называемые посттрансляционной модификацией.
ПРИМЕРЫ БЕЛКОВ
Белки широко используются в повседневной жизни. Большая часть структуры органов и тканей состоит из белков. Вот несколько примеров:
- кератин
- актин
- миозин
- гемоглобин
- коллаген
- эластин
- альбумин
- фибрин
- инсулин
- иммуноглобулины (антитела)
- каталаза (и все ферменты)
.
функций белков | 5 основных функций, что, где и как
Белки — это самые распространенные органические молекулы, присутствующие на Земле. Они в изобилии присутствуют в каждой живой клетке. Белки — это полимеры, состоящие из тысяч аминокислот, связанных пептидными связями. Длинные цепи аминокислот, известные как полипептиды, складываются вокруг себя несколькими способами, образуя сложные структуры, называемые белками.
Функции, выполняемые белками, можно разделить на различные категории.Некоторые функции необходимы на клеточном уровне, в то время как другие необходимы для лучшей работы организма в целом. Здесь мы попытаемся понять различные функции, выполняемые белками в нашем организме, на различных примерах.
Все ферменты — это белки


Ферменты — это белки, которые необходимы для любой химической реакции в нашем организме. Они катализируют биохимическую реакцию, чтобы жизнь продолжалась.
Пример ферментативной реакции в нашем организме — гликолиз.Это процесс высвобождения энергии из молекулы глюкозы. Эта энергия требуется для выполнения нескольких процессов, происходящих внутри клетки. Процесс гликолиза включает около 10 этапов, каждый из которых требует определенного фермента. Отсутствие единственного фермента останавливает процесс, и энергия из глюкозы не может быть получена.
Для синтеза белков также необходимы определенные ферменты. Синтез белка включает транскрипцию ДНК в мРНК, а затем трансляцию мРНК рибосомами.Оба эти шага требуют ферментов, которые являются белками. Например;
- РНК-полимераза — это фермент, необходимый для соединения нуклеотидов РНК в процессе транскрипции.
- Аминоацил тРНК синтетаза — это фермент, который присоединяет определенные аминокислоты к тРНК, чтобы ее можно было использовать в синтезе белка.
Таким образом, от получения энергии до производства белков, все химические процессы в живых организмах нуждаются в ферментах, и все ферменты являются белками. Роль белков как ферментов — самая важная и важная функция, выполняемая белками.
Белки действуют как рецепторы на клеточных мембранах
Белки являются важными компонентами всех клеточных мембран и мембран органелл. Одна из функций этих мембранных белков состоит в том, что они действуют как рецепторы. Гормоны, нейротрансмиттеры и другие сигнальные молекулы связываются с этими рецепторами и передают сигналы клеткам. Таким образом, белки играют роль в передаче сигналов клетками, которая необходима для скоординированной функции всех клеток, присутствующих в нашем теле. Рассмотрим следующий пример, чтобы понять роль белков как рецепторов.
- Инсулин — это гормон, контролирующий уровень глюкозы в крови. Он выполняет свою функцию, связываясь со своим рецептором, который является белком. Инсулин связывается со своим рецептором, который посылает сигналы для открытия каналов глюкозы, так что глюкоза может поступать из крови в печень и мышечные клетки. Если рецепторы инсулина отсутствуют, уровень глюкозы в крови нельзя регулировать.
Этот и другие различные примеры в нашем организме доказывают, почему белки необходимы для передачи сигналов клетками и координации клеточных функций.
Некоторые гормоны также являются белками
Белки действуют не только как клеточные рецепторы, но и как гормоны. Инсулин и глюкагон — два гормона, которые по своей природе являются белками. Оба эти гормона необходимы для регулирования уровня глюкозы в крови. Они контролируют поглощение и высвобождение глюкозы клетками, гликолиз и глюконеогенез, а также синтез и деградацию гликогена. Роли этих гормонов в нашем организме перечислены ниже;
- Инсулин высвобождается поджелудочной железой при высоком уровне глюкозы в крови.Он способствует усвоению клетками глюкозы, ее расщеплению, а также хранению в виде гликогена. Он также подавляет синтез новых молекул глюкозы из неуглеводных источников (глюконеогенез).
- Глюкагон высвобождается поджелудочной железой при низком уровне глюкозы в крови. Он способствует расщеплению гликогена с высвобождением глюкозы. Он также способствует глюконеогенезу.
Белки действуют как транспортные каналы в клеточных мембранах
Белки, присутствующие в клеточных мембранах, также действуют как транспортные каналы.Вещества, которые не проницаемы через мембраны из-за своего размера или заряда, могут проникать в клетку через эти белковые каналы. Один белковый канал специфичен для одного или нескольких веществ. Примеры белковых каналов приведены ниже;
- Аквапорины — это белковые каналы, которые позволяют молекулам воды проходить через клетки
- GLUT (переносчик глюкозы) — переносчики молекул глюкозы
- Натриевые каналы позволяют проходить ионам натрия внутри клетки
- Калиевые каналы пропускают только калий ионы проходят через них
- Кальциевые каналы характерны только для ионов кальция
Это несколько примеров белковых каналов, присутствующих в мембранах.
Белки поддерживают форму и структуру клетки
Это еще одна важная клеточная функция, выполняемая белками. Цитоскелет состоит из нескольких связанных между собой белковых нитей. Белки в цитоскелете организованы в виде микротрубочек, микрофиламентов и промежуточных филаментов. Все эти компоненты цитоскелета расположены определенным образом, сохраняя форму клетки. Важные белки, из которых состоит цитоскелет, включают актин и тубулин.В отсутствие этих белков клетка не могла бы поддерживать свою структуру.
Белки участвуют в делении клеток
Деление клеток — это процесс, посредством которого зрелая взрослая родительская клетка делится на дочерние клетки. Белки также необходимы для этого процесса.
Во время деления клетки хромосомы разделяются на две половины путем отрыва. Это разделение хромосом осуществляется белками, известными как волокна веретена.
Белки также необходимы для деления цитоплазмы, которое происходит после разделения хромосом.
Белки необходимы для транспорта внутри клетки
Определенные транспортные белки необходимы для внутриклеточного транспорта различных веществ. Различные белки, которые участвуют во внутриклеточных белках, известны как моторные белки. Эти белки используют энергию в форме АТФ и перемещаются по микротрубочкам для транспортировки различных веществ в цитоплазме клетки. Примером моторных белков является белок кинезин. Он участвует в транспорте различных веществ в аксонах нейронов.
Белки необходимы для транспорта кислорода
Эта функция белков важна для выживания организма в целом. В этом процессе участвуют два белка, гемоглобин и миоглобин.
Гемоглобин


Это белок, присутствующий в красных кровяных тельцах. Гемоглобин состоит из четырех полипептидных цепей, двух альфа-цепей и двух бета-цепей, которые намотаны друг на друга. Каждая из этих полипептидных цепей несет одну гемовую группу (содержащую атом железа).
Этот белок отвечает за перенос кислорода из легких в тканевую жидкость. Одна молекула кислорода может связываться с четырьмя молекулами кислорода. Он связывается с молекулами кислорода, присутствующими в воздухе, проходя через легкие. Эти молекулы кислорода высвобождаются, когда кровь проходит через ткани.
Любой недостаток или отклонение от нормы гемоглобина нарушает перенос кислорода кровью. Наши клетки не могут выжить без кислорода. Любое нарушение подачи кислорода приведет к гибели клеток в пораженных тканях.
Миоглобин
Миоглобин — еще один белок, участвующий в транспортировке кислорода. Он состоит из одной полипептидной цепи с гемовой группой. Это цитоплазматический белок, имеющий более высокое сродство к молекулам кислорода, что означает, что он может связываться с кислородом даже при высокой концентрации кислорода. Его функция — транспортировать кислород из тканевой жидкости к клеткам.
Из-за своего высокого сродства к кислороду миоглобин выделяет кислород в очень низких концентрациях. Эта особенность миоглобина отвечает за хранение кислорода в тканях.
Белки необходимы для транспортировки различных веществ в крови
Хотя кровь действует как транспортная среда, белки необходимы для удержания и транспортировки некоторых веществ, которые не могут растворяться в крови. Эта функция белков также важна для правильного функционирования организма. Некоторые примеры транспортных белков, присутствующих в крови, следующие.
- Альбумин является основным транспортным белком крови. Он действует как переносчик жирных кислот, стероидов, гормонов щитовидной железы, липофильных препаратов, тяжелых металлов, ионов кальция и билирубина.
- Преальбумин — еще один транспортный белок в крови, который переносит стероидные гормоны, тироксин и витамин A.
- Гаптоглобин является транспортным средством. белок, несущий свободный гемоглобин, присутствующий в плазме
- Связывающий тироксин белок специфичен для гормона щитовидной железы
- ЛПВП — это липопротеин, который транспортирует холестерин из тканей в печень
- ЛПНП — еще один липопротеин, который транспортирует холестерин из печени в ткани
Белки участвуют в сокращении мышц
Сокращение мышц — это процесс, который позволяет нам выполнять повседневные задачи, такие как ходьба, бег, сидение, стояние, письмо и даже речь.Этот процесс сокращения мышц также происходит из-за белков. Сократительные белки присутствуют в мышечных волокнах. Эти белки взаимодействуют определенным образом, что позволяет сокращать и расслаблять мышцы. Наиболее важные сократительные присутствия:


Белки предотвращают отек
Отек — это состояние, при котором избыточная жидкость вытекает из кровеносных сосудов и собирается в тканевых пространствах. Потеря жидкости из крови приводит к снижению артериального давления. Это потенциально смертельное состояние, которое может поставить под угрозу эффективную доставку крови к тканям организма.
Белки, присутствующие в крови, известные как белки плазмы, предотвращают утечку жидкости через капилляры благодаря своему осмотическому эффекту. Онкотическое давление из-за белков плазмы удерживает воду в кровеносных сосудах, предотвращая ее попадание в тканевые жидкости, предотвращая отек. Если эти белки отсутствуют, отек развивается в разных частях тела.
Белки защищают наш организм от болезней
Эту функцию выполняют антитела. Антитела или иммуноглобулины — это белки плазмы, которые вырабатываются в ответ на попадание различных болезнетворных агентов в наш организм.Они борются с этими патогенами и защищают наш организм от их вредного воздействия. Если в нашем организме уже присутствуют антитела против патогена, они уничтожают патоген до того, как он вызовет какое-либо заболевание. Этот процесс известен как иммунитет.
Белки необходимы для пищеварения
Процесс пищеварения включает расщепление сложных веществ, присутствующих в нашем рационе, на более простые, чтобы они могли всасываться в кровь. Расщепление различных диетических веществ на более простые молекулы происходит в нашей пищеварительной системе ферментами, которые по своей природе являются белками.
Белки также действуют как запасные вещества
Белки представляют собой полимеры аминокислот. Они действуют как запасные вещества, в которых хранятся тысячи аминокислот. Эти аминокислоты высвобождаются из белков, когда они необходимы организму. Примеры запасных белков:
- Казеин в молоке
- Альбумин в яйце
Эти белки обеспечивают незаменимые аминокислоты, необходимые организму для производства нескольких белков. Более того, во время голодания белки, присутствующие в организме, также могут использоваться в качестве источника энергии для обеспечения калорий, необходимых для выполнения различных функций организма.
Белки контролируют экспрессию генов
Экспрессия генов — это процесс, посредством которого информация в конкретном гене копируется в форме мРНК, а позже эта мРНК используется рибосомами для создания белка, кодируемого этим геном.
Этот процесс экспрессии генов контролируется факторами транскрипции. Эти факторы транскрипции позволяют транскрипцию генов только тех белков, которые в настоящее время необходимы организму.
Факторы транскрипции также являются белками по своей природе.Таким образом, белки регулируют свой собственный синтез, регулируя экспрессию генов.
Резюме
Белки — это полимеры, состоящие из аминокислот. Они участвуют практически во всех процессах, происходящих в нашем организме. Сводка функций, выполняемых белками, выглядит следующим образом;
- Как ферменты, белки необходимы для всех химических процессов в живых организмах
- Как гормоны и клеточные рецепторы, они необходимы для передачи сигналов и координации клеток
- Как транспортные каналы, белки необходимы для проникновения ионов и более -размерные частицы в клетки
- Являясь компонентами цитоскелета, они поддерживают форму клеток
- Волокна веретена — это белковые волокна, которые необходимы для деления клеток
- Гемоглобин и миоглобин являются белками, необходимыми для транспорта кислорода
- Альбумин и другая плазма белки необходимы для транспорта липидов, лекарств и других веществ в крови
- Сократительные белки необходимы для сокращения мышц
- Антитела — это белки, которые защищают наш организм от вредоносных болезней
- Белки плазмы поддерживают баланс жидкости в нашем организме
- Они регулируют экспрессию генов.
- Белки также обеспечивают к телу во время голода
Ссылки
- Lodish H, Berk A, Matsudaira P, Kaiser CA, Krieger M, Scott MP, Zipurksy SL, Darnell J (2004).Молекулярная клеточная биология (5-е изд.). Нью-Йорк, Нью-Йорк: WH Freeman and Company
- Zhang C, Kim SH (февраль 2003 г.). «Обзор структурной геномики: от структуры к функции» . Текущее мнение в химической биологии. 7 (1): 28–32. DOI : 10.1016 / S1367-5931 (02) 00015-7 . PMID 12547423
- Sleator RD (2012).«Прогнозирование функций белков». Функциональная геномика. Методы молекулярной биологии. 815 . С. 15–24. DOI : 10.1007 / 978-1-61779-424-7_2 . ISBN 978-1-61779-423-0 . PMID 22130980
.
6 Основные функции белков | Здоровое питание
Эллен Свонсон Topness Обновлено 20 декабря 2018 г.
Белок — важное вещество, которое содержится в каждой клетке человеческого тела. На самом деле, за исключением воды, белок — самое распространенное вещество в вашем теле. Этот белок вырабатывается вашим организмом с использованием потребляемых вами пищевых белков. Он используется во многих жизненно важных процессах и поэтому требует постоянной замены. Вы можете добиться этого, регулярно потребляя продукты, содержащие белок.
Ремонт и техническое обслуживание
Белок называют строительным блоком организма. Это называется так, потому что белок жизненно важен для поддержания тканей тела, включая развитие и восстановление. Волосы, кожа, глаза, мышцы и органы состоят из белка. Вот почему детям нужно больше белка на фунт веса тела, чем взрослым; они растут и развивают новые белковые ткани.
Энергия
Белок является основным источником энергии. Если вы потребляете больше белка, чем нужно для поддержания тканей тела и других необходимых функций, ваше тело будет использовать его для получения энергии.Если в этом нет необходимости из-за достаточного потребления других источников энергии, таких как углеводы, белок будет использоваться для создания жира и становится частью жировых клеток.
Гормоны
Белок участвует в выработке некоторых гормонов. Эти вещества помогают контролировать функции организма, связанные с взаимодействием нескольких органов. Инсулин, небольшой белок, является примером гормона, регулирующего уровень сахара в крови. Он предполагает взаимодействие таких органов, как поджелудочная железа и печень.Секретин — еще один пример белкового гормона. Это вещество помогает в процессе пищеварения, стимулируя поджелудочную железу и кишечник, чтобы вырабатывать необходимые пищеварительные соки.
Ферменты
Ферменты — это белки, которые увеличивают скорость химических реакций в организме. Фактически, большинство необходимых химических реакций в организме не могло бы происходить эффективно без ферментов. Например, один тип ферментов помогает переваривать большие молекулы белка, углеводов и жиров в более мелкие молекулы, а другой помогает создавать ДНК.
Транспортировка и хранение молекул
Белок является важным элементом в транспортировке определенных молекул. Например, гемоглобин — это белок, который переносит кислород по всему телу. Белок также иногда используется для хранения определенных молекул. Ферритин — это пример белка, который в сочетании с железом хранится в печени.
Антитела
Белок образует антитела, которые помогают предотвратить инфекции, болезни и болезни. Эти белки идентифицируют и помогают уничтожить антигены, такие как бактерии и вирусы.Они часто работают вместе с другими клетками иммунной системы. Например, эти антитела идентифицируют антигены и затем окружают их, чтобы удерживать их, пока они не будут уничтожены лейкоцитами.
.