Строение белков
Среди органических веществ белки, или протеины, — самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 — 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами. Кроме углерода, кислорода, водорода и азота, в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (—NH2) с основными свойствами, другая — карбоксильной группой (—COOH) с кислотными свойствами. Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами.
Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами.
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между —CO- и —NH- группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру.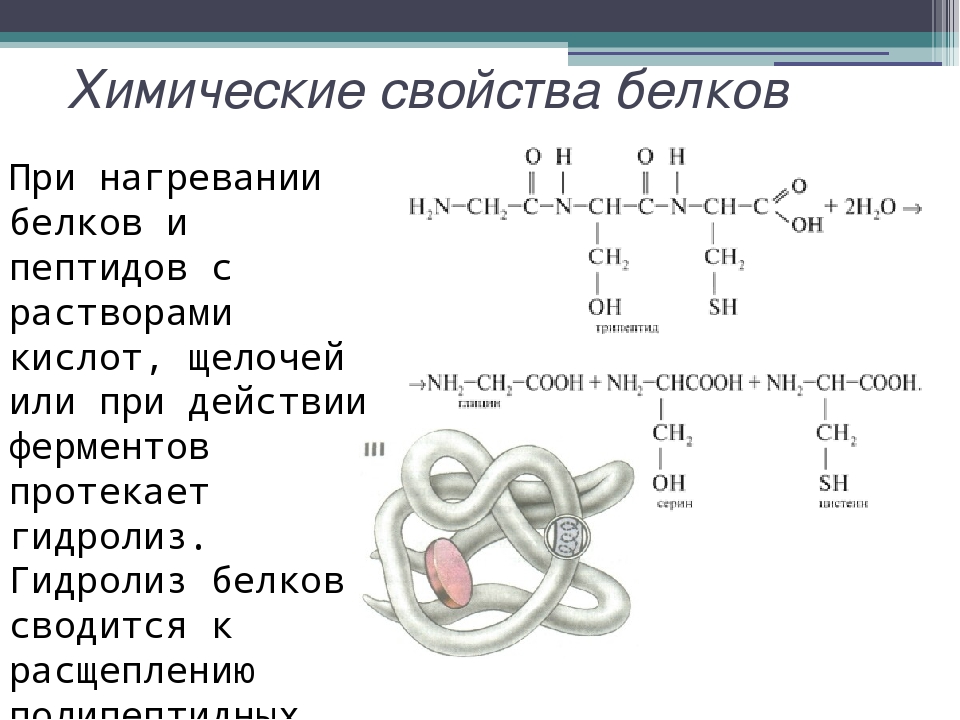 Эта спираль — вторичная структура белка.
Эта спираль — вторичная структура белка.
Третичная структура — трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация — глобула. Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков, состоящих только из аминокислот, есть еще и сложные белки
Другие заметки по биологии
Строение белков — урок. Химия, 8–9 класс.
Белки являются обязательной составной частью любого живого организма и играют важнейшую роль в обеспечении процессов жизнедеятельности.
В состав белков обязательно входят четыре химических элемента: углерод, водород, кислород и азот. Многие белки содержат серу. В состав некоторых входит фосфор. Есть белки, содержащие атомы металлов.
Белки — природные высокомолекулярные вещества (полимеры), состоящие из остатков аминокислот.
Аминокислотные остатки соединены в макромолекулах белков пептидной группой −NH−CO−, поэтому белки относят к полипептидам.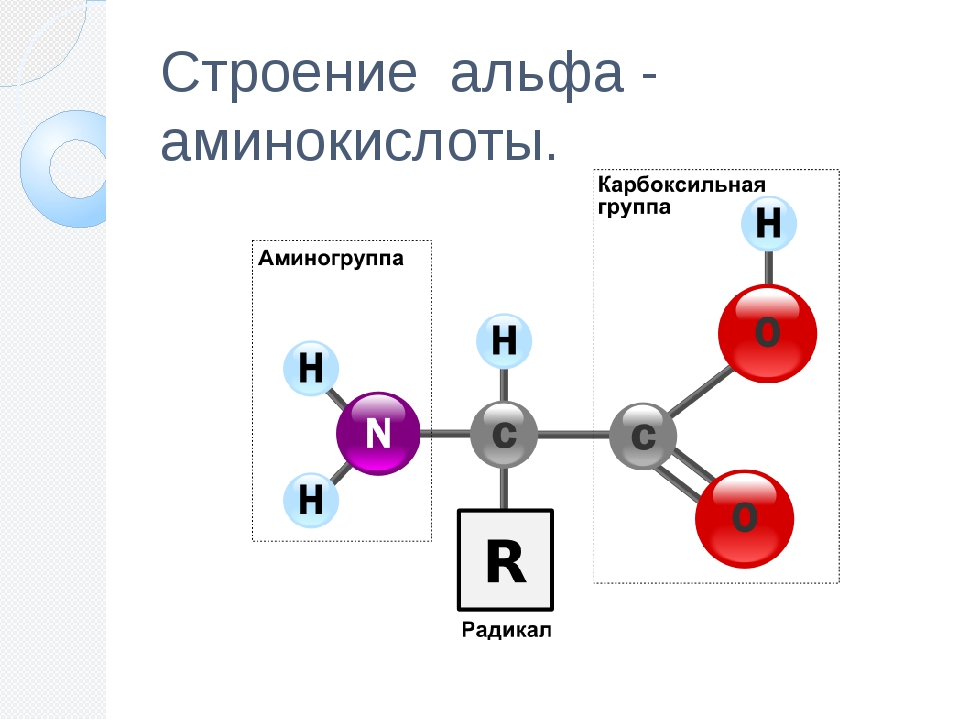
В состав белков входят двадцать аминокислот строения Nh3−C|H−COOHR. Аминокислотные остатки соединяются в макромолекулы белков в различной последовательности. Число аминокислотных остатков в молекулах тоже может быть разное. Поэтому разнообразие белков практически безгранично и у каждого живого существа набор белковых молекул особый, неповторимый.
Белковые молекулы могут содержать от одного до нескольких сотен и даже тысяч аминокислотных остатков, поэтому их относительные молекулярные массы изменяются от десятков тысяч до нескольких миллионов. Так, относительная молекулярная масса гемоглобина равна \(68 000\), яичного белка — \(44 000\), а вируса гриппа — \(32 000 000\).
Свойства белка в первую очередь определяются порядком соединения аминокислотных остатков в полипептидной цепи.
Последовательность аминокислотных остатков в макромолекуле называется первичной структурой белка.
Первичная структура
Существуют вторичная (спираль) и третичная (клубок) структуры белковых молекул. Они образуются в результате внутримолекулярного взаимодействия частей полипептидной цепи.
Они образуются в результате внутримолекулярного взаимодействия частей полипептидной цепи.
Вторичная структура
Третичная структура
Несколько белковых молекул могут соединяться друг с другом и образовывать четвертичную структуру.
Четвертичная структура
Сложнейшая задача молекулярной биологии покорилась искусственному интеллекту
Более полувека ученые-биологи бились над проблемой предсказания трехмерной структуры белка по составляющим его аминокислотам. Хотя и решаемая, эта задача требовала огромных вычислительных ресурсов. Теперь же благодаря алгоритмам глубинного машинного обучения процесс, занимавший месяцы, может сократиться до пары недель или — на мощном оборудовании — нескольких часов.
Белковые молекулы — цепочки, составленные из аминокислот — представляют собой основу жизни и являются основным предметом изучения в молекулярной биологии, биохимии и многих областях медицины. Однако зная лишь формулу белка, предсказать варианты его взаимодействия с другими молекулами и клетками (а, значит, функции белка в организме) невозможно. Дело в том, что его свойства зависят от формы «укладки» полипептидной цепочки — а на эту форму влияет огромное число факторов. Например, гидрофобность, гидрофильность или электрический заряд составляющих белок аминокислот.
Однако зная лишь формулу белка, предсказать варианты его взаимодействия с другими молекулами и клетками (а, значит, функции белка в организме) невозможно. Дело в том, что его свойства зависят от формы «укладки» полипептидной цепочки — а на эту форму влияет огромное число факторов. Например, гидрофобность, гидрофильность или электрический заряд составляющих белок аминокислот.
Решить так называемую задачу фолдинга («укладки») белка с достаточной точностью смогла последняя версия разработанного британской компанией DeepMind (принадлежит, наряду с Google, холдингу Alphabet) алгоритма AlphaFold. В компании накануне сообщили, что их разработку признали эффективной (точность предсказания — выше 90%) организаторы программы мониторинга исследований в области предсказания структуры белка (Critical Assessment of protein Structure Prediction, CASP).
Не имея способа быстро предсказывать пространственную структуру белка, ученые прибегали к сложным и дорогостоящим техникам — от спектроскопии ядерного магнитного резонанса до рентгеноструктурного анализа. Однако все они так или иначе подразумевали поиск решения методом проб и ошибок. Новый вычислительный инструмент позволит, в частности, гораздо быстрее находить лекарства от многих болезней или создавать белки-ферменты, которые смогут эффективно перерабатывать загрязняющие окружающую среду вещества.
Однако все они так или иначе подразумевали поиск решения методом проб и ошибок. Новый вычислительный инструмент позволит, в частности, гораздо быстрее находить лекарства от многих болезней или создавать белки-ферменты, которые смогут эффективно перерабатывать загрязняющие окружающую среду вещества.
Первую версию AlphaFold DeepMind представила в 2018-м году — уже тогда это решение лидировало по эффективности среди аналогов в предыдущем обзоре CASP. С тех пор алгоритм, основанный на глубинном обучении, был усовершенствован с учетом последних открытий в области биологии, физики и искусственного интеллекта. Тренировали его на доступных данных о примерно 170 000 белковых структур, а также базах данных о белках с известной последовательностью аминокислот, но неизвестной структурой.
Урок 12. аминокислоты. белки — Химия — 10 класс
Химия, 10 класс
Урок № 12. Аминокислоты. Белки
Перечень вопросов, рассматриваемых в теме: урок посвящён аминокислотам, их строению, номенклатуре, знакомству с пептидной группой и пептидной связью, химическими свойствами аминокислот, пептидам и полипептидам, знакомству с глицином как представителем аминокислот, биологической роли аминокислот, белкам, их структуре, химическим свойствам.
Глоссарий
Аминокислота – это азотсодержащее органическое соединение, в составе которой есть как аминогруппа, так и карбоксильная группа.
Белки – органические полимеры, в состав которых входят остатки аминокислот, соединённые пептидной связью. Количество аминокислотных остатков в белках обычно более 50.
Биуретовая реакция – качественная цветная реакция на пептидные связи. При добавлении к белку раствора щёлочи и сульфата меди (II) раствор приобретает красно-фиолетовую окраску.
Гидролиз белка – распад белка на отдельные аминокислоты в водном растворе кислот или щелочей.
Денатурация белка – разрушение вторичной, третичной и четвертичной структуры белка при нагревании, действии растворов солей тяжёлых металлов, кислот и щелочей. При денатурации белок сворачивается и выпадает в осадок.
Ксантопротеиновая реакция – качественная цветная реакция концентрированной азотной кислоты с белками, содержащими остатки ароматических аминокислот. При добавлении концентрированной азотной кислоты к белку и нагревании сначала происходит денатурация белка, а затем появляется жёлтое окрашивание.
При добавлении концентрированной азотной кислоты к белку и нагревании сначала происходит денатурация белка, а затем появляется жёлтое окрашивание.
Олигопептиды – органические соединения, состоящие из 10–20 остатков аминокислот, связанных пептидными связями.
Пептидная группа – группа атомов в составе пептидов, состоящая из атомов углерода, кислорода, азота и водорода.
Пептидная связь – связь между атомами углерода и азота в пептидной группе.
Пептиды – органические соединения, состоящие из нескольких аминокислотных остатков, соединённых пептидной связью.
Полипептиды – макромолекулы, состоящие из 20–50 аминокислотных остатков, соединенных пептидной связью.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии.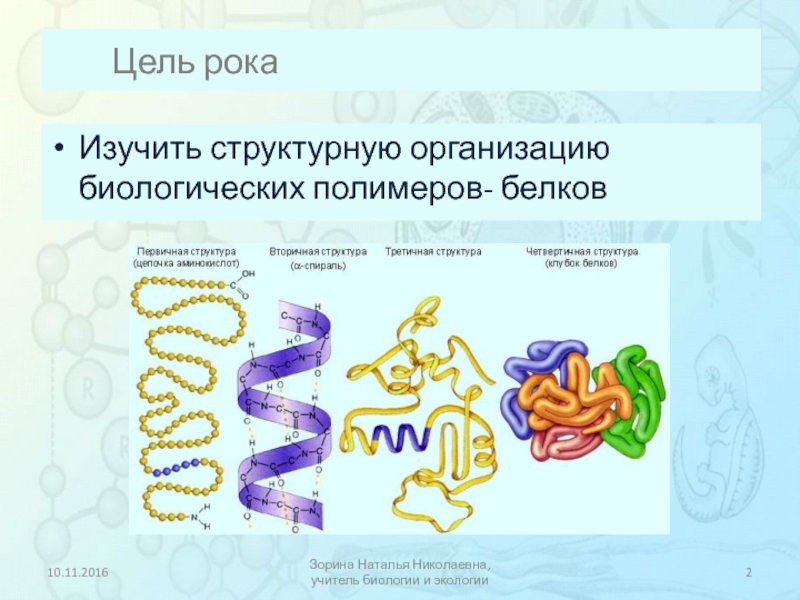 К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Аминокислоты – это азотсодержащие органические соединения, в состав которых входят как аминогруппа, так и карбоксильная группа
Простейшим представителем аминокислот является глицин – аминоуксусная (аминоэтановая) кислота
По международной номенклатуре нумерация углеродных атомов начинается от углерода карбоксильной группы.
Достаточно часто в литературе можно встретить обозначения углеродных атомов в аминокислотах с помощью букв греческого алфавита. При этом атом углерода карбонильной группы не имеет обозначения.
При этом атом углерода карбонильной группы не имеет обозначения.
Для некоторых аминокислот существуют тривиальные названия.
Изомеры аминокислот различаются строением углеводородного радикала и положением аминогруппы.
Все α-аминокислоты, кроме глицина, имеют в своем составе асимметрический атом, который следует сразу за карбоксильной группой. У этого атома углерода все заместители разные.
Благодаря этому атому, для α-аминокислот характерна оптическая изомерия. В природе распространены только L-α-аминокислоты.
Биологическое значение аминокислот
Из аминокислот наибольшее значение имеют α-аминокислоты, так как они входят в состав белковых молекул, из которых построено всё живое вещество.
Растения и бактерии способны самостоятельно синтезировать все необходимые для них аминокислоты. Млекопитающие, в том числе и человек, не могут синтезировать ряд аминокислот, они должны поступать в организм с пищей. К таким незаменимым аминокислотам относятся метионин, треонин, фенилаланин, лейцин, изолейцин, валин, лизин, триптофан.
α-Аминокислоты необходимы человеку для образования белков. Большую часть аминокислот для этих целей человек получает с пищей. Некоторые аминокислоты можно синтезировать. Для регулирования обменных процессов аминокислоты применяются как лекарства (например, глицин).
Получение аминокислот
В промышленности α-аминокислоты получают гидролизом белков.
Можно синтезировать аминокислоты из хлорпроизводных карбоновых кислот и аммиака.
Cl-CH2-COOH + 2NH3 → NH2-CH2-COOH + NH4Cl
Физические и химические свойства аминокислот
Аминокислоты – кристаллические вещества без цвета и запаха, сладковатые на вкус. Хорошо растворяются в воде.
Аминокислоты – амфотерные соединения, так как аминогруппа проявляет основные свойства, а карбоксильная группа – кислотные.
Карбоксильная группа в составе аминокислот позволяет им реагировать со спиртами. В результате реакции образуются сложные эфиры.
Ион водорода от карбоксильной группы может переходить к аминогруппе, в результате образуется биполярный ион.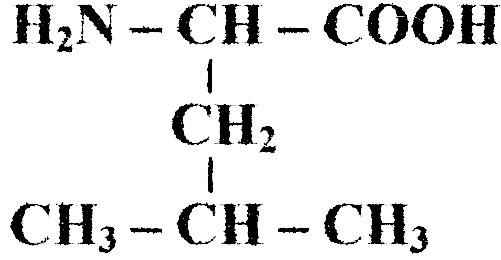
Пептиды
Аминокислоты могут реагировать друг с другом, аминогруппа одной кислоты соединяется с карбоксильной группой другой кислоты, при этом происходит выделение воды.
Группа атомов СО-NH называется пептидной (или амидной) группой, а связь между атомами углерода и азота – пептидной (амидной) связью.
Соединения, образованные из нескольких аминокислот с помощью пептидной связи, называются пептидами.
Называют пептиды перечислением тривиальных названий аминокислот, входящих в состав пептида, начиная с аминокислотного остатка со свободной аминогруппой (N-конец), заменяя в названии аминокислот окончание «ин» на «ил». Последней называют аминокислоту со свободной карбоксильной группой (С-конец), её название не изменяется. Часто название пептида записывают с помощью трёхбуквенных латинских сокращённых наименований аминокислот.
Молекулы, в состав которых входит 10–20 остатков аминокислот, называют олигопептидами.
Макромолекулы, образованные 20–50 остатками аминокислот называют полипептидами.
Полипептиды входят в состав многих гормонов. Нейропептиды регулируют работу мозга, процессы сна, обучения, обладают обезболивающим эффектом.
Белки
Полипептиды, содержащие в своём составе более 50 остатков аминокислот, называются белками. Это природные полимеры, которые образуют клетки всех живых организмов. Без белков невозможны обмен веществ, размножение и рост живых организмов.
Белки образованы атомами углерода, водорода, кислорода и азота. Кроме этих атомов, макромолекулы белков могут содержать атомы фосфора, серы, железа и других элементов.
Относительная молекулярная масса белковых молекул может быть от нескольких десятков до сотен атомных единиц массы.
Структура белков
Последовательность остатков аминокислот в молекуле белка образует первичную структуру белка.
Между атомом кислорода в группе С=О и атомом водорода в амидной группе – NH – образуется водородная связь, в результате чего макромолекула белка закручивается в спираль.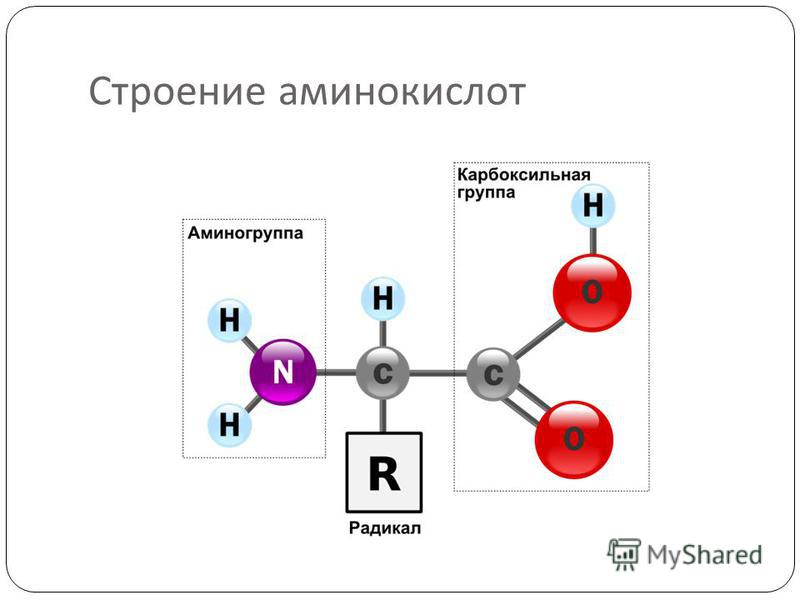 Образуется вторичная структура белка.
Образуется вторичная структура белка.
Функциональные группы, расположенные на внешней стороне спирали, могут взаимодействовать с другими функциональными группами этой же макромолекулы. Например, между атомами серы образуется сульфидный мостик, между карбоксильной и гидроксильной группами возникает сложноэфирный мостик.
В результате образуется третичная структура белка, которая определяет специфическую биологическую активность белков. Именно благодаря уникальной третичной структуре биологические катализаторы – ферменты обладают уникальной избирательностью.
Благодаря различным функциональным группам белковые молекулы могут соединяться друг с другом, в результате формируется четвертичная структура белка.
Химические свойства белков
В зависимости от молекулярной массы и функциональных групп белки могут как хорошо растворяться в воде, так и не растворяться в ней.
Под действием температуры, растворов солей тяжёлых металлов, кислот и щелочей происходит разрушение вторичной, третичной и четвертичной структуры белка, называемое денатурацией.
При нагревании в присутствии кислоты или щёлочи белки подвергаются гидролизу, распадаясь на исходные аминокислоты.
Белки в щелочной среде в присутствии сульфата меди (II) окрашивают раствор в красно-фиолетовый цвет. Это реакция на пептидную группу (биуретовая реакция).
Концентрированная азотная кислота при нагревании окрашивает белки в жёлтый цвет, если в состав белка входят остатки ароматических аминокислот, например, фенилаланина (ксантопротеиновая реакция).
Для обнаружения в составе белка атомов серы проводят реакцию с ацетатом свинца в щелочной среде при нагревании. В результате образуется чёрный осадок (цистеиновая реакция).
Превращения белков в организме
Белки являются обязательными компонентами в пищевом рационе человека. В организме человека белки, поступившие с пищей, под действием ферментов подвергаются гидролизу и разлагаются на отдельные аминокислоты. Эти аминокислоты – строительный материал для образования новых белков, необходимых человеку. Для синтеза белков необходима энергия, которую поставляет в организме АТФ. Также энергия выделяется при распаде жиров и углеводов. Кроме синтеза белков происходит их распад с образованием углекислого газа, аммиака, мочевины и воды.
Для синтеза белков необходима энергия, которую поставляет в организме АТФ. Также энергия выделяется при распаде жиров и углеводов. Кроме синтеза белков происходит их распад с образованием углекислого газа, аммиака, мочевины и воды.
Успехи в изучении и синтезе белков
В 1954 г. британский биолог Фредерик Сенгер впервые расшифровал строение белка инсулина. Каждая молекула инсулина состоит из двух полипептидов, в одном из которых 21 остаток аминокислоты, а в другом – 30 аминокислотных остатков.
В 1967 г. был создан прибор – секвенатор, позволяющий определять последовательность остатков аминокислот в макромолекуле белка.
Первый белок, синтезированный в лаборатории в 1953 г. был окситоцин.
В настоящее время развивается наука, которая занимается синтезом искусственных белков, – генная инженерия.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Решение задачи на вычисление массовой доли элемента в молекуле аминокислоты.
Условие задачи: вычислите массовую долю азота в молекуле аспаргина
. Ответ запишите с точностью до десятых долей.
Ответ запишите с точностью до десятых долей.
Шаг первый: вычислить относительную молекулярную массу молекулы аспаргина:
М = 4·12 + 8·1 + 2·14 + 3·16 = 132 а.е.м.
Шаг второй: определить количество атомов азота в молекуле аспаргина и определить их относительную атомную массу:
2·14 = 28 а.е.м.
Шаг третий: определить массовую долю азота как отношение относительной атомной массы азота к относительной молекулярной массе аспаргина:
(28 : 132)·100 = 21,2 %.
Ответ: 21,2.
2. Решение задачи на определение количества различных олигопептидов, которые можно получить из определённого набора аминокислот.
Условие задачи: Сколько ди- и трипептидов можно составить из двух молекул аланина и одной молекулы цистеина?
Шаг первый: определить количество возможных дипептидов.
Из двух молекул аланина и одной молекулы цистеина можно составить три дипептида: Ala-Ala, Ala-Cys и Cys-Ala (два последних дипептида – разные соединения, так как в молекуле Ala-Cys карбоксильная группа аланина соединяется с аминогруппой цистеина, а в молекуле Cys-Ala карбоксильная группа цистеина соединяется с аминогруппой аланина).
Шаг второй: определить количество возможных трипептидов.
Ala-Ala-Cys, Ala-Cys-Ala, Cys-Ala-Ala – возможно составить 3 трипептида.
Ответ: 3 дипептида и 3 трипептида.
Белки. Химические и физические свойства. Биологические функции.
Белки — высокомолекулярные органические соединения, состоящие из остатков аминокислот, соединённых в длинную цепочку пептидной связью.
В состав белков живых организмов входит всего 20 типов аминокислот, все из которых относятся к альфа-аминокислотами, а аминокислотный состав белков и их порядок соединения друг с другом определяются индивидуальным генетическим кодом живого организма.
Одной из особенностей белков является их способность самопроизвольно формировать пространственные структуры характерные только для данного конкретного белка.
| первичная | последовательность соединения остатков аминокислот | |
| вторичная |
локальное упорядочивание фрагмента полипептидной цепи в спирали |
|
| третичная |
пространственная ориентация полипептидной спирали или способ ее укладки определенном объеме в глобулы (клубки) или фибриллы (нити) |
Из-за специфики своего строения белки могут обладать разнообразными свойствами.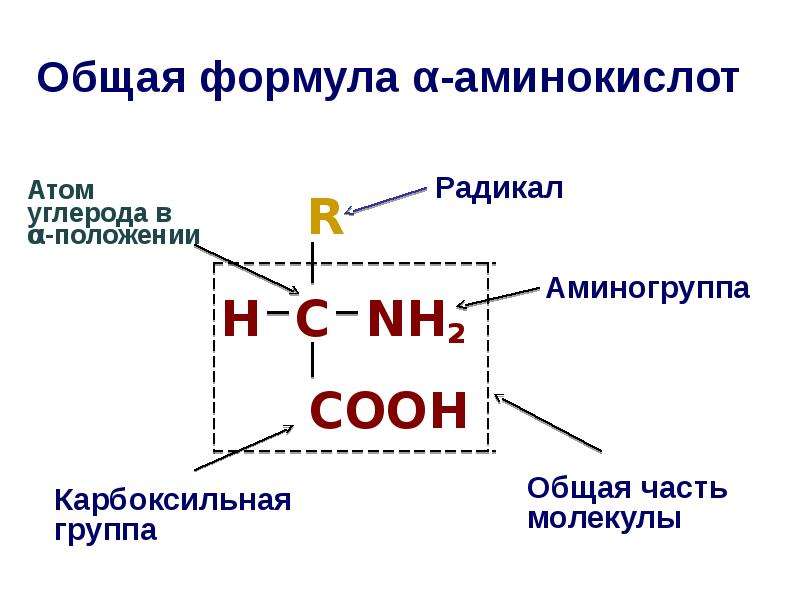 Например, белки, имеющие глобулярную четвертичную структуру, в частности белок куриного яйца, растворяются в воде с образованием коллоидных растворов. Белки, обладающие фибриллярной четвертичной структурой в воде не растворяются. Фибриллярными белками, в частности, образованы ногти, волосы, хрящи.
Например, белки, имеющие глобулярную четвертичную структуру, в частности белок куриного яйца, растворяются в воде с образованием коллоидных растворов. Белки, обладающие фибриллярной четвертичной структурой в воде не растворяются. Фибриллярными белками, в частности, образованы ногти, волосы, хрящи.
Химические свойства белков
Гидролиз
Все белки способны вступать в реакцию гидролиза. В случае полного гидролиза белков образуется смесь из α-аминокислот:
Белок + nH2O => смесь из α-аминокислот
Денатурация
Разрушение вторичной, третичной и четвертичной структур белка без разрушения его первичной структуры называют денатурацией. Денатурация белка может протекать под действием растворов солей натрия, калия или аммония – такая денатурация является обратимой:
Денатурация же протекающая под действием излучения (например, нагрева) или обработке белка солями тяжелых металлов является необратимой:
Так, например, необратимая денатурация белка наблюдается при термической обработке яиц в процессе их приготовления. В результате денатурации яичного белка его способность растворяться в воде с образованием коллоидного раствора исчезает.
В результате денатурации яичного белка его способность растворяться в воде с образованием коллоидного раствора исчезает.
Качественные реакции на белки
Биуретовая реакция
Если к раствору, содержащему белок добавить 10%-й раствор гидроксида натрия, а затем небольшое количество 1 %-го раствора сульфата меди, то появится фиолетовое окрашивание.
раствор белка + NаОН(10%-ный р-р) + СuSO4 = фиолетовое окрашивание
Ксантопротеиновая реакция
растворы белка при кипячении с концентрированной азотной кислотой окрашиваются в желтый цвет:
раствор белка + HNO3(конц.) => желтое окрашивание
Биологические функции белков
| каталитическая | ускоряют различные химические реакции в живых организмах | ферменты |
| структурная | строительный материал клеток | коллаген, белки клеточных мембран |
| защитная | защищают организм от инфекций | иммуноглобулины, интерферон |
| регуляторная | регулируют обменные процессы | гормоны |
| транспортная | перенос жизненно-необходимых веществ от одних частей организма к другим | гемоглобин переносит кислород |
| энергетическая | снабжают организм энергией | 1 грамм белка может обеспечить организм энергией в количестве 17,6 Дж |
| моторная (двигательная) | любые двигательные функции организма | миозин (мышечный белок) |
Белки, свойства белков
Белки — высокомолекулярные соединения, построенные из аминокислот и являются одними из наиболее сложных по строению и составу среди всех органических соединений.
Биологическая роль белков исключительно велика: они составляют основную массу протоплазмы и ядер живых клеток. Белковые вещества находятся во всех растительных и животных организмах. О запасе белков в природе можно судить по общему количеству живого вещества на нашей планете: масса белков составляет примерно 0,01% от массы земной коры, то есть 1016 тонн.
Молекулы белка
Белки по по своему элементному составу отличаются от углеводов и жиров: кроме углерода, водорода и кислорода они ещё содержат азот. Кроме того, Постоянной составной частью важнейших белковых соединений является сера, а некоторые белки содержат фосфор, железо и йод.
Свойства белков
1. Разная растворимость в воде. Растворимые белки образуют коллоидные растворы.
2. Гидролиз — под действием растворов минеральных кислот или ферментов происходит разрушение первичной структуры белка и образование смеси аминокислот.
3. Денатурация — частичное или полное разрушения пространственной структуры, присущей данной белковой молекуле. Денатурация происходит под действием:
- — высокой температуры
- — растворов кислот, щелочей и концентрированных растворов солей
- — растворов солей тяжёлых металлов
- — некоторых органических веществ (формальдегида, фенола)
- — радиоактивного излучения
Строение белков
Строение белков начали изучать в 19 веке. В 1888г. русский биохимик А.Я.Данилевский высказал гипотезу о наличии в белках амидной связи. Эта мысль в дальнейшем была развита немецким химиком Э.Фишером и в его работах нашла экспериментальное подтверждение. Он предложил полипептидную теорию строения белка. Согласно этой теории молекула белка состоит из одной длинной цепи или нескольких полипептидных цепей, связанных друг с другом. Такие цепи могут быть различной длины.
Фишером проведена большая экспериментальная работа с полипептидами. Высшие полипептиды, содержащие 15-18 аминокислот, осаждаются из растворов сульфатом аммония (аммиачными квасцами), то есть проявляют свойства, характерные для белков. Было показано, что полипептиды расщепляются теми же ферментами, что и белки, а будучи введёнными в организм животного, подвергаются тем же превращениям, как и белки, а весь их азот выделяется нормально в виде мочевины (карбамида).
Исследования, проведённые в 20 веке, показали, что существует несколько уровней организации белковой молекулы.
Белок тирозин
В организме человека тысячи различных белков и практически все они построены из стандартного набора 20 аминокислот. Последовательность аминокислотных остатков в молекуле белка называют первичной структурой белка. Свойства белков и их биологические функции определяются последовательностью аминокислот. Работы по выяснению первичной структуры белка впервые были выполнены в Кембриджском университете на примере одного из простейших белков — инсулина. В течение посте 10 лет английский биохимик Ф.Сенгер проводил анализ инсулина. В результате анализа выяснено, что молекула инсулина состоит из двух полипептидных цепей и содержит 51 аминокислотный остаток. Он установил, что инсулин имеет молярную массу 5687 г/моль, а его химический состав отвечает формуле C254H337N65O75S6. Анализ проводился вручную с использованием ферментов, которые избирательно гидролизуют пептидные связи между определёнными аминокислотными остатками.
В настоящее время большая часть работы по определению первичной структуры белков автоматизирована. Так была установлена первичная структура фермента лизоцима.
Тип «укладки» полипептидной цепочки называют вторичной структурой. У большинства белков полипептидная цепь свёртывается в спираль, напоминающую «растянутую пружину» (называют «А-спираль» или «А-стуктура»). Еще один распространённый тип вторичной структуры — структура складчатого листа (называют «B — структура»). Так, белок шёлка — фиброин имеет именно такую структуру. Он состоит из ряда полипептидных цепей, которые располагаются параллельно друг-другу и соединяются посредством водородных связей, большое число которых делает шёлк очень гибким и прочным на разрыв.
При всём этом практически не существует белков, молекулы которых на 100% имеют «А-структуру» или «B — структуру».
Белок фиброин — белок натурального шёлка
Пространственное положение полипептидной цепи называют третичной структурой белкой. Большинство белков относят к глобулярным, потому что их молекулы свёрнуты в глобулы. Такую форму белок поддерживает благодаря связям между разнорзаряженными ионами (-COO— и -NH3+ и дисульфидных мостиков. Кроме того, молекула белка свёрнута так, что гидрофобные углеводородные цепи оказываются внутри глобулы, а гидрофильные — снаружи.
Способ объединения нескольких молекул белка в одну макромолекулу называют четвертичной стуктурой белка. Ярким примером такого белка может быть гемоглобин. Было установлено, что, например, для взрослого человека молекула гемоглобина состоит из 4-х отдельных полипептидных цепей и небелковой части — гема.
Свойства белков объясняет их различное строение. Большинство белков аморфно, в спирте, эфире и хлороформе нерастворимо. В воде некоторые белки могут растворяться с образованием коллоидного раствора. Многие белки растворимы в растворах щелочей, некоторые — в растворах солей, а некоторые — в разбавленном спирте. Кристаллическое состояние белов встречается редко: примером могут быть алейроновые зёрна, встречающиеся в клещевине, тыкве, конопле. Кристаллизуется также альбумин куриного яйца и гемоглобин в крови.
Гидролиз белков
При кипячении с кислотами или щелочами, а также под действием ферментов белки распадаются на более простые химические соединения, образуя в конце цепочки превращения смесь A-аминокислот. Такое расщепление называется гидролизом белка. Гидролиз белка имеет большое биологическое значение: попадая в желудок и кишечник животного или человека, белок расщепляется под действием ферментов на аминокислоты. Образовавшиеся аминокислоты в дальнейшем под влиянием ферментов снова образуют белки, но уже характерные для данного организма!
В продуктах гидролиза белков кроме аминокислот были найдены углеводы, фосфорная кислота, пуриновые основания. Под влиянием некоторых факторов например, нагревания,растворов солей, кислот и щелочей, действия радиации, встряхивания, может нарушиться пространственная структура, присущая данной белковой молекуле. Денатурация может носить обратимый или необратимый характер, но в любом случае аминокислотная последовательность, то есть первичная структура, остаётся неизменной. В результате денатурации белок перестаёт выполнять присущие ему биологические функции.
Для белков известны некоторые цветные реакции, характерные для их обнаружения. При нагревании мочевины образуется биурет, который с раствором сульфата меди в присутствии щелочи даёт фиолетовое окрашивание или качественная реакция на белок, которую можно провести дома). Биуретовую реакцию даёт вещества, содержащие амидную группу, а в молекуле белка эта группа присутствует.
Ксантопротеиновая реакция заключается в том, что белок от концентрированной азотной кислоты окрашивается в жёлтый цвет. Эта реакция указывает на наличие в белке бензольной группы, которая имеется в таких аминокислотах, как фениланин и тирозин.
При кипячении с водным раствором нитрата ртути и азотистой кислоты, белок даёт красное окрашивание. Эта реакция указывает на наличие в белке тирозина. При отсутствии тирозина красного окрашивания не появляется.
Биологическая ценность белков кормов и методы ее оценки
Опубликовано: 17.03.2018
Автор: Долгая Н.Н., к.б.н., с.н.с., руководитель по качеству ООО «СмартБиоЛаб»
Биологическая ценность (БЦ) белков характеризует их качество, способность обеспечить пластические процессы и синтез метаболически активных субстанций, и обусловлена наличием в них незаменимых аминокислот, их соотношением с заменимыми, и усвояемостью в желудочно-кишечном тракте.
В целом можно утверждать, что БЦ белка определяется его первой лимитирующей аминокислотой. Если организм требует, например, 1 г фенилаланина ежедневно, а с пищевыми продуктами поступает 500 г белка и при этом всего 0,5 г фенилаланина, БЦ белка является очень низкой, поскольку для анаболических целей будет использована только часть белка, а остальные — выведена из организма.
Низкая БЦ белка должна быть компенсирована другими белками. Например, когда белок содержит мало лейцина, его БЦ низкая. Комбинирование такого белка с белком, который имеет высокий уровень лейцина, позволит получить белок с более высокой БЦ, чем у первого. Следует учесть, что в комбинированном белка лимитирующей аминокислотой может оказаться другая аминокислота, которая и определит БЦ результата комбинирования.
Состояние белкового обмена целостного организма зависит не только от количества принятого с пищей белка, но и от качественного его состава. В опытах на животных было показано, что получение одинакового количества различных пищевых белков приводит в ряде случаев к развитию отрицательного азотистого баланса. Так, скармливание одних и тех же количеств казеина и желатина крысам приводило к положительному азотистому балансу в первом случае и к негативному — во втором. Все дело заключается в разном аминокислотном составе белков, и послужило базой для предположения о существовании в природе якобы «неполноценных» белков.
Оказывается, из 20 аминокислот в желатине почти отсутствуют (или содержатся в малых количествах) валин, тирозин, метионин и цистеин, кроме того, желатин характеризуется другим, отличным от казеина процентным содержанием отдельных аминокислот. Этим можно объяснить, что замена в питании крыс казеина на желатин приводит к развитию отрицательного азотистого баланса. Эти данные свидетельствуют о том, что различные белки обладают неодинаковой пищевой ценностью. Поэтому для удовлетворения пластических потребностей организма нужны достаточные количества различных белков пищи. Пожалуй, справедливо положение, что чем ближе аминокислотный состав принятого пищевого белка в аминокислотному составу белков тела, тем выше его биологическая ценность. Следует, однако, отметить, что степень усвоения пищевого белка зависит от эффективности его распада под действием ферментов желудочно-кишечного тракта. Ряд белковых веществ (например, шерсть, волосы, перья и т.д.), несмотря на их близкий аминокислотный состав к белкам тела человека, почти не используются в качестве пищевого белка, поскольку они не гидролизируются протеиназами кишечника человека и большинства животных.
Для оценки биологической ценности пищевого белка важное значение имеет его аминокислотный состав. Так, скармливание крысам казеина (белок молока) и белка зеина, выделенного из кукурузы, который не содержит в своем составе лизина и триптофана, показало, что при получении казеина рост животных не нарушался. Замена казеина на зеин приводила к постепенному отставанию в росте и снижению массы тела животных. Добавление к зеину только триптофана предотвращало снижение массы тела, но не увеличивало рост; а добавлении в рацион еще и лизина способствовала тому, что масса тела животных прогрессивно нарастала. Таким образом, скармливание выделенного из кукурузного зерна белка зеина, который не содержит двух незаменимых аминокислот, приводит к остановке роста, уменьшение массы тела животных и развитию отрицательного азотистого баланса.
Однако человек и животные питаются не искусственно выделенными, а натуральными белками, входящими в состав смешанной пищи, в которой обычно содержится весь набор незаменимых аминокислот. Так, например, цельное кукурузное зерно содержит 2,5% лизина, 0,7% триптофана, в то время как зеин не содержит лизина вообще, а триптофана всего 0,1%. Этот пример лишний раз свидетельствует о том, что в природе неполноценных белков почти не существует и что следует, очевидно, только различать биологически более ценные и менее ценные (в питательном отношении) белки.
Различия в усвояемости влияют на утилизацию белков, в связи с чем вводят поправки на усвояемость при пересчете потребности в эталонных белках в соответствующие безопасные уровни потребления обычных смесей пищевых белков. Поскольку оценка безопасных уровней потребления основана на данных, полученных при использовании белков молока, яиц, мяса и рыбы, усвояемость других белков выражают в сопоставлении с усвояемостью белков вышеперечисленных продуктов.
Биологическую ценность белков оценивают химическими, биохимическими и биологическими методами (см. Таблицу 1).
Нужно отметить, что химическая оценка биологической ценности белков пассивная, поскольку отражает лишь потенциальную возможность белка в удовлетворении потребностей человека и животных. Конечный же результат зависит от особенностей структуры белка и действием на него со стороны пищеварительных протеиназ (пепсин, химотрипсин, трипсин и др.).
Показатель качества протеина зависит от того, какой именно из данных методов использовался. Например, при использовании одной методики оценки яичный белок может иметь высокий показатель качества, при использовании другой таким белком будет казеин. Еще одним, и, пожалуй, более важным фактором является то, что полученный показатель качества протеина будет напрямую зависеть от физиологических потребностей объекта исследования.
Таким образом, первый вопрос, который требует ответа: какая из методик оценки качества протеинов является идеальной и оптимальной?
Ответ ни одна, поскольку все они используют при расчетах допущение или основываются на моделях, достоверность которых не бесспорна.
Несмотря на существование большого количества различных методик оценки качества протеинов, только некоторые из них реально используются. Среди них: химический скоринг, оценка биологической ценности, оценка коэффициента эффективности, а также скорректирована по аминокислотам оценка усвояемости протеина.
Таблица 1. — Показатели биологической ценности белков
| Химические | Биохимические | Биологические |
|---|---|---|
|
Химический гидролиз белков
Определение аминокислотного состава белков
Сравнение аминокислотного состава белков по стандартной аминокислотной шкале
|
Ферментативный гидролиз белков в моделях in vitro
Определение скорости и глубины расщепления исследуемого белка по сравнению со стандартным белком
|
Исследование усвоения и использования белков в метаболизме людей, животных, микроорганизмов
|
Химические методы
Для расчета биологической ценности белка используют следующие методы:
Метод оценки по «химическому числу», где каждая незаменимая аминокислота (АК) продукта исследуется и выражается в процентном отношении к содержанию этой аминокислоты (АК) в белке цельного куриного яйца. Полученные проценты всех незаменимых аминокислот суммируются и делятся на количество взятых для расчета аминокислот, что и принимается как показатель биологической ценности.
Расчет «химического числа» проводят по формуле:
Метод «аминокислотного скора». В этом методе в качестве идеальной шкалы вместо аминокислот белка куриного яйца используется аминокислотная шкала стандарта ФАО / ВОЗ.
Расчет «аминокислотного скора» проводят по формуле:
Метод «индекс Осера» — представляет собой среднее геометрическое соотношение содержания отдельных аминокислот в исследуемом белке (г) к таким же показателям в белке цельного куриного яйца (s).
Расчет «индекса Осера» проводят по формуле:
где, In. Osera – индекс Осера;
а – отношение количества каждой незаменимой аминокислоты (НЗАК) в исследуемом белке в ее же количества к белку цельного куриного яйца;
n – количество НЗАК; где n — число аминокислот, которые учитываются.
Данный метод расчета имеет свои недостатки, так как в этой методике, как и в других, описанных выше, не учитываются заменимые аминокислоты, которые также играют важную роль в белковом питании животных.
Метод Карпаци — Линдера — Варга, основанный на сравнении аминокислотного состава исследуемого белка к стандарту, в качестве которого используется аминокислотный состав белка куриного яйца. При этом в расчете учитываются и заменимые аминокислоты.
Расчет по 10-и незаменимым проводят по формуле:
где, ax1 – содержание НЗАК у исследуемом белке, количество которого меньше, чем в белке яйца, %;
aя1 – содержание этих же аминокислот в белке яйца, %;
бя1 – содержание НЗАК, колличество которых в белке яйца меньше, чем в исследуемом белке, %;
бx1 – содержание этих же АК в белке яйца, %;
Рx – сумма заменимых АК в исследуемом белке, %;
Ря – сумма заменимых АК в белке яйца, %;
Модифицированный метод Карпаци — Линдера — Варга, где в качестве стандарта взят аминокислотный состав белка сои (по справочным данным), потому что соя — зернобобовая культура, которая наиболее широко используется в мировом кормопроизводстве.
где, ax1 – содержание НЗАК в исследуемом белке, количество которого меньше, чем в белке сои, %;
aя1 – содержание этих же аминокислот в белке сои,%;
бя1 – содержание НЗАК, количество которых в белке сои меньше, чем в исследуемом белке,%;
бx1 – содержание этих же аминокислот в исследуемом белке, %;
Рx – сумма заменимых АК в исследуемом белке,%;
Ря – сумма заменимых АК в белке сои,%.
Метод «комплетного белка», основанный на методе «аминокислотного скора» для отдельных аминокислот.
Расчет проводят по формуле:
КБ – содержание комплетного белка, %;
СБ – содержание сырого белка в опытном образце, %.
Для злаковых культур КБ определяют по аминокислотному скором лимитирующей аминокислоты. Для других кормовых культур — по аминокислотному скором для лизина.
КБ = 10% — является стандартом;
КБ = 11,0-9,0% — полноценный продукт;
КБ = 9,0-7,5 % — удовлетворительное;
КБ = 7,5- 5,5% — низкокачественный;
КБ < 5,5% — некачественный;
КБ > 11,0% — белковая добавка.
В российской научной школе при оценке БЦ белков используют коэффициент различия АК исследуемого белка (КРАС), который рассчитывают по формуле
где, ΔРАС – разница аминокислотного скора аминокислот, рассчитывается по формуле:
где, Сі – избыток СКОРА первой лимитирующей незаменимой аминокислоты, %;
Сmin – минимальный из скоров незаменимой аминокислоты белка, который исследуется, по отношению к эталону, %;
n — количество незаменимых аминокислот.
Величину биологической ценности определяют по формуле:
При этом, чем меньше величина КРАС, тем выше качество белка.
Показателем, характеризующим белок по степени его усвоения, использования с пользой, является коэффициент утилитарности (U или Ку), который учитывает сбалансированность АК состава не только по лимитирующим аминокислотами, но и по их избытку (по отношению к потребности).
Для оценки коэффициента утилизации аі каждой АК используют формулу:
где, АКС min – минимальный аминокислотный скор;
АКС і НЗАК – аминокислотный скор і-й незаменимой аминокислоты.
Коэффициент утилитарности белка (Ку) рассчитывают по формуле:
где, содержание iНЗАК – содержание каждой незаменимой аминокислоты в исследуемом белке;
АКС iНЗАК – аминокислотный скор каждой незаменимой аминокислоты в исследуемом белке;
аiНЗАК, % — коэффициент утилизации каждой незаменимой аминокислоты в исследуемом белке.
Метод определения БЦ белка по скорректированному аминокислотному скором с учетом лимитирующей аминокислоты и «видимой» переваримости белка — PDCAAS предложено ФАО/WHO в 1991 по формуле G.Schaafsma, 2000.
где, КП – коэффициент «видимой» переваримости белка продукта.
DIAAS – относительно новый метод, рекомендуется ФАО/ВОЗ и используется как основной при оценке белковой ценности белка. Он оценивает биологическую ценность по аминокислотному скору, скорректированному с усвояемостью незаменимых аминокислот в подвздошной кишке, основанный на измерении усвояемости каждой отдельной эссенциальной (незаменимой) аминокислоты в подвздошной кишке, и противопоставляется традиционно принятому методу определения усвояемости протеина, измеряемого в фекалиях.
Метод рекомендуется ФАО/ВОЗ и используется как основной при оценке БЦ белка. Продовольственная и сельскохозяйственная организация Объединенных Наций (ФАО в 2013 году) опубликовала доклад с рекомендациями по применению нового, усовершенствованного метода для оценки качества белков.
Метод получил название DIAAS, и его предложено использовать вместо PDCAAS. Применение метода DIAAS позволяет обеспечить более точное измерение количества аминокислот, которые усваиваются организмом, дифференцировать источники белка по их способности поставлять аминокислоты для использования.
У таблице 2 приведены рассчитанные данные по оценке биологической ценности белков различными методами, показано, что наибольший расчетный коэффициент для кормовых дрожжей максимальный по методу «Химического числа», соотношению НЗАК/ЗАК и АКС, однако по методу КРАС, коэффициенту утилитарности Ку и комплектному белку он 12-й, 5 -й и 2-й соответственно. Не на самом высоком уровне они и при расчете при использовании в качестве эталонов белка сои.
То есть оценка биологической ценности достаточно условный показатель, и не может корректно использоваться для оценки качества белка в кормлении животных.
Таблица 2. — Биологическая ценность белка кормов для сельскохозяйственных животных, рассчитанная различными методическими подходами, %
белков
белков
Белки :
Белки представляют собой сложную молекулу, состоящую из аминокислот и необходимых
для химических процессов, происходящих в живых организмах.
Белки являются основными составляющими всех живых организмов. Их
центральная роль в биологических структурах и функционировании была признана
химиками в начале 19 века, когда они придумали название для
эти вещества от греческого слова proteios, что означает «сначала удерживать
место ». Белки составляют около 80 процентов от сухой массы
мышцы, 70 процентов кожи и 90 процентов крови.Внутреннее вещество растительных клеток также частично состоит из
белки. Важность белков больше связана с их
функции, чем их количество в организме или ткани. Все известные
ферменты, например, являются белками и могут появиться в очень короткие сроки
суммы; тем не менее, эти вещества катализируют все метаболические процессы.
реакции, позволяющие организмам накапливать химические
вещества — другие белки, нуклеиновые кислоты, углеводы и
липиды — необходимые для жизни.
Белки иногда называют макромолекулярными полипептидами.
потому что они очень большие молекулы и потому что аминокислоты
которые они состоят, соединены пептидными связями.(Пептидная связь
представляет собой связь между аминогруппой [-Nh3] одной аминокислоты и
карбоксильная группа [-COOH] следующей аминокислоты в белковой цепи.)
Хотя аминокислоты могут иметь другие формулы, в протеине
неизменно имеют общую формулу RCH (Nh3) COOH, где C — углерод,
H — водород, N — азот, O — кислород, R — группа, варьирующаяся
по составу и структуре, называется боковой цепью. Аминокислоты
соединены вместе в длинные цепочки; большинство обычных белков
содержат более 100 аминокислот.
Подавляющее большинство белков, обнаруженных в живых организмах, являются
состоит всего из 20 различных видов аминокислот, повторяющихся многими
раз и соединены в определенном порядке. Каждый тип протеина
имеет свою уникальную последовательность аминокислот; эта последовательность, известная как
его первичная структура, фактически определяет форму и функцию
белок.
Взаимодействие между аминокислотами заставляет белковую цепь принимать
характерная вторичная структура и, при некоторых обстоятельствах,
третичная структура.Вторичная структура является функцией
углы, образованные пептидными связями, которые связывают амино
кислоты. Эти валентные углы удерживаются на месте за счет развития
водородные связи между атомом водорода, связанным с азотом одной амино
кислотная единица и атом кислорода другого. Обычно водород
связи заставляют цепь принимать спиральную вторичную структуру, т. е.
остов цепи напоминает веревку, спирально намотанную на
воображаемая трубка.
Третичная структура относится к зацикливанию и складыванию
белковая цепочка обратно на себя.Такая структура характеризует
глобулярные белки (т.е. имеющие более или менее сферическую форму).
Третичная структура в значительной степени определяется боковыми цепями
аминокислоты. Некоторые боковые цепи настолько велики, что нарушают
регулярная спиральная вторичная структура цепи, обуславливающая ее
перегибы и изгибы. Кроме того, боковые цепи, несущие противоположные
электрические заряды притягиваются друг к другу и образуют ионные связи; те
с одинаковыми электрическими зарядами отталкиваются друг от друга. Гидрофобная сторона
цепи — i.е., те, которые нерастворимы в воде, объединяются в группы на
центр свернутого белка, избегая воздействия водной
окружающая обстановка. Гидрофильные боковые цепи, которые легко образуют водород
связи с молекулами воды, остаются снаружи белка
состав.
Некоторые белки, такие как гемоглобин, состоят более чем из одного
субъединица белка (полипептидная цепь). Пространственное оформление
эти цепи известны как четвертичная структура. Четвертичный
структура поддерживается теми же силами, которые определяют
третичная структура.
Выдержка из Британской энциклопедии без разрешения.
Белки | Биология для майоров I
Опишите структуру и функции белков
Белки представляют собой полимеры аминокислот. Каждая аминокислота содержит центральный атом углерода, водород, карбоксильную группу, аминогруппу и переменную группу R. Группа R указывает, к какому классу аминокислот она принадлежит: электрически заряженные гидрофильные боковые цепи, полярные, но незаряженные боковые цепи, неполярные гидрофобные боковые цепи и особые случаи.
Белки имеют разные «слои» структуры: первичный, вторичный, третичный, четвертичный.
Белки выполняют в клетках самые разные функции. Основные функции включают действие в качестве ферментов, рецепторов, транспортных молекул, белков, регулирующих экспрессию генов, и так далее. Ферменты — это биологические катализаторы, которые ускоряют химическую реакцию без постоянных изменений. У них есть «активные центры», где связывается субстрат / реагент, и они могут быть либо активированы, либо ингибированы (конкурентные и / или неконкурентные ингибиторы).
Цели обучения
- Продемонстрировать знакомство с мономерными единицами белков: аминокислоты
- Определите различные слои структуры белка
- Определите несколько основных функций белков
Аминокислоты
Белки являются одними из наиболее распространенных органических молекул в живых системах и обладают самым разнообразным набором функций среди всех макромолекул. Белки могут быть структурными, регуляторными, сократительными или защитными; они могут служить для транспортировки, хранения или перепонки; или они могут быть токсинами или ферментами.Каждая клетка в живой системе может содержать тысячи белков, каждый из которых выполняет уникальную функцию. Их структуры, как и их функции, сильно различаются. Однако все они представляют собой полимеры из аминокислот и , расположенных в линейной последовательности.
Рис. 1. Аминокислоты имеют центральный асимметричный углерод, к которому присоединены аминогруппа, карбоксильная группа, атом водорода и боковая цепь (R-группа).
Аминокислоты — это мономеры, из которых состоят белки. Каждая аминокислота имеет одинаковую фундаментальную структуру, которая состоит из центрального атома углерода, также известного как альфа ( α ) углерода, связанного с аминогруппой (Nh3), карбоксильной группой (COOH) и атомом водорода. .Каждая аминокислота также имеет другой атом или группу атомов, связанных с центральным атомом, известную как группа R (рис. 1).
Название «аминокислоты» происходит от того факта, что они содержат как аминогруппу, так и карбоксильную кислотную группу в своей основной структуре. Как уже упоминалось, в белках присутствует 20 аминокислот. Десять из них считаются незаменимыми аминокислотами у человека, потому что человеческий организм не может их производить, и они получают их с пищей.
Для каждой аминокислоты группа R (или боковая цепь) отличается (рис. 2).
Практический вопрос
Рис. 2. В белках обычно встречаются 20 общих аминокислот, каждая из которых имеет свою R-группу (вариантная группа), которая определяет его химическую природу.
Какие категории аминокислот вы ожидаете найти на поверхности растворимого белка, а какие — внутри? Какое распределение аминокислот вы ожидаете найти в белке, встроенном в липидный бислой?
Показать ответ
Полярные и заряженные аминокислотные остатки (остаток после образования пептидной связи) с большей вероятностью будут обнаружены на поверхности растворимых белков, где они могут взаимодействовать с водой, и неполярные (например.g., боковые цепи аминокислот) с большей вероятностью будут обнаружены внутри, где они изолированы от воды. В мембранных белках неполярные и гидрофобные боковые цепи аминокислот связаны с гидрофобными хвостами фосфолипидов, в то время как полярные и заряженные боковые цепи аминокислот взаимодействуют с полярными головными группами или с водным раствором. Однако бывают исключения. Иногда положительно и отрицательно заряженные боковые цепи аминокислот взаимодействуют друг с другом внутри белка, а полярные или заряженные боковые цепи аминокислот, которые взаимодействуют с лигандом, могут быть обнаружены в кармане связывания лиганда.
Химическая природа боковой цепи определяет природу аминокислоты (то есть, является ли она кислотной, основной, полярной или неполярной). Например, аминокислота глицин имеет атом водорода в качестве группы R. Аминокислоты, такие как валин, метионин и аланин, неполярны или гидрофобны по природе, тогда как аминокислоты, такие как серин, треонин и цистеин, полярны и имеют гидрофильные боковые цепи. Боковые цепи лизина и аргинина заряжены положительно, поэтому эти аминокислоты также известны как основные аминокислоты.Пролин имеет группу R, которая связана с аминогруппой, образуя кольцеобразную структуру. Пролин является исключением из стандартной структуры анимокислоты, поскольку его аминогруппа не отделена от боковой цепи (рис. 2).
Аминокислоты обозначаются одной заглавной буквой или трехбуквенным сокращением. Например, валин обозначается буквой V или трехбуквенным символом val. Так же, как некоторые жирные кислоты необходимы для диеты, некоторые аминокислоты также необходимы. Они известны как незаменимые аминокислоты, а у людей они включают изолейцин, лейцин и цистеин.Незаменимые аминокислоты относятся к тем, которые необходимы для построения белков в организме, но не производятся организмом; Какие аминокислоты являются незаменимыми, варьируется от организма к организму.
Рис. 3. Образование пептидной связи — это реакция синтеза дегидратации. Карбоксильная группа одной аминокислоты связана с аминогруппой входящей аминокислоты. При этом выделяется молекула воды.
Последовательность и количество аминокислот в конечном итоге определяют форму, размер и функцию белка.Каждая аминокислота присоединена к другой аминокислоте ковалентной связью, известной как пептидная связь, которая образуется в результате реакции дегидратации. Карбоксильная группа одной аминокислоты и аминогруппа входящей аминокислоты объединяются, высвобождая молекулу воды. Полученная связь представляет собой пептидную связь (рис. 3).
Продукты, образованные такими связями, называются пептидами. По мере того, как к этой растущей цепи присоединяется больше аминокислот, полученная цепь называется полипептидом. Каждый полипептид имеет свободную аминогруппу на одном конце.Этот конец называется N-концом или амино-концом, а другой конец имеет свободную карбоксильную группу, также известную как C или карбоксильный конец. Хотя термины полипептид и белок иногда используются взаимозаменяемо, полипептид технически представляет собой полимер аминокислот, тогда как термин белок используется для полипептида или полипептидов, которые объединились вместе, часто имеют связанные непептидные простетические группы, имеют различную форму. , и имеют уникальную функцию. После синтеза (трансляции) белков большинство белков модифицируются.Они известны как посттрансляционные модификации. Они могут подвергаться расщеплению, фосфорилированию или могут потребовать добавления других химических групп. Только после этих модификаций белок становится полностью функциональным.
Эволюционное значение цитохрома c
Цитохром c является важным компонентом цепи переноса электронов, частью клеточного дыхания, и обычно он находится в клеточной органелле, митохондрии. Этот белок имеет простетическую группу гема, и центральный ион гема попеременно восстанавливается и окисляется во время переноса электрона.Поскольку роль этого важного белка в производстве клеточной энергии имеет решающее значение, за миллионы лет он очень мало изменился. Секвенирование белков показало, что существует значительная гомология аминокислотной последовательности цитохрома с среди различных видов; другими словами, эволюционное родство можно оценить путем измерения сходства или различий между последовательностями ДНК или белков различных видов.
Ученые определили, что цитохром с человека содержит 104 аминокислоты.Для каждой молекулы цитохрома с от разных организмов, которая была секвенирована на сегодняшний день, 37 из этих аминокислот появляются в одном и том же положении во всех образцах цитохрома с. Это указывает на то, что, возможно, был общий предок. При сравнении последовательностей белков человека и шимпанзе различий в последовательностях не обнаружено. Когда сравнивали последовательности человека и макаки-резуса, единственное обнаруженное различие заключалось в одной аминокислоте. В другом сравнении секвенирование человека и дрожжей показывает разницу в 44-м положении.
Структура белка
Как обсуждалось ранее, форма белка имеет решающее значение для его функции. Например, фермент может связываться со специфическим субстратом в сайте, известном как активный сайт. Если этот активный сайт изменяется из-за локальных изменений или изменений в общей структуре белка, фермент может быть неспособен связываться с субстратом. Чтобы понять, как белок приобретает свою окончательную форму или конформацию, нам необходимо понять четыре уровня структуры белка: первичный, вторичный, третичный и четвертичный.
Первичная структура
Уникальная последовательность аминокислот в полипептидной цепи — это ее первичная структура. Например, гормон поджелудочной железы инсулин имеет две полипептидные цепи, А и В, и они связаны между собой дисульфидными связями. N-концевой аминокислотой A-цепи является глицин, а C-концевой аминокислотой — аспарагин (рис. 4). Последовательности аминокислот в цепях A и B уникальны для инсулина.
Рис. 4. Инсулин бычьей сыворотки — это белковый гормон, состоящий из двух пептидных цепей: A (длиной 21 аминокислота) и B (длиной 30 аминокислот).В каждой цепи первичная структура обозначена трехбуквенными сокращениями, которые представляют названия аминокислот в порядке их присутствия. Аминокислота цистеин (cys) имеет сульфгидрильную (SH) группу в качестве боковой цепи. Две сульфгидрильные группы могут реагировать в присутствии кислорода с образованием дисульфидной (S-S) связи. Две дисульфидные связи соединяют цепи A и B вместе, а третья помогает цепи A свернуться в правильную форму. Обратите внимание, что все дисульфидные связи имеют одинаковую длину, но для ясности показаны разные размеры.
Уникальная последовательность каждого белка в конечном итоге определяется геном, кодирующим этот белок. Изменение нуклеотидной последовательности кодирующей области гена может привести к добавлению другой аминокислоты к растущей полипептидной цепи, вызывая изменение структуры и функции белка. При серповидно-клеточной анемии цепь гемоглобина β (небольшая часть которой показана на рисунке 5) имеет единственную аминокислотную замену, вызывающую изменение структуры и функции белка.
Рис. 5. Бета-цепь гемоглобина имеет длину 147 остатков, однако единственная аминокислотная замена приводит к серповидно-клеточной анемии. В нормальном гемоглобине аминокислота в седьмом положении — глутамат. В серповидно-клеточном гемоглобине этот глутамат заменен валином.
В частности, аминокислота глутаминовая кислота заменена валином в цепи β . Примечательно, что молекула гемоглобина состоит из двух альфа-цепей и двух бета-цепей, каждая из которых состоит примерно из 150 аминокислот.Таким образом, молекула содержит около 600 аминокислот. Структурное различие между нормальной молекулой гемоглобина и молекулой серповидноклеточных клеток — что резко снижает продолжительность жизни — состоит в одной из 600 аминокислот. Что еще более примечательно, так это то, что эти 600 аминокислот кодируются тремя нуклеотидами каждая, а мутация вызвано одним изменением основания (точечной мутацией), 1 из 1800 оснований.
Рис. 6. В этом мазке крови, визуализированном при 535-кратном увеличении с помощью светлопольной микроскопии, серповидные клетки имеют форму полумесяца, а нормальные клетки имеют форму диска.(кредит: модификация работы Эда Усмана; данные шкалы от Мэтта Рассела)
Из-за этого изменения одной аминокислоты в цепи молекулы гемоглобина образуют длинные волокна, которые искажают двояковогнутые или дискообразные красные кровяные тельца и принимают форму полумесяца или «серпа», что закупоривает артерии (рис. 6). Это может привести к множеству серьезных проблем со здоровьем, таких как одышка, головокружение, головные боли и боли в животе у людей, страдающих этим заболеванием.
Вторичная структура
Локальное сворачивание полипептида в некоторых областях приводит к вторичной структуре белка.Наиболее распространены листовые структуры α, -спираль и β (рис. 7). Обе структуры представляют собой структуру α -спираль — спираль, форма которой удерживается водородными связями. Водородные связи образуются между атомом кислорода в карбонильной группе одной аминокислоты и другой аминокислотой, которая находится на четыре аминокислоты дальше по цепи.
Рис. 7. α-спираль и β-складчатый лист — это вторичные структуры белков, которые образуются из-за образования водородных связей между карбонильной и аминогруппой в основной цепи пептида.Некоторые аминокислоты имеют склонность образовывать α-спираль, в то время как другие имеют склонность образовывать β-складчатый лист.
Каждый виток альфа-спирали содержит 3,6 аминокислотных остатка. Группы R (вариантные группы) полипептида выступают из цепи α -спирали. В листе β с складками «складки» образованы водородными связями между атомами в основной цепи полипептидной цепи. Группы R прикреплены к атомам углерода и проходят выше и ниже складок складки.Гофрированные сегменты выстраиваются параллельно или антипараллельно друг другу, а водородные связи образуются между частично положительным атомом азота в аминогруппе и частично отрицательным атомом кислорода в карбонильной группе основной цепи пептида. Спиральные структуры α и складчатые листы β обнаружены в большинстве глобулярных и волокнистых белков, и они играют важную структурную роль.
Третичная структура
Уникальная трехмерная структура полипептида — это его третичная структура (рис. 8).Эта структура частично обусловлена химическими взаимодействиями в полипептидной цепи. В первую очередь, взаимодействия между группами R создают сложную трехмерную третичную структуру белка. Природа групп R, присутствующих в задействованных аминокислотах, может противодействовать образованию водородных связей, описанных для стандартных вторичных структур. Например, группы R с одинаковыми зарядами отталкиваются друг от друга, а группы с разными зарядами притягиваются друг к другу (ионные связи). Когда происходит сворачивание белка, гидрофобные группы R неполярных аминокислот лежат внутри белка, тогда как гидрофильные группы R лежат снаружи.Первые типы взаимодействий также известны как гидрофобные взаимодействия. Взаимодействие между боковыми цепями цистеина образует дисульфидные связи в присутствии кислорода, единственную ковалентную связь, образующуюся во время сворачивания белка.
Рис. 8. Третичная структура белков определяется множеством химических взаимодействий. К ним относятся гидрофобные взаимодействия, ионные связи, водородные связи и дисульфидные связи.
Все эти взаимодействия, слабые и сильные, определяют окончательную трехмерную форму белка.Когда белок теряет свою трехмерную форму, он может больше не функционировать.
Четвертичная структура
В природе некоторые белки образованы из нескольких полипептидов, также известных как субъединицы, и взаимодействие этих субъединиц образует четвертичную структуру. Слабые взаимодействия между субъединицами помогают стабилизировать общую структуру. Например, инсулин (глобулярный белок) имеет комбинацию водородных и дисульфидных связей, из-за которых он в основном собирается в шар.Инсулин начинается как отдельный полипептид и теряет некоторые внутренние последовательности в присутствии посттрансляционной модификации после образования дисульфидных связей, которые удерживают вместе оставшиеся цепи. Шелк (волокнистый белок), однако, имеет складчатую структуру листа β , которая является результатом водородных связей между различными цепями.
Четыре уровня структуры белка (первичный, вторичный, третичный и четвертичный) показаны на Рисунке 9.
Рисунок 9.На этих иллюстрациях можно увидеть четыре уровня белковой структуры. (кредит: модификация работы Национального исследовательского института генома человека)
Денатурация и сворачивание белков
Каждый белок имеет свою уникальную последовательность и форму, которые удерживаются вместе за счет химических взаимодействий. Если белок подвержен изменениям температуры, pH или воздействию химикатов, структура белка может измениться, потеряв свою форму без потери своей первичной последовательности в так называемой денатурации.Денатурация часто обратима, поскольку первичная структура полипептида сохраняется в процессе, если денатурирующий агент удаляется, позволяя белку возобновить свою функцию. Иногда денатурация необратима, что приводит к потере функции. Одним из примеров необратимой денатурации белка является жарение яйца. Белок альбумина в жидком яичном белке денатурируется при помещении на горячую сковороду. Не все белки денатурируются при высоких температурах; например, бактерии, которые выживают в горячих источниках, содержат белки, функционирующие при температурах, близких к температуре кипения.Желудок также очень кислый, имеет низкий pH и денатурирует белки как часть процесса пищеварения; однако пищеварительные ферменты желудка в этих условиях сохраняют свою активность.
Сворачивание белка имеет решающее значение для его функции. Первоначально считалось, что сами белки несут ответственность за процесс сворачивания. Только недавно было обнаружено, что часто они получают помощь в процессе сворачивания от белков-помощников, известных как шапероны (или шаперонины), которые связываются с целевым белком во время процесса сворачивания.Они действуют, предотвращая агрегацию полипептидов, составляющих полную структуру белка, и отделяются от белка, как только целевой белок сворачивается.
Чтобы получить дополнительную информацию о белках, просмотрите этот анимационный ролик под названием «Биомолекулы: белки».
Функция белков
Основные типы и функции белков перечислены в таблице 1.
| Таблица 1. Типы и функции белков | ||
|---|---|---|
| Тип | Примеры | Функции |
| Пищеварительные ферменты | Амилаза, липаза, пепсин, трипсин | Помощь в переваривании пищи за счет катаболизма питательных веществ до мономерных единиц |
| Транспорт | Гемоглобин, альбумин | Переносит вещества в крови или лимфе по всему телу |
| Строительный | Актин, тубулин, кератин | Создавать различные структуры, например цитоскелет |
| Гормоны | Инсулин, тироксин | Координировать деятельность различных систем организма |
| Оборона | Иммуноглобулины | Защитите организм от инородных патогенов |
| Сокращение | Актин, миозин | Эффект сокращения мышц |
| Хранилище | Запасные белки бобовых, яичный белок (альбумин) | Обеспечить питание на ранних этапах развития зародыша и проростка |
Два специальных и распространенных типа белков — это ферменты и гормоны. Ферменты , которые вырабатываются живыми клетками, являются катализаторами биохимических реакций (например, пищеварения) и обычно представляют собой сложные или конъюгированные белки. Каждый фермент специфичен для субстрата (реагента, который связывается с ферментом), на который он действует. Фермент может помочь в реакциях разложения, перегруппировки или синтеза. Ферменты, которые расщепляют свои субстраты, называются катаболическими ферментами, ферменты, которые строят более сложные молекулы из своих субстратов, называются анаболическими ферментами, а ферменты, влияющие на скорость реакции, называются каталитическими ферментами.Следует отметить, что все ферменты увеличивают скорость реакции и, следовательно, считаются органическими катализаторами. Примером фермента является амилаза слюны, которая гидролизует свою субстратную амилозу, компонент крахмала.
Гормоны — это химические сигнальные молекулы, обычно небольшие белки или стероиды, секретируемые эндокринными клетками, которые контролируют или регулируют определенные физиологические процессы, включая рост, развитие, метаболизм и размножение. Например, инсулин — это белковый гормон, который помогает регулировать уровень глюкозы в крови.
Белки имеют разную форму и молекулярную массу; некоторые белки имеют глобулярную форму, тогда как другие имеют волокнистую природу. Например, гемоглобин — это глобулярный белок, а коллаген, обнаруженный в нашей коже, — это волокнистый белок. Форма белка имеет решающее значение для его функции, и эта форма поддерживается многими различными типами химических связей. Изменения температуры, pH и воздействие химикатов могут привести к необратимым изменениям формы белка, что приведет к потере функции, известной как денатурация.Все белки состоят из 20 одних и тех же аминокислот по-разному.
Вкратце: Белки
Белки — это класс макромолекул, которые выполняют широкий спектр функций для клетки. Они помогают метаболизму, обеспечивая структурную поддержку и действуя как ферменты, переносчики или гормоны. Строительными блоками белков (мономеров) являются аминокислоты. Каждая аминокислота имеет центральный углерод, связанный с аминогруппой, карбоксильной группой, атомом водорода и R-группой или боковой цепью.Существует 20 обычно встречающихся аминокислот, каждая из которых отличается по группе R. Каждая аминокислота связана со своими соседями пептидной связью. Длинная цепь аминокислот известна как полипептид.
Белки подразделяются на четыре уровня: первичный, вторичный, третичный и (необязательно) четвертичный. Первичная структура — это уникальная последовательность аминокислот. Локальное сворачивание полипептида с образованием таких структур, как спираль α и складчатый лист β , составляет вторичную структуру.Общая трехмерная структура — это третичная структура. Когда два или более полипептида объединяются, чтобы сформировать полную структуру белка, такая конфигурация известна как четвертичная структура белка. Форма и функция белка неразрывно связаны; любое изменение формы, вызванное изменениями температуры или pH, может привести к денатурации белка и потере функции.
Проверьте свое понимание
Ответьте на вопросы ниже, чтобы увидеть, насколько хорошо вы понимаете темы, затронутые в предыдущем разделе.В этой короткой викторине , а не засчитываются в вашу оценку в классе, и вы можете пересдавать ее неограниченное количество раз.
Используйте этот тест, чтобы проверить свое понимание и решить, следует ли (1) изучить предыдущий раздел дальше или (2) перейти к следующему разделу.
Структура и функции белка — Биохимия
Белки являются наиболее универсальными
макромолекул в живых системах и выполняют важные функции практически во всех биологических
процессы.Они действуют как катализаторы, переносят и хранят другие молекулы, такие как кислород, они
обеспечивают механическую поддержку и иммунную защиту, они генерируют движение, передают нервы
импульсы, и они контролируют рост и дифференциацию. Действительно, большая часть этого текста будет посвящена
понимание того, что делают белки и как они выполняют эти функции.
Несколько ключевых свойств
позволяют белкам участвовать в таком широком спектре функций.
- 1.
-
Белки представляют собой линейные полимеры
построенный из мономерных единиц, называемых аминокислотами .Строительство огромного множества
макромолекулы из ограниченного числа строительных блоков мономера — повторяющаяся тема в
биохимия. Зависит ли функция белка от линейной последовательности аминокислот? Функция
белок напрямую зависит от его трехмерной структуры (). Примечательно, что белки спонтанно складываются в трехмерные объекты.
структуры, которые определяются последовательностью аминокислот в белковом полимере. Таким образом,
Белки являются воплощением перехода от одномерного мира последовательностей к
трехмерный мир молекул, способных к разнообразным
деятельность . - 2.
-
Белки содержат
широкий спектр функциональных групп . Эти функциональные группы включают спирты, тиолы,
тиоэфиры, карбоновые кислоты, карбоксамиды и различные основные группы. В сочетании с различными
последовательности, этот набор функциональных групп отвечает за широкий спектр функций белка. Для
Например, химическая реакционная способность, связанная с этими группами, важна для функции
ферментов, белков, катализирующих определенные химические реакции в биологических
системы (см. главы 8–10). - 3.
-
Белки могут взаимодействовать друг с другом и с другими биологическими макромолекулами с образованием сложных ансамблей . Белки в этих сборках могут действовать синергетически, генерируя возможности, не предоставляемые отдельными составляющими белками (). Эти сборки включают макромолекулярные машины, которые выполняют точную репликацию ДНК, передачу сигналов внутри клеток и многие другие важные процессы.
- 4.
-
Некоторые белки довольно жесткие, тогда как другие обладают ограниченной гибкостью . Жесткие единицы могут функционировать как структурные элементы в цитоскелете (внутреннем каркасе внутри клеток) или в соединительной ткани. Части белков с ограниченной гибкостью могут действовать как шарниры, пружины и рычаги, которые имеют решающее значение для функции белка, для сборки белков друг с другом и с другими молекулами в сложные единицы, а также для передачи информации внутри и между клетками () .
Рисунок
Кристаллы человеческого инсулина. Инсулин — это белковый гормон, имеющий решающее значение для поддержания необходимого уровня сахара в крови. (Ниже) Цепочки аминокислот в определенной последовательности (первичная структура) определяют такой белок, как инсулин. Эти цепочки складываются в четко определенные (подробнее …)
Рисунок 3.1
Структура определяет функцию. Белковый компонент механизма репликации ДНК окружает часть двойной спирали ДНК. Структура белка позволяет копировать большие сегменты ДНК без диссоциации механизма репликации (подробнее…)
Рисунок 3.2
Комплексный белковый узел. Электронная микрофотография ткани полета насекомого в поперечном сечении показывает гексагональный массив из двух видов белковых нитей. [Любезно предоставлено доктором Майклом Риди.]
Рис. 3.3
Гибкость и функциональность. Связывая железо, белок лактоферрин претерпевает конформационные изменения, которые позволяют другим молекулам различать формы, не содержащие железа, и связанные с железом.
- 3.1. Белки построены из набора из 20 аминокислот
- 3.2. Первичная структура: аминокислоты связаны пептидными связями с образованием полипептидных цепей
- 3.3. Вторичная структура: полипептидные цепи могут складываться в регулярные структуры, такие как альфа-спираль, бета-лист, витки и петли
- 3.4. Третичная структура: водорастворимые белки складываются в компактные структуры с неполярными ядрами
- 3.5. Четвертичная структура: полипептидные цепи могут собираться в многосубъединичные структуры
- 3.6. Аминокислотная последовательность белка определяет его трехмерную структуру
- Резюме
- Приложение: Кислотно-основные понятия
- Проблемы
Белки | Основы биологии
Белки — это строительные блоки жизни.Они жизненно важны для нашего существования и присутствуют в каждом организме на Земле.
Белки — это наиболее распространенные молекулы, обнаруживаемые в клетках. Фактически, они составляют больше сухого вещества клетки, чем липиды, углеводы и все другие молекулы вместе взятые.
Белок состоит из одной или нескольких полипептидных цепей, и каждая полипептидная цепь построена из более мелких молекул, называемых «аминокислотами». Всего существует 20 аминокислот, которые можно упорядочить в триллионы и триллионы различных способов для создания белков, выполняющих огромное количество функций.
Белки на самом деле являются наиболее структурно сложными молекулами, известными биологии.
Функции белков
Белки бывают самых разных форм и выполняют широкий спектр функций. Примеры белков включают ферменты, антитела и некоторые гормоны, которые помогают ускорить химические реакции, защищают от болезней и регулируют активность клеток.
Белки также играют роль в движении, структурной поддержке, хранении, связи между клетками, пищеварении и транспортировке веществ по телу.
Движение
Моторные белки, такие как миозин и динеины, обладают способностью преобразовывать химическую энергию в движение. Миозин — это белок, содержащийся в мышцах, который вызывает сокращение мышечных волокон в мышцах.
Динеины обеспечивают питание жгутиков. Жгутики — это длинные тонкие структуры, прикрепленные к внешней стороне определенных клеток, таких как сперматозоиды, и отвечают за их подвижность.
Структура и поддержка
Многие белки обеспечивают структурную поддержку определенных частей организма.Например, кератин — это белок, содержащийся во внешних слоях кожи, который делает кожу сильным защитным слоем для внешнего мира. Кератин также является структурным белком, из которого состоят волосы, рога и ногти.
Сотовая связь
Клетки взаимодействуют с окружающей средой и другими клетками. Рецепторные белки в клеточной мембране получают сигналы извне клетки и передают сообщения в клетку. Как только сигнал попадает в клетку, он обычно передается между несколькими белками, прежде чем достигнет своего конечного пункта назначения (также чаще всего белка).
Пищеварение
Пищеварение обеспечивается, как вы уже догадались, белками. Ферменты — это белки, которые стимулируют пищеварение, ускоряя химические реакции.
Пищеварение — это расщепление пищи из крупных нерастворимых молекул на более мелкие, которые могут растворяться в воде. Поскольку более мелкие молекулы растворимы в воде, они могут попадать в кровь и переноситься по телу.
Пищеварительные ферменты — это ферменты, ответственные за расщепление молекул пищи на более мелкие водорастворимые молекулы.Вот некоторые примеры пищеварительных белков:
- Амилаза — фермент в слюне, который расщепляет крахмал на растворимые сахара
- Липаза — расщепляет жиры и другие липиды
- Пепсин — расщепляет белки в пище
Транспорт кислорода
Гемоглобин — еще один чрезвычайно важный белок для животных, таких как млекопитающие и птицы. Это белок крови, который связывается с кислородом, чтобы кислород мог транспортироваться по телу.
Гемоглобин содержит атом железа.Химическая структура гемоглобина вокруг атома железа позволяет кислороду связываться с железом, а затем высвобождаться в ткани, лишенные кислорода.
Очевидно, что белки чрезвычайно важны для здорового функционирования организма. Большинство примеров, которые я использовал, являются белками животного происхождения, но белки не менее важны для других форм жизни, таких как растения, грибы и бактерии.
Строительные блоки белков
Аминокислоты являются строительными блоками белков.Всего в природе существует 20 различных аминокислот. Аминокислоты могут связываться друг с другом самыми разными способами, создавая разные белки.
Химическая структура аминокислот — ключ к тому, почему белки стали основой жизни. Аминокислота состоит из карбоксильной группы (химическая структура -COOH), аминогруппы (-NH₂) и боковой цепи, состоящей в основном из углерода и водорода.
Сайдчейн часто называют группой R. Различия в группе R — это то, что отличает 20 аминокислот друг от друга.
В зависимости от структуры группы R аминокислота может быть водорастворимой (полярной), нерастворимой в воде (неполярной) или содержать положительный или отрицательный заряд. Эти характеристики, в свою очередь, влияют на поведение аминокислот при связывании и влияют на общую форму и функцию белка.
Все 20 аминокислот необходимы для хорошего здоровья. Если в организме мало одной из 20 аминокислот, определенные белки не могут быть построены, и потеря их функций вызовет проблемы со здоровьем для организма.
Некоторые аминокислоты могут быть созданы организмом с использованием других молекул, в то время как другие аминокислоты должны быть получены из пищи. Аминокислоты, которые необходимо употреблять в пищу, известны как «незаменимые аминокислоты», потому что они являются неотъемлемой частью здорового питания. Аминокислоты, которые может производить наш организм, известны как «заменимые аминокислоты».
Полипептиды
Полипептид представляет собой цепочку аминокислот и является простейшей формой белка. Аминокислоты связываются вместе, образуя длинные линейные цепи, длина которых может составлять более 2000 аминокислот.
Порядок, в котором аминокислоты связаны друг с другом, определяет окончательную форму и структуру полипептидной цепи. Белок будет содержать один полипептид или несколько полипептидов, связанных вместе с образованием больших сложных белков.
Аминокислоты связаны вместе между аминогруппой (-NH₂) одной аминокислоты и карбоксильной группой (-COOH) второй аминокислоты.
Поскольку две аминокислоты связываются вместе, два иона водорода удаляются из аминогруппы, а кислород удаляется из карбоксильной группы.Аминогруппа и карбоксильная группа связываются вместе, и в качестве побочного продукта образуется молекула воды. Связь известна как «пептидная связь».
Соединение нескольких аминокислот вместе пептидными связями создает основу полипептида с группой R, отходящей от каждой аминокислоты. Как упоминалось ранее, каждая группа R из 20 аминокислот имеет свою уникальную структуру и химические свойства. Структура и химические свойства (такие как реакционная способность и температура кипения) полипептида и, в конечном итоге, белка определяются уникальной последовательностью групп R, которые отходят от основной цепи полипептида.Когда группы R притягиваются или отталкиваются друг от друга, полипептидная цепь изгибается и скручивается в белок уникальной формы.
Структура белка
Белки имеют четыре уровня структуры, все из которых мы уже упоминали на этой странице. Эти четыре уровня известны как первичная, вторичная, третичная и четвертичная структура белка.
Первичная структура
Первичная структура — это определенная последовательность аминокислот, то есть порядок, в котором они связаны друг с другом.Точный порядок связывания аминокислот определяется информацией, хранящейся в генах.
Посредством процессов, называемых транскрипцией и трансляцией, ДНК предоставляет клеткам всю необходимую информацию для создания точной первичной структуры для тысяч различных белков. Первичная структура определяет вторичную и третичную структуры белков.
Вторичная структура
Вторичная структура белка образована водородными связями между атомами вдоль основной цепи полипептидной цепи.
Помня, что каждая аминокислота имеет карбоксильную группу и аминогруппу, небольшой отрицательный заряд кислорода карбоксильной группы образует слабую связь с небольшим положительным зарядом атома водорода аминогруппы другой аминокислоты. Водородные связи слабые, но многие из них создают достаточно прочности, чтобы влиять на форму полипептидной цепи.
Водородные связи заставляют основную цепь полипептида складываться и скручиваться в две возможные формы — α-спираль и β-складчатые листы.Спираль α (греческая буква «альфа») представляет собой спираль, похожую на двойную спираль известной цепи ДНК, но только с одной спиралью, и образована водородными связями между каждой четвертой аминокислотой. Спираль α обычна в структурных белках, таких как кератин.
Складчатые листы β (греческая буква «бета») образуются, когда водородные связи возникают между двумя или более соседними полипептидными цепями и являются обычными для глобулярных белков (см. Ниже в разделе «Типы белков»).
Третичная структура
Третичная структура — это окончательная форма, которую принимает полипептидная цепь, и определяется группами R.Притяжение и отталкивание между различными группами R изгибает и складывает полипептид, создавая окончательную трехмерную форму белка.
Четвертичная структура
Не все белки имеют четвертичную структуру. Четвертичная структура возникает только тогда, когда несколько полипептидных цепей объединяются вместе с образованием большого сложного белка. В таких случаях каждый полипептид называют «субъединицей».
Гемоглобин является примером белка с четвертичной структурой. У большинства животных гемоглобин состоит из четырех глобулярных субъединиц.
Типы белков
Существует четыре основных типа белков. Наиболее известны глобулярные белки. Остальные три типа белков — это волокнистые, мембранные и неупорядоченные белки.
Глобулярные белки
Глобулярные белки — это любой белок, имеющий сферическую форму в своей третичной структуре. К ним относятся многие ферменты, антитела и белки, такие как гемоглобин.
Глобулярные белки растворимы в воде и создаются за счет притяжения и отталкивания различных R-групп водой.Полярные R-группы аминокислот в белках растворимы в воде, а неполярные R-группы нерастворимы в воде. Глобулярные белки образуются, потому что неполярные группы R прячутся во внутренних частях белка, а полярные группы R располагаются на внешней поверхности, которая подвергается воздействию окружающей воды.
Волокнистые белки
Волокнистые белки представляют собой удлиненные белки, не имеющие какой-либо третичной структуры. Вместо того, чтобы изгибаться и складываться с образованием глобулярного белка, волокнистые белки остаются в своей линейной вторичной структуре.Часто они являются важными структурными и поддерживающими белками.
Волокнистые белки нерастворимы в воде и часто имеют повторяющиеся структуры аминокислот вдоль их полипептидной цепи. Примеры волокнистых белков включают коллаген, кератин и шелк.
Мембранные белки
Мембранный белок — это любой белок, обнаруженный внутри или прикрепленный к клеточной мембране. Это уникальные белки из-за уникальной среды, в которой они существуют.
Клеточные мембраны состоят из двойного слоя фосфолипидов.Внутренние части клеточной мембраны неполярны, а внешние — полярны. Чтобы мембранные белки успешно существовали через клеточную мембрану, они должны содержать определенные неполярные и полярные участки.
Неупорядоченные белки
Открытие неупорядоченных белков в начале 2000-х годов бросило вызов историческому мышлению о белках. До этого считалось, что функция белка зависит от его фиксированной трехмерной структуры. Однако неупорядоченные белки не имеют упорядоченной структуры своей формы.
Некоторые белки могут быть полностью неструктурированными, в то время как другие частично структурированы с определенными неструктурированными участками. Другие белки обладают способностью существовать как неупорядоченные белки только для образования фиксированной структуры после связывания с другими молекулами.
Последний раз редактировалось: 23 апреля 2016 г.
БЕСПЛАТНЫЙ 6-недельный курс
Введите свои данные, чтобы получить доступ к нашему БЕСПЛАТНО 6-недельному вводному курсу электронной почты по биологии.
Узнайте о животных, растениях, эволюции, древе жизни, экологии, клетках, генетике, областях биологии и многом другом.
Успех! Письмо с подтверждением было отправлено на адрес электронной почты, который вы только что указали. Проверьте свою электронную почту и убедитесь, что вы щелкнули ссылку, чтобы начать наш 6-недельный курс.
3.7: Белки — Биология LibreTexts
Протеиновый коктейль
Напитки, подобные этому коктейлю, содержат много белка. Такие напитки популярны среди людей, которые хотят нарастить мышцы, потому что мышечная ткань состоит в основном из белка. Составление мышц — лишь одна из множества функций этого удивительно разнообразного класса биохимических веществ.
Рисунок \ (\ PageIndex {1} \): протеиновый коктейль
Что такое белки?
Рисунок \ (\ PageIndex {2} \): Общая структура аминокислот. Эта модель показывает общую структуру всех аминокислот. Только боковая цепь R варьируется от одной аминокислоты к другой. Например, в аминокислоте глицине боковая цепь представляет собой просто водород (H). В отличие от глутаминовой кислоты боковой цепью является \ (\ ce {Ch3Ch3COOH} \) Ch3Ch3COOH. Различные боковые цепи придают аминокислотам разные химические свойства. Порядок аминокислот вместе со свойствами аминокислот определяет форму белка, а форма белка определяет функцию белка.КЛЮЧ: H = водород, N = азот, C = углерод, O = кислород, R = переменная боковая цепь.
Белки — это органические соединения, содержащие углерод, водород, кислород, азот и, в некоторых случаях, серу. Эти соединения выполняют множество важных функций внутри клетки (см. Ниже). Белки состоят из более мелких единиц, называемых аминокислотами . Для производства белков необходимо 20 различных распространенных аминокислот. Все аминокислоты имеют одинаковую базовую структуру, которая показана на рисунке \ (\ PageIndex {3} \).Только боковая цепь (обозначенная на рисунке буквой R) отличается от одной аминокислоты к другой. Эти боковые цепи могут варьироваться по размеру от одного атома водорода в глицине до большой гетероциклической группы в триптофане. Вариабельная боковая цепь придает каждой аминокислоте уникальные свойства. Боковые цепи также могут характеризовать аминокислоту как (1) неполярную или гидрофобную, (2) нейтральную (незаряженную), но полярную, (3) кислую, с чистым отрицательным зарядом, и (4) основную, с чистым положительным зарядом при нейтральный pH.
Белки могут отличаться друг от друга количеством и последовательностью (порядком) аминокислот.Именно из-за боковых цепей аминокислот белки с разными аминокислотными последовательностями имеют разные формы и разные химические свойства. Маленькие белки могут содержать всего несколько сотен аминокислот. Белки дрожжей содержат в среднем 466 аминокислот. Самыми крупными известными белками являются тайтины, содержащиеся в мышцах и состоящие из более чем 27 000 аминокислот.
Структура белка
Аминокислоты соединяются в молекулу, называемую дипептидом. -ОН карбоксильной группы одной аминокислоты соединяется с атомом водорода аминогруппы другой аминокислоты с образованием воды.Это называется реакцией конденсации — реакцией, в которой две молекулы объединяются, образуя единую молекулу с выделением воды. На рисунке \ (\ PageIndex {3} \)) показан этот процесс. В верхней части изображения показаны две аминокислоты; Обратите внимание, что -OH в аминокислоте 1 и -H в аминокислоте два выделены. Это атомы, которые будут удалены из аминокислот с образованием воды. Это позволяет образовывать ковалентную связь между углеродом карбоксильной группы одной аминокислоты и азотом амина второй аминокислоты.Эта реакция образует молекулу, называемую дипептидом, а ковалентная связь углерод-азот называется пептидной связью и . При многократном повторении в конечном итоге образуется длинная молекула, называемая полипептидом . Очень длинные полипептиды с функциональной конфигурацией называются белками .
Рисунок \ (\ PageIndex {3} \): Аминокислоты соединяются и образуют молекулу, называемую дипептидом. Связь C-N называется пептидной связью. Порядок аминокислот условно показан со свободной аминогруппой слева и свободной карбоксильной группой справа.
Белки могут иметь до четырех уровней структуры, от первичного до четвертичного, как описано и показано на диаграмме ниже, что дает им потенциал для огромного разнообразия:
- Первичная структура белка — это последовательность аминокислот в его полипептидной цепи (ах). Эта последовательность аминокислот определяет более высокие уровни структуры белка и кодируется генами.
- Вторичная структура белка состоит из регулярно повторяющихся локальных структур, стабилизированных водородными связями между карбоксильными и аминогруппами основной цепи.Наиболее распространенные вторичные структуры включают альфа-спираль и бета-лист. Поскольку вторичные структуры являются локальными, в одной и той же молекуле белка может присутствовать множество областей различных вторичных структур.
- Третичная структура белка относится к общей трехмерной форме одной молекулы белка. Это определяется пространственным соотношением нековалентных и ковалентных связей между группами «R» удаленных аминокислот в полипептиде. Третичная структура — это то, что контролирует основную функцию белка.
- Не все белки имеют окончательную, четвертичную структуру. Это структура, образованная несколькими белковыми молекулами, которые функционируют вместе как единый белковый комплекс.
Рисунок \ (\ PageIndex {4} \): Уровни структуры белка, называемого гемоглобином.
Функции белков
Разнообразие белковых структур объясняет, как этот класс биохимических соединений может играть столь важную роль в живых существах. Каковы роли белков?
- Некоторые белки имеют структурные функции.Они могут помочь клеткам сохранять форму или образовывать мышечные ткани.
- Многие белки представляют собой ферменты, ускоряющие химические реакции в клетках. Ферменты обычно очень специфичны и ускоряют только одну или несколько химических реакций. Известно, что тысячи различных биохимических реакций катализируются ферментами, в том числе большинство реакций, участвующих в метаболизме. Реакция без фермента может занять миллионы лет, тогда как с правильным ферментом она может занять всего несколько миллисекунд!
- Другие белки являются антителами.Это белки, которые связываются с определенными чужеродными веществами, такими как белки на поверхности бактериальных клеток. Это нацелено на разрушение клеток.
- Тем не менее, другие белки несут сообщения или материалы. Например, белок под названием миоглобин — это связывающий кислород белок, обнаруженный в мышечных тканях большинства млекопитающих, включая человека. Вы можете увидеть модель третичной структуры миоглобина на рисунке ниже.
Рисунок \ (\ PageIndex {5} \): Миоглобин — это белок, который содержится в мышечных тканях большинства млекопитающих.Он связывается с кислородом, чтобы снабдить клетки этим элементом. Модель показывает трехмерную структуру белка.
Основная характеристика белков, обеспечивающая их разнообразный набор функций, — это их способность специфически и прочно связывать другие молекулы. Например, миоглобин может специфически и прочно связываться с кислородом. Область белка, отвечающая за связывание с другой молекулой, известна как сайт связывания . Этот сайт часто представляет собой углубление на молекулярной поверхности, в значительной степени определяемое третичной структурой белка.
Потребление, переваривание и синтез белка
Белки необходимы для питания человека и других животных. Мы не можем производить все необходимые нам аминокислоты, поэтому мы должны получать некоторые из них из продуктов, которые мы потребляем. В процессе пищеварения мы расщепляем белки пищи на свободные аминокислоты, которые затем можно использовать для синтеза наших собственных белков. Синтез белка из мономеров аминокислот происходит во всех клетках и контролируется генами. После того, как синтезируются новые белки, они, как правило, не хранятся очень долго, прежде чем они расщепятся и их аминокислоты будут переработаны.Продолжительность жизни белка в клетках млекопитающих обычно составляет всего день или два.
Обзор
- Что такое белки?
- Как две аминокислоты соединяются вместе, чтобы образовать дипептид?
- Обозначьте четыре уровня структуры белка.
- Определите четыре функции белков.
- Объясните, почему белки могут выполнять так много разных функций в живых организмах.
- Какова роль белков в рационе человека?
- Можно ли получить белок как с альфа-спиралью, так и с бета-листом? Почему или почему нет?
- Если в гене есть мутация, которая вызывает кодирование другой аминокислоты, чем та, которая обычно кодируется в этом положении в белке, повлияет ли это на:
- Первичная структура белка? Поясните свой ответ.
- Высшие структуры (вторичные, третичные, четвертичные) белка? Поясните свой ответ.
- Функция белка? Поясните свой ответ.
- Как называется область белка, отвечающая за связывание с другой молекулой? Какие уровни белковой структуры создают эту область?
- Расположите в порядке от самого маленького до самого большого уровня организации:
- пептид; белок; аминокислота; полипептид
- Верно или неверно. Вы можете определить функцию всех белков по их четвертичной структуре.
- Объясните, что означает чтение, когда говорится, что аминокислоты «перерабатываются».
Посмотрите видео ниже, чтобы узнать, как протеомика, изучение белков, может быть использована в исследованиях рака.
2.3: Структура и функции — Белки I
Синтез белков происходит в рибосомах и происходит путем присоединения карбоксильного конца первой аминокислоты к аминоконцу следующей (Рисунок 2.19). Конец белка, имеющий свободную α-аминогруппу, называют аминоконцом или N-концом. Другой конец называется карбоксильным концом или С-концом, поскольку он содержит единственную свободную α-карбоксильную группу. Все другие α-аминогруппы и α-карбоксильные группы связаны с образованием пептида. Рис. 2.19. Связывание аминокислот посредством связей образования пептидных связей, которые соединяют соседние аминокислоты вместе. Белки синтезируются, начиная с аминоконца и заканчивая карбоксильным концом.
Схематично на рисунке 2.18 мы можем видеть, как последовательные R-группы белка расположены в чередующейся ориентации по обе стороны от полипептидной цепи. Подобная организация R-групп не случайна. Стерические затруднения могут возникать, когда последовательные R-группы ориентированы на одной стороне пептидного остова (рис. 2.20)
Первичная структура
Первичная структура является определяющим фактором общей конформации белка. Первичная структура любого белка достигла своего текущего состояния в результате мутации и отбора в течение эволюционного времени.Первичная структура белков определяется последовательностью кодирующей ее ДНК в геноме. Области ДНК-специфических белков известны как кодирующие области (или гены).
Последовательности оснований этих областей непосредственно определяют последовательность аминокислот в белках с однозначным соответствием между кодонами (группами из трех последовательных оснований) в ДНК и аминокислотами в кодируемом белке. Последовательность кодонов в ДНК, скопированная в информационную РНК, определяет последовательность аминокислот в белке.(Рисунок 2.21).
Рисунок 2.21 — От РНК к аминокислотам — генетический код Wikipedia
Порядок, в котором аминокислоты соединяются вместе при синтезе белка, начинает определять набор взаимодействий между аминокислотами, даже когда синтез происходит. То есть полипептид может сворачиваться даже в процессе производства. Порядок структур R-группы и результирующие взаимодействия очень важны, потому что ранние взаимодействия влияют на более поздние взаимодействия. Это потому, что взаимодействия начинают создавать структуры — вторичные и третичные.Если спиральная структура (вторичная структура), например, начинает формироваться, возможности взаимодействия конкретной аминокислоты R-группы могут быть другими, чем если бы спираль не образовалась (рис. 2.22). Взаимодействия R-группы также могут вызывать изгибы в полипептидной последовательности (третичной структуре), и эти изгибы могут создавать (в некоторых случаях) возможности для взаимодействий, которые были бы невозможны без изгиба, или предотвращать (в других случаях) аналогичные возможности взаимодействия.
Вторичная структура
По мере того, как синтез белка прогрессирует, взаимодействия между аминокислотами, близкими друг к другу, начинают происходить, что приводит к возникновению локальных паттернов, называемых вторичной структурой.Эти вторичные структуры включают хорошо известные α-спираль и β-тяжи. Оба были предсказаны Линусом Полингом, Робертом Кори и Германом Брэнсоном в 1951 году. Каждая структура имеет уникальные особенности.
α-спираль
Рисунок 2.22 — α-Спираль. Водородные связи (пунктирные линии) между кислородом карбонила и водородом амина стабилизируют структуру. Изображение Алейи Ким
α-Спираль имеет спиральную структуру с 3,6 аминокислотами на один виток спирали (5 витков спирали = 18 аминокислот).Спирали преимущественно правосторонние — только в редких случаях, например, в последовательностях с большим количеством глицинов, могут образовываться левые α-спирали. В α-спирали водородные связи образуются между группами C = O и группами N-H в основной цепи полипептида, которые находятся на расстоянии четырех аминокислот. Эти водородные связи являются основными силами, стабилизирующими α-спираль.
Рисунок 2.23 — α-спирали в белке со структурным доменом лейциновой молнии. Α-Спирали показаны синим и зеленым цветом и связаны с двойной спиралью ДНК коричневого цвета.
Мы используем термины «подъем», «повторение» и «шаг» для описания параметров любой спирали. Повторение — это количество остатков в спирали, прежде чем она начнет повторяться. Для α-спирали повторение составляет 3,6 аминокислоты на оборот спирали. Подъем — это расстояние, на которое спираль поднимается с добавлением каждого остатка. Для α-спирали это 0,15 нм на аминокислоту. Шаг — это расстояние между полными витками спирали. Для α-спирали это 0,54 нм. Стабильность α-спирали повышается за счет присутствия аминокислоты аспартата.
Рисунок 2.24 — Скульптура α-спирали за пределами дома, где прошло детство Линуса Полинга, Википедия Рисунок 2.25 — Винтовое колесо Изображение α-спирали. Используется однобуквенный генетический код. Спираль начинается с серина №77 справа и заканчивается лизином №92 справа внизу. Гидрофобные аминокислоты показаны желтым цветом, а ионизирующие аминокислоты — синим. Гидрофобные аминокислоты имеют тенденцию взаимодействовать друг с другом, а не с ионизирующими аминокислотами. Википедия
β-прядь / лист
Фигура 2.26 — β-прядь
Спираль — это, конечно, трехмерный объект. Уплощенная форма спирали в двух измерениях — обычное описание β-нити. У β-прядей есть изгибы, а не витки, которые иногда называют складками, как складки на занавеске. β-нити могут быть организованы для образования тщательно организованных структур, таких как листы, бочки и другие конструкции.
β-цепочечные структуры более высокого порядка иногда называют супервторичными структурами), поскольку они включают взаимодействия между аминокислотами, не близкими по первичной последовательности.Эти структуры также стабилизируются водородными связями между карбонильными атомами кислорода и атомами водорода аминогрупп в основной цепи полипептида (рис. 2.28). В структуре более высокого порядка нити могут быть расположены параллельно (ориентации от амино к карбоксилу одинаковы) или антипараллельно (ориентации от амино к карбоксилу противоположны друг другу (на рисунке 2.27 направление нити показано стрелкой на ленте диаграммы).
Оборотов
Рисунок 2.27 — Изображения на ленте супервторичных β-листов (A-D) и расположения α-спиралей (E-F) Изображение от Aleia Kim
витков (иногда называемых обратными витками) — это тип вторичной структуры, которая, как следует из названия, вызывает поворот в структуре полипептидной цепи.Повороты в конечном итоге приводят к возникновению третичной структуры, вызывая прерывания во вторичных структурах (α-спирали и β-цепи) и часто служат связующими областями между двумя областями вторичной структуры в белке. Пролин и глицин по очереди играют общие роли, обеспечивая меньшую гибкость (начало поворота) и большую гибкость (облегчение поворота) соответственно.
Рисунок 2.28 — Компоненты β-листа в параллельном расположении. Водородные связи желтого цвета. Изображение Алейи Ким
Существует как минимум пять типов поворотов, из которых множество вариаций приводит к множеству разных поворотов.Пять типов поворотов:
• δ-витки — концевые аминокислоты разделены одной пептидной связью
• γ-витки — разделение двумя пептидными связями
• β-витки — разделение тремя пептидными связями
• α-витки — разделение четырьмя пептидными связями
• π-витки — разделение пятью связями
Из них β-витки являются наиболее распространенной формой, а δ-витки являются теоретическими, но маловероятными из-за стерических ограничений. На рисунке 2.29 изображен β-разворот.
3 10 спиралей
Рисунок 2.29 — β-разворот. R-группы показаны оранжевым цветом, атомы водорода — желтым, атомы углерода — углем, атомы азота — фиолетовым, а атомы кислорода — зеленым. Стабилизирующая водородная связь обозначена пунктирной линией. Image by Aleia Kim
Помимо α-спирали, β-цепей и различных поворотов, в белках видны и другие регулярные, повторяющиеся структуры, но встречаются гораздо реже. Спираль 3 10 является четвертой по распространенности вторичной структурой в белках, составляя около 10-15% всех спиралей.Спираль получила свое название от того факта, что она содержит 10 аминокислот на 3 витка. Это правша. Водородные связи образуются между аминокислотами, разнесенными на три остатка. Чаще всего спираль 3 10 появляется на аминном или карбоксильном конце α-спирали. Как и α-спираль, спираль 3 10 стабилизируется присутствием аспартата в ее последовательности.
Рисунок 2.30 — Вид сверху на 310 Helix. Карбонильные группы выделены красным цветом и направлены вверх. Обратите внимание на почти идеальную 3-кратную симметрию Википедии (Рисунок 2).31 — Резонанс пептидной связи Википедия Рисунок 2.32 — π-спираль Википедия
π-спирали
Рисунок 2.33 — Плоскости (светло-голубые), определяемые характером двойной связи пептидной связи Изображение Алейи Ким
π-спираль можно рассматривать как особый тип α-спирали. Некоторые источники описывают это как α-спираль с дополнительной аминокислотой, застрявшей в ней (рис. 2.32). π-спирали не совсем редки, они встречаются по крайней мере один раз в 15% всех белков. Как и α-спираль, π-спираль является правой, но если α-спираль содержит 18 аминокислот в 5 витках, то π-спираль имеет 22 аминокислоты в 5 витках.π-спирали обычно не растягиваются на очень большие расстояния. Большинство из них имеют длину всего около 7 аминокислот, и последовательность почти всегда находится в середине α-спиральной области.
Земельные участки в Рамачандране
Рисунок 2.34 — Углы вращения ω, ψ и φ в пептиде Изображение Алейи Ким
В 1963 году Г. Рамачандран, Ч. Рамакришнан и В. Сасисекхаран описали новый способ описания структуры белка. Если рассматривать основу полипептидной цепи, она состоит из повторяющегося набора из трех связей.Последовательно (в направлении от амино к карбоксилу) они представляют собой 1) вращающуюся связь (ψ) между α-углеродом и α-карбоксилом, предшествующую пептидной связи (см. ЗДЕСЬ), 2) невращающуюся пептидную связь (ω) между α -карбоксильная и α-аминная группы), и 3) вращающаяся связь (φ) между α-амином и α-углеродом, следующая за пептидной связью (см. ЗДЕСЬ). Обратите внимание на рисунки 2.33 и 2.34, что направление от амино к карбоксилу справа налево.
Присутствие карбонильного кислорода в α-карбоксильной группе позволяет пептидной связи существовать как резонансная структура, что означает, что она некоторое время ведет себя как двойная связь.Двойные связи, конечно, не могут вращаться, но связи по обе стороны от них имеют некоторую свободу вращения. Углы φ и ψ ограничены определенными значениями, потому что некоторые углы приведут к стерическим затруднениям. Кроме того, каждый тип вторичной структуры имеет характерный диапазон значений φ и ψ.
Рисунок 2.35 — Теоретический график Рамачандрана Изображение Пенелопы Ирвинг
Рамачандран и его коллеги провели теоретические расчеты энергетической стабильности всех возможных углов от 0 ° до 360 ° для каждого из углов φ и ψ и нанесли результаты на график Рамачандрана (также называемый график φ-ψ), очерчивая области углов, которые теоретически были наиболее стабильными (Рисунок 2.35).
Были идентифицированы три основные области стабильности, соответствующие углам φ-ψ β-тяжей (вверху слева), правым α-спиралям (внизу слева) и левым α-спиралям (вверху справа). Графики предсказанной стабильности удивительно точны по сравнению с углами φ-ψ реальных белков.
Прогноз вторичной структуры
Таблица 2.3 — Относительные тенденции каждой аминокислоты находиться во вторичной структуре. Более высокие значения указывают на большую тенденцию. Изображение Пенелопы Ирвинг
.
Сравнивая первичную структуру (аминокислотные последовательности) с известными трехмерными белковыми структурами, можно подсчитать каждый раз, когда аминокислота обнаруживается в α-спирали, β-цепи / листе или витке.Компьютерный анализ тысяч этих последовательностей позволяет определить вероятность появления любой данной аминокислоты в каждой из этих структур. Используя эти тенденции, можно с точностью до 80% предсказать области вторичной структуры в белке, основываясь исключительно на аминокислотной последовательности.
Это видно в таблице 2.3. Наличие в первичной последовательности трех последовательных аминокислот с относительной тенденцией выше единицы является индикатором того, что эта область полипептида находится в соответствующей вторичной структуре.Онлайн-ресурс для предсказания вторичных структур под названием PSIPRED доступен ЗДЕСЬ.
Гидрофобность
Таблица 2.4 — Оценка гидропатии
Химический состав аминокислотных R-групп влияет на структуры, в которых они чаще всего встречаются. Подмножества их химических свойств могут дать ключ к разгадке структуры, а иногда и клеточного местоположения. Ярким примером является гидрофобность (склонность к предотвращению образования воды) некоторых R-групп. Учитывая водную среду клетки, такие R-группы вряд ли находятся на внешней поверхности свернутого белка.
Однако это правило не выполняется для областей белка, которые могут быть встроены в липидные бислои мембран клеток / органелл. Это связано с тем, что области таких белков, которые образуют трансмембранные домены, находятся в гидрофобной среде в середине липидного бислоя.
Неудивительно, что сканирование первичных последовательностей на наличие участков гидрофобных аминокислот определенного размера / разнесения может помочь идентифицировать белки, обнаруженные в мембранах. В таблице 2.4 показаны значения гидрофобности для R-групп аминокислот.В этом наборе шкала изменяется от положительных значений (гидрофобные) до отрицательных (гидрофильные). График гидропатии KyteDoolittle для мембранного белка протоонкогена RET показан на рисунке 2.36. Две области белка очень гидрофобны, что видно из пиков около аминокислот 5-10 и 630-640. Можно разумно ожидать, что такие области будут располагаться либо внутри свернутого белка, либо быть частью трансмембранных доменов.
Случайные катушки
Фигура 2.36 График гидропатии Кайта-Дулиттла для протоонкогена RET Wikipedia
Некоторые участки белка не предполагают регулярной, различимой структуры и, как иногда говорят, не имеют вторичной структуры, хотя могут иметь водородные связи. Такие сегменты описаны как находящиеся в случайных спиралях и могут иметь текучесть в своей структуре, что приводит к тому, что они имеют несколько стабильных форм. Случайные катушки можно идентифицировать с помощью спектроскопических методов, таких как круговой дихроизм в Википедии и ядерный магнитный резонанс (ЯМР), при котором наблюдаются отличительные сигналы.См. Также метаморфные белки (ЗДЕСЬ) и белки с внутренней неупорядоченностью (ЗДЕСЬ).
Рисунок 2.37 — Изображение β-шпильки на ленте. Показаны две бирюзовые β-нити, взаимодействующие друг с другом.
Надвторичная структура
Другой элемент структуры белка сложнее классифицировать, поскольку он включает элементы вторичной и третичной структуры. Названные супервторичной структурой (или структурными мотивами), эти структуры содержат множество соседних компонентов вторичной структуры, расположенных определенным образом и проявляющихся во множестве белков.Поскольку существует множество способов создания вторичных структур из разных первичных структур, аналогичные мотивы могут возникать из разных первичных последовательностей. Пример структурного мотива показан на рис. 2.37.
Третичная структура
Рисунок 2.38 — Сворачивание полипептидной цепи
Белки отличаются друг от друга последовательностью составляющих их аминокислот. Последовательность аминокислот белка определяет форму белка, поскольку химические свойства каждой аминокислоты являются силами, которые вызывают межмолекулярные взаимодействия, чтобы начать создавать вторичные структуры, такие как α-спирали и β-цепи.Последовательность также определяет повороты и случайные спирали, которые играют важную роль в процессе сворачивания белка.
Поскольку форма важна для функции белка, последовательность аминокислот определяет все свойства, которыми обладает белок. По мере того как синтез белка продолжается, отдельные компоненты вторичной структуры начинают взаимодействовать друг с другом, создавая складки, которые сближают аминокислоты, которые не находятся рядом друг с другом в первичной структуре (рис. 2.38). На третичном уровне структуры взаимодействия между R-группами аминокислот в белке, а также между основной цепью полипептида и боковыми группами аминокислот играют роль в сворачивании.
Глобулярные белки
Рисунок 2.39 — Разворачивание (денатурация) белка Wikipedia
Сворачивание приводит к появлению различных трехмерных форм в белках, которые не являются волокнистыми. Эти белки называют глобулярными. Глобулярный белок стабилизируется теми же силами, которые управляют его образованием. К ним относятся ионные взаимодействия, водородные связи, гидрофобные силы, ионные связи, дисульфидные связи и металлические связи. Обработка, такая как нагревание, изменение pH, моющие средства, мочевина и меркаптоэтанол, подавляют стабилизирующие силы и заставляют белок разворачиваться, теряя свою структуру и (обычно) свою функцию (Рисунок 2.39). Благодаря способности тепла и детергентов денатурировать белки, мы готовим пищу и моем руки перед едой — такая обработка денатурирует белки в микроорганизмах на наших руках. У организмов, которые живут в среде с высокой температурой (более 50 ° C), есть белки с изменениями стабилизирующих сил — дополнительные водородные связи, дополнительные солевые мостики (ионные взаимодействия) и компактность могут играть роль в предотвращении развертывания этих белков.
Силы стабилизации белка
Прежде чем рассматривать процесс сворачивания, давайте рассмотрим некоторые силы, которые помогают стабилизировать белки.
Водородные связи
Рисунок 2.40 — Водородные связи (пунктирные линии) между двумя молекулами уксусной кислоты
Водородные связи возникают в результате частично заряженных атомов водорода, находящихся в ковалентных связях. Это происходит, когда атом, с которым связан водород, имеет большую электроотрицательность, чем сам водород, в результате чего водород имеет частичный положительный заряд, потому что он не может удерживать электроны близко к себе (рис. 2.40).
Частично заряженный таким образом водород притягивается к атомам, таким как кислород и азот, которые имеют частичный отрицательный заряд из-за большей электроотрицательности и, таким образом, удерживают электроны ближе к себе.Частично положительно заряженные атомы водорода называются донорами, а частично отрицательные атомы, к которым они притягиваются, называются акцепторами. (См. Рисунок 1.30).
Рисунок 2.41 — Водородная связь в жидкой воде Википедия
Отдельные водородные связи намного слабее ковалентной связи, но вместе они могут оказывать сильное воздействие. Рассмотрим жидкую воду, которая содержит огромное количество водородных связей (рис. 2.41). Эти силы помогают воде оставаться жидкой при комнатной температуре. Другие молекулы, не имеющие водородных связей с молекулярной массой, равной или большей, чем вода, такие как метан или диоксид углерода, являются газами при той же температуре.Таким образом, межмолекулярные взаимодействия между молекулами воды помогают «удерживать» воду вместе и оставаться жидкостью. Примечательно, что только повышение температуры воды до кипения преодолевает силы водородных связей, позволяя воде стать полностью газообразной.
Водородные связи являются важными силами в биополимерах, которые включают ДНК, белки и целлюлозу. Все эти полимеры при кипячении теряют свою естественную структуру. Водородные связи между аминокислотами, которые близки друг к другу по первичной структуре, могут давать регулярные повторяющиеся структуры, такие как спирали или складки, в белках (вторичная структура).
Ионные взаимодействия
Ионные взаимодействия являются важными силами, стабилизирующими структуру белка, которые возникают в результате ионизации R-групп в аминокислотах, составляющих белок. К ним относятся карбоксиламинокислоты (ЗДЕСЬ), амино-аминокислоты, а также сульфгидрил цистеина и иногда гидроксил тирозина.
Гидрофобные силы
Гидрофобные силы стабилизируют структуру белка в результате взаимодействий, которые способствуют исключению воды.Неполярные аминокислоты (обычно находящиеся внутри белков) способствуют связыванию друг с другом, и это имеет эффект исключения воды. Исключенная вода имеет более высокую энтропию, чем вода, взаимодействующая с гидрофобными боковыми цепями. Это связано с тем, что вода выравнивается очень регулярно и определенным образом при взаимодействии с гидрофобными молекулами.
Когда вода не может вступать в такие взаимодействия, она становится гораздо более беспорядочной, чем если бы она могла ассоциироваться с гидрофобными областями.Частично по этой причине гидрофобные аминокислоты находятся во внутренней части белка — поэтому они могут исключать воду и увеличивать энтропию.
Дисульфидные связи
Рисунок 2.42 — Образование дисульфидной связи
Дисульфидные связи, которые образуются, когда две сульфгидрильные боковые цепи цистеина сближаются, ковалентно соединяют вместе различные участки белка и могут придать большую прочность всей структуре (рисунки 2.42 и 2.43) . Ода структуре белка от Кевина Ахерна Двадцать крошечных аминокислот A определяют белок разными способами Их порядок в пептидной цепи определяет формы, которые приобретают белки И когда они скручиваются, это оставляет меня веселым, потому что это делает структуры вторичными. Это третично, мне сказали, что происходит, когда белок сворачивается. Но сложенные цепи просто страшны. Собранные вместе четвертичные. Они — чудеса природы, это точно. Создание проблем, лечение. Дурак может сочинять пептидные стихи. Но белки происходят из рибоземов. Эти соединенные остатки цистеина иногда называют цистин.Дисульфидные связи — самая сильная из сил, стабилизирующих структуру белка.
Рисунок 2.43 — Цистин — два цистеина, соединенные дисульфидной связью
силы Ван-дер-Ваальса
силы Ван-дер-Ваальса — это термин, используемый для описания различных слабых взаимодействий, в том числе вызванных притяжением между полярной молекулой и переходным диполем или между двумя временными диполями. Силы Ван-дер-Ваальса динамичны из-за флуктуирующего характера притяжения и обычно слабы по сравнению с ковалентными связями, но могут быть значительными на очень коротких расстояниях.
Посттрансляционные модификации
Посттрансляционные модификации также могут приводить к образованию ковалентных связей, стабилизирующих белки. Гидроксилирование лизина и пролина в цепях коллагена может привести к сшиванию этих групп, и полученные ковалентные связи помогают укрепить и стабилизировать коллаген.
Складные модели
В настоящее время исследуются две популярные модели сворачивания белков. В первой (модель диффузионного столкновения) процесс начинается с момента зародышеобразования, за которым следует образование вторичной структуры.Столкновения между вторичными структурами (как в β-шпильке на рис. 2.37) позволяют начать складывание. Напротив, в модели нуклеации-конденсации вторичные и третичные структуры образуются вместе.
Сворачивание белков происходит довольно быстро (от 0,1 до 1000 секунд) и может происходить во время синтеза — аминный конец белка может начать складываться еще до того, как образуется карбоксильный конец, хотя это не всегда так.
Процесс складывания
Фигура 2.44 Энергетическая модель сворачивания складывающейся воронки Wikipedia
Предполагается, что сворачивание белка происходит в энергетическом ландшафте «сворачивающейся воронки», в котором нативное состояние свернутого белка соответствует минимально возможной свободной энергии в условиях среды (обычно водного растворителя), в которой белок растворяется. Как видно на диаграмме (рис. 2.44), энергетическая воронка имеет множество локальных минимумов (провалов), в которых сворачивающийся белок может попасть в ловушку при движении вниз по энергетическому графику. Вероятно, играют роль другие факторы, такие как температура, электрические / магнитные поля и пространственные особенности.
Если внешние силы влияют на локальные минимумы энергии во время складывания, это может повлиять на процесс и конечный продукт. Как скорость автомобиля, едущего по дороге, влияет на безопасность поездки, так и энергетические соображения влияют на процесс складывания и направляют его, что в некоторых случаях приводит к полностью функциональным, правильно сложенным белкам и ошибочно свернутым «ошибкам» в других.
Зависание
По мере того, как процесс складывания приближается к минимуму энергии (нижняя часть воронки на Рисунке 2.44), белок может «застрять» в любом из локальных минимумов и не достичь конечного свернутого состояния. Хотя свернутое состояние, в общем, более организовано и, следовательно, имеет меньшую энтропию, чем развернутое состояние, есть две силы, которые преодолевают уменьшение энтропии и продвигают процесс вперед.
Первый — это величина уменьшения энергии, как показано на графике. Поскольку ΔG = ΔH -TΔS, уменьшение ΔH может преодолеть отрицательное значение ΔS, чтобы сделать ΔG отрицательным и подтолкнуть процесс складывания вперед.Благоприятные (пониженные) энергетические условия возникают с образованием ионных связей, водородных связей, дисульфидных связей и металлических связей во время процесса сворачивания. Кроме того, гидрофобный эффект увеличивает энтропию, позволяя гидрофобным аминокислотам внутри свернутого белка исключать воду, тем самым противодействуя влиянию упорядочения структуры белка, делая ΔS менее отрицательным.
Прогноз структуры
Компьютерные программы очень хороши в предсказании вторичной структуры исключительно на основе аминокислотной последовательности, но с трудом определяют третичную структуру с использованием той же информации.Частично это связано с тем, что вторичные структуры имеют повторяющиеся точки стабилизации на основе геометрии, и любая регулярная вторичная структура (например, α-спираль) очень мало меняется от одной к другой. Однако складчатые структуры имеют огромное количество возможных структур, как показывает парадокс Левинталя.
Спектроскопия
Из-за нашей неспособности точно предсказать третичную структуру на основе аминокислотной последовательности, структуры белков фактически определяются с использованием методов спектроскопии.В этих подходах белки подвергаются различным формам электромагнитного излучения, и способы их взаимодействия с излучением позволяют исследователям определять координаты атомов с разрешением Ангстрема по электронной плотности (см. Рентгеновскую кристаллографию) и тому, как взаимодействуют спины ядер (см. ЯМР).
Парадокс Левинталя
В конце 1960-х Сайрус Левинталь обрисовал масштабы сложности проблемы сворачивания белка. Он указал, что для белка из 100 аминокислот он будет иметь 99 пептидных связей и 198 соображений для углов φ и ψ.Если бы каждая из них имела только три конформации, это привело бы к 3198 различным возможным сверткам или 2,95×1094.
Даже если дать разумное количество времени (одна наносекунда) для каждой возможной складки, потребуется больше времени, чем возраст Вселенной, чтобы выполнить выборку всех из них, что ясно означает, что процесс складывания не происходит путем последовательной случайной выборки. и что попытки определить структуру белка путем случайной выборки были обречены на провал. Левинталь, следовательно, предположил, что сворачивание происходит в результате последовательного процесса, который начинается с события зародышеобразования, которое быстро направляет процесс и мало чем отличается от воронкообразного процесса, изображенного на рисунке 2.44.
Болезни неправильного сворачивания белков
Рисунок 2.45 — Неправильная укладка нормального белка PRPc, индуцированная PRPsc Изображение Пенелопы Ирвинг
Правильная укладка белков важна для их функции. Отсюда следует, что неправильная укладка белков (также называемая протеопатией) может иметь последствия. В некоторых случаях это может просто привести к неактивному белку. Неправильная упаковка белков также играет роль при многих заболеваниях, таких как коровье бешенство, болезнь Альцгеймера, болезнь Паркинсона и болезнь Крейтцфельда-Якоба.Многие, но не все, болезни неправильной укладки поражают ткани головного мозга.
Рисунок 2.46 — Коровы с коровьим бешенством теряют способность стоять
Нерастворимые отложения
Неправильно свернутые белки обычно образуют агрегаты, называемые амилоидами, которые вредны для тканей, содержащих их, потому что они меняют свою форму с растворимых на нерастворимые в воде и образуют отложения. Процесс, с помощью которого происходит неправильное свертывание (рис. 2.45), не совсем ясен, но во многих случаях было продемонстрировано, что «затравочный» белок, который неправильно свернут, может вызывать такое же неправильное свертывание в других копиях того же белка.Эти протеины семян известны как прионы, и они действуют как инфекционные агенты, приводя к распространению болезни. Список заболеваний человека, связанных с неправильной упаковкой белков, длинен и продолжает расти. Ссылка на Википедию ЗДЕСЬ.
Прионы
Рисунок 2.47 — Диффузный амилоидоз в кровеносном сосуде (красные точки) Wikipedia
Прионы — это инфекционные белковые частицы, вызывающие трансмиссивные губчатые энцефалопатии (TSE), наиболее известной из которых является коровье бешенство. Другие проявления включают болезнь, скрепи, у овец и болезни человека, такие как болезнь Крейтцфельда-Якоба (CJD), фатальная семейная бессонница и куру.Белок, участвующий в этих заболеваниях, представляет собой мембранный белок, называемый PrP. PrP закодирован в геноме многих организмов и содержится в большинстве клеток организма. PrPc — это название, данное структуре PrP, которая является нормальной и не связана с заболеванием. PrPSc — это название неправильно свернутой формы того же белка, которое связано с развитием симптомов заболевания (рис. 2.45).
Неправильно сложен
Неправильно свернутый PrPSc связан с заболеваниями TSE и действует как инфекционная частица.Третья форма PrP, называемая PrPres, может быть обнаружена в TSE, но не заразна. «Res» PrPres указывает на то, что он устойчив к протеазам. Стоит отметить, что все три формы PrP имеют одинаковую аминокислотную последовательность и отличаются друг от друга только способами складывания полипептидных цепей. Наиболее опасно неправильно свернутой формой PrP является PrPSc из-за его способности действовать как инфекционный агент — затравочный белок, который может вызывать неправильную укладку PrPc, тем самым превращая его в PrPSc.
Функция
Фигура 2.48 — Одна модель распространения прионов Wikipedia
Функция PrPc неизвестна. Мыши, лишенные гена PrP, не имеют серьезных отклонений. У них действительно проявляются проблемы с долговременной памятью, что указывает на функцию PrPc. Стэнли Прусинер, открывший прионы и придумавший этот термин, получил Нобелевскую премию по медицине в 1997 году за свою работу. Я думаю, что если бы я случайно оказался на протеине А, образующем прион, я бы его скрутил и, ради бога, не дай ему совершать ошибки складывания
Амилоиды
Амилоиды — это совокупность неправильно свернутых белковых агрегатов, которые обнаруживаются в организме человека.Вследствие неправильной укладки они нерастворимы и вызывают около двадцати заболеваний человека, включая важные неврологические, связанные с прионами. Заболевания включают (пораженный белок в скобках) — болезнь Альцгеймера (амилоид β), болезнь Паркинсона (α-синуклеин), болезнь Хантингтона (хантингтин), ревматоидный артрит (сывороточный амилоид A), фатальную семейную бессонницу (PrPSc) и другие.
Аминокислотная последовательность играет роль в амилоидогенезе. Полипептиды, богатые глутамином, часто встречаются в прионах дрожжей и человека.Тринуклеотидные повторы важны при болезни Хантингтона. Если последовательность не является фактором, гидрофобная ассоциация между β-листами может играть роль.
Амилоид β
Рисунок 2.49 — Huntingtin
Amyloid β относится к совокупности небольших белков (36-43 аминокислоты), которые, по-видимому, играют роль в болезни Альцгеймера. (Другим фактором является тау-белок.) Фактически, они являются основными компонентами амилоидных бляшек, обнаруживаемых в головном мозге пациентов, страдающих этим заболеванием, и возникают в результате протеолитического расщепления более крупного гликопротеина-предшественника амилоида, называемого амилоидным предшественником белка, интегральной мембраны. белок нервных клеток, функция которых неизвестна.Эту функцию выполняют две протеазы, β-секретаза и γ-секретаза. Амилоидные β-белки неправильно свернуты и, по-видимому, вызывают неправильную укладку других белков и, таким образом, осаждают и формируют амилоид, характерный для этого заболевания. Бляшки токсичны для нервных клеток и вызывают деменцию, характерную для этого заболевания.
Считается, что агрегация белков амилоида β во время неправильной укладки приводит к генерации активных форм кислорода и что это средство, с помощью которого нейроны повреждаются.Неизвестно, какова реальная функция амилоида β. Аутосомно-доминантные мутации в белке приводят к раннему началу заболевания, но это происходит не более чем в 10% случаев. Стратегии лечения заболевания включают ингибирование секретаз, которые генерируют пептидные фрагменты из белка-предшественника амилоида.
Хантингтин
Хантингтин является центральным геном болезни Хантингтона. Белок, сделанный из него, богат глутамином, с 6-35 такими остатками в форме дикого типа.При болезни Хантингтона этот ген мутирует, увеличивая количество глутаминов в мутантном белке от 36 до 250. Размер белка зависит от количества глутаминов в мутантном белке, но белок дикого типа содержит более 3100 аминокислот. кислоты и молекулярный вес около 350 000 Да. Его точная функция неизвестна, но хантингтин содержится в нервных клетках, причем самый высокий уровень находится в головном мозге. Считается, что он, возможно, играет роль в транспорте, передаче сигналов и защите от апоптоза.Хантингтин также необходим для раннего эмбрионального развития. Внутри клетки хантингтин локализован в основном в микротрубочках и пузырьках.
Тринуклеотидный повтор
Ген хантингтина содержит множество копий последовательности CAG (называемой тринуклеотидными повторами), которая кодирует множество глутаминов в белке. Болезнь Хантингтона возникает, когда при копировании ДНК гена образуются дополнительные копии последовательности CAG. Расширение повторяющихся последовательностей может происходить из-за скольжения полимеразы относительно матрицы ДНК во время репликации.В результате могут быть созданы несколько дополнительных копий тринуклеотидного повтора, в результате чего будут получены белки с различным числом остатков глутамина. Без проблем можно выдержать до 35 повторов. Однако количество повторов может увеличиваться в течение жизни человека с помощью того же механизма. Люди с 36-40 повторами начинают проявлять признаки болезни, а если их больше 40, болезнь будет присутствовать.
Молекулярные шапероны
Важность правильного сворачивания белков подчеркивается заболеваниями, связанными с неправильным сворачиванием белков, поэтому неудивительно, что клетки расходуют энергию для облегчения правильного сворачивания белков.Клетки используют два класса белков, известных как молекулярные шапероны, для облегчения такого складывания в клетках. Молекулярные шапероны бывают двух видов: шапероны и шаперонины. Примером первой категории является класс белков Hsp70. Hsp означает «белок теплового шока», исходя из того факта, что эти белки впервые были обнаружены в больших количествах в клетках, которые на короткое время подвергались воздействию высоких температур. Hsps помогает клеткам при стрессах, возникающих в результате теплового шока и воздействия окислительных условий или токсичных тяжелых металлов, таких как кадмий и ртуть.Однако они также играют важную роль в нормальных условиях, когда они способствуют правильной укладке полипептидов, предотвращая аберрантные взаимодействия, которые могут привести к неправильной укладке или агрегации. Белки Hsp70 обнаружены почти во всех клетках и используют гидролиз АТФ, чтобы стимулировать структурные изменения формы шаперона, чтобы приспособиться к связыванию белков-субстратов. Связывающий домен Hsp70s содержит β-цилиндрическую структуру, которая обвивает полипептидную цепь субстрата и имеет сродство к гидрофобным боковым цепям аминокислот.Как показано на рисунке 2.50, Hsp70 связывается с полипептидами, когда они выходят из рибосом во время синтеза белка. Связывание субстрата стимулирует гидролиз АТФ, чему способствует другой белок теплового шока, известный как Hsp40. Гидролиз АТФ заставляет Hsp70 принимать закрытую конформацию, которая помогает экранировать открытые гидрофобные остатки и предотвращать агрегацию или локальную неправильную укладку.
После завершения синтеза белка АДФ высвобождается и замещается АТФ, что приводит к высвобождению белка-субстрата, который затем позволяет полипептиду полной длины правильно складываться.
Рисунок 2.50 — Действие Hsp70 (синий), способствующее правильному сворачиванию белка (оранжевый) Изображение Алейи Ким
При тепловом шоке
Во время теплового шока или окислительного стресса белки Hsp70 связываются с развернутыми гидрофобными областями белков, аналогичным образом предотвращая их агрегацию и позволяя им правильно складываться. Когда белки повреждены, Hsp70 привлекает ферменты, которые убиквитинируют поврежденный белок, чтобы нацелить их на разрушение в протеасомах. Таким образом, белки Hsp70 играют важную роль не только в том, что белки правильно уложены, но и в том, что поврежденные или нефункциональные белки удаляются путем деградации в протеасоме.
шаперонины
Второй класс белков, участвующих в обеспечении правильной укладки других белков, известен как шаперонины. Есть две основные категории шаперонинов — класс I (обнаруженный в бактериях, хлоропластах и митохондриях) и класс II (обнаруженный в цитозоле эукариот и архебактерий). Наиболее изученными шаперонинами являются сложные белки GroEL / GroES, обнаруженные в бактериях (рис. 2.51).
Рисунок 2.51 — Вид снизу GroEL (слева) и комплекса GroEL / GroES (справа) Wikipedia
GroEL / GroES не может отменить агрегированные белки, но, облегчая правильное сворачивание, он обеспечивает конкуренцию за неправильное сворачивание как процесс и может уменьшить или устраните проблемы, возникающие из-за неправильного складывания.GroEL представляет собой 14-мерное кольцо с двойным кольцом с гидрофобной областью, которое может способствовать складыванию субстратов размером 15-60 кДа. GroES — это одиночный гептамер, который связывается с GroEL в присутствии ATP и действует как прикрытие над GroEL. Гидролиз АТФ шаперонинами вызывает большие конформационные изменения, которые влияют на связывание субстратных белков и их укладку. Точно неизвестно, как шаперонины сворачивают белки. Пассивные модели постулируют, что шаперониновый комплекс функционирует инертно, предотвращая неблагоприятные межмолекулярные взаимодействия или накладывая ограничения на пространства, доступные для возникновения складок.Активные модели предполагают, что структурные изменения в комплексе шаперонина вызывают структурные изменения в белке-субстрате.
Расщепление белков
Рисунок 2.52 — 26S протеасома. Активный сайт показан красным цветом Wikipedia
Другой белковый комплекс, который играет важную роль в динамике продолжительности жизни белков, — это протеасома (рис. 2.52). Протеасомы, обнаруженные у всех эукариот и архей, а также у некоторых бактерий, разрушают ненужные или поврежденные белки путем протеолитической деградации.Протеасомы помогают регулировать концентрацию некоторых белков и расщеплять те, которые неправильно свернуты. Путь протеасомной деградации играет важную роль в клеточных процессах, которые включают прохождение клеточного цикла, модуляцию экспрессии генов и ответ на окислительный стресс.
Деградация в протеасоме дает короткие пептиды длиной от семи до восьми аминокислот. Важную роль играют треониновые протеазы. Распад этих пептидов дает отдельные аминокислоты, облегчая их рециркуляцию в клетках.Белки нацелены на деградацию в протеасомах эукариот путем присоединения к множеству копий небольшого белка, называемого убиквитином (8,5 кДа — 76 аминокислот). Фермент, катализирующий реакцию, известен как убиквитинлигаза. Образовавшаяся полиубиквитиновая цепь связывается протеасомой, и начинается деградация. Убиквитин получил свое название из-за того, что он повсеместно обнаруживается в эукариотических клетках.
Убиквитин
Рисунок 2.53 — Убиквитин (боковые цепи лизина показаны желтым) Wikipedia
Убиквитин (Рисунок 2.53) представляет собой небольшой (8,5 кДа) многофункциональный белок, обнаруженный в эукариотических клетках. Обычно он добавляется к белкам-мишеням под действием ферментов убиквитинлигазы (E3 на рисунке 2.54). Могут быть добавлены одна (убиквитинирование) или несколько (полиубиквитинирование) молекул убиквитина. Присоединение убиквитина происходит через боковую цепь одного из семи различных остатков лизина в убиквитине.
Добавление убиквитина к белкам имеет множество эффектов, самый известный из которых направлен на расщепление белка в протеасоме.Протеасомное нацеливание наблюдается, когда полиубиквитинирование происходит по лизинам №29 и 48. Полиубиквитинирование или моноубиквитинирование по другим лизинам может приводить к измененному клеточному расположению и измененным межбелковым взаимодействиям. Последние могут влиять на воспаление, перенос эндоцитов, трансляцию и репарацию ДНК.
Рисунок 2.54 — Путь убиквитинирования целевого белка-субстрата Изображение Pehr Jacobson
Нарушение функции убиквитинлигазы
Паркин — это белок, связанный с болезнью Паркинсона, который при мутации связан с наследственной формой заболевания, называемой аутосомно-рецессивной ювенильной болезнью Паркинсона.Функция белка неизвестна, но он является компонентом системы убиквитинлигазы E3, ответственной за перенос убиквитина от белка E2 к боковой цепи лизина на белке-мишени. Считается, что мутации в паркине приводят к протеасомной дисфункции и, как следствие, неспособности расщеплять белки, вредные для дофаминергических нейронов. Это приводит к гибели или нарушению работы этих нейронов, что приводит к болезни Паркинсона.
Внутренне неупорядоченные белки
Фильм 2.1 — Динамическое движение цитохрома С в растворе Wikipedia
Как видно из множества примеров, описанных в другом месте книги, трехмерная структура белков важна для их функции. Но становится все более очевидным, что не все белки складываются в стабильную структуру. Исследования так называемых внутренне неупорядоченных белков (IDP) за последние пару десятилетий показали, что многие белки являются биологически активными, даже если они не могут складываться в стабильные структуры.Тем не менее, другие белки демонстрируют области, которые остаются развернутыми (области IDP), даже когда остальная часть полипептида складывается в структурированную форму.
Внутренне неупорядоченные белки и неупорядоченные области внутри белков были известны уже много лет, но рассматривались как аномалия. Только недавно, с осознанием того, что IDP и IDP области широко распространены среди эукариотических белков, было признано, что наблюдаемое нарушение является «особенностью, а не ошибкой».
Фильм 2.2 SUMO-1, белок с внутренне неупорядоченными участками Wikipedia
Сравнение IDP показывает, что у них общие характеристики последовательности, которые, по-видимому, способствуют их неупорядоченному состоянию. То есть так же, как некоторые аминокислотные последовательности могут способствовать сворачиванию полипептида в конкретную структуру, аминокислотные последовательности IDP способствуют тому, что они остаются развернутыми. Видно, что области IDP содержат мало гидрофобных остатков и необычно богаты полярными остатками и пролином. Присутствие большого количества заряженных аминокислот в IDP может ингибировать фолдинг за счет отталкивания зарядов, в то время как отсутствие гидрофобных остатков затрудняет формирование стабильного гидрофобного ядра, а пролин препятствует образованию спиральных структур.Наблюдаемые различия между аминокислотными последовательностями в IDP и структурированных белках были использованы для разработки алгоритмов для прогнозирования того, будет ли данная аминокислотная последовательность неупорядоченной.
Какое значение имеют внутренне неупорядоченные белки или области? Тот факт, что это свойство закодировано в их аминокислотных последовательностях, предполагает, что их нарушение может быть связано с их функцией. Гибкая, мобильная природа некоторых IDP-регионов может играть решающую роль в их функции, позволяя переход к складчатой структуре при связывании с белком-партнером или при посттрансляционной модификации.Некоторые ответы можно найти в исследованиях нескольких хорошо известных белков с участками IDP. Области IDP могут повышать способность белков, подобных lac-репрессору, перемещаться по ДНК для поиска специфических сайтов связывания. Гибкость IDP также может быть преимуществом во взаимодействиях белок-белок, особенно для белков, которые, как известно, взаимодействуют со многими различными белками-партнерами.
Рисунок 2.55 — Денатурация и ренатурация рибонуклеазы Википедия
Например, р53 имеет области IDP, которые могут позволить белку взаимодействовать с множеством функциональных партнеров.Сравнение известных функций белков с предсказаниями нарушений в этих белках предполагает, что IDP и области IDP могут непропорционально функционировать в передаче сигналов и регуляции, в то время как более структурированные белки смещены в сторону катализа и транспорта. Интересно, что многие белки, обнаруженные как в рибосомах, так и в сплайсосомах, имеют IDP-области, которые могут играть роль в правильной сборке этих комплексов. Несмотря на то, что ВПЛ не изучались интенсивно в течение очень долгого времени, то немногое, что о них известно, предполагает, что они играют важную и недооцененную роль в клетках.
Метаморфические белки
Другая группа белков, которая недавно изменила наше представление о структуре и функции белков, — это так называемые метаморфные белки. Эти белки способны образовывать более одного стабильного свернутого состояния, начиная с одной аминокислотной последовательности. Хотя это правда, что множественные складчатые конформации не исключаются законами физики и химии, метаморфические белки — относительно новое открытие. Конечно, было известно, что прионные белки способны складываться в альтернативные структуры, но метаморфические белки, по-видимому, могут переключаться между двумя стабильными структурами.Хотя в некоторых случаях метаморфный белок подвергается этому переключению в ответ на связывание другой молекулы, некоторые белки могут выполнять этот переход самостоятельно. Интересный пример — сигнальная молекула лимфотактин. Лимфотактин выполняет две биологические функции, которые выполняются двумя его конформерами — мономерной формой, связывающей рецептор лимфотактина, и димерной формой, связывающей гепарин. Возможно, такое переключение более распространено, чем предполагалось.
Рефолдинг денатурированных белков
Вся информация о фолдинге белка содержится в аминокислотной последовательности белка.Тогда может показаться любопытным, что большинство белков не сворачиваются в свою правильную, полностью активную форму после того, как они были денатурированы +++ и денатурант удален. На самом деле некоторые так и поступают. Хорошим примером является бычья рибонуклеаза (рис. 2.55). Его каталитическая активность очень устойчива к воздействию тепла и мочевины, и попытки денатурировать его не очень хорошо. Однако, если обработать фермент β-меркаптоэтанолом (который разрывает дисульфидные связи) перед обработкой мочевиной и / или нагреванием, активность теряется, что указывает на то, что ковалентные дисульфидные связи помогают стабилизировать общую структуру фермента, и когда они разрываются, денатурация может легко возникают.Когда смесь снова охлаждается до комнатной температуры, со временем некоторая активность фермента снова появляется, указывая на то, что рибонуклеаза повторно свернулась в новых условиях.
Интересно, что ренатурация произойдет максимально, если во время процесса в растворе останется небольшое количество β-меркаптоэтанола. Причина этого в том, что β-меркаптоэтанол позволяет восстанавливать (и разрушать) случайные неправильные дисульфидные связи во время процесса складывания. Без него эти дисульфидные связи будут препятствовать образованию правильных складок.
Необратимая денатурация
Однако большинство ферментов не ведут себя как бычья рибонуклеаза. После денатурирования их активность не может быть восстановлена до какой-либо значительной степени. Существует не так много способов инактивации РНКазы. Она стабильна как в горячем, так и в холодном состоянии, потому что дисульфиды плотно удерживаются. Если вы хотите, чтобы она остановилась, используйте горячий меркаптоэтанол. Это может показаться противоречащим идее о том, что информация о сворачивании является неотъемлемой частью последовательности аминокислот в белке.Это не.
Большинство ферментов не восстанавливаются должным образом после денатурации по двум причинам. Во-первых, нормальное сворачивание может происходить по мере образования белков. Взаимодействия между аминокислотами на ранней стадии синтеза не «сбиваются с толку» взаимодействиями с аминокислотами на более поздних этапах синтеза, потому что эти аминокислоты не присутствуют в начале процесса.
Роль шаперонинов
В других случаях процесс сворачивания некоторых белков в клетке зависел от действия белков-шаперонинов (см. ЗДЕСЬ).В отсутствие шаперонинов происходят взаимодействия, которые могут приводить к неправильной укладке, что препятствует правильной укладке. Таким образом, раннее сворачивание и помощь шаперонинов устраняют некоторые потенциальные взаимодействия «неправильного сворачивания», которые могут происходить, если вся последовательность присутствует в момент начала сворачивания.
Четвертичная структура
Четвертый уровень структуры белка — это четвертичная структура. Это относится к структурам, которые возникают в результате взаимодействий между несколькими полипептидами.Единицы могут быть идентичными множественными копиями или могут быть разными полипептидными цепями. Гемоглобин взрослого человека является хорошим примером белка с четвертичной структурой, состоящего из двух идентичных цепей, называемых α, и двух идентичных цепей, называемых β.
Хотя α-цепи очень похожи на β-цепи, они не идентичны. Как α-, так и β-цепи также связаны с одной полипептидной цепью в родственном белке, называемом миоглобином. И миоглобин, и гемоглобин имеют сходство в связывании кислорода, но их поведение по отношению к молекуле значительно различается.Примечательно, что множественные субъединицы гемоглобина (с четвертичной структурой) по сравнению с одиночной субъединицей миоглобина (без четвертичной структуры) вызывают эти различия.
Список литературы
1. https://en.wikipedia.org/wiki/Van_der_W aals_force 105
Структура и функции белков
Белки — очень важные молекулы, которые необходимы всем живым организмам. По сухому весу белки — самая крупная единица клеток. Белки участвуют практически во всех клеточных функциях, и каждой роли отводится отдельный тип белка, задачи которого варьируются от общей клеточной поддержки до передачи сигналов и передвижения.Всего существует семь типов белков.
Белки
- Белки — это биомолекулы, состоящие из аминокислот, которые участвуют почти во всех клеточных действиях.
- Происходит в цитоплазме, трансляция — это процесс, посредством которого синтезируются белки .
- Типичный белок состоит из единственного набора из аминокислот . Каждый белок специально приспособлен для своей функции.
- Любой белок в организме человека может быть создан из перестановок всего 20 аминокислот.
- Существует семь типов белков: антитела , сократительные белки, ферменты, гормональные белки, структурные белки, запасные белки и транспортные белки .
Синтез белков
Белки синтезируются в организме посредством процесса, называемого трансляцией . Трансляция происходит в цитоплазме и включает преобразование генетических кодов в белки. Генетические коды собираются во время транскрипции ДНК, где ДНК расшифровывается в РНК.Затем клеточные структуры, называемые рибосомами, помогают транскрибировать РНК в полипептидные цепи, которые необходимо модифицировать, чтобы они стали функционирующими белками.
Аминокислоты и полипептидные цепи
Аминокислоты являются строительными блоками всех белков, независимо от их функции. Белки обычно представляют собой цепочку из 20 аминокислот. Человеческое тело может использовать комбинации этих 20 аминокислот для производства любого необходимого белка. Большинство аминокислот следуют структурному шаблону, в котором альфа-углерод связан со следующими формами:
- Атом водорода (H)
- Карбоксильная группа (-COOH)
- Аминогруппа (-Nh3)
- А «переменная» группа
Среди различных типов аминокислот «вариабельная» группа наиболее ответственна за вариации, поскольку все они имеют водородные, карбоксильные группы и связи аминогруппы.
Аминокислоты соединяются посредством синтеза дегидратации, пока не образуют пептидные связи. Когда несколько аминокислот связаны между собой этими связями, образуется полипептидная цепь. Одна или несколько полипептидных цепей, скрученных в трехмерную форму, образуют белок.
Структура белка
Структура белка может быть глобулярной или волокнистой в зависимости от его конкретной роли (каждый белок является специализированным). Глобулярные белки обычно компактны, растворимы и имеют сферическую форму.Волокнистые белки обычно имеют удлиненную форму и нерастворимы. Глобулярные и волокнистые белки могут иметь один или несколько типов белковых структур.
Существует четыре структурных уровня белка: первичный, вторичный, третичный и четвертичный. Эти уровни определяют форму и функцию белка и отличаются друг от друга степенью сложности полипептидной цепи. Первичный уровень является самым основным и рудиментарным, в то время как четвертичный уровень описывает сложные связи.
Отдельная белковая молекула может содержать один или несколько из этих уровней структуры белка, и структура и сложность белка определяют его функцию. Коллаген, например, имеет суперскрученную спиральную форму, длинную, тягучую, прочную и похожую на веревку — коллаген отлично подходит для обеспечения поддержки. Гемоглобин, с другой стороны, представляет собой свернутый и компактный глобулярный белок. Его сферическая форма полезна для маневрирования по кровеносным сосудам.
Типы белков
Всего существует семь различных типов белков, к которым относятся все белки.К ним относятся антитела, сократительные белки, ферменты, гормональные белки, структурные белки, запасные белки и транспортные белки.
Антитела
Антитела — это специализированные белки, которые защищают организм от антигенов или чужеродных захватчиков. Их способность перемещаться по кровотоку позволяет им использоваться иммунной системой для идентификации и защиты от бактерий, вирусов и других чужеродных вторжений в крови. Один из способов, которым антитела противодействуют антигенам, — это их иммобилизация, чтобы они могли быть уничтожены лейкоцитами.
Сократительные белки
Сократительные белки отвечают за сокращение и движение мышц. Примеры этих белков включают актин и миозин. Эукариоты, как правило, обладают обильным количеством актина, который контролирует сокращение мышц, а также процессы клеточного движения и деления. Миозин приводит в действие задачи, выполняемые актином, снабжая его энергией.
Ферменты
Ферменты — это белки, которые облегчают и ускоряют биохимические реакции, поэтому их часто называют катализаторами.Известные ферменты включают лактазу и пепсин, белки, которые известны своей ролью в заболеваниях пищеварительной системы и в специальных диетах. Непереносимость лактозы вызвана дефицитом лактазы — фермента, расщепляющего сахарную лактозу, содержащуюся в молоке. Пепсин — это пищеварительный фермент, который в желудке расщепляет белки в пище. Нехватка этого фермента приводит к расстройству пищеварения.
Другими примерами пищеварительных ферментов являются ферменты, присутствующие в слюне: амилаза слюны, калликреин слюны и лингвальная липаза — все они выполняют важные биологические функции.Амилаза слюны — это основной фермент слюны, который расщепляет крахмал на сахар.
Гормональные белки
Гормональные белки — это белки-мессенджеры, которые помогают координировать определенные функции организма. Примеры включают инсулин, окситоцин и соматотропин.
Инсулин регулирует метаболизм глюкозы, контролируя концентрацию сахара в крови в организме, окситоцин стимулирует схватки во время родов, а соматотропин — гормон роста, который стимулирует выработку белка в мышечных клетках.
Структурные белки
Структурные белки являются волокнистыми и вязкими, что делает их идеальными для поддержки различных других белков, таких как кератин, коллаген и эластин.
Кератины укрепляют защитные покрытия, такие как кожа, волосы, иглы, перья, рога и клювы. Коллаген и эластин поддерживают соединительные ткани, такие как сухожилия и связки.
Хранение белков
Запасные белки запасают аминокислоты для организма до тех пор, пока они не будут готовы к употреблению.Примеры запасных белков включают яичный альбумин, который содержится в яичных белках, и казеин, белок на основе молока. Ферритин — еще один белок, который хранит железо в транспортном белке, гемоглобине.
Транспортные белки
Транспортные белки — это белки-переносчики, которые перемещают молекулы из одного места в другое в организме. Гемоглобин является одним из них и отвечает за транспортировку кислорода через кровь через красные кровяные тельца. Цитохромы, другой тип транспортных белков, действуют в цепи переноса электронов как белки-переносчики электронов.
.