Нарушение обмена веществ
Нехватка калия по-научному называется гипокалиемия. А сильный дефицит магния — гипомагниемия. Обычно эти состояния поддаются корректировке и баланс калия и магния восстанавливается за короткий срок.
Но как распознать дефицит калия и/или магния?
Этот вопрос является ключевым. Обычно само лечение не представляет такой сложности, как своевременная корректная диагностика нехватки этих веществ.
Первые симптомы не ярко выражены и люди живут с ними годами. Основной сигнал от организма: усталость. Но ощущая себя «выжатым как лимон» , человек редко идет к врачу. Пока у него не возникнут дополнительные симптомы:
- судороги
- повышение или понижение артериального давления, и другие проблемы сердечно-сосудистой системы (тахикардия, аритмия,)
- мышечная слабость
- тошнота, рвота, диарея
- повышенная нервная возбудимость, раздражительность
Уровни калия и магния определяются целым спектром анализов. Самые первые из них: биохимический анализ крови и исследование содержания этих микроэлементов в 24х-часовой моче.
Самые первые из них: биохимический анализ крови и исследование содержания этих микроэлементов в 24х-часовой моче.
Средняя норма калия при весе в 65-70 кг составляет 3500 ммоль/л. Критический показатель 2 ммоль/л.
Средняя норма магния для взрослых – от 0,75 до 1,26 ммоль/л. Уровень магния от 0,5-0,7 ммоль/л говорит о гипомагниемии.
Причины дефицита калия
В процессе обмена калия огромную роль играют почки (львиная доля этого микроэлемента выводится с мочой), поэтому причиной его стремительной утечки оказываются именно проблемы с почками. Часто это происходит на фоне приема специфических лекарств: диуретиков (кроме калийсберегающих), группы пенициллинов, больших дозах гентамицина, лечении амфотерицином В или теофиллином. На работу почек также влияют сбои в гормональной системе, что также приводит к падению уровня калия в крови: заболевания надпочечников, опухоли, злокачественная гипертензия.
Но калий легко потерять даже при исправной работе почек! Достаточно регулярно нагружать себя сильными физическими нагрузками или пережить сильное эмоциональное потрясение.
Причины дефицита магния
Как и в случае с калием, на усвоение и удержание магния в организме, влияет много факторов. Бывает, что его дефицит — состояние врожденное, связанное с аномалией метаболизма этого микроэлемента на фоне различных заболеваний. Тогда врачи говорят о хронической (врожденной) гипомагниемии. Она достаточно распространена, но выявить ее не просто. Почему так происходит? Употребляемые человеком масло, молоко, жирное мясо нейтрализуют количество магния, которое также поступает в организм с пищей из других продуктов (бобовые, зеленые овощи, сухофрукты и т.д.). Человек живет с уверенностью, что его питание сбалансировано и дефицита микроэлементов просто быть не может, а на самом деле страдать хронической гипомагниемией.
Вторичный дефицит магния обычно возникает по иным причинам:
- алкоголизм
- хроническое недоедание
- нарушение работы желудочно-кишечного тракта
- парентеральное питание
- беременность
- гиперфункция щитовидной железы
- прием гормональных препаратов
- физические нагрузки
- частое посещение сауны, бани, проживание в жарком климате
Лечение и профилактика гипокалиемии и гипомагниемии
Первым делом врачи рекомендуют специальную диету, богатую необходимыми микроэлементами, а также «смягчение» ритма жизни.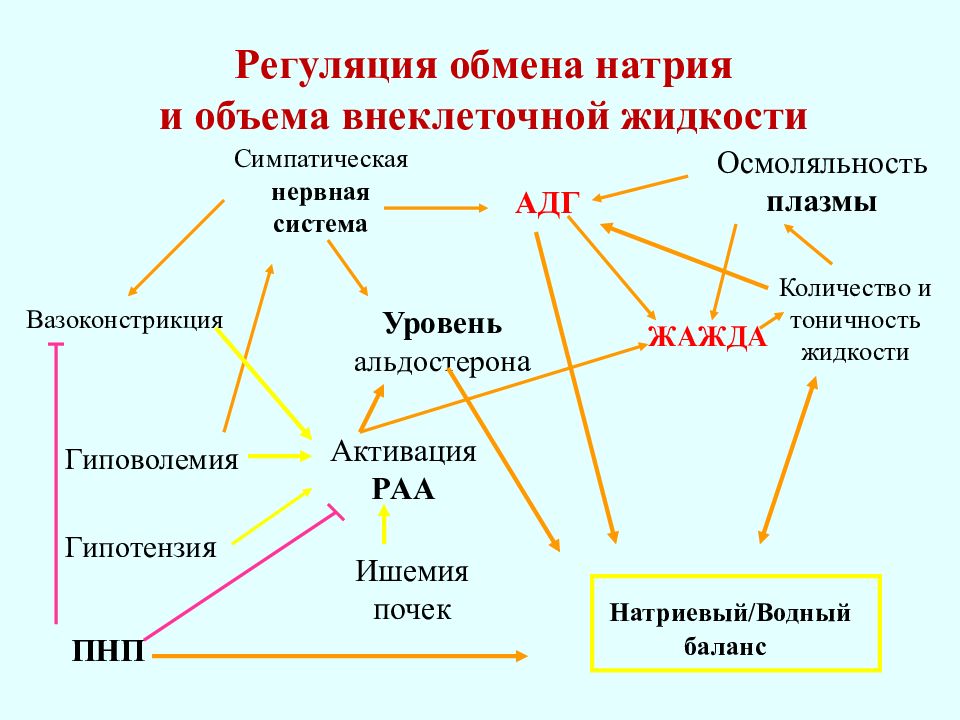 Нередко при дефиците калия обнаруживается и нехватка магния. Поэтому так важно пропить курс препаратов, содержащих сбалансированный уровень этих микроэлементов.
Нередко при дефиците калия обнаруживается и нехватка магния. Поэтому так важно пропить курс препаратов, содержащих сбалансированный уровень этих микроэлементов.
Одним из них является «Панангин», отлично зарекомендовавший себя при лечении дефицитных состояний калия и магния.
Симфония здоровья, или Зачем нашему организму необходим калий и магний
Организм человека — это сложнейшая и вместе с тем прекраснейшая гармония, для сохранения которой детали имеют первоочередное значение. Ведь недостаток веществ, которые, казалось бы, необходимы в очень маленьком количестве, может иметь для здоровья нашего организма несравнимо большее значение, чем их удельный вес в рационе питания. Это утверждение абсолютно справедливо по отношению к макроэлементам, таким как калий и магний. Дневная потребность в этих веществах измеряется в миллиграммах — это так мало, что даже рассмотреть порой трудно, однако от их наличия в нашем организме зависит очень многое. Поэтому в данной публикации речь пойдет именно о деталях, которые обусловливают здоровье, хорошее самочувствие и отличное настроение. За что в нашем организме отвечают калий и магний и почему они всегда «ходят» в неразрывной связке? Какие признаки недостатка этих макроэлементов и как его восполнить?
За что в нашем организме отвечают калий и магний и почему они всегда «ходят» в неразрывной связке? Какие признаки недостатка этих макроэлементов и как его восполнить?
Магний: сердце, мышцы и нервы в порядке
Магний вовлечен в работу около 300 ферментов нашего организма. Таким образом, магний принимает участие во многих процессах, происходящих в организме — это и энергетический обмен, и синтез белков, жиров и нуклеиновых кислот, и участие в различных сигнальных каскадах. Магний способствует расслаблению гладких мышц, выступая в качестве некоего противовеса по отношению к кальцию. При этом пятая часть всего магния в нашем организме находится в сердце, и уже одно это свидетельствует о том, какое огромное значение имеет этот макроэлемент для функционирования нашего главного мотора. Также магний играет важную роль в защите нервной системы от разрушительных стрессов (Ярош А.К., 2010). Ежедневная потребность в магнии для мужчин составляет 350 мг, для женщин — 300 мг, а для молодых людей, беременных и кормящих грудью эта цифра может увеличиваться еще на 150 мг. При этом общее количество магния в организме человека составляет всего лишь около 24 г, большая часть которого содержится в мышечной и костной ткани. Следует отметить, что потребность в магнии значительно увеличивается при физических нагрузках, стрессе, в условиях жаркого климата, при посещении бани, злоупотреблении алкоголем, несбалансированных ограничительных диетах и синдроме хронической усталости (Недогода С.В., 2009). Из каких продуктов мы получаем магний? Во-первых, магний содержится в обычной питьевой воде, однако его концентрация может значительно варьировать. В некоторых регионах с «мягкой» водой его уровень в воде значительно ниже. Кроме того, некоторые вещества, например, содержащиеся в чае, способны негативно влиять на усвояемость магния в пищеварительном тракте. Магнием богаты орехи, черный шоколад и бобовые, но существенное увеличение потребления данных продуктов может привести к появлению пары-тройки лишних килограммов из-за их высокой калорийности. Среди прочих менее питательных продуктов можно назвать шпинат, брокколи и ревень, однако они не способны обеспечить суточную потребность организма в магнии.
При этом общее количество магния в организме человека составляет всего лишь около 24 г, большая часть которого содержится в мышечной и костной ткани. Следует отметить, что потребность в магнии значительно увеличивается при физических нагрузках, стрессе, в условиях жаркого климата, при посещении бани, злоупотреблении алкоголем, несбалансированных ограничительных диетах и синдроме хронической усталости (Недогода С.В., 2009). Из каких продуктов мы получаем магний? Во-первых, магний содержится в обычной питьевой воде, однако его концентрация может значительно варьировать. В некоторых регионах с «мягкой» водой его уровень в воде значительно ниже. Кроме того, некоторые вещества, например, содержащиеся в чае, способны негативно влиять на усвояемость магния в пищеварительном тракте. Магнием богаты орехи, черный шоколад и бобовые, но существенное увеличение потребления данных продуктов может привести к появлению пары-тройки лишних килограммов из-за их высокой калорийности. Среди прочих менее питательных продуктов можно назвать шпинат, брокколи и ревень, однако они не способны обеспечить суточную потребность организма в магнии. К тому же в пищеварительном тракте усваивается только 30% магния, который мы получаем с пищей. Негативно на усвояемость магния влияет избыточное потребления кальция, натрия, белка или жира с пищей, что существенно снижает поступление магния в организм из-за образования его невсасывающихся комплексов. Таким образом, наиболее распространенной причиной дефицита магния является именно недостаточное поступление его с пищей. К дефициту магния может привести и прием некоторых препаратов, например, диуретиков, кофеина, некоторых антибиотиков и эстрогенсодержащих лекарственных средств (Постникова С.Л. и соавт., 2007). В результате — дефицит магния может отмечаться у 40% населения (Недогода С.В., 2009).
К тому же в пищеварительном тракте усваивается только 30% магния, который мы получаем с пищей. Негативно на усвояемость магния влияет избыточное потребления кальция, натрия, белка или жира с пищей, что существенно снижает поступление магния в организм из-за образования его невсасывающихся комплексов. Таким образом, наиболее распространенной причиной дефицита магния является именно недостаточное поступление его с пищей. К дефициту магния может привести и прием некоторых препаратов, например, диуретиков, кофеина, некоторых антибиотиков и эстрогенсодержащих лекарственных средств (Постникова С.Л. и соавт., 2007). В результате — дефицит магния может отмечаться у 40% населения (Недогода С.В., 2009).
Калий: сердца пламенный мотор
Калий — основной внутриклеточный катион, поддержание определенного соотношения концентраций которого в клетках и внеклеточном пространстве чрезвычайно важно для нормального функционирования нервной и мышечной ткани. Поддержание необходимого соотношения осуществляется благодаря работе фермента, который переносит ионы калия в клетку, а ионы натрия — из нее. А для нормального функционирования этого фермента необходим магний. Интересно, что потеря калия из внеклеточного пространства быстро компенсируется за счет его поступления из клеток, благодаря чему концентрация этого иона во внеклеточном пространстве на протяжении достаточно длительного времени может оставаться в пределах нормы. В результате критический дефицит калия, чреватый сердечно-сосудистыми и нервно-мышечными нарушениями, часто остается незамеченным при стандартных исследованиях (Ляшенко Е.А., 2012). Дефицит калия в основном развивается вследствие его недостаточного поступления с пищей, интенсивной потери жидкости (диарея, повышенное потоотделение, прием диуретиков или слабительных средств), а также, что очень важно, — дефицита магния. Кроме того, пациенты с сахарным диабетом находятся в группе риска относительно развития дефицита калия (Ляшенко Е.А., 2012).
А для нормального функционирования этого фермента необходим магний. Интересно, что потеря калия из внеклеточного пространства быстро компенсируется за счет его поступления из клеток, благодаря чему концентрация этого иона во внеклеточном пространстве на протяжении достаточно длительного времени может оставаться в пределах нормы. В результате критический дефицит калия, чреватый сердечно-сосудистыми и нервно-мышечными нарушениями, часто остается незамеченным при стандартных исследованиях (Ляшенко Е.А., 2012). Дефицит калия в основном развивается вследствие его недостаточного поступления с пищей, интенсивной потери жидкости (диарея, повышенное потоотделение, прием диуретиков или слабительных средств), а также, что очень важно, — дефицита магния. Кроме того, пациенты с сахарным диабетом находятся в группе риска относительно развития дефицита калия (Ляшенко Е.А., 2012).
Калий+Магний = Неразлучная парочка
Уровни этих элементов в нашем организме связаны — дефицит одного негативно влияет на уровень другого и наоборот.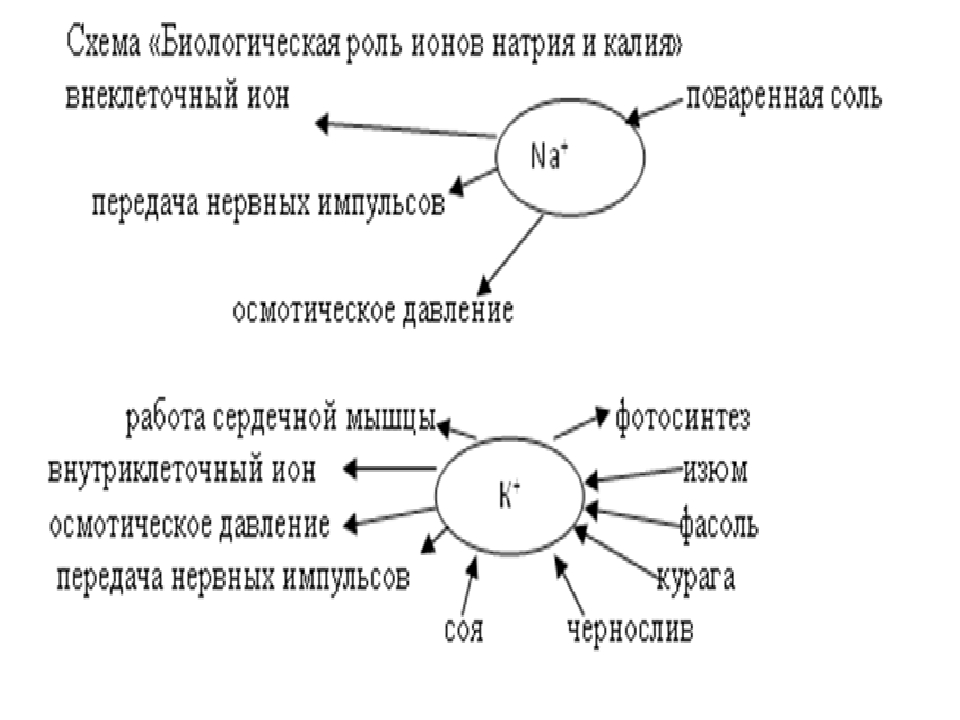 Магний препятствует потере калия, способствуя его фиксации в клетке и нормализации его внутриклеточного содержания (Ярош А.К., 2010). Таким свойствам магний обязан тому, что участвует в работе фермента, «закачивающего» калий в клетку. Исследование клеточных моделей подтвердило критическую роль магния в поддержании уровня внутриклеточного калия (Котова О.В., Рябоконь И.В., 2012). Стоит отметить, что при восполнении магниевого дефицита потери калия сокращаются. Вместе с тем содержание магния зависит от концентрации калия (Постникова С.Л. и соавт., 2007). При этом у большинства пациентов с дефицитом калия могут также отмечать дефицит магния. Это делает целесообразным применение препаратов, содержащих одновременно как магний, так и калий.
Магний препятствует потере калия, способствуя его фиксации в клетке и нормализации его внутриклеточного содержания (Ярош А.К., 2010). Таким свойствам магний обязан тому, что участвует в работе фермента, «закачивающего» калий в клетку. Исследование клеточных моделей подтвердило критическую роль магния в поддержании уровня внутриклеточного калия (Котова О.В., Рябоконь И.В., 2012). Стоит отметить, что при восполнении магниевого дефицита потери калия сокращаются. Вместе с тем содержание магния зависит от концентрации калия (Постникова С.Л. и соавт., 2007). При этом у большинства пациентов с дефицитом калия могут также отмечать дефицит магния. Это делает целесообразным применение препаратов, содержащих одновременно как магний, так и калий.
Повод задуматься
Дефицит магния проявляется множеством симптомов — от хронической усталости, снижения умственной работоспособности и головной боли до артериальной гипертензии, склонности к тромбообразованию и сердечных аритмий. Могут отмечаться повышенная раздражительность, депрессия, тревога, нарушения сна. Кроме того, возможны спастические сокращения любых мышц: судороги скелетных мышц, спастические сокращения кишечника, бронхоспазм, повышение сократимости матки и т.д. (Постникова С.Л. и соавт., 2007). При этом дополнительный прием магния при его дефиците обеспечивает антиаритмический, антиишемический эффект, способствует снижению артериального и внутричерепного давления, оказывает спазмолитическое и противосудорожное действие. Магний способен нормализовать уровень артериального давления, эффективен в терапии при различных нарушениях сердечного ритма. Кроме того, применение магния благотворно влияет на функционирование нервной системы и улучшает сон. Профилактика дефицита магния способна значительно снизить вероятность развития инфаркта миокарда (Постникова С.Л. и соавт., 2007). Дефицит калия негативно отражается на функционировании сердечно-сосудистой системы: наблюдаются обменные нарушения и функциональная недостаточность миокарда, аритмия, тахикардия, глухота сердечного тона, возникновение сердечных приступов, сердечная недостаточность, сниженное артериальное давление (Косарев В.
Кроме того, возможны спастические сокращения любых мышц: судороги скелетных мышц, спастические сокращения кишечника, бронхоспазм, повышение сократимости матки и т.д. (Постникова С.Л. и соавт., 2007). При этом дополнительный прием магния при его дефиците обеспечивает антиаритмический, антиишемический эффект, способствует снижению артериального и внутричерепного давления, оказывает спазмолитическое и противосудорожное действие. Магний способен нормализовать уровень артериального давления, эффективен в терапии при различных нарушениях сердечного ритма. Кроме того, применение магния благотворно влияет на функционирование нервной системы и улучшает сон. Профилактика дефицита магния способна значительно снизить вероятность развития инфаркта миокарда (Постникова С.Л. и соавт., 2007). Дефицит калия негативно отражается на функционировании сердечно-сосудистой системы: наблюдаются обменные нарушения и функциональная недостаточность миокарда, аритмия, тахикардия, глухота сердечного тона, возникновение сердечных приступов, сердечная недостаточность, сниженное артериальное давление (Косарев В. В., Бабанов С.А., 2012). Дефицит калия связан с повышением вероятности развития аритмий и уровня артериального давления. Так, поступление калия с пищей обратно пропорционально уровню артериального давления, а увеличение его потребления рекомендуется в качестве профилактики и лечения при артериальной гипертензии. Также прием препаратов калия способствует значительному снижению риска смерти от инсульта (Ляшенко Е.А., 2012).
В., Бабанов С.А., 2012). Дефицит калия связан с повышением вероятности развития аритмий и уровня артериального давления. Так, поступление калия с пищей обратно пропорционально уровню артериального давления, а увеличение его потребления рекомендуется в качестве профилактики и лечения при артериальной гипертензии. Также прием препаратов калия способствует значительному снижению риска смерти от инсульта (Ляшенко Е.А., 2012).
восполняем запасы с ПАНАНГИНОМ
Одним из таких препаратов, который более 40 лет присутствует на рынке и заслужил доверие специалистов здравоохранения и пациентов, является ПАНАНГИН от компании «Рихтер Гедеон», в состав которого входит аспарагинат калия и магния. Аспарагинат является транспортером ионов через клеточную мембрану, облегчая проникновение калия и магния во внутриклеточное пространство. В свою очередь, наличие в ПАНАНГИНЕ эндогенного аспарагината способствует более быстрому и эффективному вхождению калия и магния в миоциты, оказывает положительное влияние на метаболизм миокарда (Шилов А. М. и соавт., 2012). Эффективность ПАНАНГИНА при терапии различных заболеваний сердечно-сосудистой системы и профилактике дефицита магния и калия доказана длительным успешным опытом применения. Так, комбинированные препараты магния и калия, такие как ПАНАНГИН, показали высокую клиническую эффективность при лечении различных видов аритмий (Постникова С.Л. и соавт., 2007). Также применение комбинации магния и калия целесообразно при желудочковой тахикардии и повышает эффективность лечения сердечной недостаточности, снижает риск развития инсульта (Ляшенко Е.А., 2012). Не менее важна роль ПАНАНГИНА и для стабилизации электролитного гомеостаза у пациентов, принимающих диуретики, что приводит иногда к колебаниям в составе электролитов, которые могут усугублять течение заболевания. Благодаря комбинации магния и калия ПАНАНГИН способен оказывать целый комплекс эффектов, благоприятно влияющих на состояние сердечно-сосудистой системы:
М. и соавт., 2012). Эффективность ПАНАНГИНА при терапии различных заболеваний сердечно-сосудистой системы и профилактике дефицита магния и калия доказана длительным успешным опытом применения. Так, комбинированные препараты магния и калия, такие как ПАНАНГИН, показали высокую клиническую эффективность при лечении различных видов аритмий (Постникова С.Л. и соавт., 2007). Также применение комбинации магния и калия целесообразно при желудочковой тахикардии и повышает эффективность лечения сердечной недостаточности, снижает риск развития инсульта (Ляшенко Е.А., 2012). Не менее важна роль ПАНАНГИНА и для стабилизации электролитного гомеостаза у пациентов, принимающих диуретики, что приводит иногда к колебаниям в составе электролитов, которые могут усугублять течение заболевания. Благодаря комбинации магния и калия ПАНАНГИН способен оказывать целый комплекс эффектов, благоприятно влияющих на состояние сердечно-сосудистой системы:
- снижает уровень артериального давления у больных с артериальной гипертензией;
- способствует поддержанию эластичности стенок сосудов;
- снижает риск развития аритмий;
- улучшает сократительную функцию миокарда и обеспечивает профилактику развития сердечной недостаточности;
- улучшает функцию эндотелия сосудов, снижает риск и темп развития атеросклероза;
- уменьшает вязкость крови и тромбообразование (Ляшенко Е.
 А., 2012).
А., 2012).
Таким образом, ПАНАНГИН показан в качестве дополнительной терапии при хронических заболеваниях сердца (сердечная недостаточность и в постинфарктный период), нарушениях ритма сердца, прежде всего при желудочковых аритмиях, а также как дополнение для увеличения количества магния и калия, поступающих с пищей. Применять ПАНАНГИН взрослым рекомендуется по 1–2 таблетки 3 раза в сутки после еды.
Безопасная профилактика — это важно
Еще одним доводом в пользу применения ПАНАНГИНА с целью повышения поступления магния и калия и таким образом профилактики их дефицита является то, что данный препарат отпускается без рецепта. Кроме того, невозможно обойти вниманием тот факт, что в отличие от диетических добавок, широко использующихся с целью пополнения рациона биологически активными веществами, к лекарственным препаратам предъявляются более высокие требования при регистрации, в том числе в аспекте предоставления сведений относительно эффективности и (что очень важно при длительном применении) — профиля безопасности. Так, говоря о профиле безопасности лекарственного средства, следует отметить, что ПАНАНГИН – нетоксичный препарат, не проявляет кумулятивный эффект (Шилов А.М. и соавт., 2012). Он характеризуется ограниченным перечнем противопоказаний и побочных реакций. К тому же результаты последних исследований подтверждают успешное применение препарата и у детей (Крючкова Т.А. и соавт., 2013). Таким образом, многолетний опыт применения препарата ПАНАНГИН подтвердил его высокую эффективность и благоприятный профиль безопасности в обеспечении калиево-магниевого баланса, а также в лечении и профилактике заболеваний сердечно-сосудистой системы.
Так, говоря о профиле безопасности лекарственного средства, следует отметить, что ПАНАНГИН – нетоксичный препарат, не проявляет кумулятивный эффект (Шилов А.М. и соавт., 2012). Он характеризуется ограниченным перечнем противопоказаний и побочных реакций. К тому же результаты последних исследований подтверждают успешное применение препарата и у детей (Крючкова Т.А. и соавт., 2013). Таким образом, многолетний опыт применения препарата ПАНАНГИН подтвердил его высокую эффективность и благоприятный профиль безопасности в обеспечении калиево-магниевого баланса, а также в лечении и профилактике заболеваний сердечно-сосудистой системы.
Пресс-служба «Еженедельника АПТЕКА»
ИНФОРМАЦИЯ ДЛЯ ПРОФЕССИОНАЛЬНОЙ ДЕЯТЕЛЬНОСТИ МЕДИЦИНСКИХ И ФАРМАЦЕВТИЧЕСКИХ РАБОТНИКОВ
Панангин (PANANGIN). Состав: магния аспарагинат, калия аспарагинат. Лекарственная форма. Таблетки, покрытые пленочной оболочкой. Фармакологическая группа. Минеральные вещества. Препараты магния. Код АТС А12С С30. Показания. Дополнительная терапия при хронических заболеваниях сердца (при сердечной недостаточности, в постинфарктный период), нарушениях ритма сердца, прежде всего при желудочковых аритмиях. Дополнительная терапия при лечении препаратами наперстянки. Как дополнение для повышения уровня магния и калия, поступающих с пищей. Противопоказания. Повышенная чувствительность к действующим веществам или любому из вспомогательных веществ препарата. Острая и хроническая почечная недостаточность, болезнь Аддисона, AV-блокада III степени, кардиогенный шок (артериальное давление <90 мм рт. ст.). Побочные эффекты. Со стороны желудочно-кишечного тракта: при применении в высоких дозах возможно повышение частоты дефекации. По некоторым данным, могут возникать тошнота, рвота и боль в животе. Производитель. ОАО «Гедеон Рихтер»/Gedeon Richter Plc. Н-1103, Будапешт, ул. Демреи, 19–21, Венгрия/H-1103, Budapest, Gyomroi ut. 19–21, Hungary. Р.с. № UA/7315/01/01 с 10.08.2012 по 10.08.2017.
Дополнительная терапия при хронических заболеваниях сердца (при сердечной недостаточности, в постинфарктный период), нарушениях ритма сердца, прежде всего при желудочковых аритмиях. Дополнительная терапия при лечении препаратами наперстянки. Как дополнение для повышения уровня магния и калия, поступающих с пищей. Противопоказания. Повышенная чувствительность к действующим веществам или любому из вспомогательных веществ препарата. Острая и хроническая почечная недостаточность, болезнь Аддисона, AV-блокада III степени, кардиогенный шок (артериальное давление <90 мм рт. ст.). Побочные эффекты. Со стороны желудочно-кишечного тракта: при применении в высоких дозах возможно повышение частоты дефекации. По некоторым данным, могут возникать тошнота, рвота и боль в животе. Производитель. ОАО «Гедеон Рихтер»/Gedeon Richter Plc. Н-1103, Будапешт, ул. Демреи, 19–21, Венгрия/H-1103, Budapest, Gyomroi ut. 19–21, Hungary. Р.с. № UA/7315/01/01 с 10.08.2012 по 10.08.2017.
Панангін
Цікава інформація для Вас:
Патогенетическая роль дефицита калия и магния в развитии неврологических заболеваний | Котова О.
 В., Рябоконь И.В.
В., Рябоконь И.В.
Калий
Калий – основной внутриклеточный катион. В норме концентрация калия в плазме равна 3,5–5 ммоль/л, а в клетках – 150 ммоль/л. Обмен калия обусловлен его поступлением извне и выведением почками с мочой. Этот объем составляет 1,9–5,9 г калия в сутки. Содержание калия во внеклеточной жидкости составляет менее 2% от общего его содержания в организме. Высокое внутриклеточное содержание калия обеспечивается работой так называемого «натрий–калиевого насоса» – особой белковой структуры, расположенной в клеточной мембране, для работы которой требуются энергия молекул аденозинтрифосфата (АТФ) и присутствие ионов магния. Натрий–калиевый насос начинает усиленно работать при повышении уровня калия в крови под действием альдостерона, «гормонов стресса» катехоламинов (адреналина и норадреналина) и инсулина [1]. Так создается трансмембранный потенциал покоя, наличие которого чрезвычайно важно для нормального функционирования нервной и мышечной ткани.
Калий – основной внутриклеточный катион. В норме концентрация калия в плазме равна 3,5–5 ммоль/л, а в клетках – 150 ммоль/л. Обмен калия обусловлен его поступлением извне и выведением почками с мочой. Этот объем составляет 1,9–5,9 г калия в сутки. Содержание калия во внеклеточной жидкости составляет менее 2% от общего его содержания в организме. Высокое внутриклеточное содержание калия обеспечивается работой так называемого «натрий–калиевого насоса» – особой белковой структуры, расположенной в клеточной мембране, для работы которой требуются энергия молекул аденозинтрифосфата (АТФ) и присутствие ионов магния. Натрий–калиевый насос начинает усиленно работать при повышении уровня калия в крови под действием альдостерона, «гормонов стресса» катехоламинов (адреналина и норадреналина) и инсулина [1]. Так создается трансмембранный потенциал покоя, наличие которого чрезвычайно важно для нормального функционирования нервной и мышечной ткани.
В норме концентрация калия в плазме равна 3,5–5 ммоль/л, а в клетках – 150 ммоль/л. Обмен калия обусловлен его поступлением извне и выведением почками с мочой. Этот объем составляет 1,9–5,9 г калия в сутки. Содержание калия во внеклеточной жидкости составляет менее 2% от общего его содержания в организме. Высокое внутриклеточное содержание калия обеспечивается работой так называемого «натрий–калиевого насоса» – особой белковой структуры, расположенной в клеточной мембране, для работы которой требуются энергия молекул аденозинтрифосфата (АТФ) и присутствие ионов магния. Натрий–калиевый насос начинает усиленно работать при повышении уровня калия в крови под действием альдостерона, «гормонов стресса» катехоламинов (адреналина и норадреналина) и инсулина [1]. Так создается трансмембранный потенциал покоя, наличие которого чрезвычайно важно для нормального функционирования нервной и мышечной ткани.
Поскольку потери калия из внеклеточной жидкости быстро компенсируются за счет его притока из клеток, концентрация этого иона во внеклеточном пространстве на протяжении достаточно длительного времени изменяется очень мало. В результате критический дефицит калия, который может привести к сердечно–сосудистым и нервно–мышечным нарушениям, часто остается незамеченным при стандартных исследованиях.
В результате критический дефицит калия, который может привести к сердечно–сосудистым и нервно–мышечным нарушениям, часто остается незамеченным при стандартных исследованиях.
На распределение калия в организме влияют гормоны, кислотно–щелочное равновесие, скорость обновления клеток. Так, на активность Na+, K+–АТФ–азы опосредованно действует инсулин (способствует перемещению калия в мышечные клетки и клетки печени), повышая эту активность, поэтому больные сахарным диабетом находятся в группе риска по развитию гипокалиемии. Другими причинами гипокалиемии являются: недостаточное поступление с пищей (голодание, диеты), интенсивная потеря жидкости (диарея, потоотделение, прием тиазидных диуретиков или слабительных), гипергликемия, гиперальдостеронизм, гипомагниемия и др. [2].
Рацион современного человека богат натрием, входящим в состав поваренной соли, пекарской соды и др., что способствует перегрузке организма натрием, с одной стороны, и дефициту калия, с другой. Избыток поступления ионов натрия способствует увеличению объема циркулирующей в организме жидкости и развитию артериальной гипертензии (АГ) [3].
Показано, что снижение содержания калия в крови является причиной ряда заболеваний и усугубляет нежелательные побочные эффекты некоторых лекарственных препаратов [4].
Гипокалиемия может быть диагностирована, если уровень калия в сыворотке составляет менее 3,6 ммоль/л. Проявления гипокалиемии включают в себя генерализованную слабость мышц, паралитическую непроходимость кишечника и сердечные аритмии (предсердная тахикардия/блокада, предсердно–желудочковая диссоциация, желудочковая тахикардия, желудочковая фибрилляция).
Магний
Магний является универсальным регулятором биохимических и физиологических реакций, протекающих во всем организме [5]. Существует более 500 видов белков, взаимодействующих с магнием и участвующих более чем в 100 различных молекулярных каскадах клеток [6]. Этим объясняется многообразие проявлений нарушения гомеостаза данного макроэлемента в организме.
По содержанию в организме – это четвертый элемент после натрия, калия и кальция, по содержанию в клетке – второй (после калия). До 80–90% внутриклеточного магния находится в митохондриях в комплексе с АТФ (аденозинтрифосфатом – главным высокоэнергетическим продуктом во всех живых клетках). Учитывая подобную привязанность микроэлемента к митохондриям, больше всего (около 40%) Mg2+ содержится в плаценте и головном мозге, особенно в сером веществе, а также в сердце, мышцах, печени, почках. Остальные 50–60% минерала концентрируются в дентине и эмали зубов, скелете. При дефиците Mg2+ может высвобождаться из костей, предотвращая снижение его концентрации в сыворотке крови, которая в норме составляет 0,8–1,2 ммоль/л.
Магний принимает участие в регуляции состояния клеточной мембраны и трансмембранном переносе ионов кальция и натрия, самостоятельно участвует во многих метаболических реакциях по образованию, накоплению, переносу и утилизации энергии, свободных радикалов и продуктов их окисления. Поэтому микроэлемент в первую очередь определяет нормальную работу нервной системы.
Недостаток магния в организме – очень распространенное явление в современной популяции [7]. Наиболее часто возникает алиментарный дефицит магния: недостаточное его содержание в пище, воде или недоедание, а также избыток поступающих с пищей кальция, натрия, белка или жира существенно снижают его поступление в организм [8]. Происхождение магниевого дефицита можно связать с наличием стереотипов питания, недостатком в рационе морепродуктов, свежих овощей и фруктов и низким содержанием магния в них на фоне повышенной потребности в элементе. Магниевый дефицит часто возникает по принципу антагонизма с натрием, что связано с пищевыми традициями избыточного потребления поваренной соли, а также с избытком бария и алюминия, усиливающим выведение магния из организма [6]. Бор содержится в керамической и эмалированной посуде, консервантах. Накопление алюминия встречается при использовании воды из–под крана, алюминиевой посуды и упаковки. Бариты могут накапливаться в растениях и воде рядом с объектами керамической, бумажной, металлургической промышленности, поступать в организм при употреблении консервированных продуктов [9]. Усугубляют дефицит магния факторы, связанные с его недостаточным всасыванием, увеличением выведения или повышенным расходованием, такие как стресс, физическое перенапряжение, злоупотребление алкоголем, сахарный диабет [10,11].
Дефицит магния характеризуется множеством симптомов и синдромов, наиболее ранними из которых являются отклонения в функционировании нервной, сердечно–сосудистой систем, формирование дисплазии соединительной ткани.
Доказательная медицина и эпидемиологические исследования обобщили многочисленные данные, что вследствие дефицита магния и кальция в диете (магнийдефицитная пища и мягкая вода) повышена частота гипертонической болезни. Это объясняется участием магния в механизмах регуляции артериального давления. Применение магния способствует вазопротекции, снижению уровня липидов в крови, что тормозит атеросклеротическое поражение сосудов.
Негативным последствием магниевого дефицита являются повышенная агрегация тромбоцитов и увеличение риска тромбоэмболических осложнений. Дисбаланс Ca2+, Mg2+ приводит к избыточному тромбообразованию на фоне дефицита магния. Дефицит Mg2+ может задерживать образование артериального тромба путем ингибирования активности тромбоцитов. Магний потенцирует антикоагулянтные эффекты ацетилсалициловой кислоты и позволяет минимизировать ее дозу.
К долговременным последствиям дефицита магния относятся развитие АГ, сердечно–сосудистой патологии, повышенный риск инфаркта миокарда, инсульта мозга, атеросклероза (потенцируется дефицитом пиридоксина), диабета и ряда онкологических проблем [12].
Калий и магний и основные факторы риска развития инсульта: АГ,
нарушения ритма сердца
Высокое потребление калия снижает риск развития мозгового инсульта независимо от других факторов. Сразу в нескольких независимых исследованиях показано, что повышение суточного потребления калия на 10 ммоль снижает относительный риск развития инсульта на 40% [5,13]. Данные экспериментов на животных и эпидемиологических исследований также подтверждают этот факт. Хотя часть защитного эффекта калия может развиваться вследствие понижения артериального давления, анализ экспериментов на животных показывает, что калий может характеризоваться другими защитными механизмами, которые включают уменьшение формирования свободных радикалов, пролиферации гладкомышечных сосудов, артериального тромбоза. Также было показано экспериментально, что калий может уменьшать макрофагальную адгезию к сосудистой стенке, снижая риск развития атеросклероза.
Относительный риск связанной с инсультом летальности был значительно ниже при высоком потреблении калия. Это подтверждает исследование, проведенное в 1998 г. Авторы определили, что использование калиевых добавок обратно пропорционально связано с риском инсульта, особенно у мужчин с АГ. Они предположили, что это могло быть связано с уменьшением риска гипокалиемии. Авторы рекомендовали увеличение потребления калия, заменяя обработанные пищевые продукты и напитки с низким содержанием калия на фрукты, овощи и соки, а также предлагали применять калиевые добавки у лиц с АГ [13]. При поступлении в организм с пищей достаточного количества калия и магния существенно снижается риск развития АГ.
Данные эпидемиологических и клинических исследований подтвердили роль дефицита калия в патогенезе эссенциальной АГ. Увеличение поступления калия имеет гипотензивный эффект, который обусловлен такими механизмами, как увеличенный натрийурез, усиленная барорефлекторная чувствительность, прямое сосудорасширение и понижение сердечно–сосудистой реактивности к норэпинефрину или ангиотензину II [14].
Был проведен метаанализ рандомизированных контролируемых исследований влияния потребления калия внутрь на артериальное давление. Этот анализ включал 33 клинических исследования (n=2609). В данных исследованиях потребление калия было единственным различием между группами. Дозировка калия (главным образом в форме хлорида калия) составляла от 60 до более 100 ммоль/сут. Результаты показали, что поступление калия было связано со значительным снижением среднего систолического и диастолического артериального давления (–4,4 мм рт.ст. и –2,4 мм рт.ст. соответственно; р
Необходимо также помнить, что некоторые мочегонные средства, являющиеся эффективными лекарственными препаратами для лечения АГ и сердечной недостаточности, в качестве нежелательного побочного действия могут вызывать выведение калия и магния из организма [4].
Одним из мощнейших регуляторов сосудистого тонуса в организме человека является ангиотензин. Выбрасываясь в кровь в небольших количествах, ангиотензин оказывает выраженное сосудосуживающее действие, следствием которого является повышение АД. Некоторые современные лекарственные средства, предназначенные для лечения АГ, имеют в качестве основного механизма действия систему ангиотензина. Калий и магний также ослабляют выраженность сосудосуживающих эффектов, вызванных ангиотензином [16]. Таким образом, у лиц с повышенным АД очень важно избегать снижения уровня калия и магния в крови.
Не менее важную роль в профилактике инсульта играет коррекция уровня калия в связи с возможностью развития аритмий, которые могут стать причиной кардиоэмболий. Умеренная гипокалиемия может увеличить вероятность аритмий у больных ИБС, с сердечной недостаточностью или гипертрофией левого желудочка. Изменения уровней калия меняют электрофизиологические свойства мембраны и могут влиять на генерацию импульса и проведение его по сердцу. Снижение концентрации калия приводит к повышению активности пейсмейкера, активируются гетеротопные очаги возбуждения, что может сопровождаться нарушениями ритма. Дефицит калия, так же, как и блокада калиевых каналов, может привести к длительной реполяризации – патогенетическому фактору развития трепетаний и мерцаний. В международном клиническом исследовании показано, что снижение уровня калия в крови на 1 ммоль/л повышало риск развития желудочковых аритмий на 28% [17].
Влияние гипокалиемии на реполяризацию усиливается при многих заболеваниях, включая гипертрофию левого желудочка, застойную сердечную недостаточность, миокардиальную ишемию и инфаркт миокарда.
Калий и магний
и диабетическая полинейропатия
Наиболее частой среди соматических заболеваний, приводящих к поражению периферической нервной системы, является диабетическая нейропатия, которая встречается в 20–40% случаев. По оценкам ВОЗ, более 180 млн человек в мире больны диабетом, и к 2030 г. эта цифра может возрасти более чем в 2 раза. К факторам риска развития полинейропатии у больных сахарным диабетом относят длительность самого заболевания, уровень и значительные колебания HbA1С (гликозилированный гемоглобин является показателем компенсации углеводного обмена на протяжении последних 60–90 дней) в крови, дислипидемию, высокий индекс массы тела, альбуминурию, АГ и курение [18].
Ряд авторов выделяют несколько теорий патогенетических механизмов развития нейропатии, среди которых: повышение внутриклеточной осмолярности как следствие накопления сорбитола и образующейся из него фруктозы, не способных преодолевать клеточную оболочку, тем самым повреждая клетку; нарушение деятельности K+/Na+–насоса; нарушение трофики нерва и др. Нарушение обмена K+ приводит к изменению возбудимости нервов и мышц. Активный ионный транспорт поддерживает высокий градиент K+ через плазменную мембрану. Отдельно рассматривают гипокалиемию, не связанную с потерями калия, а обусловленную его перемещением из плазмы крови и внеклеточного пространства внутрь клеток. Снижение сывороточного уровня калия, индуцированное избытком инсулина, секретировавшегося в ответ на гипергликемию или при введении его препаратов, нередко наблюдают у больных сахарным диабетом [19].
Интересно, что магниевый дефицит уменьшал чувствительность инсулина, а при устранении магниевого дефицита во время 4–недельного периода исследования улучшалась утилизация глюкозы в тканях у пожилых людей с сахарным диабетом. У пациентов с диабетом 2–го типа пероральный прием магния во время 16–недельного периода исследования улучшал чувствительность инсулина в тканях. Высказано предположение, что гипомагниемия может изменять транспорт глюкозы в клетку и снижать чувствительность клеточных рецепторов к инсулину. Гипомагниемия часто присутствует у больных сахарным диабетом, однако нет точного разъяснения механизма развития последствий дефицита магния при сахарном диабете. С другой стороны, замечено, что несоответствующий метаболический контроль может привести к уменьшению в крови концентрации магния, вызывая гипомагниемию, которая в свою очередь может непосредственно вызывать микро– и макрососудистые осложнения, ретинопатию и нейропатию, т.е. недостаток магния приводит к более раннему развитию осложнений сахарного диабета. В экспериментах на животных длительный дефицит магния вызвал истощение и гибель b–клеток поджелудочной железы.
Некоторые авторы предполагают, что гипомагниемия может быть связана с высоким риском развития язв на стопах у больных сахарным диабетом. Действительно, чаще гипомагниемия наблюдается среди пациентов с язвами диабетической стопы по сравнению с пациентами без язвенных поражений (93,9% – пациенты с язвами диабетической стопы по сравнению с 73,1% пациентов без язв) [20].
Магний и калий и черепно–мозговая травма и эпилепсия
Глобальная ишемия мозга при черепно–мозговой травме (ЧМТ) приводит к нарушению функции глутаматных рецепторов в коре (в тяжелых случаях на 90–100%). Это вызывает перевозбуждение или даже смерть нейронов за счет повышения проницаемости мембраны нейрона для ионов Са2+ и уменьшения митохондриального пула Mg2+, а также повышения уровня свободного цитозольного Mg2+ в нейроне, признанного маркера начала каскада апоптоза. Ионы Mg2+ являются универсальными стабилизаторами всех подтипов NMDA–рецепторов, контролируя работу вольтаж–зависимого ионного канала для Ca2+, Na+, К+. При дефиците Mg2+ рецепторы к глутамату возбуждаются, ток ионов Ca2+ в нейроны усиливается, потенцируется развитие эксайтотоксичности.
Снижение внутриклеточной концентрации магния характерно для эпилепсии. Реализация наркотического, снотворного, седативного, анальгетического и противосудорожного эффектов магнийсодержащих препаратов связана с одним из важнейших эффектов магния – способностью к торможению процессов возбуждения в коре головного мозга. Применение препаратов, содержащих магний, у больных с эпилепсией повышает восприимчивость к противосудорожным препаратам (вальпроат натрия, карбамазепин), снижает тяжесть эпилептических приступов [21].
Панангин
Исследование клеточных моделей подтвердило критическую роль магния в поддержании уровня внутриклеточного калия и доказало, что эти механизмы многофакторные. Совместный дефицит калия и магния может привести к недостаточному насыщению калием [22].
Панангин – лекарственный препарат, содержащий калий и магний в виде солей аспарагиновой кислоты, способствующей лучшему их усвоению организмом. Панангин является источником ионов калия и магния. Препарат улучшает обмен веществ в миокарде, повышает переносимость сердечных гликозидов, обладает антиаритмической активностью. Чаще всего Панангин назначают в качестве дополнительного средства терапии при хронических заболеваниях сердца (сердечная недостаточность, состояние после инфаркта миокарда), нарушениях сердечного ритма (преимущественно при желудочковых аритмиях), лечении сердечными гликозидами (для повышения их эффективности и улучшения переносимости), а также у лиц со сниженным уровнем калия и магния в крови, вызванным их недостаточным поступлением с пищей. Если говорить о профилактике инсульта, то следует помнить о возможных положительных свойствах Панангина, а именно: снижение уровня артериального давления у больных с АГ; снижение риска развития аритмий; улучшение сократительной функции миокарда и профилактика развития сердечной недостаточности; уменьшение вязкости крови и тромбообразования.
Взрослым пациентам препарат назначают внутрь по 1–2 таблетки 3 р./сут. Дозу можно повысить до 3 таблеток 3 р./сут. Кислое содержимое желудка может снижать усвоение препарата, поэтому Панангин целесообразно принимать после еды. Противопоказан Панангин только при острой и хронической почечной недостаточности и выраженной гиперкалиемии. Препарат высокоэффективен и очень хорошо переносится пациентами, поэтому может быть рекомендован широкому кругу больных как в профилактических, так и в лечебных целях при различных неврологических заболеваниях.
Литература
1. Clausen T., Everts M.E. Regulation of the Na, K–pump in skeletal muscle // Kidney Int. 1989. Vol. 35. P. 1–13
2. Физиология человека: в 3–х томах; пер. с англ./ Под ред. Р. Шмидта и Г Тевса. – 3–е изд. – М.: Мир, 2004.
3. Schulman M., Narins R.G. Hypokalemia and cardiovascular disease // Amer. J. Cardiol. 1990. Vol. 65. P. 4–9.
4. Hoes A.W., Grobbee D.E., Peet T.M., Lubsen J. Do non–potassium–sparing diuretics increase the risk of sudden cardiac death in hypertensive patients? // Recent. evidence. Drugs. 1994. Vol. 47. P. 711–733.
5. Maier J.A., Malpuech–Brugere C. et al. Low magnesium promotes endothelial cell dysfunction: implications for atherosclerosis, inflammation and thrombosis // Biochim. Biophys. Acta. 2004. Vol. 24;1689(1). P. 13–21.
6. Громова О.А. Магний и пиридоксин: основы знаний.– М., 2006. – 223 с.
7. Schimatschek H.F., Rempis R. Prevalence of hypomagnesemia in an unselected German population of 16,000 individuals // Magnes Res. 2001. Vol. 14(4). P. 283–290.
8. Galan P., Preziosi P., Durlach V. et al. Dietary magnesium intake in a French adult population // Magnes Res. 1997. Vol. 10(4). P. 321–328.
9. Калачева А.Г., Громова О.А., Гришина Т.Р. Роль магния в сбалансированном питании детей и подростков // Фарматека. – 2008. – № 20. – С. 34–38.
10. Grases G., Perez–Castello J.A. Anxiety and stress among science students. Study of calcium and magnesium alterations // Magnes Res. 2006. Vol. 19(2). P. 102–106.
11. Акарачкова Е.С., Вершинина С.В., Котова О.В. Магний в лечении и профилактике цереброваскулярных заболеваний // Кардиология. – 2012. – № 9. – С. 80–86.
12. Акарачкова Е.С. Дефицит магния: клиника, диагностика, терапия // Фарматека. – 2007. – № 20. – C. 25–30.
13. Ascherio A., Rimm E.B., Hernan M.A. et al. Intake of potassium, magnesium, calcium, and fiber and risk of stroke among U.S. men // Circulation. 1998. Vol. 98. P. 1198–1204.
14. Young D.B., Lin H., McCabe R.D. Potassium’s cardiovascular protective mechanisms // Amer. J. Physiol. 1995. Vol. 268. P. R825–837.
15. Whelton P.K., He J. Potassium in preventing and treating high blood pressure // Semin. Nephrol. 1999. Vol. 19(5). P. 494–499
16. Campbell W.B., Schmitz J.M. Effect of alterations in dietary potassium on the pressor and steroidogenic effects of angiotensins II and III // Endocrinol. 1978. Vol. 103. P. 2098–2104.
17. Cohen J.D., Neaton J.D., Prineas R.J., Daniels K.A. Diuretics, serum potassium and ventricular arrhythmias in the Multiple Risk Factor Intervention trial // Amer. J. Cardiol. 1987. Vol. 60. P. 548–554.
18. Бегма А.Н., Бегма И.В. Комплексное лечение язвенных дефектов у больных с синдромом диабетической стопы // Фарматека. – 2004. ¬– C. 19–20.
19. Дедов И.И., Анциферов М.Б., Галстян Г.Р. и др. Синдром диабетической стопы: клиника, диагностика, лечение. – М., 1998.
20. Городецкий В. В. Лечение диабетической полинейропатии и других дистрофически–дегенеративных и воспалительных заболеваний периферической нервной системы метаболическими препаратами: метод. рекомендации. – М.: Медпрактика–М, 2002. – С. 36.
21. Шварков С.Б., Акарачкова Е.С. Коррекции энергетического и электролитного баланса препаратами магния и пиридоксина при неврологических заболеваниях // Мед. технология. – 2007. – 31с.
22. Whang R., Whang D.D., Ryan M.P. Refractory potassium repletion. A consequence of magnesium deficiency // Arch. Intern. Med. 1992. Vol. 152(1). P. 40–45.
.
Водно-электролитный обмен в организме здорового человека: основные составляющие
Рассмотрение метаболических путей нормально функционирующего организма невозможно без описания обмена низкомолекулярных соединений — минеральных солей и воды. Как известно, вода у взрослого человека составляет 60% от массы тела, то есть 40 — 45 литров. Биологическое значение воды, содержащейся в организме человека, трудно переоценить. Вода и растворенные в ней вещества создают внутреннюю среду организма. Вода обеспечивает транспорт веществ и тепловой энергии по организму. Значительная часть химических реакций организма протекает в водной фазе. Вода участвует в реакциях гидролиза, гидратации, дегидратации. Определяет пространственное строение и свойства гидрофобных и гидрофильных молекул. Поскольку вода является средой, в которой осуществляются процессы обмена веществ в клетках, органах и тканях, непрерывное поступление воды в организм является одним из основных условий поддержания его жизнедеятельности. Основная масса (около 71 %) всей воды в организме входит в состав протоплазмы клеток, составляя так называемую внутриклеточную воду. Внеклеточная вода входит в состав межклеточной, или интерстициалъной, жидкости (около 21%) и воды плазмы крови (около 8%). Содержание воды в организме варьирует в зависимости от органов и тканей. В головном мозге содержится 70-84% воды от всей массы органа, в почках – 82%, в сердце и легких – 79%, в мышцах – 76%, в коже – 72%, в печени – 70%, в костной ткани – 10%. Вода, которая поступает алиментарным путем называется экзогенной, а образовавшаяся в качестве продукта биохимических превращений – эндогенной. Кроме того, различают свободную воду, связанную воду и конституционную воду. Связанная вода удерживается коллоидными системами в виде так называемой воды набухания, Конституционная или внутримолекулярная вода входит в состав молекул белков, жиров и углеводов и освобождается при их окислении. Разные ткани характеризуются различным соотношением свободной, связанной и конституционной воды. Вся вода организма обновляется примерно через месяц, а внеклеточное водное пространство — за неделю.
Водный баланс организма складывается из отребления и выделения воды. С пищей человек получает в сутки около 1100 мл воды, в виде напитков и чистой воды — около 1200 мл. Около 300 мл воды образуется в процессе метаболизма при окислении белков, углеводов и жиров. При испарении с поверхности кожи и альвеол легких в сутки выделяется около 900 мл воды. 1500 мл воды необходимо для растворения экскретируемых почкой осмотически активных веществ при максимальной осмолярности мочи. Секреция воды в пищеварительную трубку составляет 8200 мл, реабсорбция — 8100 мл. 100 мл воды выводится с фекалиями. Простые подсчеты показывают. что средняя суточная потребность человека в воде составляет около 2500 мл.
Водный баланс организма человека.
|
Средние величины параметров водного баланса организма человека (мл/сут)
|
|||
|
Потребление и образование воды
|
Выделение воды
|
||
|
Питье и жидкая пища
|
1200
|
С мочой
|
1500
|
|
Твердая пища
|
1100
|
С потом
|
500
|
|
Эндогенная «вода окисления»
|
300
|
С выдыхаемым воздухом
|
400
|
|
С калом
|
100
|
||
|
Итого Поступление
|
2500
|
Итого Выделение
|
2500
|
|
Внутренний цикл жидкостей желудочно-кишечного тракта (мл/сут)
|
|||
|
Секреция
|
Реабсорбция
|
||
|
Слюна
|
1500
|
||
|
Желудочный сок
|
2500
|
||
|
Желчь
|
500
|
||
|
Сок pancreas
|
700
|
||
|
Кишечный сок
|
3000
|
||
|
Итого
|
8200
|
8100
|
|
|
Итого 8200 — 8100 = вода в кале 100 мл
|
|||
Очевидно, что обмен воды неразрывно связан в организме с обменом электролитов. Системы регуляции водно-солевого обмена обеспечивают поддержание общей концентрации ионов натрия, калия, кальция, магния, хлора в плазме крови, во внутриклеточной и внеклеточной жидкости на одном и том же уровне. В плазме крови человека концентрация ионов поддерживается с высокой степенью постоянства и составляет (в ммоль/л): натрия — 130—156, калия — 3, 4—5, 3, кальция — 2, 3—2, 75 (в т. ч. ионизированного, не связанного с белками — 1, 13), магния — 0, 7—1, 2, хлора — 97—108, бикарбонатного иона — 27, сульфатного иона — 1, 0, неорганического фосфата — 1—2. По сравнению с плазмой крови и межклеточной жидкостью клетки отличаются более высоким содержанием ионов калия, магния, фосфатов и низкой концентрацией ионов натрия, кальция, хлора и ионов бикарбоната. Различия в солевом составе плазмы крови и тканевой жидкости обусловлены низкой проницаемостью капиллярной стенки для белков. Точная регуляция водно-солевого обмена у здорового человека позволяет поддерживать не только постоянный состав, но и постоянный объем жидкостей тела, сохраняя практически одну и ту же концентрацию осмотически активных веществ и кислотно-щелочное равновесие.
Минеральные вещества поступают в организм в свободном или связанном виде. Ионы всасываются уже в желудке, основная часть минеральных веществ – в кишечнике путем активного транспорта при участии белков–переносчиков. Из желудочно-кишечного тракта минеральные вещества поступают в кровь и лимфу, где связываются со специфическими транспортными белками. Выделяются минеральные вещества главным образом в виде солей и ионов. С мочой выделяются натрий, калий, кальций, магний, хлор, кобальт, йод, бром, фтор. С калом выделяются железо, кальций, медь, цинк, марганец, молибден, и тяжелые металлы.
Наиболее важное значение в водно-электролитном гомеостазе имеют ионы натрия, калия, кальция, хлора. Натрий (Na+) является основным катионом внеклеточных жидкостей. Его содержание во внеклеточной среде в 6—12 раз превышает содержание в клетках. Натрий в количестве 3—6 г в сутки поступает в организм в виде NaCl и всасывается преимущественно в тонком отделе кишечника. Натрий участвует в поддержании равновесия кислотно-основного состояния, осмотического давления внеклеточных и внутриклеточных жидкостей, принимает участие в формировании потенциала действия, оказывает влияние на деятельность практически всех систем организма. Баланс натрия в организме в основном поддерживается деятельностью почек.
Калий (К+) является основным катионом внутриклеточной жидкости. В клетках содержится 98% калия. Суточная потребность человека в калии составляет 2—3 г. Основным источником калия в пище являются продукты растительного происхождения. Особое значение калий имеет благодаря своей потенциалобразующей роли как на уровне поддержания мембранного потенциала, так и в генерации потенциала действия. Мембранный потенциал покоя, т. е. разность потенциалов между клеточным содержимым и внеклеточной средой, сознается благодаря способности клетки активно с затратой энергии поглощать ионы К+ из внешней среды в обмен на ионы Na+ (так называемый К+, Na+-насос) и вследствие более высокой проницаемости клеточной мембраны для ионов К+ чем для ионов Na+. Из-за высокой проницаемости неточной мембраны для ионов К+ дает небольшие сдвиги в содержании калия в клетках (в норме это величина постоянная) и плазму крови ведут к изменению величины мембранного потенциала и возбудимости нервной и мышечной ткани. Калий принимает также участие в регуляции кислотно-основного состояния на конкурентных взаимодействиях между ионами К+ и Na+, а также К+ и Н+ и является фактором поддержания осмотического давления в клетках. Регуляция его выведения осуществляется преимущественно почками.
Кальций (Са2+) обладает высокой биологической активностью. Он является основным структурным компонентом костей скелета, где содержится около 99% всего Са2+. В сутки взрослый человек должен получать с пищей 800—1000 мг кальция. Всасывается кальций преимущественно в двенадцатиперстной кишке в виде одноосновных солей фосфорной кислоты. Примерно 3/4 кальция выводится пищеварительным трактом, куда эндогенный кальций поступает с секретами пищеварительных желез, остальная часть выводится почками. Кальций принимает участие в генерации потенциала действия, в инициации мышечного сокращения, является необходимым компонентом свертывающей системы крови, повышает рефлекторную возбудимость спинного мозга и обладает симпатикотропным действием.
Магний (Mg2+) по содержанию в организме занимает четвертое место среди катионов организма и второе место среди внутриклеточных катионов. Количество общего магния, содержащегося в организме взрослого, составляет 20–28 г. Около 1 % магния находится во внеклеточной жидкости, приблизительно 60 % — в костях, 20% — в мышцах. Остальные 20% приходятся на другие ткани организма, причем большая часть сосредоточена в клетках печени. В плазме крови концентрация магния составляет 0, 75–1, 25 ммоль/л. Из этого количества 55–60 % магния плазмы ионизировано, 15 % связано с органическими и неорганическими кислотами. Биологически активным является только ионизированный магний, концентрация которого в плазме составляет 0, 45–0, 75 ммоль/л. Магний выполняет следующие физиологические функции: входит в состав костей, является антагонистом кальция, влияет на проницаемость биологических мембран, активирует фибринолиз, участвует в функционировании многих ферментов, связанных с обменом АТФ, в качестве кофактора.
Содержание хлора (Cl—) в организме составляет около 100 г. В плазме (сыворотке) крови его концентрация достигает 97–108 ммоль/л. Его физиологическая функция связана с участием в формировании трансмембранного потенциала. Являясь основным анионом внеклеточной жидкости, ион хлора активно участвует в обеспечение электронейтральности. Благодаря наличию в мембранах клеток и митохондрий специальных хлорных каналов, хлорид ионы регулируют объем жидкости, трансэпителиальный транспорт ионов, что создает и стабилизирует мембранный потенциал Механизмы регуляции хлора связаны с процессами, стабилизирующими содержание натрия. В связи с тем, что хлорид-ионы способны проникать через мембрану клеток, они вместе с ионами натрия и калия поддерживают осмотическое давление и регулируют водно-солевой обмен. Хлор является составной частью соляной кислоты желудочного сока, денатурирующей белки и активирующей пепсиноген. создают благоприятную среду в желудке для действия протеолитических ферментов желудочного сока. Кроме того, ионы хлора участвуют в создании и поддержании рН в клетках и биологических жидкостях организма.
Фосфор (Р) относится к структурным (тканеобразующим) макроэлементам, его содержание в организме взрослого человека составляет около 700 г.
Большая часть фосфора (85-90%) находится в костной ткани и в зубах, остальное – в мягких тканях и жидкостях. Около 70% общего фосфора в плазме крови входит в органические фосфолипиды, около 30% — представлено неорганическими соединениями (10% соединения с белком, 5% комплексы с кальцием или магнием, остальное – анионы ортофосфата). Биологическая роль фосфора в организме сводится к следующему. Фосфор входит в состав многих веществ организма (фосфолипиды, фосфопротеиды, нуклеотиды, коферменты, ферменты). Фосфолипиды являются основным компонентом мембран всех клеток в организме человека. В костях фосфор находится в виде гидроксилапатита, в зубах в виде фторапатит, выполняя структурную функцию. Остатки фосфорной кислоты входят в состав нуклеиновых кислот и нуклеотидов, а также в состав аденозинтрифосфорной кислоты (АТФ) и креатинфосфата. Остатки фосфорной кислоты входят в состав буферной системы крови, регулируя ее рН.
Статья добавлена 31 мая 2016 г.
Калий — натрий: заклятая дружба?
А. Мотыляев
«Химия и жизнь» №7, 2020
Повышенное потребление натрия в виде поваренной соли плохо сказывается на здоровье, а именно способствует гипертонии, об этом знают все. Однако отнюдь не все считают натрий таким уж врагом человечества. Не исключено, что во всем виноват не именно натрий, а древний механизм регулирования в организме, придуманный для контроля его родного брата — калия.
Древний калий
Соображения о том, что калий, в отличие от натрия, должен помогать здоровью, следуют скорее всего из идей о возврате к диете наших далеких предков. Действительно, все млекопитающие, в том числе и люди, сформировались в мире, где еда обогащена калием, а натрия в ней немного (см. «Химию и жизнь», 2020, № 5/6). Причина понятна: калий, в отличие от натрия, — жизненно важный элемент для растений. Поэтому все их части обогащены калием в противовес натрию. Соответственно, травоядным достается с едой много калия, а потом он оказывается в организмах и всеядных, и хищников.
Дальние предки людей были именно травоядными — питались фруктами, побегами и листьями растений тропического леса. Тогда-то в целом и сформировались органы пищеварения и механизмы регулирования химического состава тела. Есть мнение, что и гораздо позже калий в пище людей продолжал превосходить натрий; исследователи древней диеты утверждают человек каменного века в день съедал 15 граммов калия! При этом современный человек потребляет не более 2 граммов калия в день при рекомендации 3,5 грамма, натрия же он съедает в два раза больше: 4–5 граммов. Так соотношение этих двух щелочных металлов с близкими свойствами в современной диете оказалось обратным тому, к которому изначально был приспособлен человеческий организм.
Калий и ВОЗ
Исследователи, стремящиеся понять хитросплетения калий-натриевой игры, ведут наблюдения за потреблением людьми обоих элементов и пытаются связать полученные данные с информацией о здоровье. Иногда это удается сделать, иногда не очень. Сегодня можно считать доказанным, а ВОЗ именно так и считает, что у гипертоников увеличение потребления калия с гарантией снижает давление и чем выше при этом потребление натрия, тем сильнее действует калий. Почему только у гипертоников? А потому, что основные исследования проведены именно с участием таких пациентов. Например, когда в 2012 году ВОЗ готовила рекомендации по потреблению калия, ее эксперты отобрали 22 исследования, из которых только три было выполнены с участием людей без гипертонии.
Удивительно, но в этих работах не удалось выявить прямую связь потребления калия с риском развития сердечно-сосудистых заболеваний. Однако, как указывают эксперты ВОЗ, раз связь гипертонии с ними доказана, значит, увеличение потребления калия должно благотворно сказаться и на их статистике. А вот благотворное влияние повышенного потребления калия на статистику инсультов доказано строго.
Сколь велико снижение давления от потребления калия? В среднем, при рекомендуемом ВОЗ уровне, выходит 3 мм рт. ст., однако если потребление калия выше, тогда верхнее давление снижается на 5,8, а нижнее — на 3,5 мм рт. ст. Перевод этих чисел в социальные последствия таков. В США снижение артериального давления на 2 мм уменьшает на 17% риск развития гипертонии, на 6% число инфарктов и на 15% число инсультов. В Великобритании снижение давления на 5 мм уменьшает вероятность гипертонии в два раза.
Как показывает статистика, детям увеличение потребления калия в разумных пределах тоже полезно. Помимо того что калий способствует общему укреплению костей и мышц, он также слегка снижает давление, а ведь известно, что, если у ребенка в детстве есть склонность к гипертонии, она обязательно проявит себя в будущем. Правда, ВОЗ уточняет, что рекомендации действительны для возраста более 24 месяцев, а дозу калия надо соизмерять с весом ребенка; 3,5 грамма в день — это для людей старше 16 лет.
Калий увеличивает отток жидкостей из организма, поэтому у врачей были опасения, что из-за уменьшения объема крови в ней может подняться концентрация холестерина. Это опасение не подтвердилось. Также не было выявлено негативное влияние повышенного потребления калия на почки здорового человека. Причем повредить не могут даже огромные дозы калия, сравнимые с палеодиетой; по крайней мере исследования продолжительностью в несколько недель не выявили вреда. В целом, как считает ВОЗ, если источником калия служит пища, а не пищевые добавки, переборщить с этим элементом нельзя, в отличие от натрия. Однако именно калий может оказаться очень действенным средством против натрия. Более того, не исключено, что благотворное влияние калия на сердце и сосуды связано именно с противодействием разрушительному действию натрия на них.
Немного физиологии
В отличие от натрия, ионы которого в основном находятся в жидкостях организма, ионы калия главным образом сосредоточены во внутриклеточных жидкостях. В клетках находится 90% калия организма, причем основное его хранилище — клетки мышц. Остальной калий циркулирует в плазме крови, и его концентрация там должна быть строго постоянна. Однако поступление калия в организм человека в течение дня меняется очень сильно: от нуля в период покоя до граммов в час во время еды. Организм с такими всплесками вынужден бороться, для этого у него есть несколько механизмов.
Калий всасывается в кишечнике непосредственно, за счет диффузии, то есть не используя какие-то клеточные каналы. Значит, его всасывание организм регулировать не может. Поэтому он регулирует выведение, и, в сущности, весь съеденный калий должен вскоре выйти: 90% с мочой и 10% с калом. Похоже, что организм считает калий крайне нежелательным элементом и стремится избавиться от него как можно скорее. Так, каким-то непостижимым пока для физиологов образом, как только калий начинает поступать в кишечник, почки сразу же принимаются усиленно отгонять его из плазмы крови в мочу, будто зная, что нужно готовить свободное место для новых поступлений.
Одновременно с поглощением пищи включается и независимый механизм утилизации калия, инсулиновый. Да, этот гормон способствует усвоению глюкозы, но, удивительно, он же активирует и канал перекачки калия внутрь мышечных клеток, обеспечивая его временное хранение. Причем так получается, даже если калия в пище мало и почки вполне могут с ним справиться: активируется-то инсулин не калием, а глюкозой. Что происходит с калием в клетках мышц, к истории с натрием особого отношения не имеет. Поэтому обратимся к почкам, которые выводят свежесъеденный калий в мочу.
Прочь из почек!
Организм расстаться со съеденным калием все-таки не спешит — вдруг надо пополнить запасы в клетках? Поэтому не весь калий сразу отправляется в мочу — большую его часть, до 80%, почки возвращают в кровь. А тот, что не вернулся, надо отправить на выделение, и тут начинается партия натрия. Ключевым элементом при этом оказался специальный белок, так называемый Na+–Cl− котранспортер (NCC). Как видно из его названия, он работает вовсе не с калием, а с натрием, а задача этого белка — возвращение натрия из почек в кровь. Когда белок активируется, он отправляет натрий в кровь, а когда дезактивируется, то открывает ворота на пути натрия в мочу.
Этот белок известен давно, и сведения о его роли помогают создавать, например, мочегонные препараты. Однако почти полвека биохимики не догадывались, что с этим белком активно работает калий. В 2009 году Волкер Валлон и его коллеги из Калифорнийского университета в Сан-Диего (American Journal Physiology. Renal Physiology, 297, 3) установили, что включением / отключением NCC заведует отнюдь не натрий, а калий: малое содержание калия в плазме крови его активирует, а большое — дезактивирует. Выходит, что, когда калия мало, организм, вопреки логике, перестает выводить в мочу прежде всего натрий! Сделано так потому, что калий попадает в мочу из соответствующих клеток почек в обмен на всасывание ионов своего брата. Чтобы заблокировать действие этого механизма, и нужно снизить содержание натрия в моче: не станет там натрия, и калий туда не попадет. Это разумно — зачем выводить калий, когда его и так мало?
Однако соучастие в этой операции натрия портит все дело: получается, что натрий возвращается в кровь независимо от своей концентрации, но в зависимости от содержания калия. Значит, при недостатке калия концентрация натрия в крови будет неизбежно повышаться, сколько бы натрия не было в еде. А у организма не так уж много способов бороться с таким ростом, и главный из них — добавлять воду в кровь: тогда концентрация натрия снизится, ведь подавляющая его часть находится именно в крови. Увеличение объема жидкости в замкнутой системе неизбежно ведет к росту давления. Если же калия много, белок NCC дезактивируется, натрий идет в мочу, увлекая за собой как калий, так и излишнюю воду. Объем жидкости в организме уменьшается, и давление падает. Причина этих сложных взаимоотношений двух элементов, видимо, в том, что организму надо поддерживать постоянный уровень калия в крови, но он не может это делать за счет манипуляции с объемом жидкости, как получается с натрием. Ведь в крови находится ничтожная доля всего калия организма.
Когда наши предки жили в тропическом лесу и питались фруктами да зелеными побегами, калия в пище было заведомо больше, чем натрия. В таких условиях натрий надо было экономить, и изложенный механизм прекрасно работал: выводить или сохранять оба щелочных элемента в организме можно было, ориентируясь на концентрацию одного из них, более распространенного. При современной диете с превышением натрия над калием этот механизм выглядит анахронизмом, поэтому и работает со сбоями. Однако исправить его невозможно. Значит, надо это принять и соответствующим образом изменять привычки человека, чтобы довести соотношение калия с натрием в пище до 1:1, а то и больше. ВОЗ считает, что, если соблюдать ее рекомендации и есть 3,5 грамма калия и 2,5 грамма натрия в день, — так оно и получится.
Подготовлено с использованием обзоров:
1. Naohiro Nomura E. A. Clinical importance of potassium intake and molecular mechanism of potassium regulation // Clinical and Experimental Nephrology, 2019, 23.
2. Alicia A. McDonough E. A. Potassium Homeostasis: The Knowns, the Unknowns, and the Health Benefits // Physiology (Bethesda), 2017, 32, 2.
5 серьезных причин, почему калий важен для спортсменов
Ежедневное потребление калия должно составлять минимум 2 г в день для взрослых, здоровых людей. Тем не менее, оптимальное потребление калия составляет от 4,7 г до 5,1 г.Необходимая дневная порция калия, в зависимости от возраста и пола, приведена в таблице. [24]
| Возраст | Мужчины | Женщины | Во время беременности | Во время кормления |
|---|---|---|---|---|
| До 6 месяцев | 400 мг | 400 мг | ||
| 7 – 12 месяцев | 700 мг | 700 мг | ||
| 1 – 3 года | 3000 мг | 3000 мг | ||
| 4 – 8 лет | 3800 мг | 3800 мг | ||
| 9 – 13 лет | 4500 мг | 4500 мг | ||
| 14 – 18 лет | 4700 мг | 4700 мг | 4700 мг | 5100 мг |
| 19 – 50 лет | 4700 мг | 4700 мг | 4700 мг | 5100 мг |
| 51+ лет | 4700 мг | 4700 мг |
Опрос, проведенный в Соединенных Штатах показал, что менее 2% американцев получают достаточно калия, в то время как женщины потребляют еще меньше этого элемента, чем мужчины. [1] Исследование проведенное в европе, с задействованием людей разного пола и возраста, показало низкий уровень калия в организме пожилых участников. Результаты также колебались в зависимости от образа жизни участников. [25]
Если вы по той, либо иной причине не можете получить рекомендуемую порцию калия из рациона питания, вам следует обратиться за помошью к подходящей пищевой добавке. К группам риска часто относятся люди с низким потреблением фруктов и овощей, пожилые люди, алкоголики, спортсмены и люди подвергнутые высокой физической нагрузке.
Кроме того, если вы находитесь на восстановительной диете, с употреблением менее 1000 калорий в день, вам следует подумать о добавлении калия в виде пищевых добавок.
Дефицит калия в организме
Снижение уровня калия в организме в течении длительного периода времени вызывает гипокалиемию. Это может быть обусловлено чрезмерным выделением калия из организма и его недостаточным восполнением. В группу риска входят:
- спортсмены, тренирующиеся более часа в день
- люди, которые придерживаются низкокалорийной диеты
- люди с проблемами пищеварения
- диабетики
- люди с больными почками
- алкоголики
Гипокалиемия – это реакция организма на частое мочеиспускание, потоотделение, диарею или рвоту, когда количество минералов вымывается из организма. При недостатке калия начинют проявлятся такие симптомы:
- отеки
- гипертония
- нарушения ритма сердца
- артрит
- нервность
- повышенная утомляемость
- слабость мышц
- запор
Гипокалиемия может быть обнаружена с помощью анализов крови. Если уровень калия падает до 2,2-2,5 ммоль / л, это уже опасное для жизни состояние, которое может вызвать паралич тела, разрушение мышц, проблемы с дыханием и фатальные нарушения ритма сердца. [18] [25] Поэтому необходимо поддерживать и регулярно дополнять уровень калия в организме.
Избыточное потребление калия
Повышенный уровень калия в организме называется гиперкалиемией и может привести к серьезным нарушениям обмена веществ. Это состояние, при котором уровень калия повышается до 5,3-8 ммоль / л ( оптимальный диапазон от 3,6 до 5,2 ммоль / л). При этом также может проявляться:
- мышечная боль
- усталость
- тошнота
- покалывание в конечностях
К более серьезным симптомам гиперкалиемии относятся низкое давление, нарушения сердечного ритма, в худшем случае сердечные приступы. Однако не стоит беспокоится раньше времени, ведь гиперкалиемия встречается только у людей с заболеваниями почек или диабетиков. Также чрезмерное употребление калия может служить для того, чтобы вызвать рвоту или выделение избытка жидкости с мочой. [26]
Практические примеры того, как увеличить потребление калия
Чтобы получить достаточно калия, целесообразно ограничить потребление натрия, особенно в количестве потребляемой соли. [4] Еще один хороший шаг – употреблять богатые калием овощи в качестве гарнира к основной еде, например заменить рис на брокколи. Важно добавить в рацион достаточное количество овощей и фруктов. Попробуйте использовать в качестве перекуса курагу, изюм или орехи. Также отлично подойдут фрукты или овощи в виде смузи. Хорошей альтернативой служат пищевые добавки, например калий в форме таблеток.
Как вы считаете, достаточный ли уровень калия в вашем организме? Узнали ли вы что-то новое из этой статьи? Поделитесь с нами оставив комментарий, а также расскажите друзьям об этой статье.
ИСТОЧНИКИ:
[1] Summary of Potassium, primary information, benefits, effects, and Importan Facts – https://examine.com/supplements/potassium/
[2] Potassium intake – http://apjcn.nhri.org.tw/server/info/books-phds/books/foodfacts/html/data/data5b.html
[3] Joe Cohen – Top 14 health benefits of potassium – https://www.selfhacked.com/blog/potassium/#Health_Benefits_of_Potassium
[4] Jacob Farr – Potassium: You make my heart Beat – https://www.foodinsight.org/potassium-ingredient-benefits-health
[5] Rodriguez CJ, Bibbins – Domingo, Jin Z, Daviglus ML, Goff DC Jr, Jacobs DR Jr. – Association of sodium and potassium intake with left ventriculat mass: coronary artery risk dvelopment in young adults. – https://www.ncbi.nlm.nih.gov/pubmed/21788603
[6] Tobian L – Dietary sodium chloride and potassium have effects on the pathoúhysiology of gypertension in humans and animals – https://academic.oup.com/ajcn/article/65/2/606S/4655379
[7] Siani A, Strazzullo P, Giacco A, Pacioni D, Celentano E, Mancini M – Increasing the dietary potassium intake reduces the need for antihypertensive medication. – https://www.ncbi.nlm.nih.gov/pubmed/1929022
[8] Lemann J Jr, Pleuss JA, Gray RW, Hoffmann RG – Potassium administration reduces and potassium deprivation increases urinary calcium excretion in healthy adults. – https://www.ncbi.nlm.nih.gov/pubmed/1648646/
[9] Gregory NS, Kumar R, Stein EM, Alexander E, Christos P, Bockman RS, Rodman JS – Potassium citrate decreases bone resorption in postmenopausal wone with osteopenia: a randomized, double-blind clinical trial. – https://www.ncbi.nlm.nih.gov/pubmed/26401577
[10] Dawson-Hughes B, Harris SS, Ceglia L – Alkaline diets favor lean tissue mass in older adults. – https://www.ncbi.nlm.nih.gov/pubmed/18326605
[11] Curhan GC, Willett WC, Rimm EB, Stampfer MJ – A prospective study of dietary calcium and other nutrients and the risk of symptomatic kidney stones. – https://www.ncbi.nlm.nih.gov/pubmed/8441427/
[12] Tobian L. – High-potassium diets markedly protect against stroke deaths and kidney disease in hypertensive rats, an echo from prehistoric days. – https://www.ncbi.nlm.nih.gov/pubmed/3464706/
[13] Liu DT, Wang MX, Kincaid-Smith P, Whitworth JA. – The effects of dietary potassium on vascular and glomerular lesions in hypertensive rats. – https://www.ncbi.nlm.nih.gov/pubmed/7920452
[14] Pere AK, Lindgren Leena, Tuomainen P., Krogerus L., Rauhala P., Laakso J., Karppanen H., Vaúaatalo H., Mervaala MA. – Dietary potassium and magnesium supplementation in cyclosporine-induced hypertension and nephrotoxicity. – https://www.sciencedirect.com/science/article/pii/S0085253815473624
[15] Brain Miller – 15 foods that are high in potassium – https://nuteksalt.com/blog/15-foods-that-are-high-in-potassium
[16] Gillman MW, Cupples LA, Gagnon D, Posner BM, Ellison RC, Castelli WP, Wolf PA – Protective effect of fruits and vegetables on development of stroke in men. – https://www.ncbi.nlm.nih.gov/pubmed/7707599/
[17] Khaw KT, Barrett-Connor E – Dietary potassium and stroke-associated mortality. A 12-year prospective population study. – https://www.ncbi.nlm.nih.gov/pubmed/3796701/
[18] Šubrtová M, Kašpárková D – Nutritional aspects of potassium – https://is.muni.cz/th/b77fu/Bakalarska_prace-_oprava.pdf
[19] Xia Wang, Yingying Ouyang, Jun Liu, Minmin Zhu, Gang Zhao, Wei Bao, Frank B Hu – Fruit and vegetable consumption and mortality from all causes, cardiovascular disease, and cancer: systematic review and dose-response meta-analysis of prospective cohort studies. – https://www.bmj.com/content/349/bmj.g4490
[20] Shin D, Joh HK, Kim KH, Park SM – Benefits of potassium intake on metabolic syndrome: The fourth Korean National Health and Nutrition Examination Survey. – https://www.ncbi.nlm.nih.gov/pubmed/23958257
[21] John W. Rowe, Jordan D. Tobin, Robert M. Rosa, Reubin Andres – Effect of experimental potassium deficiency on glucose and insulin metabolism. – http://www.metabolismjournal.com/article/0026-0495(80)90074-8/abstract
[22] Uffe Sagild, Vagn Andersen, Per Buch Andreasen – Glucose Tolerance and insulin responsiveness in experimental potassium depletion. – https://onlinelibrary.wiley.com/doi/abs/10.1111/j.0954-6820.1961.tb07829.x
[23] Lanfranco D´Elia MD, Giavincenzo Barba MD, Francesco P. Cappuccio, Pasquale Strazzullo – Potassium intake, stroke, and cardiovascular disease: A meta-analysis of prospective studies. – https://www.sciencedirect.com/science/article/pii/S0735109710049764
[24] National Institutes of Health – Potassium – Fact sheet for health proffesionals – https://ods.od.nih.gov/factsheets/Potassium-HealthProfessional/
[25] Etická fitness aliance – Draslík a proč je pro tělo duležitý a co hrozí při jeho nedostatku https://www.efia.cz/2017/07/21/draslik-proc-telo-dulezity-hrozi-pri-nedostatku/
[26] Boris Dudík – Prečo klesá draslík v tele? Ako ho nájsť v potravinách? https://www.slovenskypacient.sk/draslik-v-tele-potravinach-tabletkach-nadbytok-draslika-ucinky/
[27] What is potassium & how does it benefit for athletes? https://us.myprotein.com/thezone/nutrition/potassium-benefit-athletes/
[28] Three key benefits of eating bananas – https://www.stack.com/a/three-key-benefits-from-eating-bananas
[29] Holmes N., Bates G., Zhao Y., Sherriff J., Miller V. – The effect of exercise intensity on sweat rate and sweat odium and potassium losses in trained endurance athletes – https://espace.curtin.edu.au/handle/20.500.11937/30752
[30] Four ways potassium matters to your sporrt performance – http://saltstick.com/2015/07/27/four-ways-potassium-matters-to-your-sports-performance/
[31] This is why potassium is so important to exercise performance – http://saltstick.com/2017/05/24/potassium-important-exercise-performance/
Элетролиты (натрий, калий, хлор, кальций)
Натрий, калий и хлор являются основными электролитами организма.
Электролиты – это минеральные соединения, которые способны проводить электрический заряд. Находясь в тканях и крови в виде растворов солей, они помогают перемещению питательных веществ в клетки и выводу продуктов обмена веществ из клеток, поддерживают в них водный баланс и необходимый уровень кислотности.
Метод исследования
Ионселективные электроды.
Единицы измерения
Ммоль/л (миллимоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Не принимать пищу в течение 12 часов перед анализом.
- Не курить в течение 30 минут до сдачи крови.
Общая информация об исследовании
Электролиты — это минеральные соединения, обладающие электрическим зарядом. Они находятся в тканях организма и в крови в виде растворов солей. Электролиты способствуют продвижению в клетки организма питательных веществ и выводу из них продуктов обмена, поддержанию водного баланса клеток и стабилизации кислотности (рН).
Основные электролиты в организме человека: натрий (Na+), калий (K+) и хлор (Cl-).
Большая часть натрия содержится в межклеточных жидкостях. Калий находится главным образом внутри клеток, однако небольшое, но жизненно важное его количество есть в плазме, жидкой части крови.
Контроль за уровнем калия очень важен. Даже его незначительные изменения могут повлиять на сердечный ритм и на способность сердца к сокращениям. Хлориды мигрируют через мембрану то внутрь, то наружу клетки и тем самым поддерживают ее электронейтральность. Уровень хлоридов обычно соответствует уровню натрия.
Натрий, калий и хлориды поступают в организм вместе с едой, тогда как почки участвуют в выводе их из организма. Баланс этих химических элементов является важным показателем здоровья человека, в частности того, как функционируют почки и сердце.
Совместное измерение уровней натрия, калия и хлоридов позволяет определить анионовое «окно» – разницу в содержании анионов и катионов в крови. Его аномальная величина не является специфичным показателем, однако предполагает присутствие в организме токсических веществ или вероятность метаболических отклонений, вызванных голоданием или сахарным диабетом.
Ионизированный кальций — катион, свободно циркулирующий в крови и составляющий 46-50 % от всего кальция крови. Его уровень возрастает при понижении pH крови и снижается при защелачивании. На каждые 0,1 единицы понижения pH ионизированный кальций отвечает повышением на 1,5-2,5 %.
Поскольку электролитный и кислотно-щелочной дисбалансы сопутствуют широкому спектру острых и хронических заболеваний, анализ на электролиты может быть назначен как уже госпитализированным пациентам, так и только что обратившимся в отделения экстренной медицинской помощи.
Для чего используется исследование?
- Для скрининга электролитов и исследования кислотно-щелочного дисбаланса.
- Для контроля за эффективностью лечения дисбаланса, влияющего на функционирование определенных органов.
- Показателя общего кальция крови часто хватает для предварительной оценки кальциевого обмена. Обычно он отражает количество свободного кальция, находящегося в крови, так как часто баланс между связанным и свободным кальцием – величина стабильная и достаточно предсказуемая. Однако у некоторых людей это соотношение нарушено, так что уровень общего кальция не является критерием для оценки всего кальциевого обмена. В таких случаях проверка ионизированного кальция становится необходимой.
Что означают результаты?
Референсные значения
| Электролит | Референсные значения |
|---|---|
| Калий | 3,5 — 5,1 ммоль/л |
| Натрий | 136 — 146 ммоль/л |
| Хлор | 98 — 106 ммоль/л |
| Кальций | 1,16 — 1,32 ммоль/л |
Уровни калия, натрия и хлора зависят от их потребления с пищей, от содержания воды в организме и количества электролитов, выводимого почками. Кроме того, на него влияют натрийуретические белки, способствующие выведению натрия почками, а также гормон альдостерон, который поддерживает на постоянном уровне концентрацию натрия и увеличивает потерю организмом калия.
Среди всех электролитов наиболее важными показателями для человека являются уровни калия и натрия. При нарушении функционирования почек организм иногда может удерживать избыточное количество жидкости для разбавления натрия и хлоридов таким образом, что их концентрация падает ниже нормы.
При сильной потере жидкости концентрация калия, натрия и хлоридов может резко возрастать. Некоторые формы сердечных заболеваний, проблемы с мышцами, нервной системой и сахарный диабет также приводят к отклонениям от нормы уровня одного или нескольких электролитов.
Для определения причины электролитного нарушения и назначения правильного лечения важно выяснить, баланс какого именно электролита нарушен. Если такие отклонения не лечить, пациенту грозят головокружения, судороги, нерегулярное сердцебиение и даже смерть.
Причины повышения уровня ионизированного кальция:
Вопрос: Валентина | 28 Июля, 2021
Здравствуйте могу ли я сдать анализ Концентрацию токролимуса в крови у вас?
Здравствуйте. Данное исследование мы не делаем
Вопрос: Наталья | 13 Июля, 2021
Возможен ли забор крови на анализы на дому
Здравствуйте. Нет, на дом на период пандемии не выезжаем
Регулирование гомеостаза калия | Американское общество нефрологов
Abstract
Калий — самый распространенный катион во внутриклеточной жидкости, и поддержание правильного распределения калия через клеточную мембрану имеет решающее значение для нормального функционирования клеток. Долгосрочное поддержание гомеостаза калия достигается за счет изменения почечной экскреции калия в ответ на изменение потребления. Понимание механизма и регулирующих влияний, управляющих внутренним распределением и почечным клиренсом калия при нормальных обстоятельствах, может обеспечить основу для подхода к расстройствам калия, обычно встречающимся в клинической практике.В этой статье рассматриваются ключевые аспекты нормальной регуляции метаболизма калия, и она предназначена для использования в качестве легко доступного обзора для хорошо информированного клинициста, а также в качестве ресурса для обучения стажеров и студентов-медиков.
Введение
Калий играет ключевую роль в поддержании функции клеток. Почти все клетки обладают Na + -K + -ATPase, которая перекачивает Na + из клетки и K + в клетку и приводит к градиенту K + через клеточную мембрану (K + in > K + out ), который частично отвечает за поддержание разности потенциалов на мембране.Эта разность потенциалов имеет решающее значение для функции клеток, особенно в возбудимых тканях, таких как нервы и мышцы. В организме выработаны многочисленные механизмы защиты сыворотки K + . Эти механизмы служат для поддержания надлежащего распределения K + в организме, а также для регулирования общего содержания K + в организме.
Внутренний баланс K
+
Почка в первую очередь отвечает за поддержание общего содержания K + в организме путем согласования потребления K + с выделением K + .Регулировка почечной экскреции K + происходит в течение нескольких часов; следовательно, изменения во внеклеточной концентрации K + первоначально буферизируются движением K + в скелетную мышцу или из нее. Регулирование распределения K + между внутриклеточным и внеклеточным пространством называется внутренним балансом K + . Наиболее важными факторами, регулирующими это движение в нормальных условиях, являются инсулин и катехоламины (1).
После еды постпрандиальное высвобождение инсулина не только регулирует концентрацию глюкозы в сыворотке, но и перемещает диетические K + в клетки до тех пор, пока почки не выведут нагрузку K + , восстанавливая гомеостаз K + .Эти эффекты опосредованы связыванием инсулина с рецепторами клеточной поверхности, что стимулирует захват глюкозы в тканях, чувствительных к инсулину, за счет встраивания белка-переносчика глюкозы GLUT4 (2,3). Увеличение активности Na + -K + -ATPase опосредует захват K + (рис. 1). У пациентов с метаболическим синдромом или ХБП поглощение глюкозы, опосредованное инсулином, нарушено, но клеточное поглощение K + остается нормальным (4,5), демонстрируя дифференциальное регулирование опосредованного инсулином поглощения глюкозы и поглощения K + .
Рисунок 1.
Клеточная модель иллюстрирует β 2 -адренергические и инсулино-опосредованные регуляторные пути для K + поглощения . β 2 -Адренергический агент и инсулин приводят к захвату K + , стимулируя активность насоса Na + -K + -АТФазы в основном в скелетных мышцах, но они делают это через разные сигнальные пути. β 2 -Адренергическая стимуляция приводит к увеличению активности насоса через путь, зависимый от цАМФ и протеинкиназы A (PKA).Связывание инсулина с его рецептором приводит к фосфорилированию субстратного белка рецептора инсулина (IRS-1), который, в свою очередь, связывается с фосфатидилинозитид-3-киназой (PI3-K). Взаимодействие IRS-1 – PI3-K приводит к активации 3-фосфоинозитид-зависимой протеинкиназы-1 (PDK1). Стимулирующий эффект инсулина на поглощение глюкозы и поглощение K + в этой точке расходятся. Akt-зависимый путь отвечает за встраивание в мембрану транспортера глюкозы GLUT4, тогда как активация атипичной протеинкиназы C (aPKC) приводит к встраиванию в мембрану насоса Na + -K + -ATPase (см.3).
Катехоламины регулируют внутреннее распределение K + с нарушением α -адренергических рецепторов и β -адренергических рецепторов, способствующих проникновению в клетки K + . β 2 -индуцированная рецептором стимуляция захвата K + опосредуется активацией насоса Na + -K + -ATPase. Эти эффекты играют роль в регулировании клеточного высвобождения K + во время упражнений (6).
В нормальных условиях упражнения связаны с перемещением внутриклеточного K + в интерстициальное пространство скелетных мышц.Увеличение интерстициального K + может достигать 10–12 мМ при тяжелых физических нагрузках. Накопление K + является фактором, ограничивающим возбудимость и сократительную силу мышц, что приводит к развитию утомления (7,8). Кроме того, увеличение интерстициального K + играет роль в быстром расширении сосудов, что позволяет увеличить кровоток в тренирующих мышцах (9). Во время упражнений высвобождение катехоламинов посредством стимуляции β 2 ограничивает рост внеклеточной концентрации K + , который в противном случае происходит в результате нормального высвобождения K + сокращающимися мышцами.Хотя механизм, вероятно, будет многофакторным, истощение всего тела K + может притупить накопление K + в интерстициальном пространстве, ограничивая приток крови к скелетным мышцам и объясняя связь гипокалиемии с рабдомиолизом.
Изменения тонуса плазмы и кислотно-щелочные нарушения также влияют на внутренний баланс K + . Гипергликемия приводит к перемещению воды из внутриклеточного во внеклеточное пространство. Это движение воды способствует истечению K + из ячейки в процессе увлечения растворителем.Кроме того, сжатие клеток вызывает увеличение внутриклеточной концентрации K + , создавая более благоприятный градиент концентрации для оттока K + . Минеральный ацидоз, но не органический ацидоз, может быть причиной сдвига клеток в K + . Как недавно было рассмотрено, общий эффект ацидемии, вызывающий потерю K + из клеток, происходит не из-за прямого обмена K + -H + , а, скорее, из-за очевидной связи, возникающей в результате эффектов ацидоза. на транспортерах, которые обычно регулируют pH клеток в скелетных мышцах (10) (рис. 2).
Рисунок 2.
Влияние метаболического ацидоза на внутренний баланс K + в скелетных мышцах . (A) При метаболическом ацидозе, вызванном неорганическими анионами (минеральный ацидоз), снижение внеклеточного pH снижает скорость обмена Na + -H + (NHE1) и подавляет скорость поступления Na + -3HCO 3 котранспорт (NBCe1 и NBCe2). Результирующее падение внутриклеточного Na + снизит активность Na + -K + -ATPase, вызывая чистую потерю клеточного K + .Кроме того, падение внеклеточной концентрации HCO 3 увеличит поступательное движение Cl — за счет обмена Cl-HCO —, дополнительно увеличивая отток K + за счет котранспорта K + -Cl —. (B) Потеря K + из клетки намного меньше по величине при метаболическом ацидозе, вызванном органическим ацидозом. В этом случае существует сильный поток внутрь органического аниона и H + через переносчик монокарбоксилата (MCT; MCT1 и MCT4).Накопление кислоты приводит к большему падению внутриклеточного pH, тем самым стимулируя движение внутрь Na + посредством обмена Na + -H + и котранспорта Na + -3HCO 3 . Накопление внутриклеточного Na + поддерживает активность Na + -K + -ATPase, тем самым сводя к минимуму любые изменения во внеклеточной концентрации K + .
Внутриклеточный K + служит резервуаром для ограничения падения внеклеточных концентраций K + , возникающих при патологических условиях, когда происходит потеря K + из организма.Эффективность этого эффекта показали призывники, проходящие летнюю подготовку (11). Эти субъекты были в состоянии поддерживать близкую к норме концентрацию K + в сыворотке, несмотря на ежедневные потери пота K + > 40 ммоль и 11-дневный кумулятивный дефицит K + всего тела на уровне примерно 400 ммоль.
Исследования на крысах с использованием метода зажима K + позволили понять роль скелетных мышц в регулировании внеклеточной концентрации K + (12).При использовании этого метода инсулин вводится с постоянной скоростью, и одновременно вводится K + со скоростью, предназначенной для предотвращения любого падения концентрации K + в плазме. Предполагается, что вводимое количество K + равно количеству K + , попадающему во внутриклеточное пространство скелетных мышц.
У крыс, лишенных K + в течение 10 дней, концентрация K + в плазме снизилась с 4,2 до 2,9 ммоль / л. Инсулино-опосредованное исчезновение K + снизилось более чем на 90% по сравнению с контрольными значениями.Это снижение поглощения K + сопровождалось снижением активности и экспрессии мышечной Na + -K + -АТФазы более чем на 50%, что позволяет предположить, что снижение активности помпы может быть причиной снижения эффекта инсулина. Это снижение поглощения мышцами K + в условиях истощения K + может ограничивать чрезмерное падение внеклеточной концентрации K + , которое происходит в условиях стимуляции инсулином. Одновременно снижение экспрессии и активности помпы способствует способности скелетных мышц буферизовать снижение внеклеточных концентраций K + , отдавая некоторые компоненты своих внутриклеточных запасов.
Есть различия между скелетной и сердечной мышцами в реакции на хроническое истощение K + . Хотя скелетная мышца легко отдает K + , чтобы минимизировать падение концентрации K + в плазме, содержание K + в сердечной ткани остается относительно хорошо сохраненным. В отличие от снижения активности и экспрессии Na + -K + -АТФазы в скелетных мышцах, размер пула сердечной Na + -K + -АТФазы увеличивается у животных с дефицитом K + .Это различие объясняет более высокую общую способность к клиренсу K + после острого введения внутривенного KCl крысам, получавшим диету без K + в течение 2 недель, по сравнению с контрольными группами с полным K + (13, 14). Сердечная мышца накапливает значительное количество K + при острой нагрузке. При выражении на основе веса сердечная емкость для поглощения K + сравнима с емкостью скелетных мышц в условиях истощения K + и может фактически превышать емкость скелетных мышц в контрольных условиях.
Почечная обработка калия
Калий свободно фильтруется клубочками. Основная часть отфильтрованного K + реабсорбируется в проксимальном канальце и петле Генле, так что менее 10% отфильтрованной нагрузки достигает дистального отдела нефрона. В проксимальном канальце абсорбция K + в основном пассивна и пропорциональна Na + и воде (Рисунок 3). Реабсорбция K + в толстой восходящей конечности Генле происходит как по трансклеточным, так и по параклеточным путям.Трансклеточный компонент опосредуется транспортом K + на апикальной мембране Na + -K + -2Cl — котранспортером (рис. 4). Секреция K + начинается в раннем дистальном извитом канальце и постепенно увеличивается вдоль дистального нефрона в кортикальный собирательный проток (Рисунок 5). Большая часть мочевого K + может быть объяснена электрогенной секрецией K + , опосредованной основными клетками в начальном собирательном канале и кортикальном собирательном канале (рис. 6).На апикальной поверхности дистального нефрона также присутствует электронейтральный механизм котранспорта K + и Cl — (15). В условиях обеднения K + происходит реабсорбция K + в собирательном канале. Этот процесс опосредуется активацией апикально расположенной H + -K + -АТФазы на α -интеркалированных клетках (16) (рис. 7).
Рисунок 3.
Клеточная модель для транспорта K + в проксимальном канальце .Реабсорбция K + в проксимальном канальце в основном происходит через параклеточный путь. Активная реабсорбция Na + вызывает реабсорбцию чистой жидкости через проксимальный каналец, что, в свою очередь, вызывает реабсорбцию K + через механизм увлечения растворителем. По мере того, как жидкость течет по проксимальному канальцу, напряжение в просвете смещается от слегка отрицательного до слегка положительного. Сдвиг трансэпителиального напряжения обеспечивает дополнительную движущую силу, способствующую диффузии K + через межклеточный путь с низким сопротивлением.Экспериментальные исследования предполагают, что может быть небольшой компонент трансцеллюлярного транспорта K + ; однако значение этого пути неизвестно. Поглощение K + через насос Na + -K + -ATPase может выходить из базолатеральной мембраны через проводящий путь или соединяться с Cl —. Апикально расположенный канал K + функционирует для стабилизации отрицательного потенциала клетки, особенно в условиях совместного переноса глюкозы и аминокислот с Na + , который имеет деполяризующий эффект на напряжение клетки.
Рис. 4.
Модель ячейки для транспорта K + в толстой восходящей ветви Генле . Реабсорбция K + происходит как с помощью параклеточных, так и трансцеллюлярных механизмов. Базолатеральный насос Na + -K + -ATPase поддерживает низкий уровень внутриклеточного Na + , обеспечивая тем самым благоприятный градиент для управления апикально расположенным котранспортером Na + -K + -2Cl — (пример вторичного активного транспорта).Апикально расположенный почечный наружный медуллярный канал K + (ROMK) обеспечивает путь для K + для рециркуляции из клетки в просвет и обеспечивает адекватное поступление K + для поддержания Na + -K + -2Cl — cotransport. Это движение через ROMK создает положительное напряжение в просвете, обеспечивая движущую силу для пассивной реабсорбции K + через параклеточный путь. Часть K + , попадая в клетку через котранспортер, покидает клетку через базолатеральную мембрану, обеспечивая трансцеллюлярную реабсорбцию K + .K + может выходить из клетки по токопроводящему пути или при котранспорте с Cl — . ClC-Kb является основным путем оттока Cl — через базолатеральную мембрану.
Рис. 5.
Модель клетки для транспорта K + в дистальном извитом канальце (DCT) . На ранней стадии DCT поглощение Na + в просвете опосредуется апикально расположенным тиазид-чувствительным котранспортером Na + -Cl — .Транспортер получает энергию от базолатеральной Na + -K + -АТФазы, которая поддерживает низкую внутриклеточную концентрацию Na + , обеспечивая тем самым благоприятный градиент для входа Na + в клетку посредством вторичного активного транспорта. Котранспортер в изобилии экспрессируется в DCT1, но постепенно снижается в DCT2. ROMK экспрессируется через DCT и в кортикальный собирательный проток. Экспрессия эпителиального канала Na + (ENaC), который обеспечивает чувствительную к амилориду абсорбцию Na + , начинается в DCT2 и интенсивно экспрессируется в нижних соединительных канальцах и кортикальном собирательном канале.DCT2 является началом альдостерон-чувствительного дистального нефрона (ASDN), что определяется наличием как минералокортикоидного рецептора, так и фермента 11 β -гидроксистероиддегидрогеназы II. Этот фермент поддерживает рецептор минералокортикоидов свободным, чтобы связывать альдостерон только путем метаболизма кортизола до кортизона, последний из которых не имеет сродства к рецептору. Электрогенно-опосредованный транспорт K + начинается в DCT2 с комбинированным присутствием ROMK, ENaC и чувствительности к альдостерону.Электронейтральный К + -Cl — котранспорт присутствует в ДКП и коллекторном канале. Условия, вызывающие низкую концентрацию Cl — в просвете, увеличивают секрецию K + по этому механизму, который происходит при доставке плохо реабсорбируемых анионов, таких как сульфат, фосфат или бикарбонат.
Рис. 6.
Клетка, которая отвечает за секрецию K + в начальном собирающем канале и кортикальном собирательном канале, является основной клеткой .Эта клетка обладает базолатеральной Na + -K + -ATPase, которая отвечает за активный транспорт K + из крови в клетку. Результирующая высокая концентрация K + в клетке обеспечивает благоприятный градиент диффузии для перемещения K + из клетки в просвет. Помимо установления высокой внутриклеточной концентрации K + , активность этого насоса снижает внутриклеточную концентрацию Na + , тем самым поддерживая благоприятный градиент диффузии для перемещения Na + из просвета в клетку.Оба движения Na + и K + через апикальную мембрану происходят через четко определенные каналы Na + и K + .
Рисунок 7.
Реабсорбция HCO 3 в дистальном нефроне опосредуется апикальной секрецией H + интеркалированной α клеткой . Два транспортера секретируют H + , вакуолярную H + -АТФазу и H + -K + -АТФазу.H + -K + -ATPase использует энергию, полученную в результате гидролиза АТФ, для секреции H + в просвет и реабсорбции K + электронейтральным образом. Активность H + -K + -ATPase увеличивается при истощении K + и, таким образом, обеспечивает механизм, с помощью которого истощение K + усиливает секрецию как собирательного протока H + , так и секрецию K + . абсорбция.
В большинстве гомеостатических условий доставка K + в дистальный нефрон остается небольшой и довольно постоянной.Напротив, скорость секреции K + дистальным нефроном варьирует и регулируется в соответствии с физиологическими потребностями. Клеточные детерминанты секреции K + в основной клетке включают внутриклеточную концентрацию K + , просветную концентрацию K + , разность потенциалов (напряжений) на просветной мембране и проницаемость просветной мембраны для K + . Условия, которые увеличивают концентрацию клеточного K + , уменьшают концентрацию K + в просвете или делают просвет более электроотрицательным, увеличивают скорость секреции K + .Условия, которые увеличивают проницаемость просветной мембраны для K + , увеличивают скорость секреции K + . Двумя основными детерминантами секреции K + являются минералокортикоидная активность и дистальная доставка Na + и воды.
Альдостерон является основным минералокортикоидом у человека и влияет на несколько клеточных детерминант, описанных выше, что приводит к стимуляции секреции K + . Во-первых, альдостерон увеличивает внутриклеточную концентрацию K + , стимулируя активность Na + -K + -ATPase в базолатеральной мембране.Во-вторых, альдостерон стимулирует реабсорбцию Na + через просветную мембрану, что увеличивает электроотрицательность просвета, тем самым увеличивая электрический градиент, способствующий секреции K + . Наконец, альдостерон оказывает прямое действие на просветную мембрану, увеличивая проницаемость K + (17).
Второй основной детерминант, влияющий на секрецию K + , — это скорость дистальной доставки Na + и воды. Повышенная дистальная доставка Na + стимулирует дистальную абсорбцию Na + , что делает просвет просвета более отрицательным и, таким образом, увеличивает секрецию K + .Повышенная скорость потока также увеличивает секрецию K + . Когда K + секретируется в собирательный канал, концентрация K + в просвете повышается, что снижает градиент диффузии и замедляет дополнительную секрецию K + . При более высоких скоростях потока в просвете такое же количество секреции K + будет разбавлено большим объемом, так что повышение концентрации K + в просвете будет меньше. Таким образом, увеличение дистальной доставки Na + и воды стимулирует секрецию K + , снижая концентрацию K + в просвете и делая потенциал просвета более отрицательным.
Две популяции каналов K + были идентифицированы в клетках кортикального собирательного протока. Почечный наружный медуллярный канал K + (ROMK) считается основным K + -секреторным путем. Этот канал характеризуется низкой проводимостью и высокой вероятностью открытия в физиологических условиях. Канал maxi-K + (также известный как канал с большой проводимостью K + [BK]) характеризуется большой проводимостью одного канала и покоем в базовом состоянии и активацией в условиях повышенного потока (18).В дополнение к увеличенной доставке Na + и разбавлению просвета концентрации K + , привлечение каналов maxi-K + способствует зависящему от потока увеличению секреции K + . Каналы Renal K + являются предметом обширных обзоров (19–21).
Эффект увеличения канальцевого кровотока для активации каналов maxi-K + может быть опосредован изменениями внутриклеточной концентрации Ca 2+ (22). Канал активирован Ca 2+ , и резкое увеличение потока увеличивает внутриклеточные концентрации Ca 2+ в основной клетке.Было высказано предположение, что центральная ресничка (структура, присутствующая в основных клетках) может способствовать трансдукции сигналов повышенного потока в повышенную внутриклеточную концентрацию Ca 2+ . В культивируемых клетках изгиб первичных ресничек приводит к временному увеличению внутриклеточного Ca 2+ , эффект блокируется антителами к полицистину 2 (23). Хотя он присутствует почти во всех сегментах нефрона, канал maxi-K был идентифицирован как медиатор индуцированной потоком секреции K + в дистальном отделе нефрона и кортикальном собирательном канале (24).
Развитие гипокалиемии при синдроме Барттера II типа иллюстрирует важность каналов maxi-K + в почечной экскреции K + (25). Пациенты с синдромом Барттера II типа имеют мутацию потери функции в ROMK, проявляющуюся клиническими особенностями заболевания в перинатальном периоде. ROMK обеспечивает путь рециркуляции K + через апикальную мембрану в толстой восходящей конечности Генле. Эта рециркуляция создает положительный для просвета потенциал, который управляет параклеточной реабсорбцией Ca 2+ и Mg 2+ и обеспечивает просвет K + для котранспортера Na + -K + -2Cl — ( Рисунок 4).
Мутации в ROMK снижают реабсорбцию NaCl и жидкости в толстой конечности, имитируя петлевой диуретический эффект, вызывающий истощение объема. Несмотря на увеличение дистальной доставки Na + , истощение K + не наблюдается постоянно, потому что ROMK также является основным секреторным путем K + для регулируемой экскреции K + в собирательном канале. Фактически, в перинатальном периоде у младенцев с этой формой синдрома Барттера часто наблюдается преходящая гиперкалиемия, связанная с потерей функции ROMK в собирательном канале.Однако со временем у этих пациентов развивается гипокалиемия в результате увеличения секреции K + , опосредованной потоком, через каналы maxi-K + . Исследования на модели синдрома Барттера типа II на мышах с дефицитом ROMK согласуются с этим механизмом (26). Преходящая гиперкалиемия, наблюдаемая в перинатальном периоде, вероятно, связана с тем фактом, что каналы ROMK в ходе развития функционально экспрессируются раньше, чем каналы maxi-K + .
В связи с этим растущие младенцы и дети находятся в состоянии положительного баланса K + , который коррелирует с ростом и увеличением количества клеток.На ранних этапах развития способность дистального нефрона секретировать K + ограничена из-за нехватки как апикально расположенных каналов ROMK, так и maxi-K + каналов. Увеличение секреторной способности K + с созреванием первоначально является результатом повышенной экспрессии ROMK. Несколькими неделями позже развивается экспрессия каналов maxi-K + , позволяющая происходить опосредованной потоком секреции K + (см. Ссылку 27). Ограничение в дистальной секреции K + является канально-специфическим, поскольку электрохимический градиент, благоприятствующий секреции K + , определяемый активностью Na + -K + -ATPase и реабсорбцией Na + , составляет не ограничивая.Кроме того, увеличение скорости потока сопровождается соответствующим увеличением реабсорбции Na + и внутриклеточной концентрации Ca 2+ в дистальном отделе нефрона, несмотря на отсутствие стимулирующего эффекта на секрецию K + (28). Активность H + — K + -АТФазы, которая связывает реабсорбцию K + с секрецией H + в интеркалированных клетках, одинакова у новорожденных и взрослых. Реабсорбция K + через этот насос в сочетании со сниженной экспрессией секреторных каналов K + помогает поддерживать состояние положительного баланса K + во время соматического роста после рождения.Эти особенности дистального воздействия K + развивающейся почкой являются вероятным объяснением высокой частоты неолигурической гиперкалиемии у недоношенных детей (29).
Другим физиологическим состоянием, характеризующимся периодом положительного баланса K + , является беременность, при которой сохраняется примерно 300 мэкв K + (30). Высокий циркулирующий уровень прогестерона может играть роль в этой адаптации за счет стимулирующего воздействия на транспорт K + и H + с помощью H + -K + α 2 изоформы -АТФазы в дистальных отделах нефрона. (31).
В дополнение к стимуляции каналов maxi-K + было показано, что усиленный канальцевый ток стимулирует абсорбцию Na + через эпителиальный канал Na + (ENaC) в собирательном канале. Это увеличение абсорбции происходит не только из-за увеличения доставки Na + , но также, по-видимому, является результатом механочувствительных свойств, присущих каналу. Повышенный поток создает напряжение сдвига, которое активирует ENaC, увеличивая вероятность открытия канала (32,33).
Была выдвинута гипотеза, что биомеханическая регуляция почечного канальцевого транспорта Na + и K + в дистальном нефроне могла развиваться как ответ на защиту от внезапного увеличения внеклеточной концентрации K + , которое происходит в ответ на прием внутрь. К + -богатых рационов, типичных для ранних позвоночных (22). Согласно этой гипотезе, увеличение СКФ после приема пищи, богатой белком, приведет к увеличению дистального кровотока, активируя ENaC, увеличивая внутриклеточную концентрацию Ca 2+ и активируя каналы maxi-K + .Эти события будут усиливать секрецию K + , тем самым обеспечивая буфер для защиты от развития гиперкалиемии.
У пациентов с ХБП потеря массы нефронов уравновешивается адаптивным увеличением секреторной скорости K + в оставшихся нефронах, так что гомеостаз K + обычно хорошо сохраняется до тех пор, пока СКФ не упадет ниже 15-20 мл / мл. мин (34). Считается, что природа адаптивного процесса аналогична адаптивному процессу, который происходит в ответ на высокое потребление K + с пищей у нормальных субъектов (35).Хроническая нагрузка K + у животных увеличивает секреторную способность дистального нефрона, и, следовательно, почечная экскреция K + значительно увеличивается для любого заданного уровня K + в плазме. Повышенная секреция K + в этих условиях происходит в связи со структурными изменениями, характеризующимися клеточной гипертрофией, повышенной плотностью митохондрий и пролиферацией базолатеральной мембраны в клетках дистального отдела нефрона и основных клетках собирательного канала.Повышенные сывороточные K + и минералокортикоиды независимо инициируют процесс амплификации, который сопровождается увеличением активности Na + -K + -ATPase.
Aldosterone Paradox
В условиях истощения объема активация ренин-ангиотензиновой системы приводит к увеличению высвобождения альдостерона. Увеличение циркулирующего альдостерона стимулирует удержание в почках Na + , способствуя восстановлению объема внеклеточной жидкости, но происходит без заметного воздействия на почечную секрецию K + .В условиях гиперкалиемии высвобождение альдостерона опосредуется прямым действием K + на клетки клубочковой зоны. Последующее увеличение циркулирующего альдостерона стимулирует почечную секрецию K + , восстанавливая концентрацию сывороточного K + до нормального уровня, но делает это без сопутствующей задержки Na + в почках.
Способность альдостерона сигнализировать почкам о стимулировании удержания соли без секреции K + при истощении объема и стимулировать секрецию K + без удержания соли при гиперкалиемии была названа парадоксом альдостерона (36).Частично эту способность можно объяснить взаимной зависимостью между скоростью потока мочи и дистальной доставкой Na + с уровнями циркулирующего альдостерона. В условиях истощения объема проксимальное поглощение соли и воды увеличивается, что приводит к снижению дистальной доставки Na + и воды. Хотя уровни альдостерона увеличиваются, почечная экскреция K + остается довольно постоянной, поскольку стимулирующий эффект повышенного альдостерона уравновешивается уменьшенной доставкой фильтрата к дистальному нефрону.В условиях увеличенного объема внеклеточной жидкости дистальная доставка фильтрата увеличивается в результате снижения реабсорбции жидкости в проксимальных канальцах. И снова почечная экскреция K + остается относительно постоянной в этих условиях, потому что уровни циркулирующего альдостерона подавлены. Только при патофизиологических условиях повышенный уровень Na + в дистальных отделах и доставка воды сочетаются с повышенным уровнем альдостерона. Почечная атрофия K + будет происходить в этом случае (37) (Рисунок 8).
Рисунок 8.
В нормальных условиях доставка Na + в дистальный нефрон обратно пропорциональна уровню сывороточного альдостерона . По этой причине почечная экскреция K + не зависит от изменений объема внеклеточной жидкости. Гипокалиемия, вызванная почечным истощением K + , может быть объяснена патофизиологическими изменениями, которые приводят к сочетанию повышенной дистальной доставки Na + и эффектов альдостерона или альдостерона.При приближении к гипокалиемии, вызванной почечным истощением K + , необходимо определить, является ли первичное нарушение повышением активности минералокортикоидов или увеличением дистальной доставки Na + . EABV — эффективный объем артериальной крови.
Почечная секреция K + также остается стабильной при изменениях скорости потока в результате изменений циркулирующего вазопрессина. В связи с этим вазопрессин оказывает стимулирующее действие на почечную секрецию K + (38,39).Это калиуретическое свойство может служить противодействием тенденции к удержанию K + в условиях антидиуреза, когда в противном случае могло бы произойти падение в дистальных канальцах секреции K + , зависящее от низкой скорости потока. Напротив, подавление эндогенного вазопрессина приводит к снижению активности дистального K + -секреторного механизма, тем самым ограничивая чрезмерные потери калия в условиях полной гидратации и водного диуреза.
Хотя обратная зависимость между уровнями альдостерона и дистальной доставкой соли и воды служит для сохранения почечной экскреции K + независимо от состояния объема, недавние обзоры предложили более сложный механизм, основанный на отсутствии лизина [K] 4 (WNK4 ) протеинкиназа в дистальном отделе нефрона (40,41).WNK4 является одним из четырех членов семейства серин-треониновых киназ, каждая из которых кодируется другим геном и характеризуется атипичным размещением каталитического остатка лизина, который присутствует в большинстве других протеинкиназ. Инактивирующие мутации в WNK4 приводят к развитию псевдогипоальдостеронизма II типа (PHAII; синдром Гордона). Это заболевание наследуется по аутосомно-доминантному типу и характеризуется гипертонией и гиперкалиемией (42). Уровень циркулирующего альдостерона низкий, несмотря на наличие гиперкалиемии.Тиазидные диуретики особенно эффективны при лечении гипертонии и гиперкалиемии (43).
WNK4 дикого типа снижает поверхностную экспрессию тиазид-чувствительного котранспортера Na + -Cl — , а также стимулирует клатрин-зависимый эндоцитоз ROMK в собирательном канале (44,45). Инактивирующая мутация WNK4, ответственного за PHAII, приводит к увеличению активности котранспортера и дополнительно стимулирует эндоцитоз ROMK. Чистый эффект заключается в увеличении реабсорбции NaCl в сочетании с уменьшением секреции K + .Мутировавший WNK4 также увеличивает проницаемость для параклеточного Cl —, вызванную повышенным фосфорилированием клаудинов, белков плотных контактов, участвующих в регуляции транспорта параклеточных ионов (46). Помимо увеличения удерживания Na + , это изменение проницаемости дополнительно ухудшает секрецию K + , потому что отрицательное напряжение в просвете, которое обычно служит движущей силой для секреции K + , рассеивается.
Поскольку развитие артериальной гипертензии и гиперкалиемии в результате PHAII-мутированного белка WNK4 можно рассматривать как преувеличенную реакцию на уменьшение объема внеклеточной жидкости (удержание соли без увеличения секреции K + ), было предложено, что дикого типа WNK4 может действовать как молекулярный переключатель, определяющий баланс между почечной реабсорбцией NaCl и секрецией K + (45,47).В условиях истощения объема переключение будет изменено способом, напоминающим мутант PHAII, так что реабсорбция NaCl увеличивается, но секреция K + дополнительно ингибируется. Однако, когда повышенная концентрация K + в сыворотке происходит в отсутствие истощения объема, изменения WNK4 приводят к максимальной почечной секреции K + без удержания Na + .
Ангиотензин II (AII) стал важным модулятором этого переключателя.В условиях истощения объема повышаются уровни AII и альдостерона (рис. 9). Помимо эффектов, ведущих к усилению реабсорбции NaCl в проксимальном канальце, AII активирует котранспортер Na + -Cl — зависимым от WNK4 образом, и он в основном располагается в начальной части дистального извитого канальца (DCT). ; DCT1) (48,49). AII также активирует ENaC, который находится в чувствительном к альдостерону дистальном нефроне (ASDN), состоящем из второго сегмента DCT (DCT2), соединительного канальца и собирательного канала (50).Активация ENaC с помощью AII дополняет активацию альдостерона (51). Таким образом, AII и альдостерон действуют согласованно, чтобы стимулировать удержание Na + . В то же время AII ингибирует ROMK с помощью как WNK4-зависимых, так и независимых механизмов (52,53). Этот ингибирующий эффект на ROMK наряду со снижением доставки Na + в собирательный проток, вызванный стимуляцией AII реабсорбции Na + в проксимальном нефроне, и DCT1 позволяет одновременно сохранять Na + без потери K + .
Рисунок 9.
Парадокс альдостерона относится к способности почки стимулировать удержание NaCl с минимальной секрецией K + в условиях истощения объема и максимальной секрецией K + секреции без Na + удержание при гиперкалиемии . При истощении объема (левая панель) повышенные уровни циркулирующего ангиотензина II (AII) стимулируют котранспортер Na + -Cl — на ранней стадии DCT.В ASDN AII вместе с альдостероном стимулируют ENaC. В этом последнем сегменте AII оказывает ингибирующее действие на ROMK, тем самым обеспечивая механизм максимального сохранения соли и минимизации почечной секреции K + . Когда гиперкалиемия или повышенное потребление K + с пищей происходит с нормоволемией (правая панель), низкие уровни циркулирующего AII или прямые эффекты K + приводят к ингибированию активности котранспорта Na + -Cl — наряду с повышенной активностью РОМК.В результате доставка Na + в ENaC оптимизирована для связанной электрогенной секреции K + через ROMK. Как обсуждается в тексте, в отсутствие лизина [K] 4 (WNK4) белки интегрально участвуют в сигналах, вызывающих парадокс. Следует подчеркнуть, что белки WNK являются частью сложной сигнальной сети, которая еще полностью не выяснена. Заинтересованный читатель может ознакомиться с несколькими недавними обзорами и достижениями по этой теме (48,51,91–93).
Гиперкалиемия, или увеличение потребления K + с пищей, может увеличить почечную секрецию K + независимо от изменения активности минералокортикоидов и без сохранения объема.Этот эффект был показан на крысах Wistar, получавших диету с очень низким содержанием NaCl и K + в течение нескольких дней и получавшую фармакологическую дозу дезоксикортикостерона для обеспечения постоянного и неизменного эффекта минералокортикоидов (54,55). После введения KCl в брюшную полость были отмечены две отдельные фазы. В первые 2 часа наблюдалось значительное увеличение скорости почечной экскреции K + , что в значительной степени было вызвано увеличением концентрации K + в кортикальном собирательном канале.Во время этой ранней фазы поток через собирающий канал увеличился лишь незначительно, что позволяет предположить, что изменения в концентрации K + в значительной степени были вызваны увеличением секреторной способности K + собирательного канала. Этот эффект согласуется с известными эффектами диетической добавки K + на увеличение плотности каналов как ROMK, так и maxi-K + (56).
В последующие 4 часа почечная экскреция K + оставалась высокой, но во время этой второй фазы калиурез в основном объяснялся повышенным потоком через собирательный проток.Повышенный кровоток был приписан ингибирующему эффекту увеличения интерстициальной концентрации K + на реабсорбцию NaCl в восходящей восходящей конечности Генле, эффект, подтвержденный исследованиями микроперфузии в прошлом (57,58). По-видимому, важна синхронизация двух фаз, потому что более высокие потоки будут наиболее эффективными в продвижении калиуреза только после установления повышенной плотности каналов. Хотя более ранние исследования согласуются с уменьшением всасывания Na + в толстой конечности и проксимальном нефроне после увеличения потребления K + , ингибирующим эффектам в этих высокопроизводительных сегментах не хватает точности и времени, необходимых для обеспечения доставки ниже по потоку Na +. подходит для максимальной стимуляции секреции K + и в то же время не является чрезмерным, предрасполагающим к истощению объема, особенно в условиях диеты с низким содержанием Na + (57–59).
Низкая пропускная способность DCT и его расположение непосредственно выше по потоку от ASDN делают этот сегмент более вероятным местом для изменений в диетическом потреблении K + для модуляции транспорта Na + и обеспечения доставки Na + в нисходящем направлении. — это именно то количество, которое необходимо для поддержания гомеостаза K + , не вызывая нежелательных эффектов на объем. В связи с этим повышенное потребление K + с пищей приводит к ингибирующему эффекту на транспорт Na + в этом сегменте, и это происходит за счет воздействия на WNK1, другого члена семейства киназ WNK (60,61).WNK1 повсеместно экспрессируется по всему телу в множественных сплайсированных формах. Напротив, более короткий транскрипт WNK1, лишенный аминоконцевых 1–437 аминокислот длинного транскрипта, высоко экспрессируется в почках, но не в других тканях, и его называют почко-специфическим WNK1 (KS-WNK1). KS-WNK1 ограничен DCT и частью соединительного протока и функционирует как физиологический антагонист действия длинного WNK1. Изменения соотношения KS-WNK1 и длинного WNK1 в ответ на диетический K + вносят вклад в физиологическую регуляцию почечной экскреции K + (62–65).
В нормальных условиях длинный WNK1 предотвращает способность WNK4 ингибировать активность котранспортера Na + -Cl — в DCT. Таким образом, повышенная активность длинного WNK1 приводит к чистому увеличению реабсорбции NaCl. Диетическая загрузка K + увеличивает количество KS-WNK1. Повышенный KS-WNK1 противодействует ингибирующему эффекту длинного WNK1 на WNK4. Чистый эффект заключается в ингибировании котранспорта Na + -Cl — в DCT и увеличении доставки Na + в более дистальные части канальца.Кроме того, увеличенный KS-WNK1 противодействует эффекту длинного WNK1 для стимуляции эндоцитоза ROMK. Кроме того, KS-WNK1 оказывает стимулирующее действие на ENaC. Таким образом, увеличение KS-WNK1 в ответ на диетическую загрузку K + способствует секреции K + за счет комбинированных эффектов увеличения доставки Na + за счет подавления котранспорта Na + -Cl — в DCT, повышенная электрогенная реабсорбция Na + через ENaC и большее количество ROMK.
Повышенные уровни альдостерона в ответ на диету с высоким содержанием K + приводят к эффектам, которые дополняют эффекты KS-WNK1 (66,67). Сывороточная и глюкокортикоид-зависимая протеинкиназа (SGK1) является непосредственной транскрипционной мишенью связывания альдостерона с рецептором минералокортикоидов. Активация SGK1 приводит к фосфорилированию WNK4, что приводит к потере способности WNK4 ингибировать ROMK и ENaC (66,68). Активация SGK1, индуцированная альдостероном, также приводит к увеличению экспрессии и активности ENaC, вызывая фосфорилирование убиквитин протеинлигазы Nedd4–2.Фосфорилированный Nedd4–2 приводит к меньшему извлечению ENaC из апикальной мембраны (69). Следует подчеркнуть, что отсутствие AII является критическим фактором в способности высокого потребления K + вызывать изменения, необходимые для облегчения секреции K + без чрезмерной реабсорбции Na + .
Роль в гипертонии
Изменения в KS-WNK1 и длинном WNK1, которые происходят в ответ на потребление K + с пищей, влияют на почечную обработку Na + таким образом, что это может иметь значение для наблюдаемой взаимосвязи между диетическими K + потребление и гипертония.Эпидемиологические исследования установили, что потребление K + обратно пропорционально распространенности гипертонии (70). Кроме того, добавка K + и предотвращение гипокалиемии снижает АД у пациентов с гипертонией. Напротив, АД повышается у пациентов с гипертонией, находящихся на диете с низким содержанием K + . Это повышение АД связано с повышенной почечной реабсорбцией Na + (71).
K + дефицит увеличивает отношение длинных WNK1 к KS-WNK1. Длинный WNK1 связан с повышенным извлечением ROMK, таким образом обеспечивая соответствующий ответ для ограничения секреции K + .Однако длинный WNK1 также приводит к стимулирующему эффекту на активность ENaC, а также к высвобождению ингибирующего эффекта WNK4 на реабсорбцию Na + , опосредованную котранспортером NaCl в DCT (72,73). Эти эффекты предполагают, что снижение секреции K + в условиях дефицита K + будет происходить за счет увеличения удерживания Na + .
Почечная консервация K + и Na + в условиях дефицита K + может считаться эволюционной адаптацией, поскольку диетический дефицит K + и Na + , вероятно, имел место вместе у ранних людей (74) .Однако такой эффект потенциально пагубен в наших нынешних условиях, потому что в ходе эволюции наблюдалось значительное увеличение соотношения потребления с пищей Na + по сравнению с K + . Эффекты повышенного отношения WNK1 к KS-WNK1 в почках в условиях современной диеты с высоким содержанием Na + / низким содержанием K + могут быть центральными в патогенезе солочувствительной гипертензии (75).
Энтерический датчик K
+
Имеются данные, подтверждающие существование энтеральных датчиков растворенных веществ, способных реагировать на пищевые Na + , K + и фосфат, которые сигнализируют почкам о быстром изменении экскреции или реабсорбции ионов. (76–78).У экспериментальных животных и с использованием протоколов для поддержания идентичной концентрации K + в плазме калийуретический ответ на нагрузку K + выше при приеме во время еды по сравнению с внутривенным вливанием (79). Эти исследования показывают, что потребление K + с пищей через внутренний механизм восприятия может сигнализировать об увеличении почечной экскреции K + независимо от изменений концентрации K + в плазме или альдостерона (см. Ссылку 80).
Хотя точный механизм передачи сигналов неизвестен, недавние исследования предполагают, что почечный ответ может быть из-за быстрого и почти полного дефосфорилирования котранспортера Na + -Cl — в DCT, вызывая снижение активности транспортера и , таким образом, улучшая доставку Na + в ASDN (81,82).В этих исследованиях доставка в желудок K + приводила к дефосфорилированию котранспортера в течение нескольких минут независимо от альдостерона и на основании исследований in vitro , независимо от изменений во внеклеточной концентрации K + . Связанное во времени увеличение почечной экскреции K + является результатом более благоприятной электрохимической движущей силы, вызванной нисходящим сдвигом реабсорбции Na + от DCT к ENaC в ASDN, а также увеличением канала maxi-K + K + секреция, вызванная усилением кровотока.Этот быстрый натрийуретический ответ на увеличение потребления K + с пищей согласуется с эффектом снижения АД рационов с высоким содержанием K + , обсуждавшимся ранее.
Циркадный ритм K
+ Секреция
В течение 24-часового периода экскреция K + с мочой изменяется в ответ на изменения активности и колебания потребления K + , вызванные интервалом между приемами пищи. Однако даже когда потребление и активность K + равномерно распределены в течение 24-часового периода, сохраняется циркадный ритм, в соответствии с которым экскреция K + ниже ночью и в ранние утренние часы, а затем увеличивается днем (83 –86).Этот циркадный паттерн является результатом изменений внутриканальцевой концентрации K + в собирательном канале, в отличие от изменений скорости потока мочи (87).
В дистальном нефроне мышей циркадный ритм существует для транскриптов генов, которые кодируют белки, участвующие в секреции K + (88). Экспрессия гена ROMK выше в периоды активности, тогда как экспрессия H + -K + -ATPase выше во время покоя, что соответствует периодам, когда почечная экскреция K + больше и меньше, соответственно (89 ).Изменения уровня альдостерона в плазме могут играть определенную роль, поскольку в надпочечниках описан циркадный ритм синтеза и секреции глюкокортикоидов. Кроме того, экспрессия часовых генов в клетках дистального нефрона предполагает, что функция водителя ритма, регулирующая транспорт K + , может быть внутренним компонентом почек, способным работать независимо от внешнего воздействия.
Клиническое значение этой ритмичности в K + и других секрециях электролитов неизвестно.Данные свидетельствуют о том, что нарушение регуляции циркадных ритмов может способствовать отсутствию ночного снижения АД с возможным развитием устойчивой гипертензии, а также ускорением ХБП и сердечно-сосудистых заболеваний (85, 90).
- Авторские права © 2015 Американского общества нефрологов
Метаболизм калия — обзор
2 Гипернатриемия с нормальным общим количеством воды в организме и натрием
55-летний мужчина принимает литий в качестве лекарства от биполярного заболевания в течение нескольких лет.Ему потребовались большие дозы, но он достиг превосходного контроля психических симптомов. Сейчас у него проблемы с частым мочеиспусканием и неутолимой жаждой. По его оценкам, он выпивает от 4 до 6 литров жидкости в день и ходит в туалет каждые 2 или 3 часа. Он обращается в клинику с этими симптомами.
У него нормальное артериальное давление (130/80 мм рт. Ст. Без ортостатических изменений), нормальная частота пульса, периферических отеков нет. Анализы крови показывают следующее: уровень натрия 145 ммоль / л, уровень калия 3.7 ммоль / л, уровень хлорида 111 ммоль / л, уровень бикарбоната 28 ммоль / л, уровень кальция 9,5 мг / дл, уровень глюкозы 90 мг / дл, уровень креатинина 1,5 мг / дл, и уровень АМК 28 мг / дл. Оценка его мочи показывает осмоляльность 250 мОсм / кг и концентрацию натрия 33 ммоль / л.
Физическая оценка пациента показывает, что его объем почти нормальный. Нет свидетельств уменьшения внутрисосудистого объема или увеличения объема ECF. У пациента может наблюдаться небольшое уменьшение объема внутриклеточной жидкости, потому что его сывороточный натрий находится на верхней границе нормы.У него нет нарушений обмена калия или кальция, сахарного диабета. Повышение уровня креатинина в сыворотке и уровня азота мочевины указывает на то, что у него хроническое заболевание почек, возможно, в результате отравления литием. Ключевым элементом является история приема лития, который является известным антагонистом действия АДГ на собирательный проток, а также частое мочеиспускание и жажда, что предполагает дисфункцию системы АДГ. Исследования мочи показывают, что его моча разбавленная, хотя расчетная осмоляльность сыворотки составляет 305 мОсм / кг (уровень натрия 145 × 2 + глюкоза [90/18] + АМК 28/2.8). Эта информация согласуется с отсутствием действия АДГ на почки (т. Е. Несахарного диабета).
Несахарный диабет можно разделить на две категории: центральный и нефрогенный (вставки 3-6 и 3-7). При центральном несахарном диабете снижается продукция АДГ гипофизом. Это может быть результатом повреждения гипофиза в результате травмы, компрессии гипофиза в результате злокачественного образования (первичной или метастатической опухоли) или инсульта. Почечный несахарный диабет возникает либо в результате наследственного дефекта (Х-сцепленный рецессивный) в рецепторе V2 в собирательном канале, либо в результате приобретенной устойчивости к действию АДГ.Приобретенная форма связана с заболеваниями, поражающими клетки канальцев (например, поликистоз почек, пиелонефрит, постобструктивная уропатия), электролитным дисбалансом (например, гипокалиемия, гиперкальциемия) или лекарствами (например, литием). В приобретенных случаях дефект может быть неполным или временным. Признаки и симптомы несахарного диабета (полиурия и полидипсия) могут проявляться периодически. Гипернатриемия часто развивается, когда пациент не может пить достаточно воды, чтобы восполнить потерю почек.
Тест на водную депривацию полезен для оценки дефектов в действии ADH. С помощью этого теста оценивается максимальная способность почки концентрировать мочу с добавлением экзогенного АДГ и без него. Во-первых, пациент воздерживается от приема жидкости на ночь. Утром осмоляльность сыворотки и мочи измеряется каждый час. Когда достигается максимальная осмоляльность мочи (т.е. в образцах мочи не отмечается дальнейшего увеличения осмоляльности или пациент теряет от 3% до 5% веса тела), пациенту вводят подкожную инъекцию 5 единиц водного раствора вазопрессина (АДГ). ).Если почка может реагировать на АДГ, будет наблюдаться дальнейшее повышение осмоляльности мочи, что указывает на центральный несахарный диабет. Отсутствие такого роста свидетельствует о несахарном почечном диабете.
Одна мешающая переменная — это роль градиента растворенного вещества в мозговом веществе почек. В некоторых случаях (например, у пациентов с длительным водным диурезом [психогенной полидипсией] или недостаточностью питания почек) почки не могут генерировать значительную концентрацию растворенных веществ мочевины и хлорида натрия в интерстиции мозгового вещества.Без этих растворенных веществ в мозговом веществе способность почек концентрировать мочу будет снижена. Следовательно, увеличение осмоляльности мочи будет меньше максимального.
Хотя прекращение терапии литием может помочь в восстановлении ответа канальцев на АДГ, для уменьшения объема мочи можно использовать другие стратегии. Реабсорбция натрия и воды в проксимальных канальцах может быть усилена за счет незначительного уменьшения объема при диете с низким содержанием натрия и использовании низких доз тиазидного диуретика.Изменение осмоляльности мочи с 50 до 200 мОсм / кг означает значительное уменьшение объема мочи. Пациентов с центральным несахарным диабетом можно лечить синтетическим АДГ (например, десмопрессином), вводимым путем инъекции или в виде назального спрея.
NORD (Национальная организация редких заболеваний)
УЧЕБНИКИ
Beers MH, Berkow R., eds. Руководство Merck, 17-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1999135-38.
Берков Р., изд. Руководство Merck для дома.Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1997: 653, 670.
Bennett JC, Plum F. Eds. Сесил Учебник медицины. 20-е изд. W.B. Saunders Co., Филадельфия, Пенсильвания; 1996: 539-41.
ОБЗОР СТАТЬИ
Фервенца Ф.К., Рабкин Р. Роль факторов роста и аммиака в генезе гипокалиемической нефропатии. J Ren Nutr. 2002; 12: 151-59.
Gennari FJ. Нарушения гомеостаза калия. Гипокалиемия и гиперкалиемия. Crit Care Clin. 2002; 18: 273-88, vi.
Riggs JE.Неврологические проявления электролитных нарушений. Neurol Clin. 2002; 20: 227-39, vii.
Шаер А.Дж. Унаследованный первичный почечный канальцевый гипокалиемический алкалоз: обзор синдромов Гительмана и Бартерра. Am J Med Sci. 2001; 322: 316-32.
Rastegar A, Soleimani M, Rastergar A. Гипокелемия и гиперкаелемия. Postgrad Med J. 2001; 77: 759-64.
Schepkens H, Lameire N. Синдром Гительмана: недооцененная причина хронической гипокалиемии и гипоимагниемии у взрослых. Acta Clin Belg.2001; 56: 248-54.
Капур М., Чан ГЗ. Нарушения жидкости и электролитов. Crit Care Clin. 2001; 17: 503-29.
ИЗ ИНТЕРНЕТА
Salem MM, Batlle DC. Гиперкалиемия и гипокалиемия. Лучшая практика медицины. Последнее изменение: 2 апреля 2001 г.: 18 стр.
www.merck.praxis.md/bpm/bpm.asp?page=CPM01MP258
Электролитный дисбаланс. Гипокалиемия. Нефрологический канал. nd. 2 стр.
www.nephrologychannel.com/hypokalemia.shtml
Гипокалиемия. Записная книжка по семейной практике.nd. 2 стр.
www.fpnotebook.com/REN107.htm
Ледерер Э., Эрбек К. Гипокалиемия. eMedicine. Последнее обновление: 25 сентября 2002 г. 27pp.
www.emedicine.com/med/topic1124.htm
Верив М., Яимович Д. Гипокалиемия. eMedicine. eMedicine Journal. 2001; 2: 11с.
www.emedicine.com/PED/topic1121.htm
Гарт Д. Гипокалиемия. eMedicine. Последнее обновление: 21 июля 2001 г. 9pp
www.emedicine.com/EMERG/topic273.htm
Калий — питание человека
Калий — это самый распространенный положительно заряженный ион внутри клеток.Девяносто процентов калия содержится во внутриклеточной жидкости, около 10 процентов — во внеклеточной жидкости и только 1 процент — в плазме крови. Как и в случае с натрием, уровень калия в крови строго регулируется. Гормон альдостерон в первую очередь контролирует уровень калия, но другие гормоны (например, инсулин) также играют роль. Когда уровень калия в крови увеличивается, надпочечники выделяют альдостерон. Альдостерон действует на собирательные протоки почек, где стимулирует увеличение количества натриево-калиевых насосов.Затем реабсорбируется натрий и выводится больше калия. Поскольку калий необходим для поддержания уровня натрия и, следовательно, баланса жидкости, каждый день организм теряет около 200 миллиграммов калия.
Другие функции калия в организме
В нервном импульсе участвует не только натрий, но и калий. Нервный импульс движется по нерву за счет движения ионов натрия в клетку. Чтобы прекратить импульс, ионы калия устремляются из нервной клетки, тем самым уменьшая положительный заряд внутри нервной клетки.Это уменьшает стимул. Чтобы восстановить исходную концентрацию ионов между внутриклеточной и внеклеточной жидкостью, натрий-калиевый насос выводит ионы натрия в обмен на ионы калия внутрь. По завершении восстановленных концентраций ионов нервная клетка готова к получению следующего импульса. Точно так же в мышечных клетках калий участвует в восстановлении нормального мембранного потенциала и прекращении мышечного сокращения. Калий также участвует в синтезе белка, энергетическом обмене и функции тромбоцитов, а также действует как буфер в крови, играя роль в кислотно-щелочном балансе.
Дисбаланс калия
Недостаточный уровень калия в организме (гипокалиемия) может быть вызван низким потреблением калия с пищей или высоким потреблением натрия, но чаще всего это является следствием приема лекарств, увеличивающих экскрецию воды, в основном диуретиков. Признаки и симптомы гипокалиемии связаны с функциями калия в нервных клетках и, следовательно, с сокращением скелета и гладких мышц. Признаки и симптомы включают мышечную слабость и судороги, респираторную недостаточность и запор.Сильное истощение калия может вызвать аномальные сокращения сердца и даже привести к летальному исходу. Высокий уровень калия в крови или гиперкалиемия также влияет на сердце. Это тихое состояние, поскольку часто не проявляет никаких признаков или симптомов. Чрезвычайно высокий уровень калия в крови нарушает электрические импульсы, стимулирующие сердце, и может вызвать его остановку. Гиперкалиемия обычно является результатом дисфункции почек.
Потребности и источники калия с пищей
IOM основывает свои AI для калия на уровнях, связанных со снижением артериального давления, снижением чувствительности к соли и минимальным риском образования камней в почках.Для взрослых мужчин и женщин старше девятнадцати лет адекватное потребление калия составляет 4700 граммов в день. AI для других возрастных групп перечислены в Таблице 3.8 «Достаточное потребление калия».
Таблица 3.8 Достаточное потребление калия
| Возрастная группа | мг / день |
| Младенцы (0–6 месяцев) | 400 |
| Младенцы (6–12 месяцев) | 700 |
| Дети (1–3 года) | 3 000 |
| Дети (4–8 лет) | 3,800 |
| Дети (9–13 лет) | 4,500 |
| Подростки (14–18 лет) | 4,700 |
| Взрослые (> 19 лет) | 4,700 |
Нормы потребления с пищей: вода, калий, натрий, хлориды и сульфаты.Институт медицины. http://www.iom.edu/Reports/2004/Dietary-Reference-Intakes-Water-Potassium-Sodium-Chloride-and-Sulfate.aspx. Обновлено 11 февраля 2004 г. Проверено 22 сентября 2017 г.
Источники пищи для калия
Фрукты и овощи, содержащие большое количество калия, включают шпинат, салат, брокколи, горох, помидоры, картофель, бананы, яблоки и абрикосы. Цельное зерно и семена, определенная рыба (например, лосось, треска и камбала) и мясо также богаты калием.Диетические подходы к остановке гипертонии (диета DASH) делает упор на продукты, богатые калием, и будут обсуждаться более подробно в следующем разделе.
Биодоступность
Более 90 процентов пищевого калия всасывается в тонком кишечнике. Несмотря на высокую биодоступность, калий является очень растворимым минералом и легко теряется во время приготовления и обработки пищевых продуктов. Свежие и замороженные продукты являются лучшими источниками калия, чем консервы.
Заболевания калия: гипокалиемия и гиперкалиемия
1.Пэйс Би Джей,
Патерсон КР,
Оньянга-Омара Ф,
Доннелли Т,
Серый JM,
Лоусон Д.Х.
Запись исследования связи гипокалиемии у госпитализированных пациентов. Postgrad Med J .
1986; 62 (725): 187–191 ….
2. Lippi G,
Фавалоро Э.Дж.,
Монтаньяна М,
Guidi GC.
Распространенность гипокалиемии: опыт большой академической больницы. Intern Med J .
2010. 40 (4): 315–316.
3. Лиамис Г.,
Роденбург Е.М.,
Хофман А,
Zietse R,
Stricker BH,
Hoorn EJ.Электролитные нарушения у субъектов сообщества: распространенность и факторы риска. Am J Med .
2013. 126 (3): 256–263.
4. Шемер Дж.,
Модан М,
Эзра Д,
Кабили С.
Заболеваемость гиперкалиемией у госпитализированных пациентов. ISR J Med Sci .
1983; 19 (7): 659–661.
5. Пэйс Б,
Серый JM,
Макбрайд Д,
Доннелли Т,
Лоусон Д.Х.
Гиперкалиемия у пациентов в стационаре. Br Med J (Clin Res Ed) .1983; 286 (6372): 1189–1192.
6. Gennari FJ.
Гипокалиемия. N Engl J Med .
1998. 339 (7): 451–458.
7. Weiner ID,
Wingo CS.
Гипокалиемия — последствия, причины и способы устранения. Дж. Ам Соц Нефрол .
1997. 8 (7): 1179–1188.
8. Gennari FJ.
Нарушения гомеостаза калия. Гипокалиемия и гиперкалиемия. Клиника интенсивной терапии .
2002. 18 (2): 273–288.
9. Рейд А.,
Джонс Джи,
Айлс К.Гипокалиемия: обычные вещи встречаются часто — ретроспективный опрос. JRSM Короткое описание .
2012; 3 (11): 80.
10. Шульман М,
Нариньш Р.Г.
Гипокалиемия и сердечно-сосудистые заболевания. Ам Дж. Кардиол .
1990; 65 (10): 4E – 9E.
11. Гринберг А.
Диуретические осложнения. Am J Med Sci .
2000. 319 (1): 10–24.
12. Дхалла И.А.,
Гомеш Т,
Яо З,
и другие.
Хлорталидон в сравнении с гидрохлоротиазидом для лечения артериальной гипертензии у пожилых людей: популяционное когортное исследование. Энн Интерн Мед. .
2013. 158 (6): 447–455.
13. Morgan DB,
Дэвидсон К.
Гипокалиемия и диуретики: анализ публикаций. Br Med J .
1980. 280 (6218): 905–908.
14. Mount DB, Занди-Неджад К. Нарушения баланса калия. В: Taal MW, Chertow GM, Marsden PA, Brenner BM, Rector FC, ред. Бреннер и Ректор Почка. Филадельфия, Пенсильвания: Эльзевьер / Сондерс; 2012.
15. Macdonald JE,
Struthers AD.
Каков оптимальный уровень калия в сыворотке крови у пациентов с сердечно-сосудистыми заболеваниями? Джам Колл Кардиол .2004. 43 (2): 155–161.
16. Ван Р,
Ван ДД,
Райан MP.
Рефрактерное восполнение калия. Следствие дефицита магния. Arch Intern Med .
1992. 152 (1): 40–45.
17. Миллейн Т.А.,
Ward DE,
Camm AJ.
Является ли гипомагниемия аритмогенной? Клин Кардиол .
1992. 15 (2): 103–108.
18. Камель К.С.,
Этье JH,
Ричардсон Р.М.,
Медведь РА,
Гальперин МЛ.
Электролиты и осмоляльность мочи: когда и как их использовать. Ам Дж. Нефрол .
1990. 10 (2): 89–102.
19. Диркс ДБ,
Шумаик ГМ,
Харриган Р.А.,
Брэди WJ,
Чан ТК.
Электрокардиографические проявления: электролитные нарушения. J Emerg Med .
2004. 27 (2): 153–160.
20. Уивер В.Ф.,
Берчелл HB.
Калий в сыворотке и электрокардиограмма при гипокалиемии. Тираж .
1960; 21: 505–521.
21. Урожай MJ,
Хорн Э.Дж.,
Линдеманс Дж.,
Цитце Р.Гипокалиемия и последующая гиперкалиемия у госпитализированных пациентов. Циферблат нефрола .
2007. 22 (12): 3471–3477.
22. Ким Г.Х.,
Han JS.
Лечебный подход к гипокалиемии. Нефрон .
2002; 92 (приложение 1): 28–32.
23. Ingram TC,
Olsson JM.
Вкратце: гипокалиемия. Педиатр Ред. .
2008; 29 (9): e50 – e51.
24. Эванс К.Дж.,
Гринберг А.
Гиперкалиемия: обзор. J Intensive Care Med .
2005. 20 (5): 272–290.
25. Fordjour KN,
Уолтон Т,
Доран Дж. Дж.
Лечение гиперкалиемии у госпитализированных пациентов. Am J Med Sci .
2014; 347 (2): 93–100.
26. Аронсон П.С.,
Гибиш Г.
Влияние pH на калий: новые объяснения старых наблюдений. Дж. Ам Соц Нефрол .
2011; 22 (11): 1981–1989.
27. Perazella MA.
Гиперкалиемия, вызванная лекарствами: старые виновники и новые преступники. Am J Med .
2000. 109 (4): 307–314.
28. Raebel MA.
Гиперкалиемия, связанная с применением ингибиторов ангиотензинпревращающего фермента и блокаторов рецепторов ангиотензина. Cardiovasc Ther .
2012; 30 (3): e156 – e166.
29. Брутто П,
Пистрош Ф.
Гиперкалиемия: снова. Циферблат нефрола .
2004. 19 (9): 2163–2166.
30. Альфонсо А., Соар Дж., Мактиер Р. и др. Лечение острой гиперкалиемии у взрослых.1 марта 2014 г. http://www.renal.org/guidelines/joint-guidelines/treatment-of-acute-hyperkalaemia-in-adults#sthash.o9MgdJbw.dpbs. По состоянию на 1 сентября 2014 г.
31. Smellie WS.
Ложная гиперкалиемия. BMJ .
2007. 334 (7595): 693–695.
32. Montague BT,
Уэллетт-младший,
Буллер Г.К.
Ретроспективный обзор частоты изменений ЭКГ при гиперкалиемии. Clin J Am Soc Nephrol .
2008. 3 (2): 324–330.
33.Максвелл А.П.,
Линден К,
О’Доннелл С,
Гамильтон П.К.,
Маквей Г.Е.
Лечение гиперкалиемии. J R Coll Physitors Edinb .
2013. 43 (3): 246–251.
34. Чарытан Д,
Гольдфарб Д.С.
Показания к госпитализации больных гиперкалиемией. Arch Intern Med .
2000. 160 (11): 1605–1611.
35. Soar J,
Перкинс Г.Д.,
Аббас Г,
и другие.
Рекомендации Европейского совета по реанимации по реанимации, 2010 г., раздел 8.Остановка сердца при особых обстоятельствах: нарушение электролитного баланса, отравление, утопление, случайное переохлаждение, гипертермия, астма, анафилаксия, кардиохирургия, травма, беременность, поражение электрическим током. Реанимация .
2010. 81 (10): 1400–1433.
36. Lexicomp онлайн. https://online.lexi.com/crlsql/servlet/crlonline [требуется подписка]. Проверено 23 сентября 2014 г.
37. Weisberg LS.
Управление тяжелой гиперкалиемией. Crit Care Med .
2008. 36 (12): 3246–3251.
38. Линза ХМ,
Montoliu J,
Случаи А,
Campistol JM,
Вернуть L.
Лечение гиперкалиемии при почечной недостаточности: сальбутамол против инсулина. Циферблат нефрола .
1989. 4 (3): 228–232.
39. Махони Б.А.,
Смит WA,
Lo DS,
Цой К,
Тонелли М,
Clase CM.
Экстренные вмешательства при гиперкалиемии. Кокрановская база данных Syst Rev .
2005; (2): CD003235.
40. Аллон М,
Шанклин Н.Влияние введения бикарбоната на калий плазмы у диализных пациентов: взаимодействие с инсулином и альбутеролом. Am J Kidney Dis .
1996. 28 (4): 508–514.
41. Lillemoe KD,
Ромоло JL,
Гамильтон С.Р.,
Пеннингтон Л. Р.,
Бурдик Дж. Ф.,
Уильямс GM.
Некроз кишечника из-за полистирола натрия (кайексалата) в клизмах с сорбитолом: клиническое и экспериментальное подтверждение гипотезы. Хирургия .
1987. 101 (3): 267–272.
42. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. MedWatch. Кайексалат (сульфонат полистирола натрия) порошок. Январь 2011 г. http://www.fda.gov/Safety/MedWatch/SafetyInformation/ucm186845.htm. По состоянию на 23 сентября 2014 г.
43. Harel Z,
Харел С,
Шах П.С.,
Вальд Р.,
Perl J,
Bell CM.
Желудочно-кишечные нежелательные явления при использовании полистиролсульфоната натрия (кайексалата): систематический обзор. Am J Med .
2013; 126 (3): 264.e9 – e24.
44. Себастьян А,
Шамбелан М,
Sutton JM.
Улучшение гиперхлоремического ацидоза с помощью терапии фуросемидом у пациентов с хронической почечной недостаточностью и почечным канальцевым ацидозом 4 типа. Ам Дж. Нефрол .
1984. 4 (5): 287–300.
Рефидирование и метаболические синдромы: две стороны одной медали
Боатенг А.А., Шрирам К., Мегид М.М., Крук М. Синдром возобновления питания: рекомендации по лечению, основанные на коллективном анализе литературных историй болезни. Nutrition 2010; 26 : 156–167.
PubMed
Google Scholar
Fuentebella J, Kerner JA. Синдром возобновления питания. Pediatr Clin N Am 2009; 56 : 1201–1210.
Google Scholar
Национальный институт сердца, легких и крови. Третий отчет экспертной группы Национальной образовательной программы по холестерину (NCEP) по выявлению, оценке и лечению повышенного холестерина в крови у взрослых (Группа лечения взрослых III).Заключительный отчет. Тираж 2002 г .; 106 : 3143–3421.
Хан И.Р., Ахмед Дж., Хан С., МакФл Дж. Синдром возобновления питания: обзор литературы. Гастроэнтерол Рес и Прак 2011; 2011 DOI: 10.1155 / 2011/410971.
CAS
Google Scholar
Cox CL, Stanhope KL, Schwarz JM, Graham JL, Hatcher B, Griffen SC. Употребление подслащенных фруктозой напитков в течение 10 недель снижает чистое окисление жиров и расход энергии у мужчин и женщин с избыточным весом / ожирением. евро J Clin Nutr 2012; 66 : 201–208.
CAS
PubMed
Google Scholar
Хаттаб М., дит Эль-Хури Д., Азар С., Маттар М., Обейд О. Влияние фосфора на пероральный тест на толерантность к глюкозе. Proc Nutr Soc 2011; 70 : E60.
Google Scholar
Попкин Б.М. Глобальная динамика питания: мир быстро переходит на диету, связанную с неинфекционными заболеваниями. Am J Clin Nutr 2006; 84 : 289–298.
CAS
PubMed
Google Scholar
Попкин Б.М., Гордон-Ларсен П. Переход к питанию: динамика ожирения во всем мире и их детерминанты. Int J Obes 2004; 28 : S2 – S9.
Google Scholar
Johnson RJ, Titte S, Cade JR, Rideout BA, Оливер В. Мочевая кислота, эволюция и примитивные культуры. Сем Нефрол 2005; 25 : 3–8.
CAS
Google Scholar
Юсуф С., Редди С., Оуноу С., Ананд С. Глобальное бремя сердечно-сосудистых заболеваний. Часть I: общие соображения, эпидемиологический переход, факторы риска и влияние урбанизации. Тираж 2001 г .; 104 : 2746–2753.
CAS
PubMed
PubMed Central
Google Scholar
Эсмаиллзаде А., Кимиагер М., Мехраби Ю., Азадбахт Л., Ху Ф. Б., Уиллетт В.Особенности питания, инсулинорезистентность и распространенность метаболического синдрома у женщин. Am J Clin Nutr 2007; 85 : 910–918.
CAS
PubMed
Google Scholar
Лютси П.Л., Стеффен Л.М., Стивенс Дж. Диетическое питание и развитие метаболического синдрома: исследование риска атеросклероза в сообществах. Тираж 2008 г .; 117 : 754–761.
PubMed
Google Scholar
Накагава Т., Таттл К.Р., Шорт Р.А., Джонсон Р.Дж.Гипотеза: гиперурикемия, вызванная фруктозой, как причинный механизм эпидемии метаболического синдрома. Nat Clin Pract 2005; 1 : 80–87.
CAS
Google Scholar
Karczmar GS, Kurtz T, Tavares NJ, Weiner MW. Регулирование уровня неорганического фосфата и АТФ в печени в ответ на нагрузку фруктозой: исследование in vivo 31P-ЯМР. Biochem Biophys Acta 1989; 1012 : 121–127.
CAS
PubMed
Google Scholar
Lingelbach LB, McDonald RB. Описание долгосрочных липогенных эффектов пищевых углеводов у самцов крыс Fischer 344. J Nutr 2004; 130 : 3077–3084.
Google Scholar
Teff KL, Elliott SS, Tschop M, Kieffer TJ, Raeder D, Heiman M et al . Пищевая фруктоза снижает циркулирующий инсулин и лептин, ослабляет постпрандиальное подавление грелина и увеличивает уровень триглицеридов у женщин. J Clin Endocrinol Metab 2004; 89 : 2963–2972.
CAS
PubMed
Google Scholar
Заммит В.А., Уотерман И.Дж., Топпинг Д., Маккей Г. Инсулиновая стимуляция секреции триацилглицерина в печени и этиология инсулинорезистентности. J Nutr 2001; 131 : 2074–2077.
CAS
PubMed
Google Scholar
Продовольственная и сельскохозяйственная организация Объединенных Наций / FAOSTAT.ПК. Продовольственные сбалансированные ведомости 2009. По состоянию на 10 января 2014 года.
Drewnowski A. Ожирение, диеты и социальное неравенство. Nutr Ред. 2009 г .; 67 (Дополнение 1): S36 – S39.
PubMed
Google Scholar
Древновски А, Попкин Б.М. Переход к питанию: новые тенденции в мировом питании. Nutr Rev 1997; 55 : 31–43.
CAS
PubMed
Google Scholar
Попкин Б.М., Нильсен С.Дж.Сладость мировой диеты. Obes Res 2003; 11 : 1325–1332.
PubMed
Google Scholar
French S, Story M, Neumark-Sztainer D, Fulkerson JA, Hannan P. Использование ресторанов быстрого питания среди подростков: ассоциации с потреблением питательных веществ, выбором пищи, а также поведенческими и психосоциальными переменными. Int J Obes Relat Metab 2001; 25 : 1823–1833.
CAS
Google Scholar
Нильсен С, Сега-Риз А, Попкин Б.Тенденции в потреблении энергии в США в период с 1977 по 1996 год: аналогичные изменения наблюдаются во всех возрастных группах. Obes Res 2002; 10 : 370–378.
PubMed
Google Scholar
Нильсен С., Сега-Риз А, Попкин Б.М. Тенденции в отношении мест и источников питания среди подростков и молодых людей. Prev Med 2002; 35 : 107–113.
PubMed
Google Scholar
Haines P, Hama M, Guilkey DK, Popkin BM.Еда в выходные в Соединенных Штатах связана с повышенным потреблением энергии, жира и алкоголя. Obes Res 2003; 11 : 945–949.
PubMed
Google Scholar
Джеффри Р., Аттер Дж. Изменение окружающей среды и ожирение населения в США. Obes Res 2003; 11 : 12S – 22S.
PubMed
Google Scholar
Нильсен С., Попкин Б.М.Модели и тенденции в размерах порций, 1977–1998 гг. JAMA 2003; 289 : 450–453.
PubMed
Google Scholar
Брей Г.А., Нильсен С.Дж., Попкин Б.М. Потребление кукурузного сиропа с высоким содержанием фруктозы в напитках может сыграть роль в эпидемии ожирения. Am J Clin Nutr 2004; 79 : 537–543.
CAS
PubMed
Google Scholar
Гатри Дж, Лин Б., Фразао Э.Роль еды, приготовленной вне дома, в рационе американцев, 1977–1978 гг. По сравнению с 1994–1996 гг .: изменения и последствия. J Nutr Educ Behav 2002; 34 : 140–150.
PubMed
Google Scholar
Paeratakul S, Ferdinand DP, Champagne CM, Ryan DH, Bray GA. Потребление фаст-фуда взрослыми и детьми в США: профиль потребления питательных веществ и питательных веществ. J Am Diet Assoc 2003; 103 : 1332–1338.
PubMed
Google Scholar
Håglin L.Гипофосфатемия: причина нарушения обмена веществ при метаболическом синдроме. Med Hypotheses 2001; 56 : 657–663.
PubMed
Google Scholar
Lippi G, Montagnana M, Salvagno GL, Targher G, Guidi GC. Взаимосвязь между сывороточным фосфатом и факторами риска сердечно-сосудистых заболеваний в большой когорте взрослых амбулаторных пациентов. Diabetes Res Clin Pract 2009; 84 : e3 – e5.
CAS
PubMed
Google Scholar
Haap M, Heller E, Thamer C, Tschritter O, Stefan N, Fritsche A.Связь уровней фосфата в сыворотке с толерантностью к глюкозе, чувствительностью к инсулину и секрецией инсулина у субъектов, не страдающих диабетом. евро J Clin Nutr 2006; 60 : 734–739.
CAS
PubMed
Google Scholar
Фридман М.И. Ожирение и печеночный контроль пищевого поведения. Drug News Perspect 2007; 20 : 9.
Google Scholar
Наир С., Чако В.П., Арнольд К., Диль М.Запасы АТФ в печени и эффективность восполнения: сравнение нормальных людей с ожирением и без него. Am J Gastroenterol 2003; 98 : 466–470.
CAS
PubMed
Google Scholar
Обейд О.А., Димачкие С, Глайс С. Повышенное содержание фосфора при предварительной нагрузке подавляет потребление энергии ad libitum при последующем приёме пищи. Int J Obes 2010; 34 : 1446–1448.
CAS
Google Scholar
Назар К., Кациуба-Усьцилко Х, Щепаник Я., Земба А.В., Крук Б., Хвалбинска-Монета Я. и др. .Добавление фосфатов предотвращает снижение уровня трийодтиронина и увеличивает скорость метаболизма в состоянии покоя во время низкокалорийной диеты. J. Physiol Pharmacol 1996; 47 : 373–383.
CAS
PubMed
Google Scholar
Jaedig S, Lindgärde F, Arborelius M. Повышенный расход энергии после приема пищи у женщин с ожирением после перорального приема калия и магния. Miner Electrolyte Metab 1994; 20 : 147–152.
CAS
PubMed
Google Scholar
Белин Р.Дж., Хе К. Физиология магния и патогенетические механизмы, способствующие развитию метаболического синдрома. Magnes Res 2007; 20 : 107–129.
CAS
PubMed
Google Scholar
Обейд О. Низкий уровень фосфора может способствовать развитию ожирения. Obes Rev 2013; 14 : 659–664.
CAS
PubMed
Google Scholar
Челик Н, Андиран Н. Связь между уровнями фосфатов в сыворотке крови с детским ожирением и инсулинорезистентностью. J Pediatr Endocrinol Metab 2011; 24 : 81–83.
CAS
PubMed
Google Scholar
Holecki M, Chudek J, Wiecek A, Titz-Bober M, Dulawa J. Сывороточный уровень фактора роста фибробластов-23 и кальций-фосфатный гомеостаз у женщин с ожирением в перименопаузе. Int J Endocrinol 2011; 2011 : 707126.
CAS
PubMed
PubMed Central
Google Scholar
Alonso A, Nettleton JA, Ix JH, de Boer IH, Folsom AR, Bidulescu A et al . Пищевой фосфор, артериальное давление и частота гипертонии в риске атеросклероза в исследовании сообществ и многоэтническом исследовании атеросклероза. Гипертония 2010; 55 : 776–784.
CAS
PubMed
PubMed Central
Google Scholar
Foley RN, Collins AJ, Herzog CA, Ishani A, Kalra PA. Уровни фосфора в сыворотке крови связаны с атеросклерозом коронарных артерий у молодых людей. J Am Soc Nephrol 2009; 20 : 397–404.
CAS
PubMed
PubMed Central
Google Scholar
Park W., Kim BS, Lee JE, Huh JK, Kim BJ, Sung KC и др. .Уровни фосфатов в сыворотке и риск сердечно-сосудистых заболеваний и метаболического синдрома: палка о двух концах. Diabetes Res Clin Pract 2009; 83 : 119–125.
CAS
PubMed
Google Scholar
Дхингра Р., Салливан Л.М., Фокс С.К., Ван Т.Дж., Д’Агостино Р.Б., Газиано Дж. М. и др. . Связь уровней фосфора и кальция в сыворотке с частотой сердечно-сосудистых заболеваний в обществе. Arch Intern Med 2007; 167 : 879–885.
CAS
PubMed
Google Scholar
Kalaitzidis R, Tsimihodimos V, Bairaktari E, Siamopoulos KC, Elisaf M. Нарушения фосфатного обмена: еще одна особенность метаболического синдрома. Am J Kidney Dis 2005; 45 : 851–858.
CAS
PubMed
Google Scholar
Haglin L, Lindbland A, Bygren LO. Гипофосфатемия при метаболическом синдроме.Гендерные различия в массе тела и уровне глюкозы в крови. евро J Clin Nutr 2001; 55 : 493–498.
CAS
PubMed
Google Scholar
Ljunghall S, Hvarfner A, Lind L. Клинические исследования метаболизма кальция при гипертонической болезни. Eur Heart J 1987; 8 (Дополнение B): 37–44.
PubMed
Google Scholar
Фарханги М.А., Остадрахими А, Махдуб С.Кальций, магний, фосфор и липидный профиль сыворотки у здоровых иранских женщин в пременопаузе. Biochemia Medica 2011; 21 : 312–320.
CAS
PubMed
Google Scholar
Gudmundsdottir H, Starnd AH, Kjeldsen SE, Hoieggen A, Os I. Фосфат сыворотки, артериальное давление и метаболический синдром — 20-летнее наблюдение за мужчинами среднего возраста. J Clin Hypertens (Гринвич) 2008; 10 : 814–821.
CAS
Google Scholar
Vyssoulis G, Karpanou E, Tzamou V, Kyvelou SM, Michaelidis A, Stefanadis C. Фосфат сыворотки у пациентов с гипертонической болезнью в белом халате: акцент на статусе падения и метаболическом синдроме. Hypertens Res 2010; 33 : 825–830.
CAS
PubMed
Google Scholar
Elliott P, Kesteloot H, Appel LJ, Duer AR, Ueshima H, Chan Q.Пищевой фосфор и артериальное давление: международное исследование макро- и микронутриентов и артериального давления. Гипертония 2008; 51 : 669–675.
CAS
PubMed
Google Scholar
Хаджар I, Котчен Т. Региональные вариации артериального давления в США связаны с региональными вариациями в рационе питания: данные NHANES-III. J Nutr 2003; 133 : 211–214.
CAS
PubMed
Google Scholar
Kesteloot H, Joossens JV. Связь сывороточного натрия, калия, кальция и фосфора с артериальным давлением. Бельгийские межвузовские исследования питания и здоровья. Гипертония 1988; 12 : 589–593.
CAS
PubMed
Google Scholar
Kjeldesen SE, Os I, Westheim A, Frederichsen P, Hjermann I, Eide I.K.Снижение сывороточного фосфата при эссенциальной гипертензии. Связано с повышенным симпатическим тонусом. Am J Hypertens 1988; 1 : 403–409.
Google Scholar
Харлан В.Р., Халл А.Л., Шмоудер Р.Л., Лэндис Дж.Р., Томпсон Ф.Е., Ларкин Ф.А. Артериальное давление и питание у взрослых. Национальное обследование здоровья и питания. Am J Epidemiol 1984; 120 : 17–28.
CAS
PubMed
Google Scholar
Дэниэлс Дж., Гудман Д.А.Гипертония и гиперпаратиреоз. Обратная связь уровня фосфата в сыворотке крови и артериального давления. Am J Med 1983; 75 : 17–23.
CAS
PubMed
Google Scholar
Хэвлик Р.Дж., Гарнизон Р.Дж., Фейнлейб М., Паджетт С., Кастелли В.П., Макнамара П.М. Доказательства дополнительного артериального давления коррелируют у взрослых 20-56 лет. Тираж 1980 г .; 61 : 710–715.
CAS
PubMed
Google Scholar
Касс Л., Уикс Дж., Карпентер Л.Влияние добавок магния на артериальное давление: метаанализ. евро J Clin Nutr 2012; 66 : 411–418.
CAS
PubMed
Google Scholar
Gums JG. Магний при сердечно-сосудистых и других заболеваниях. Am J Health-Syst Pharm 2004; 61 : 1569–1576.
CAS
PubMed
Google Scholar
Геррера М.П., Вольпе С.Л., Мао Дж. Дж.Терапевтическое использование магния. Am Fam Physician 2009; 80 : 157–162.
PubMed
Google Scholar
He K, Liu K, Daviglus ML, Morris SJ, Loria CM, Van Horn L и др. . Потребление магния и частота метаболического синдрома среди молодых людей. Тираж 2006 г .; 113 : 1675–1682.
CAS
PubMed
Google Scholar
Сонг Й., Ридкер П.М., Мэнсон Дж. Э., Кук Н. Р., Бурнинг Дж. Е., Лю С.Потребление магния, С-реактивного белка и распространенность метаболического синдрома у американских женщин среднего и старшего возраста. Уход за диабетом. 2005; 28 : 1438–1444.
CAS
PubMed
Google Scholar
Ford ES, Li C, McGuire LC, Mokdad AH, Liu S. Потребление магния с пищей и распространенность метаболического синдрома среди взрослых в США. Ожирение 2007; 15 : 1139–1146.
CAS
PubMed
Google Scholar
Lima ML, Cruz T, Rodrigues LE, Bomfim O, Melo J, Correia R и др. .Сывороточный и внутриклеточный дефицит магния у пациентов с метаболическим синдромом — доказательства его связи с инсулинорезистентностью. Diabetes Res Clin Pract 2009; 83 : 257–262.
CAS
Google Scholar
Corica F, Corsonello A, Ientile R, Cucinotta D, Di Bendetto A, Perticone F. Уровни ионизированного магния в сыворотке в связи с метаболическим синдромом у пациентов с диабетом 2 типа. J Am Coll Nutr 2006; 25 : 210–215.
CAS
PubMed
Google Scholar
Yajnik CS, Smith RF, Hockaday TDR, Ward NI. Концентрация магния в плазме натощак и утилизация глюкозы при диабете. Br Med J 1984; 288 : 1032–1035.
CAS
Google Scholar
Зофкова И., Недвидково Ю., Замразил В., Симецкова А. Влияние магния на толерантность к глюкозе острая гипомагниемия снижает толерантность к глюкозе независимо от гормональных показателей. Horm Metabol Res 1987; 19 : 228–229.
CAS
Google Scholar
Кишимото Ю., Тани М., Уто-Кондо Х, Сайта Е., Иидзука М., Соне Х. Влияние магния на липидные реакции сыворотки после приема пищи у здоровых людей. Br J Nutr 2010; 103 : 469–472.
CAS
PubMed
Google Scholar
Witteman JC, Grobee DE, Derkx FH, Bouillon R, de Bruijn AM, Hofman A.Снижение артериального давления с помощью пероральных добавок магния у женщин с легкой и умеренной гипертензией. J Clin Nutr 1994; 60 : 129–135.
CAS
Google Scholar
He FJ, MacGregor GA. Благотворное влияние калия на здоровье человека. Physiol Plant 2008; 133 : 725–735.
CAS
PubMed
Google Scholar
Роу Дж. У., Тобин Дж. Д., Роза Р. М., Андрес Р.Влияние экспериментального дефицита калия на метаболизм глюкозы и инсулина. Метаболизм 1980; 29 : 498–505.
CAS
Google Scholar
Длухи Р.Г., Аксельрод Л., Уильямс Г.Х. Сывороточный иммунореактивный инсулин и реакция гормона роста на инфузию калия у нормального человека. J Appl Physiol 1972; 33 : 22–27.
CAS
PubMed
Google Scholar
Резник Л.М., Барбагалло М., Домингес Л.Дж., Вениеро Дж. М., Николсон Дж. П., Гупта Р.К.Связь клеточного калия с другими минеральными ионами при гипертонии и диабете. Гипертония 2001; 38 : 709–712.
CAS
PubMed
Google Scholar
Терамото Т, Кавамори Р., Миядзаки С., Терамукай С. Потребление натрия мужчинами и потребление калия женщинами определяют распространенность метаболического синдрома у японских пациентов с гипертонией: исследование OMEGA. Hypertens Res 2011; 34 : 957–962.
CAS
PubMed
PubMed Central
Google Scholar
Fujita T, Sato Y. Натрийуретический и антигипертензивный эффекты калия у крыс с гипертонической болезнью DOCA-соли. Kidney Int 1983; 24 : 731–739.
CAS
PubMed
Google Scholar
Fujita T, Ando K. Гемодинамические и эндокринные изменения, связанные с добавлением калия у гипертоников, нагруженных натрием. Гипертония 1984; 6 : 184–192.
CAS
PubMed
Google Scholar
Огихара Т., Асано Т., Андо К. и др. . Диета с высоким содержанием соли усиливает передачу сигналов инсулина и вызывает резистентность к инсулину у чувствительных к соли крыс Даля. Гипертония 2002; 40 : 83–89.
CAS
PubMed
PubMed Central
Google Scholar
Fujita T.Инсулинорезистентность и солеочувствительная гипертензия при метаболическом синдроме. Циферблат нефрола 2007; 22 : 3102–3107.
CAS
PubMed
Google Scholar
Azadbakht L, Mirmiran P, Esmaillzadeh A, Azizi T, Azizi F. Благоприятное влияние диетических подходов для прекращения приема пищи при гипертонии на особенности метаболического синдрома. Уход за диабетом 2005; 28 : 2823–2831.
CAS
PubMed
Google Scholar
Ли Х, Ли Дж, Хван С., Ким С., Чин Х. Дж., Хан Дж. Потребление калия и распространенность метаболического синдрома: Национальное исследование здоровья и питания Кореи, 2008-2010 гг. PLoS One 2013; 8 : 1–9.
Google Scholar
Яновский Дж., Парих С. Дж., Янофф Л. Б., Денкингер Б. И., Калис К. А., Рейнольдс Дж.Влияние добавок кальция на массу тела и ожирение у взрослых с избыточным весом и ожирением: рандомизированное исследование. Ann Intern Med 2009; 150 : W145 – W146.
Google Scholar
Ye EQ, Chacko SA, Chou EL, Kugizaki M, Liu S. Повышенное потребление цельнозерновых продуктов связано с более низким риском диабета 2 типа, сердечно-сосудистых заболеваний и увеличения веса. J Nutr 2012; 142 : 1304–1313.
CAS
PubMed
PubMed Central
Google Scholar
Дженкинс DJ, Кендалл С.В., Огюстин Л.С., Мартини М.С., Аксельсен М., Фолкнер Д.Влияние пшеничных отрубей на гликемический контроль и факторы риска сердечно-сосудистых заболеваний при диабете 2 типа. Diabetes Care 2002; 25 : 1522–1528.
CAS
PubMed
Google Scholar
Паула Ф.Дж., Plens AE, Foss MC. Влияние гипофосфатемии на толерантность к глюкозе и секрецию инсулина. Horm Metab Res 1998; 30 : 281–284.
CAS
PubMed
Google Scholar
Калий | eClinpath
Физиология
Калий является основным внутриклеточным катионом (внутриклеточная концентрация K + составляет приблизительно 140 мэкв / л) и важен для поддержания мембранного потенциала покоя клеток, особенно мышц и нервов.60-75% калия в организме содержится в мышечных клетках, а остальная часть — в костях. Только 5% калия находится во внеклеточной жидкости (ВКЖ), поэтому концентрация калия в крови не всегда является отражением общего уровня калия в организме. Плазма (ECF) K + , концентрация строго регулируется ; довольно небольшие изменения могут оказывать заметное влияние на функцию органов, при этом серьезные отклонения от нормы K + в плазме являются опасными для жизни ситуациями.
Плазма [K
+ ] Постановление
Регулирование плазмы K + в основном достигается за счет почечной экскреции и перемещения K + из внеклеточной жидкости во внутриклеточную (транслокация).Если эти механизмы работают нормально, количество проглоченного K + мало влияет на плазменный K + . Прием в меньшей степени влияет на уровень калия в плазме, однако, если один или несколько регуляторных механизмов неисправны, то количество проглоченного K + может усугубить нарушения в плазме K + . У некоторых видов с пищей с высоким содержанием калия (например, жвачных) изменения в потреблении могут влиять только на концентрацию в плазме.
- Поступление : Попадание внутрь K + неселективно всасывается в желудке и тонком кишечнике.Если диетический K + недостаточен, почечная экскреция K + уменьшается (но все еще происходит), но выведение может увеличиваться при состояниях хронического высокого K + в рационе. Коровы потребляют значительное количество калия в своем рационе и, как следствие, имеют высокий уровень выделения калия почками (Sattler and Fecteau, 2014, Schneider et al, 2016).
- Экскреция : Калий выводится почечными канальцами и толстой кишкой, причем последний вносит лишь небольшой вклад в общее выведение K + .Дополнительным источником выделения калия является слюна жвачных животных (Sockett et al 1986). Контроль экскреции K + с мочой происходит в дистальных канальцах.
- Около 70% отфильтрованного K + абсорбируется в проксимальных извитых канальцах почек независимо от баланса K + (за счет увлечения растворителем водой и пассивной параклеточной диффузии)
- Около 20% абсорбируется в восходящей ветви петли Генле (через параклеточное и трансцеллюлярное всасывание, последнее происходит через транспортер Na-K-2Cl).Некоторое количество калия также может выводиться в этом сегменте.
- Оставшиеся 10% попадают в дистальный отдел нефрона. Здесь K + может выводиться или резорбироваться в зависимости от приема с пищей (дефицит = преобладает абсорбция, хронический избыток = происходит умеренное выделение). Почки более эффективно выводят калий из организма, чем его сохраняют.
- Экскреция в дистальном нефроне происходит в основном через почечный наружный мозговидный калиевый канал или каналы ROMK в основных клетках в соединительном канальце, кортикальном собирательном канале и первой части мозгового собирательного канала.Этот канал открыт в основных условиях, но его активность также связана с абсорбцией Na + транспортерами натрия (ENaC), которая стимулируется альдостероном. Базолатеральные насосы Na / K (также стимулируемые альдостероном) перемещают калий из крови в клетки почечных канальцев для выведения. В дистальном нефроне есть и другие K-каналы, включая каналы maxi-K, которые активируются увеличением скорости потока в дистальных канальцах (или доставкой натрия, то есть опосредованной ENaC абсорбцией натрия, которая создает отрицательную разность потенциалов в просвете, что способствует выведению калия). и считаются безмолвными во время базальных состояний.Экскреция K + дистальным нефроном регулируется следующим, хотя основными регуляторами являются абсорбция натрия в дистальных канальцах и альдостерон:
- Альдостерон : В условиях гипохлоремии или гиповолемии высвобождение альдостерона стимулирует абсорбцию натрия через ENaC, что создает отрицательный электрический заряд просвета, который способствует выведению калия. Альдостерон увеличивает активность базолатерального насоса Na / K, увеличивая внутриклеточные концентрации калия, тем самым способствуя экскреции K + в обмен на натрий.Это также напрямую вызывает потерю калия за счет увеличения проводимости (проницаемости) просветной мембраны. Альдостерон также способствует выведению K + в толстую кишку. Когда секреция альдостерона стимулируется высоким содержанием калия через прямое воздействие на надпочечники (по сравнению с ренин-ангиотензиновой системой при стимуляции низким содержанием хлоридов или гиповолемией), натрий не сохраняется, но калий выводится через повышенную проницаемость просветной мембраны и стимуляцию базолатерального отдела. Насос Na / K, который увеличивает внутриклеточную концентрацию калия.
- Скорость потока в дистальных канальцах : Увеличение скорости потока (осмотический диурез, увеличение потока мочи после инфузионной терапии, диуретики, увеличение доставки натрия в собирательные канальцы из-за снижения абсорбции натрия выше в нефроне) увеличивает секрецию K + в просвет канальца (выведение). Это работает за счет вымывания K и увеличения дистальной доставки натрия с увеличением абсорбции натрия через ENaC (повышенная электроотрицательность просвета, вызванная абсорбцией натрия, способствует выведению калия).Снижение скорости потока, например, вызванное повышенной резорбцией проксимальных почечных канальцев в условиях гиповолемии, может привести к снижению доставки натрия к дистальному нефрону, с уменьшением скорости потока, уменьшением экскреции K + и, таким образом, может способствовать гиперкалиемии.
- Внеклеточная концентрация K + : Стимулирует высвобождение альдостерона, если оно высокое, вызывая выведение калия без всасывания натрия.
- Электроотрицательность просвета канальцев почек : Повышенная электроотрицательность в собирающих канальцах усиливает секрецию (выведение) калия в просвет канальцев.Это может быть вторичным по отношению к увеличению абсорбции натрия из-за увеличения доставки натрия (см. Выше скорость дистального потока) или высоких концентраций отрицательно заряженных молекул, таких как кетокислоты и некоторые антибиотики.
- pH: Ацидемия снижает выведение калия (см. Механизмы ниже в разделе «Причины гиперкалиемии»). Алкалиемия способствует потере калия, заставляя его перемещаться внутриклеточно в клетку канальцев в обмен на водород. Высокий уровень внутриклеточного калия создает благоприятный градиент концентрации, облегчая выведение.Алкалиемия также стимулирует переносчик натрия, ENaC, который увеличивает электроотрицательность просвета за счет поглощения натрия.
- Диета: Дефицит K + в пище будет стимулировать резорбцию (хотя некоторое количество K + всегда теряется с мочой), тогда как хронический избыток будет стимулировать выведение (за счет стимуляции высвобождения альдостерона и базолатерального Na / K насоса).
- ADH : Стимулирует секрецию в просвет канальцев (открывая каналы Na / K в просветной мембране в основных клетках собирательного кортикального протока), но также снижает экскрецию (вызывая абсорбцию воды, что снижает скорость дистального потока, уменьшая выведение калия) .Таким образом, АДГ, вероятно, не влияет на концентрацию калия в сыворотке или плазме.
- Поглощение в дистальном нефроне происходит трансцеллюлярно через α-интеркалированные клетки с использованием насоса HK-ATPase на апикальной мембране) в остальной части мозгового собирательного канала (кроме начальной части) в обмен на H + (активность эти клетки приводят к избыточной секреции водорода, что способствует метаболическому алкалозу в состояниях гипокалиемии).
- Экскреция в дистальном нефроне происходит в основном через почечный наружный мозговидный калиевый канал или каналы ROMK в основных клетках в соединительном канальце, кортикальном собирательном канале и первой части мозгового собирательного канала.Этот канал открыт в основных условиях, но его активность также связана с абсорбцией Na + транспортерами натрия (ENaC), которая стимулируется альдостероном. Базолатеральные насосы Na / K (также стимулируемые альдостероном) перемещают калий из крови в клетки почечных канальцев для выведения. В дистальном нефроне есть и другие K-каналы, включая каналы maxi-K, которые активируются увеличением скорости потока в дистальных канальцах (или доставкой натрия, то есть опосредованной ENaC абсорбцией натрия, которая создает отрицательную разность потенциалов в просвете, что способствует выведению калия). и считаются безмолвными во время базальных состояний.Экскреция K + дистальным нефроном регулируется следующим, хотя основными регуляторами являются абсорбция натрия в дистальных канальцах и альдостерон:
- Транслокация :
- Инсулин и катехоламины: Транслокация K + в клетки из ECF в значительной степени зависит от инсулина и катехоламинов, которые стимулируют поглощение клетками, особенно в скелетных мышцах.Катехоламины стимулируют насос Na / K-АТФазы, который выводит Na наружу и K внутрь (таким образом уменьшая содержание K в сыворотке / плазме) в скелетных мышцах. Инсулин связывается с рецептором на поверхности клеток (рецептор-1 субстрата инсулина). Передача сигналов ниже по течению с этим рецептором вызывает захват калия и глюкозы (последняя через рецепторы GLUT-4).
- Некроз тканей также может вызывать высвобождение внутриклеточного калия, особенно в скелетных мышцах.
- Изменения кислотно-основного статуса: сдвиги K + в клетки и из клеток также могут происходить с изменениями pH ECF.В частности, алкалоз (при доминирующем нарушении или в щелочных состояниях) заставляет калий перемещаться в клетки, что приводит к гипокалиемии. Минеральный метаболический ацидоз (гиперхлоремический) может напрямую вызывать преходящую гиперкалиемию, стимулируя перемещение калия из клеток или снижение поглощения калия клетками. Это опосредовано падением внеклеточного pH, которое ингибирует обмен Na / H (H out, Na в клетку) и снижает внутриклеточные концентрации натрия. Снижение внутриклеточного натрия снижает активность насоса Na / K (который выводит 3Na на 2K дюйма), что зависит от внутриклеточных концентраций натрия.Напротив, накопление нехлоридсодержащей кислоты при титровании или ацидоз с высокой анионной щелью не вызывает непосредственно гиперкалиемии из-за транслокации. Это связано с тем, что органическая кислота (например, L-лактат) и H, который она несет, перемещаются вместе в клетку (через переносчики монокарбоксилата, например, MCT1), и падение внутриклеточного pH на более серьезное, чем при минеральном ацидозе. Более низкий уровень внутриклеточного pH стимулирует обмен Na / бикарбонат или Na / H (Na на входе, бикарбонат или H на выходе), поэтому внутриклеточные концентрации Na остаются высокими и стимулируют активность Na / K (вытесняют Na и K внутрь), так что K не увеличивается в крови при ацидозе с высокой анионной щелью.Гиперкалиемия, которая часто наблюдается у животных с титрованным ацидозом, считается вторичной по отношению к снижению почечной экскреции и транслокации , а не (см. Механизмы ниже) (влияние pH на обработку калия почками рассматривается Hamm et al 2013). Фактически, в экспериментальных условиях органический ацидоз связан с нормальным или низким содержанием калия (Aronson and Giebisch 2011). При изменениях кислотно-основного статуса изменения калия (уменьшение алкалоза и увеличение минерального ацидоза) более серьезны при первичном метаболизме, чем при первичных респираторных состояниях.
- Эндотоксины: это стимулирует насос Na / K и вызывает высвобождение инсулина, оба из которых будут управлять K внутри клеток.
Методы
Концентрации этих основных электролитов в сыворотке или плазме могут быть измерены ионно-специфическими электродами или пламенной фотометрией. Измерение электролитов ионно-специфическими электродами называется потенциометрией. Существует два типа потенциометрии: прямая и непрямая. Прямая потенциометрия используется в аппаратах для определения газов крови и не требует разбавления пробы.Косвенная потенциометрия используется автоматическими химическими анализаторами, такими как те, что используются в Корнельском университете, и включает разбавление образца перед анализом. Это различие важно, потому что эндогенные факторы, такие как липемия, могут ложно снижать концентрацию электролитов с помощью косвенной, но не прямой потенциометрии.
Техника, используемая в Корнелле
Прямая (анализатор газов крови) или непрямая (химический анализатор) потенциометрия. В наших биохимических профилях для получения результатов измерения калия используется непрямая потенциометрия.
Процедура
При использовании этого метода электрод, содержащий раствор внутреннего электролита, погружается в образец пациента, который отделен от внутреннего раствора мембраной, которая может определять электродвижущую силу (ЭДС), создаваемую ионами в обоих растворах. Эта ЭДС определяется разницей в концентрации тестового иона в тестовом растворе и внутреннем заполняющем растворе (тестовый ион с фиксированной концентрацией). ЭДС предсказывается уравнением Нернста (см. Методы для получения более подробной информации о методе).Для тестирования с помощью химического анализатора образец перед анализом разбавляют 1:32 (непрямая потенциометрия).
Единицы измерения
Концентрация калия измеряется в миллиэкв / л (условные единицы, используемые в Корнелльском университете), мг / дл (условные единицы) или ммоль / л (единицы СИ). Формула преобразования показана ниже:
мэкв / л x 1 = ммоль / л
мг / дл ÷ 3,9 = ммоль / л
Пример рассмотрения
Тип образца
Сыворотка, плазма и моча.Плазма дает более точные значения, чем сыворотка, потому что калий выделяется из тромбоцитов во время свертывания крови.
Антикоагулянт
Гепарин является предпочтительным антикоагулянтом. K 3 EDTA следует избегать, потому что это вызовет ложно высокие уровни K + в образце из-за калия в антикоагулянте.
- КРС : Внутренние исследования в лаборатории клинической патологии Корнельского университета на бычьей крови показывают, что значения в гепаринизированной плазме несколько выше (0-0.3 мэкв / л), чем в сыворотке (Naeves и Stokol, неопубликованные данные).
Стабильность
- Человек : Информационный лист продукта от производителя реагента
- Сыворотка и плазма : 2 недели при комнатной температуре, 2 недели в холодильнике.
- Моча : хранить при 4 ° C
- Коровья : внутренние исследования лаборатории клинической патологии Корнельского университета показывают, что калий более стабилен в гепаринизированной цельной крови по сравнению с цельной цельной кровью, не разделенной сгустками, и более стабилен при 22 ° C, чем 4 ° C.Повышенная стабильность при 4 ° C объясняется повышенным ингибированием Na / K-АТФазы в клетках (которая вытесняет калий и натрий), что приводит к увеличению внеклеточного калия.
- Гепарин / пробирки с зеленой крышкой : Результаты по калию более стабильны в гепаринизированных образцах цельной крови (неотделенных), хранящихся при 22 ° C (нет изменений в результатах через 4 или 6 часов после сбора) по сравнению с 4 ° C (увеличивается на 0,1-0,2 мэкв / л через 4 часа и 0,2-0,3 мэкв / л через 6 часов) после сбора.
- Пробирки для сгустка : Уровень калия слегка повышен в цельной крови, поддерживаемой при 4 ° C (на 0.1-0,3 мэкв / л) или 22 ° C (на 0,1-0,2 мэкв / л) в течение 4 часов (Naeves и Stokol, неопубликованные данные).
Независимо от вышеуказанных результатов у крупного рогатого скота, которые относятся только к хранению на срок до 4-6 часов, все же рекомендуется удалять сыворотку или плазму немедленно из клеток после сбора (центрифугированием), чтобы избежать ложного увеличения Уровни K + , вызванные высвобождением K + из внутриклеточных хранилищ в клетках (содержание калия в клетках намного выше, чем в ECF).Эритроциты и тромбоциты являются основными источниками внутриклеточного калия, однако только некоторые виды (лошади, некоторые породы крупного рогатого скота, такие как голштинская, свиньи, ламы) имеют высокое содержание калия в красных кровяных тельцах. У собак нет высокого содержания калия в красных кровяных тельцах, за исключением некоторых пород собак (японские или другие азиатские породы, например, акита, сиба-ину). Также ретикулоциты у всех пород собак богаты калием. Утечка калия из клеток может происходить без явного гемолиза, а также может происходить в пробирках с сепаратором сыворотки, если сыворотка не отделена от эритроцитов.Ложно высокий уровень калия — один из наиболее распространенных артефактов, которые можно увидеть на химических панелях из образцов, отправленных в Корнельскую лабораторию от лошадей, верблюдов и крупного рогатого скота (поскольку мы видим кровь, в первую очередь, от голштинцев), когда сыворотка или плазма не были отделены от клеток. .
Помехи
- Липемия : Заметная липемия (триглицериды> 600 мг / дл) может незначительно снизить калий из-за эффекта исключения растворителя. Это основано на внутренних наблюдениях, сравнивающих результаты прямой и непрямой потенциометрии на одном и том же образце от собак с выраженной гипертриглицеридемией.Влияние на калий невелико (например, снижение на 0,3-0,5 мг-экв / л) по сравнению с действием натрия и хлорида.
- Гемолиз : Гемолиз или измененная стабильность мембран эритроцитов без гемолиза (например, при хранении) может повышать уровень калия в сыворотке или плазме крови у видов или пород с высоким содержанием калия в эритроцитах (лошади, верблюды, свиньи, некоторые породы крупного рогатого скота, такие как голштинская). , некоторые азиатские породы собак) или у собак с выраженным ретикулоцитозом.
- Icterus : Нет эффекта.
Интерпретация теста
Гиперкалиемия
Гиперкалиемия увеличивает мембранный потенциал покоя (т. Е. Делает его менее отрицательным, так что его легче поляризовать или активировать, например, увеличивается с -90 до -80). Это предрасполагает клетку к чрезмерной возбудимости и приводит к возбудимости мышц и нервов, наиболее серьезным последствием которой является аритмия сердца и даже остановка (помните, что высокий уровень KCl можно использовать в качестве решения для эвтаназии, чтобы вызвать остановку сердца).Гиперкалиемия потенциально может в некоторой степени способствовать ацидозу, ингибируя почечный аммиагенез (основной способ, которым почки выводят кислоты) (Hamm et al 2013).
- Артефакт:
- Сыворотка: Сыворотка K + обычно выше, чем плазменная K + из-за высвобождения K + из тромбоцитов во время свертывания. На основании внутренних исследований в Корнелле (например, когда мы установили наши референсные интервалы для сыворотки и плазмы родственных видов) и предыдущих отчетов, разница между K + в сыворотке и плазме у животных с нормальным количеством тромбоцитов может достигать 0.7 мг-экв / л у собак, 1,6 мг-экв / л у кошек, 1,6 мг-экв / л у крупного рогатого скота голштинской породы, 0,5 мг-экв / л у крупного рогатого скота голштинской породы (это может быть связано с гемолизом в образцах) и 0,8 мг-экв / л у альпак. Эта разница может быть выше (но не сильно) у животных с тромбоцитозом (особенно, если последний отмечен, то есть> 1 млн / мкл). Таким образом, гепаринизированная плазма является предпочтительным образцом для измерения калия.
- Гемолиз (in vivo или in vitro) или утечка из эритроцитов: Внутрисосудистый ( in vivo ) гемолиз при гемолитической анемии, артефактный ( in vitro, ) гемолиз или утечка из эритроцитов при хранении или неправильном обращении с образцом, может увеличиваться K + у животных с высоким содержанием K + в эритроцитах, включая лошадей, свиней (Di Martino et al, 2015), некоторые породы крупного рогатого скота (например,г. Голштинский), карибу (внутренние исследования в Корнелле) и верблюдовые. Это будет зависеть от степени гемолиза или разрушения мембраны эритроцитов (более вероятно, если оно будет высоким). Высокий уровень калия является одним из наиболее распространенных ложно ненормальных результатов химического анализа (наряду с ложно низким уровнем глюкозы) в отправленных по почте образцах, в которых сыворотка или плазма не были отделены от клеток у этих вышеупомянутых видов. Некоторые породы собак также имеют высокий уровень K + в зрелых эритроцитах, например, акиты и другие японские породы. У всех собак высокий уровень K + в их ретикулоцитах и , поэтому K + может быть ложно увеличен в гемолизированных образцах (или образцах с отсроченным отделением от клеток) с очень высоким количеством ретикулоцитов от любой породы собак.
- Лейкоцитоз: Очень высокое количество лейкоцитов (> 100 000 / мкл) потенциально может привести к гиперкалиемии из-за утечки внутриклеточного K + из клеток. Таких случаев мы особо не выявили.
- K + EDTA антикоагулянт: Загрязнение образца сыворотки / плазмы K + EDTA приведет к очень высоким (нефизиологическим) значениям K + (> 20 мЭкв / л), а также к выраженной гипокальциемии ( <5 мг / дл; из-за хелатирования).Мы иногда видим этот неизбежный артефакт в образцах.
- Загрязнение жидкостями с высоким содержанием калия: Если образец крови взят из непромытой внутривенной линии, используемой для введения жидкостей, богатых калием, K + может быть ложно высоким.
- Физиологический:
- Возраст : Сообщается, что уровень калия выше у жеребят младше 5 месяцев, чем у взрослых лошадей. Сообщается, что у жеребят младше 1 недели K + выше, чем у жеребят старше 1 недели.
- Ятрогенный: Добавление калия во внутривенные жидкости обычно не приводит к гиперкалиемии, если функция почек нормальная.
- Патофизиологический:
- Трансклеточные сдвиги: Переход K + из внутриклеточной жидкости (ICF) в ECF происходит при значительном некрозе тканей, упражнениях (это происходит особенно у лошадей и связано с высвобождением K + из мышц, особенно скелетных мышц. которые имеют высокую массу; K + является местным сосудорасширяющим средством для мышечных клеток), уроперитонеум (у жеребят и мелких животных — смещается из брюшной полости, где моча с высоким содержанием K + , в кровь), гипертонус (т.е.г. сахарный диабет; возникает из-за увлечения растворителем), дефицита инсулина (например, сахарного диабета) и потенциально гиперхлоремического метаболического ацидоза (временная гиперкалиемия наблюдается после экспериментального введения хлорида аммония собакам). Большой анионный промежуток или метаболический ацидоз титрования (накопление нехлоридной кислоты, например, лактата, уремических фосфатных кислот) обычно не приводит к гиперкалиемии. Гиперкалиемия у животных с титровальным ацидозом обычно возникает не из-за транслокации, а, как полагают, из-за снижения почечной экскреции K + (см. Ниже).
- Гиперкалиемическая полимиопатия лошадей: Это происходит из-за генетического дефекта альфа-субъединицы натриевого канала мышечных клеток (натриевые каналы остаются постоянно открытыми), наблюдаемого у четвероногих лошадей и других сильно мускулистых пород, таких как аппалуза и пейнтс. Это семейное заболевание у четвероногих лошадей и, по-видимому, наследуется как аутосомно-доминантное заболевание. У мужчин состояние клинически ухудшается. Для него характерны периодические эпизоды фасцикуляции и слабости мышц, сопровождающиеся увеличением значений K + в сыворотке, что, вероятно, связано с утечкой из мышц из-за дефектных каналов.Описаны нормокалиемические варианты. У Quarterhorses единственная точечная мутация рецептора рианодина, внутриклеточного кальциевого канала, вызывает избыток кальция в мышцах, что приводит к миопатии с последующим высвобождением калия (Alerman et al 2009).
- Снижение почечной экскреции : Гиперкалиемия является признаком анурической или олигурической острой почечной недостаточности, обструкции или разрыва мочевыводящих путей (как указано выше) и гипоальдостеронизма (болезнь Аддисона).
- Диарея новорожденных крупного рогатого скота: Чистка телят связана с гиперкалиемией. В двух исследованиях с участием 124 и 836 телят с диареей у 28-34% была гиперкалиемия, у меньшего числа — гипокалиемия (11% в одном из исследований) (Trefz et al 20133a, Treftz et al 2013b). В обоих исследованиях гиперкалиемия была связана с серьезностью обезвоживания, о чем свидетельствуют азотемия, гиперфосфатемия и L-лактоацидоз. Азотемия может быть преренальной в результате гиповолемии или сочетанием преренальной и вторичной почечной азотемии.Гиперфосфатемию приписывали азотемии и ацидемии, вызывающей распад внутриклеточного органического фосфата (который предположительно превращается в неорганический фосфат). Гиперкалиемия у этих телят объяснялась снижением почечной экскреции, в основном из-за гиповолемии (из-за связи с азотемией и L-лактоацидозом), с возможным вкладом ацидемии. Гиповолемия будет способствовать проксимальной почечной резорбции натрия, уменьшая дистальную доставку и скорость дистального кровотока, что приводит к задержке калия (поскольку экскреция зависит от скорости потока, а более высокая скорость потока приводит к большей экскреции).Ацидемия также будет способствовать дистальной экскреции калия с помощью механизмов, указанных ниже. Гиперкалиемия не была связана с D-лактоацидозом (например, употребление алкоголя в рубце), который действительно вызывает ацидемию, но не связан с гиповолемией. Отсутствие связи между гиперкалиемией и D-лактоацидозом было постулировано как вторичное по отношению к отсутствию обезвоживания при последнем синдроме в сочетании с облигатной потерей калия с D-лактатом, который выводится почками (Trefz et al 2013a). Несмотря на то, что уровни альдостерона положительно коррелируют с концентрацией калия у этих телят (Trefz and Lorenz, 2017), другие почечные реакции (предположительно из-за гиповолемии и L-лактат-ацидоза), вероятно, преобладают.Также возможно, что у этих гиповолемических телят с диареей, в том числе с преренальной азотемией, снижена слюнная экскреция калия, что способствует гиперкалиемии.
- Уроабдомен : Собаки, кошки и лошади с мочеиспусканием часто имеют высокий уровень калия из-за пониженной почечной экскреции. Хотя у некоторых видов крупного рогатого скота с мочевым брюшком может быть гиперкалиемия (Смит и др., 1983, Хилтон и Трент, 1987), экспериментальная непроходимость мочевыводящих путей не приводила к гиперкалиемии, которую связывали с повышенной экскрецией калия со слюной (Сокетт и др., 1986).
- Болезнь Аддисона (гипоальдестеронизм) вызывает низкий уровень натрия и высокий уровень калия с соотношением натрий: калий <27: 1. Электролитные изменения (высокий K + , низкий Na + ), имитирующие болезнь Аддисона, можно увидеть при повторном дренировании грудных выпотов, тяжелой диарее (например, сальмонелле или инфекции власоглавов) и лимфангиосаркоме, хотя точный механизм неясен. Измерение отношения натрия к калию — это , а не , чувствительный или специфический диагностический тест для болезни Аддисона (это нормально при вариантах болезни Аддисона, при которых минералокортикоиды нормальны, а глюкокортикоиды недостаточны).Это чаще всего встречается у собак и редко у других видов. Сообщается, что у лошадей с хронической почечной недостаточностью может быть повышенный уровень калия, что объясняется вторичным гипоальдостеронизмом.
- Ацидоз (особенно при доминирующем нарушении) : Ацидоз (метаболический или респираторный) снижает выведение K + и способствует резорбции в дистальных отделах нефрона. Снижение экскреции происходит из-за снижения активности базолатерального Na / K насоса (который стимулирует выведение калия с мочой основными клетками дистального нефрона) и более высокого сопротивления (снижение проводимости) апикальной мембраны основных клеток.Снижение экскреции также считается вторичным по отношению к усилению почечного аммиагенеза — аммиак подавляет абсорбцию натрия эпителиальным каналом натрия в дистальных и собирательных канальцах (что связано с экскрецией калия основными клетками) и может влиять на просветные K-каналы, которые выделяют калий. в моче. Поглощение калия интеркалированными клетками также стимулируется посредством ацидоза, активирующего насос H / K (вызывающего выделение водорода из дистальных канальцев, соответствующую корректирующую реакцию на метаболический ацидоз и компенсаторную реакцию на респираторный ацидоз) в обмен на абсорбцию калия.Однако помните, что экскреция калия часто увеличивается при болезненных состояниях, связанных, в частности, с метаболическим ацидозом. Например, при гиповолемии, стимулирующей лактоацидоз, даже если ацидоз может способствовать абсорбции / снижению выведения калия (что приведет к увеличению содержания калия в крови), альдостерон и АДГ будут стимулировать резорбцию натрия и воды, а альдостерон — выведение калия. Таким образом, концентрация калия в крови будет отражать противоположные эффекты альдостерона (стимулируя выведение калия) и ацидоза (способствуя удержанию калия).У новорожденных телят с диареей, L-лактат-ацидозом и гиперкалиемией лактат, по-видимому, стимулирует удержание калия, несмотря на высокие концентрации альдостерона (Trefz and Lorenz 2017). В состояниях хронического ацидоза подавляется всасывание натрия (и воды) в проксимальных канальцах, что приводит к увеличению дистальной доставки натрия, скорости дистального потока и экскреции калия, что способствует гипокалиемии в крови (Hamm et al 2013).
- Механизмы прочие
- Снижение слюноотделения : Заметное обезвоживание у жвачных животных может вызвать гиперкалиемию из-за снижения выработки слюны, особенно при сопутствующей почечной дисфункции.Это нечасто, поскольку у крупного рогатого скота с анорексией часто бывает низкий уровень калия, который компенсирует любое увеличение от снижения выработки слюны.
- Трансклеточные сдвиги: Переход K + из внутриклеточной жидкости (ICF) в ECF происходит при значительном некрозе тканей, упражнениях (это происходит особенно у лошадей и связано с высвобождением K + из мышц, особенно скелетных мышц. которые имеют высокую массу; K + является местным сосудорасширяющим средством для мышечных клеток), уроперитонеум (у жеребят и мелких животных — смещается из брюшной полости, где моча с высоким содержанием K + , в кровь), гипертонус (т.е.г. сахарный диабет; возникает из-за увлечения растворителем), дефицита инсулина (например, сахарного диабета) и потенциально гиперхлоремического метаболического ацидоза (временная гиперкалиемия наблюдается после экспериментального введения хлорида аммония собакам). Большой анионный промежуток или метаболический ацидоз титрования (накопление нехлоридной кислоты, например, лактата, уремических фосфатных кислот) обычно не приводит к гиперкалиемии. Гиперкалиемия у животных с титровальным ацидозом обычно возникает не из-за транслокации, а, как полагают, из-за снижения почечной экскреции K + (см. Ниже).
Гипокалиемия
Гипокалиемия снижает мембранный потенциал покоя клеток (т.е. делает его более отрицательным, что гиперполяризует клетки, делая их менее чувствительными к стимулам, например, от -90 до -95). Это означает, что мышцы и нервы слабее и требуют более сильных стимулов для активации, что приводит к мышечной слабости и аритмии.Гипокалиемия также препятствует действию АДГ на почечные канальцы и изменяет кровоток через прямую вазу, истощая мозговой интерстиций растворенных веществ, что способствует нарушению способности к концентрации. Гипокалиемия также способствует (или усугубляет) или вызывает метаболический алкалоз (в состояниях хронической гипокалиемии, которая редко встречается в ветеринарии), стимулируя выведение водорода в проксимальных и дистальных канальцах. В проксимальном канальце стимулируются просветный насос Na / H и базолатеральный транспортер Na / бикарбоната, что приводит к чистой резорбции натрия и бикарбоната в обмен на потерю водорода.В дистальных канальцах стимулируются как люминальный насос Н / К, так и насос Н-АТФазы, что приводит к выведению водорода в обмен на абсорбцию калия. При уже существующем метаболическом алкалозе (например, смещении сычуга у жвачных животных) истощение запасов калия может усугубить алкалоз за счет стимуляции почечной экскреции водорода в проксимальных и дистальных канальцах (что усугубляется авидностью натрия в почках, что способствует резорбции натрия с бикарбонатом). (Хамм и др., 2013). Гипокалиемия обычно возникает из-за потери калия в желудочно-кишечном тракте или почках.Помните, что значения K + в крови не всегда являются отражением запасов K + всего тела; Значения K + в крови могут быть нормальными, несмотря на серьезный дефицит в целом в организме K + .
- Артефакт: Тяжелая липемия и, возможно, гиперглобулинемия (из-за иммуноглобулинов) может привести к легкой гипокалиемии (псевдогипокалиемии) из-за исключения растворителя / замещения объема при измерении калия с использованием разбавленной плазмы (непрямая потенциометрия; метод, обычно используемый для измерения электролитов) ).Этот артефакт можно преодолеть, используя неразбавленную плазму (прямая потенциометрия) для измерения калия (т. Е. Анализатор газов крови). Изменения калия с исключением растворителя намного меньше, чем изменения, наблюдаемые с натрием и хлоридом.
- Патофизиологический:
- Пониженное потребление: Это происходит при анорексии (не только при отсутствии аппетита или снижении аппетита) у крупных животных, включая лошадей (особенно жеребят), верблюдовых и коров (из-за их высокого потребления с пищей и высокой экскреции калия с мочой).Почки не могут снизить выведение калия достаточно быстро, чтобы предотвратить быстрое падение калия, которое происходит при анорексии у этих видов. Снижение потребления у мелких животных редко приводит к гипокалиемии, если не происходит дополнительных потерь калия. Гипокалиемия может наблюдаться у кошек, получающих диету с низким содержанием калия.
- Трансклеточные сдвиги: Сдвиг K + из ECF в ICF происходит при первичном респираторном или первичном метаболическом алкалозе, приводящем к алкалиемии (когда водород перемещается внеклеточно в обмен на калий), высвобождению инсулина (обычно всплески инсулина, такие как наблюдается после инфузии глюкозы или приема пищи) или введения, а также высвобождение катехоламинов (от адреналина, стимулирующего β2-адренорецепторы и активирующего натрий-калиевый [Na / K] АТФазный насос в мышцах).Точно так же эндотоксемия может также привести к гипокалиемии, поскольку эндотоксины также стимулируют насос Na / K-АТФазы в мышечных клетках и способствуют высвобождению инсулина. Трансцеллюлярный сдвиг из-за алкалиемии обычно вызывает небольшие изменения калия (если не происходит одновременных потерь калия). Гипокалиемия, возникающая при респираторном алкалозе, обычно носит временный характер и не наблюдается у людей с хроническим респираторным алкалозом.
- Увеличенные потери: Дефицит калия будет увеличиваться, если потребление калия уменьшится.
- Желудочно-кишечные потери: Причины включают рвоту желудочным содержимым (потеря хлорида увеличивает экскрецию K + в почках, способствуя гипокалиемии), сычужный застой (например, блуждающее пищеварение или атония), нарушение оттока или перекрут и диарея . Диарея у лошадей и крупного рогатого скота часто вызывает гипокалиемию. Сильная диарея и рвота у собак и кошек также могут привести к гипокалиемии. Слюна богата калием, и такие заболевания, как удушье у лошадей и крупного рогатого скота, могут привести к гипокалиемии.
- Потери / секвестрация третьего пространства: Накопление жидкости в полостях тела (например, перитонит) или растяжение желудочно-кишечной системы (например, заворот кишечника, кишечная непроходимость) может привести к гипокалиемии. Это может быть разжижением из-за ощущаемого истощения объема из-за потери жидкости из внутрисосудистого пространства, что приводит к секреции АДГ (задерживает воду в почках) и стимуляции жажды.
- Кожные потери: Потливость (лошади).
- Почечные потери: Почечные потери калия могут происходить через несколько механизмов, главным из которых является альдостерон, который стимулирует абсорбцию натрия в обмен на экскрецию калия в основных клетках поздних дистальных канальцев и собирательных канальцах.
- Альдостерон стимулируется ренин-ангиотензиновой системой в ответ на гиповолемию и снижение доставки хлорида (гипохлоремия) к плотному пятну. Гиперальдостеронизм — редкое заболевание, вызывающее тяжелую гипокалиемию у собак и кошек и обычно вторичное по отношению к неоплазии надпочечников (у собак) или гиперплазии (у кошек).
- Повышенная скорость кровотока в дистальных канальцах: Экскреция калия также усиливается за счет увеличения скорости кровотока в дистальных канальцах, то есть любой причины полиурии (например,г. осмотический диурез с глюкозурией, постобструктивный диурез)
- Повышенная электроотрицательность просвета , например высокие концентрации неадсорбируемых анионов в просвете почечных канальцев, например пенициллин, кетоны, уменьшают положительный заряд в просвете, что вызывает вывод положительно заряженного калия.
- Первичный метаболический алкалоз (особенно, если преобладает кислотно-щелочное нарушение со смешанными нарушениями или в состояниях алкалиемии): Водород выделяется из внутренних клеточных буферов (напр.г. гемоглобин) в кровь для буферизации накопленного бикарбоната. Для поддержания электронейтральности калий перемещается в клетки. В почечных канальцах это создаст градиент концентрации между клеткой и просветом почечных канальцев, который будет способствовать выведению калия в просвет. Кроме того, алкалоз увеличивает активность калиевых каналов в основных клетках (способствует выведению из организма). Выделению также будет способствовать повышение уровня бикарбоната в моче (увеличение электроотрицательности просвета) и низкий уровень хлорида мочи (часто наблюдается при метаболическом алкалозе — низкий уровень хлорида стимулирует активность просветного канала KCl в основной клетке) (Hamm et al 2013).
- Заболевание почечных канальцев: Истощение калия также происходит при заболевании почечных канальцев, которое препятствует нормальному всасыванию фильтрованного калия, например проксимальный почечный канальцевый ацидоз, хроническая болезнь почек у кошек.
- Петлевые диуретики : Они подавляют насос NaK2Cl в толстой восходящей конечности петли Генле. Отсутствие абсорбции K + усугубляется просветным K-каналом, который активно выделяет K + в мочу (что обычно требуется для правильной работы насоса NaK2Cl).
- Синдром гипокалиемии крупного рогатого скота : Молочный скот в первые 3 месяца после отела предрасположен к гипокалиемическому синдрому, который проявляется в слабости, лежачем положении, снижении мышечного тонуса и депрессии. Основная причина, по-видимому, заключается в применении изофлупреднонацетата, который оказывает минералокортикоидное действие, но анорексия и введение декстрозы или инсулина могут усугубить гипокалиемию. При тестировании обнаруживаются низкие концентрации калия (<2.2–2,5 мэкв / л), но может быть выше, если имеется сопутствующий некроз мышц (высвобождение внутримышечных запасов калия) у коров с депрессивным состоянием. Поскольку одновременно наблюдается мышечная слабость желудочно-кишечного тракта и застой рубца, пораженные животные также часто имеют первичный гипохлоремический метаболический алкалоз. Они могут быть одновременно гипофосфатемическими (механизм неясен). У пораженного крупного рогатого скота все еще наблюдается высокая экскреция калия с мочой, что неудивительно при введении изофлупреднонацетата, но при других обстоятельствах, например.г. анорексия может быть острым началом заболевания с продолжающейся высокой экскрецией калия с мочой (Sattler and Fecteau, 2014).
Список литературы
- Kardalos et al 2018: Гипокалиемия: обновленная клиническая информация. Endocr Connect 7: R135.
- Rose BD и Post DW. Клиническая физиология кислотно-основных и электролитных нарушений, 5-е издание, 2001 г. McGraw-Hill, Нью-Йорк, штат Нью-Йорк.
- Дибартола СП. Расстройства жидкости, электролитов и кислотно-щелочного баланса в практике мелких животных, 4-е издание, 2012 г.Эльзевье-Сондерс, Сент-Луис, Миссури.
- Gennari 2011. Патофизиология метаболического алкалоза: новая классификация, основанная на центральности стимулированного транспорта ионов собирающего протока.