Сон и гормоны
Сон и гормоны
Foto: Shutterstock
Соблюдение циркадных ритмов достигается при помощи гормонов.
Мелатонин
Главный гормон сна, который в основном вырабатывается с 12 часов ночи до 4 часов утра. По ночам по сравнению с дневным временем его синтез возрастает в 30 раз. Пик приходится на 2 часа ночи. Мелатонин регулирует циркадные ритмы, нормализует гормональный фон и артериальное давление, влияет на иммунную систему и др.
Соматотропин
Гормон роста. Хотя цикл его производства имеет периодичность 4-5 часов, максимальное количество соматотропина мы получаем в период сна, через 1-2 часа после засыпания. Гормон влияет на регенерацию клеток, ускоряет заживление ран, участвует в формировании костной ткани и укрепляет иммунитет.
Тестостерон
Половой гормон, отвечающий за «мужские» репродуктивные функции и массу других процессов. Максимум выработки приходится на период сна.
Фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ) гормоны
Гормоны, влияющие на репродуктивную функцию женщин и другие процессы. Максимум выработки приходится на период сна.
Лептин
Гормон сытости, который вырабатывают адипоциты (жировые клетки). При дефиците сна его выработка падает на 20%, а чем меньше лептина, тем сильнее чувство голода.
Грелин
Гормон голода, который регулирует аппетит. Если человек спит свою норма сна, то уровень грелина в плазме крови снижается — и аппетит слабеет.
Кортизол
Гормон стресса. В норме он поддерживает уровень глюкозы в крови при голодании и артериальное давление при стрессах. Когда его слишком мало — наша работоспособность на нуле. Когда его слишком много (во время стрессовой ситуации) — мы ненормально активны. Но длительно повышенный уровень кортизола чреват облысением, ухудшением качества кожи и сосудов. Днем мы активно расходуем кортизол, а ночью восстанавливаем его до нормы.
Аденома гипофиза
Гипофиз — это главная эндокринная железа организма,вес которой не более 1 грамма. . Гипофиз выделяет важнейшие регуляторные гормоны:
- гормон роста (соматотропный гормон) – стимулирует рост скелета и мягких тканей; участвует в регуляции энергетического и минерального обмена.
- тиреотропин – стимулирует синтез йодтиронинов.
- пролактин – стимулирует лактацию.
- лютеинизирующий гормон – у женщин индуцирует овуляцию, у мужчин – синтез андрогенов.
- фолликулостимулирующий гормон – у женщин стимулирует рост фолликулов, у мужчин – сперматогенез.
- кортикотропин (адренокортикотропный гормон) – стимулирует рост надпочечников и синтез кортикостероидов.
- В-липотропин – стимулирует липолиз.
- мелатропин – синтез меланинов кожи, радужной оболочки.
В норме гормоны выделяются точно в таком количестве, которое необходимо для поддержания нормальной работы организма.
К нарушению функции гипофиза могут приводить различные опухоли гипофиза, гипоталамуса и окружающих структур. Опухолевые заболевания гипофиза в большинстве случаев являются аденомами, т.е. доброкачественными опухолями — клетки гипофиза, выросший в результате неконтролируемого роста этих клеток. Причины образования и роста аденом гипофиза до конца не изучены.
Аденомы гипофиза могут быть опасны и вызывать определенные изменения в организме человека:
- Клетки аденомы могут вырабатывать в избытке какой-либо гормон. Пролактинома — вырабатывает пролактин, кортикотропинома — вырабатывает адренокортикотропный гормон, соматотропинома — вырабатывает соматотропный гормон, тиротропинома — крайне редкая опухоль, выделяет тиреотропный гормон, гонадотропинома вырабатывает лютеинизурующий гормон ЛГ и/или фолликулостимулирующий гормон ФСГ.
- Аденома может быть причиной повреждения «рабочих клеток» гипофиза, что приводит к снижению выработки гормонов гипофиза и также нарушениям обмена веществ.

- Крупные аденомы могут сдавливать ткани головного мозга, вызывая зрительные и другие неврологические нарушения.
Все эти изменения и будут являться основными симптомами аденомы гипофиза.
Диагностика аденомы гипофиза.
Золотым стандартом инструментального метода диагностики аденомы гипофиза является — магнитно-резонансная томография, которая позволяет выявить аденомы размерами менее 5 мм, однако, даже с учётом этого, примерно у 25—45% пациентов визуализировать аденому не удаётся.
Применяют также и компьютерную томографию, но реже, в основном в экстренных случаях.
Кроме этих методов важное исследование — это биохимический анализ крови на гормоны. Он позволяет на ранних стадиях развития аденомы заподозрить ее наличие. Анализы покажут, повышенная или пониженная функция у гипофиза. Обычно определяют уровень таких гормонов, как АКТ, кортизол, ТТГ, Т4, ЛГ, ФСГ, у женщин — эстрадиол, у мужчин — тестостерон, соматотропин, соматомедин-С (инсулиноподобный фактор роста-1), а также пролактин.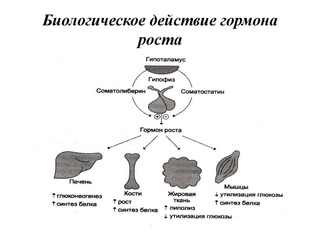
При нарушениях зрения проводится также консультация офтальмолога. При этом может потребоватся проверка зрения с оценкой периферических полей зрения.
Лечение аденомы гипофиза.
Лечение аденом гипофиза производится с применением:
— лекарственного метода;
— лучевой терапии;
— хирургического метода.
Лечением аденомы гипофиза занимается врач-нейрохирург, врач-онколог, врач-эндокринолог.
В каждом отдельном случае, для каждой из разновидностей опухоли гипофиза подбирается индивидуальный вариант лечения.
Прогноз
Прогноз во многом зависит от размеров опухоли (возможности ее радикального удаления) и ее гормональной функции.
При пролактиномах и соматотропиномах «гормональное» выздоровление наблюдают в 20-25% случаев, при микрокортикотропиномах — в 85% случаев (при опухолях размером более 1 см — значительно реже).
Считается, что макроаденому гипофиза с распространением более 2 см невозможно удалить полностью, поэтому в течение ближайших 5 лет после операции возможно возникновение рецидива.
Возврат к списку
что такое гормоны сна и как они влияют на нас (мнение эксперта)
Как известно, регулятором практически всех процессов в организме являются гормоны. Это же касается и нашего крепкого сна — благодаря выработке определенных гормонов вы засыпаем и можем восстанавливаться после насыщенного дня. Мы решили выяснить у профессионального эксперта, почему же так важно ложиться спать до полуночи, что происходит в организме в это время, какие гормоны вырабатываются и как они влияют на наше состояние в течение всего дня.
Мнение эксперта
Юлия Хурумова, эксперт Beauty Sleep
«Самый важный гормон, который принято называть гормоном сна, и мы все о нем неоднократно слышали, — мелатонин. Именно он вырабатывается исключительно в темноте, причем в полной, и даже если вы закрыли глаза, но на них падает свет — выработка гормона приостанавливается».
Именно он вырабатывается исключительно в темноте, причем в полной, и даже если вы закрыли глаза, но на них падает свет — выработка гормона приостанавливается».
Мелатонин защищает организм от депрессии, от нарушения обмена веществ, простудных заболеваний, а также замедляет старение. Стоит отметить, что выработку мелатонина снижают гаджеты, поэтому скроллить ленту инстаграма перед сном — плохая идея.
Интересный факт: процесс выработки начинается примерно с восьми вечера, а пик его концентрации (порядка 70%) приходится на период после полуночи и до четырех часов утра.
Второй гормон, который оказывает существенное влияние на наш сон, кортизол — гормон стресса. За счет него мы пробуждаемся, своего пика он достигает как раз ранним утром после трех часов. И кажется, что все максимально понятно, но представьте, что вы уснули как раз в районе 2–3 часов ночи, мелатонина у вас выработалось мало, а кортизол уже начинает продуцироваться по расписанию, но, учитывая, что вы не успели выспаться и, вероятнее всего, будете в таком случае спать до 9–10 утра, выработка кортизола все это время не будет прекращаться. Если вы живете в таком режиме регулярно, то депрессии и стресса не избежать.
Если вы живете в таком режиме регулярно, то депрессии и стресса не избежать.
Соматотропин (гормон роста и сжигания жира) — еще один немаловажный гормон, 70% которого вырабатывается именно во время сна, пик его выработки происходит в те же интервалы, что и у мелатонина: приблизительно с полуночи до 2–3 часов. Именно он помогает эффективно сжигать жир и худеть во сне. Поэтому, если у вас стоит проблема сброса веса, нужно обращать внимание на режим сна, возможно, именно этого гормона вам не хватает для грамотного похудения.
Известный нам серотонин выполняет роль «включателя и будильника» нашего организма. Ночью этот гормон продуцируется в мозге и достигает своего максимума в промежутке с шести до восьми часов утра. Далее его уровень постепенно понижается. Серотонин отвечает за хорошее настроение, бодрость и сытость. Поэтому если вы мало спали ночью, то серотонина в организме не хватает. Вот почему после бессонной ночи мы чувствуем себя разбитыми, недовольными и плюс постоянно хотим что-то съесть.
Вы наверняка замечали, что вечером руки так и тянутся к холодильнику, а глаза — к любимому сериалу. Причем такое желание почему-то не возникает утром. Все дело в дофамине — гормоне удовольствия. Он вырабатывается в течение всего дня, и если работа других гормонов (например, лептинов) нарушена и происходит недостаток «дневных удовольствий», вечером наша чувствительность к дофамину становится высокой и нас начинает тянуть к вечерним развлечениям, сладостям, активностям и так далее — из-за этого происходят недосыпание и сбой в работе гормонов.
Чтобы высыпаться и чувствовать бодрость и прилив сил с самого раннего утра, следует соблюдать гигиену сна. Во-первых, старайтесь ложиться спать до полуночи — конечно же, мы понимаем, что с нашим активным ритмом жизни это крайне непросто, но стоит лишь начать, и вы заметите большую разницу в вашем самочувствии.
Создавайте все условия для выработки мелатонина: после восьми вечера приглушите свет, а перед сном плотно зашторивайте занавески и выключите вообще все источники света, чтобы в комнате была полная темнота.
Да, даже едва уловимый свет от часов (зарядного устройства) тоже надо убрать. Также попробуйте начать использовать ночную бьюти-маску из шелка — она поможет заблокировать свет, а ее натуральный материал отлично подходит для нежной кожи вокруг глаз.
Еще один полезный вариант, который способствует выработке гормонов серотонина, дофамина и эндорфинов — специальное утяжеленное одеяло с наполнителем из стеклянных микрогранул, создающее ощущение «материнских объятий». Тем самым вы быстрее расслабитесь, успокоитесь и крепко уснете.
Крайне важно, чтобы ваша подушка обеспечивала правильное положение шеи во время ночного отдыха. Особенно удобно использовать анатомическую бьюти-подушку со специальным валиком поддержки шеи. Специфика такого валика заключается в том, что он повторяет рельеф шейно-воротниковой зоны и дает возможность спать в разных позах не только с пользой для шеи, но и с максимальным комфортом. Высота валика увеличивается от центра к краям для правильного положения шеи в позах на спине и боку. Вместе с этим вы получаете и приятный бонус для кожи — специальные выемки по краям защищают нежную кожу лица от растягивания и сдавливания во время сна на боку. Поэтому можно не бояться морщин сна, утренней отечности и не выбирать между «полезно для шеи» и «хорошо для кожи».
Вместе с этим вы получаете и приятный бонус для кожи — специальные выемки по краям защищают нежную кожу лица от растягивания и сдавливания во время сна на боку. Поэтому можно не бояться морщин сна, утренней отечности и не выбирать между «полезно для шеи» и «хорошо для кожи».
Также, чтобы правильно и комфортно спать, не следует употреблять пищу минимум за 2–3 часа до сна и пить сладкие газированные или алкогольные напитки, которые станут причиной отечности.
А утром при пробуждении возьмите в привычку выпивать большой стакан простой очищенной воды (в холодное время года лучше теплой и с лимоном) — так вы запустите процесс работы организма после ночного отдыха и настроите его на правильное функционирование в течение дня.
Читайте также: Идеальный уикенд для трудоголика: как главный редактор InStyle нашла способ восстановить силы за 3 дня
Источник фотографий: архив пресс-служб, кадры из мультфильма «Холодное сердце»
о продуктах с высоким содержанием кальция и других факторах роста
«Будь здоров, расти большой!» — такие слова хотя бы раз говорил своему ребенку, наверное, каждый родитель. Но специалисты утверждают, что такие пожелания, даже самые чистосердечные, на росте ребенка никак не сказываются. А что сказывается?
Но специалисты утверждают, что такие пожелания, даже самые чистосердечные, на росте ребенка никак не сказываются. А что сказывается?
Конечно, наследственность, роль которой очень важна. Вероятность того, что у невысоких мамы с папой вырастет сын-баскетболист или дочь-модель, невелика (впрочем, бывают и исключения). Но существуют и другие факторы.
Правильное питание и полезные продукты способствующие росту ребенка
Один из таких факторов — правильное питание. В рационе ребенка обязательно должны присутствовать продукты с достаточным содержанием кальция; для нормального роста ребенку 3−4 лет необходимо примерно 800 мг данного вещества в сутки.
Почему кальций так важен? Ответить на этот вопрос нетрудно. Кальций содержится в костной ткани, более того, является преобладающим в ней веществом. Если содержание кальция будет слишком мало, скелет ребенка не сможет формироваться правильно, кости станут хрупкими; о каком уж нормальном росте тут можно говорить.
К счастью, кальций — не такое уж редкое вещество. Оптимальным для ребенка является содержание кальция в молоке (300 мг в одном стакане) и молочных продуктах, йогуртах (около 150 мг в 100 г), твердых сырах (около 600 мг в 100 г). Кальция также много в рыбе и морепродуктах, бобовых, орехах, зеленых овощах, яйцах. Для хорошего усвоения кальция необходим витамин D — тот самый, который вырабатывается в нашем организме под воздействием солнечных лучей. Высокое содержание этого витамина обнаружено в сельди, сардинах, макрели, лососе, тунце, яйцах, печени, молоке и молочных продуктах.
Надежным способом обеспечить ребенка достаточным количеством необходимых веществ являются специальные продукты с высоким содержанием кальция — такие, как лакомства серии «Растишка», которую производит компания Danone. «Растишка» — это обогащенные кальцием и витамином D йогурты, творожки и молочные коктейли, которые производятся из свежего молока и фруктового пюре без добавления консервантов и искусственных красителей. Дети, впрочем, любят «Растишку» не за пользу, а за вкус, и это тоже хорошо: продуктами с высоким содержанием кальция можно заменить вредные кондитерские изделия и сладкие напитки.
Дети, впрочем, любят «Растишку» не за пользу, а за вкус, и это тоже хорошо: продуктами с высоким содержанием кальция можно заменить вредные кондитерские изделия и сладкие напитки.
Но, как говорится, не кальцием единым. Для роста ребенку также необходимы белки: продукты с высоким содержанием этих веществ — мясо, рыба, творог, сыр, яйца, овощи, крупы, злаки. Очень важен для роста витамин, А — в нем нуждаются клетки хрящевой ткани. Много витамина, А содержит морковь, богаты им также красный перец, зеленый лук, салат, помидоры, тыква. Чтобы витамин, А хорошо усваивался, все эти продукты лучше давать ребенку с растительным маслом или сметаной. Значительную роль играет и образ жизни. Для нормального роста (да и для развития в целом) ребенку нужно много гулять, играть в подвижные игры. Недостаток физических нагрузок и свежего воздуха — это препятствие для нормального роста.
Физиологические и психологические факторы
Нельзя не сказать и о сне, ведь большая часть соматотропина, гормона роста, вырабатывается именно тогда, когда ребенок спит.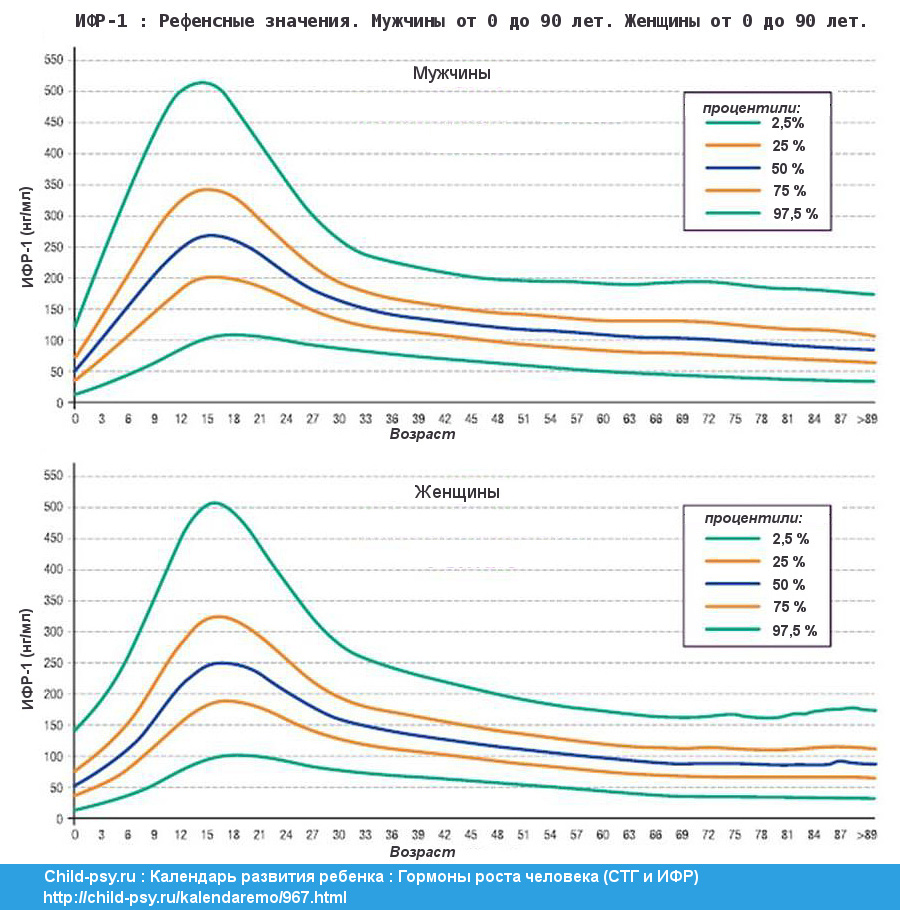 Поэтому следите за тем, чтобы ребенок соблюдал режим дня и высыпался, даже если ради этого придется пожертвовать любимыми мультфильмами. Врачи отмечают также важность атмосферы в семье: ребенку очень трудно расти большим, если он лишен психологического комфорта, любви и заботы родителей.
Поэтому следите за тем, чтобы ребенок соблюдал режим дня и высыпался, даже если ради этого придется пожертвовать любимыми мультфильмами. Врачи отмечают также важность атмосферы в семье: ребенку очень трудно расти большим, если он лишен психологического комфорта, любви и заботы родителей.
Надо сказать, что есть и чисто медицинские факторы, с которыми даже самые внимательные родители не смогут справиться без врача. Рост ребенка зависит от ряда гормонов (гормона передней доли гипофиза, уже упомянутого соматотропина, инсулина, половых гормонов). Если их вырабатывается слишком много или слишком мало, потребуется вмешательство специалистов.
Средний рост трехлетнего ребенка — от 92 см до метра, за год дети вырастают на 4−6 см. Высокими считаются дети, которые к трем годам достигают 1 м 4 см, маленькими — те, чей рост составляет 89−91 см. Если рост ребенка на 20% меньше нормы, это может быть признаком серьезного расстройства, нужно обратиться к эндокринологу.
Влияние физических нагрузок на организм спортсмена.
 Гормоны и физическая нагрузка.
Гормоны и физическая нагрузка.
Гормоны играют крайне важную роль в работе человеческого организма. Эти вещества стимулируют работу определенных клеток и систем организма. Гормоны производятся эндокринными железами и определенными тканями.
Из широкого спектра гормонов особую важность имеют анаболические и катаболические гормоны. Катаболизм – это процесс метаболического распада клеток и тканей, а также разложения сложных структур с выделением энергии в виде тепла или в виде аденозинтрифосфата. Катаболические процессы обеспечивают высвобождение большого количества энергии.
Анаболические процессы противоположны катаболическим. Под анаболическими процессами подразумевают процессы создания клеток и тканей, а также веществ, необходимых для работы организма. Течение регенеративных процессов и анаболизм мышечной ткани во многом зависят от уровня гормона роста, инсулина и тестостерона в плазме крови.
Физическая активность существенно повышает концентрацию множества гормонов в плазме крови и не только непосредственно в момент нагрузки. С начала выполнения упражнения (напр. около максимальной мощности), за первые 4-10 минут концентрация различных гормонов и продуктов метаболизма меняется самопроизвольно. Так с началом упражнения растет концентрация молочной кислоты в крови. А концентрация глюкозы начинает меняться обратно пропорционально концентрации молочной кислоты. При увеличении времени нагрузки в крови растет уровень соматотропина.
С начала выполнения упражнения (напр. около максимальной мощности), за первые 4-10 минут концентрация различных гормонов и продуктов метаболизма меняется самопроизвольно. Так с началом упражнения растет концентрация молочной кислоты в крови. А концентрация глюкозы начинает меняться обратно пропорционально концентрации молочной кислоты. При увеличении времени нагрузки в крови растет уровень соматотропина.
Другие исследования продемонстрировали, что у людей преклонного возраста (65-75 лет) после занятий на велотренажере уровень тестостерона увеличивался на 40%. Специалисты геронтологии полагают, что именно сохранение нормальной концентрации тестостерона обеспечивает бодрое, энергичное состояние в преклонные годы и, вероятно, увеличивает продолжительность жизни.
Секрецию гормонов и их попадание в кровь при физических упражнениях можно представить в виде каскада реакций. Физическое напряжение как стресс провоцирует выделение в структурах мозга либеринов, которые, в свою очередь, запускают производство тропинов гипофизом. Через кровь тропины проникают в эндокринные железы, где и осуществляется секреция гормонов.
Через кровь тропины проникают в эндокринные железы, где и осуществляется секреция гормонов.
Катаболизм обусловлен наличием в крови множества факторов, участвующих в высвобождении энергии. Один из этих факторов – кортизол. Этот гормон помогает при стрессах. Однако слишком высокий уровень кортизола нежелателен: начинается расщепление клеток мышц, нарушается доставка в них аминокислот. Совершенно ясно, что в таких условиях при попадании в организм протеинов они не смогут принять участие в анаболизме, а будут либо интенсивно выбрасываться с мочой, либо превращаться печенью в глюкозу. Еще одна отрицательная роль кортизола проявляется в его воздействии на сахаридный метаболизм в период отдыха после упражнения, когда спортсмен желает скорее восстановить силы. Кортизол ингибирует скопление гликогена в мышечной ткани. Увы, кортизол производится в человеческом организме во время тяжелых тренировок. Интенсивные тренировки, высокая физическая нагрузка – это всё стресс. Кортизол выполняет одну из главных ролей при стрессах.
Кортизол выполняет одну из главных ролей при стрессах.
Устранить катаболический эффект кортизола можно с применением анаболических стероидов. Но этот метод – крайне вреден для здоровья. Побочные явления столь опасны, что спортсмену следует найти другие эффективные анаболики, легальные и не вызывающие побочных эффектов. Получение организмом большого количества сахаридов в результате анаболической активности инсулина также благоприятствует быстрому восстановлению. Выяснилось, что и в данном случае эффект достигается ингибированием активности кортизола. Концентрация инсулина обратно пропорциональна концентрации кортизола в крови. Инсулин является полипептидным гормоном и необходим в объединении путей энергоснабжения. Анаболизм инсулина затрагивает мышечную, жировую ткань и печень. Инсулин стимулирует образование гликогена, алифатических кислот и протеинов. Также инсулин ускоряет гликолиз.
Сам механизм анаболизма инсулина состоит в ускорении попадания глюкозы и свободных аминокислот в клетки. Однако процессы образования гликогена, активируемые инсулином, провоцируют уменьшение концентрации глюкозы в крови (основной симптом гипогликемии). Инсулин замедляет катаболизм в организме, в т.ч. разложение гликогена и нейтрального жира. Ускорение анаболизма в организме, то, чего хотят большинство культуристов, возможно и без применения допинг-средств типа анаболических стероидов.
Однако процессы образования гликогена, активируемые инсулином, провоцируют уменьшение концентрации глюкозы в крови (основной симптом гипогликемии). Инсулин замедляет катаболизм в организме, в т.ч. разложение гликогена и нейтрального жира. Ускорение анаболизма в организме, то, чего хотят большинство культуристов, возможно и без применения допинг-средств типа анаболических стероидов.
Одним из важнейших агентов, активирующих производство протеина, является прогормон – соматомедин С. Специалисты утверждают, что образование этого вещества стимулируется соматотропином и осуществляется в печени и мышечной ткани. Производство соматомедина С в определенной степени зависит от объёма аминокислот, получаемых организмом. Гормоны с анаболическим эффектом после физических упражнений выполняют еще одну задачу. В результате исследований было выяснено, что при физических нагрузках волокна мышц повреждаются. Под микроскопом на специально подготовленных образцах мышечной ткани можно увидеть частые надрывы и полные разрывы волокон мышц. Факторов столь деструктивного эффекта нагрузки несколько. Первые гипотезы специалистов были связаны с деструктивным эффектом катаболических гормонов. Позже также было обосновано деструктивное воздействие свободных окислителей.
Факторов столь деструктивного эффекта нагрузки несколько. Первые гипотезы специалистов были связаны с деструктивным эффектом катаболических гормонов. Позже также было обосновано деструктивное воздействие свободных окислителей.
Эндокринная система управляет всеми видами метаболизма и, в зависимости от ситуации, может активировать резервные силы организма. Она же контролирует восстановление после тяжелых физических упражнений. Причем реакции гормональных систем сильно отличаются в соответствии со степенью нагрузки (большой или умеренной мощности).
При нагрузке умеренной мощности и долгой тренировке увеличивается уровень гормона роста и кортизола, падает уровень инсулина и увеличивается уровень трииодтиронина.
Нагрузке большой мощности сопутствует увеличение концентрации гормона роста, кортизола, инсулина и Т3. Гормон роста и кортизол обуславливают развитие специальной работоспособности, и поэтому увеличение их концентрации во время разных тренировочных циклов сопровождается улучшением спортивных показателей спортсмена.
В результате многих исследований специалистов было выяснено, что у профессиональных бегунов на сверхдальние дистанции в спокойном состоянии обнаруживается низкая или нормальная концентрация гормона роста. Однако при марафоновском забеге уровень гормона роста в крови сильно увеличивается, что обеспечивает высокую работоспособность на продолжительный срок. Гормон роста (соматотропин) – гормон, отвечающий за анаболизм в организме (рост, развитие, увеличение веса тела и различных органов). В организме взрослого человека воздействие гормона роста на функции роста в большей степени теряется, а на анаболические функции (образование протеина, сахаридный и жировой обмены) остается. Это и является причиной запрета соматотропного гормона как допинга.
Другим немаловажным гормоном адаптации служит кортизол, который отвечает за сахаридный и протеиновый метаболизм. Кортизол контролирует работоспособность путем катаболического процесса, при котором печень снабжается гликогеном и кетогенными аминокислотами. Вместе с катаболическим процессом (остановка производства протеина в лимфоидной и соединительной тканях) осуществляется сохранение концентрации глюкозы в плазме крови спортсмена на достаточном уровне. Данный гормон также запрещен в качестве допинга. Инсулин управляет концентрацией глюкозы и ее перемещением через мембраны мышечных и других клеток. Уровень инсулина в норме – 5-20 мкед/мл. Нехватка инсулина снижает работоспособность вследствие уменьшения количества глюкозы, доставляемой в клетки.
Вместе с катаболическим процессом (остановка производства протеина в лимфоидной и соединительной тканях) осуществляется сохранение концентрации глюкозы в плазме крови спортсмена на достаточном уровне. Данный гормон также запрещен в качестве допинга. Инсулин управляет концентрацией глюкозы и ее перемещением через мембраны мышечных и других клеток. Уровень инсулина в норме – 5-20 мкед/мл. Нехватка инсулина снижает работоспособность вследствие уменьшения количества глюкозы, доставляемой в клетки.
Выделение инсулина стимулируется при упражнениях большой мощности, что обеспечивает высокую проницаемость клеточных мембран для глюкозы (стимулируется гликолиз). Работоспособность достигается благодаря сахаридному обмену. При умеренной мощности упражнений уровень инсулина падает, что приводит к переходу с сахаридного метаболизма на липидный, что столь востребовано при продолжительной физической активности, когда резервы гликогена частично израсходованы.
Тиреоидные гормоны тироксин и трииодтиронин управляют основным метаболизмом, расходом кислорода и окислительным фосфорилированием. Изменение уровня тиреоидных гормонов определяет предел работоспособности и выносливости человека (возникает дисбаланс между получением кислорода и фосфорилированием, замедляется окислительное фосфорилирование в митохондриях мышечных клеток, замедляется ресинтез аденозинтрифосфата). Обследования бегунов на сверхдальние дистанции продемонстрировали связь между работоспособностью и соотношением гормона роста и кортизола.
Изменение уровня тиреоидных гормонов определяет предел работоспособности и выносливости человека (возникает дисбаланс между получением кислорода и фосфорилированием, замедляется окислительное фосфорилирование в митохондриях мышечных клеток, замедляется ресинтез аденозинтрифосфата). Обследования бегунов на сверхдальние дистанции продемонстрировали связь между работоспособностью и соотношением гормона роста и кортизола.
Обследование эндокринной системы определенного спортсмена позволяет определить его возможности и готовность выдержать физическую нагрузку с лучшими показателями. Другим существенным аспектом предсказания специальной работоспособности служит выявление способностей коры надпочечников производить кортизол в ответ на раздражение адренокортикотропным гормоном. Повышенное производство кортизола говорит о способности спортсмена работать в оптимальном режиме.
Спортивная работоспособность разных полов существенно зависит от тестостерона. Этот гормон обуславливает агрессию, темперамент и целеустремленность при исполнении задания. Гормональные средства (тестостерон и его вариации, анаболические стероиды, гормон роста, кортикотропин, гонадотропный гормон, эритропоэтин) искусственно увеличивают работоспособность человека, и поэтому считаются допингом и запрещены к употреблению в соревнованиях и на тренировках.
Гормональные средства (тестостерон и его вариации, анаболические стероиды, гормон роста, кортикотропин, гонадотропный гормон, эритропоэтин) искусственно увеличивают работоспособность человека, и поэтому считаются допингом и запрещены к употреблению в соревнованиях и на тренировках.
Зачастую употребление препаратов гормонов идет вразрез со здоровым образом жизни и в конечном счете может привести к тяжелым патологиям.
Статья подготовлена главным врачом ГУЗ «ОВФД»
Николаевой И.В.
диетолог назвал продукты для эффективного похудения во сне
Те, кто следует рекомендациям диетологов, уверены, что есть после шести вечера нельзя. Но некоторые специалисты считают, что поздний ужин допустим. Какая еда помогает сжигать лишний жир во сне, телеканалу «МИР 24» рассказал врач-диетолог, доктор медицинских наук, профессор Алексей Ковальков.
— Все же можно или нельзя есть на ночь?
Алексей Ковальков: Примерно с 12 часов ночи у нас вырабатывается важный гормон – гормон роста. Это самый сильный жиросжигающий гормон. Он существует всего 50 минут, за это время способен сжигать 150 граммов жировой ткани. Мы худеем во сне. Но есть инсулин, который запускается, в основном, углеводами. Поэтому если мы перед сном съедаем углеводы, мы блокируем соматотропный гормон, и все будет плохо.
Будет хорошо, если вы будете есть перед сном мясные продукты, белковые. Я рекомендую пациентам два яичных белка. Желтки выбрасываем, яичные белки варим, жарим, готовим с чесноком, с укропом, съедаем прямо перед сном. Они содержат аминокислоты, которые как раз стимулируют выработку ценного соматотропного гормона, или гормона роста. Благодаря этому мы худеем во сне. Есть перед сном не только можно, но и нужно. Чем раньше ко сну, тем лучше. Организм сжигает за ночь 150 граммов жировой ткани. Это легко проверить. Вы встаете на весы перед тем, как лечь в кровать, и сразу утром, и 150-300 граммов у вас улетает за ночь. Из них 150 граммов – жировая ткань.
Из них 150 граммов – жировая ткань.
— Есть ли способ растянуть действие гормона-жиросжигателя или сделать его еще более активным?
Алексей Ковальков: Он вырабатывается только в двух случаях: по ночам, в фазу глубокого сна, когда вы спите. Есть яичные белки и играть на компьютере – соматотропный гормон не выделится. И второе – фаза асфиксии, когда вы задыхаетесь, например, на беговой дорожке. Если вы усиленно работаете в спортзале, вы сжигаете жиры.
— Кто главный враг соматотропина?
Алексей Ковальков: Инсулин. Если вы перед залом или перед сном съедаете продукт, содержащий углеводы, например, бананы или яблоко, или кашу, даже если вы молочные продукты с высоким индексом едите – тот же кефир, то инсулин, который выделяется на кефир или йогурт, заблокирует действие важного гормона.
— Какой инсулиновый индекс можно считать высоким?
Алексей Ковальков: Инсулиновый индекс после 50 можно считать высоким. Есть таблица, которая показывает инсулиномические индексы. Но она не совсем точная, потому что у каждого человека поджелудочная железа реагирует по-разному. У одного на один и тот же продукт она выбрасывает много инсулина, у другого – мало. В среднем значения сохраняются. Вы их можете найти в интернете.
Есть таблица, которая показывает инсулиномические индексы. Но она не совсем точная, потому что у каждого человека поджелудочная железа реагирует по-разному. У одного на один и тот же продукт она выбрасывает много инсулина, у другого – мало. В среднем значения сохраняются. Вы их можете найти в интернете.
Что можно есть безбоязненно? Белковые продукты, кусочек мяса, рыбы, сыра. Но лучше всего яичный белок – золотой эталон диетологии. Неважно, куриные яйца, перепелиные. Если куриные, это два белка. Если перепелиные, примерно 6.
— Правда ли, что картофель фри имеет высокий инсулиновый индекс, а овсянка – низкий?
Алексей Ковальков: Неважно, вкусный продукт или невкусный. Важен фактор выделения инсулина. Если он выделяется, значит, соматотропный гормон блокируется. Овсянка имеет тоже достаточно высокий индекс. Даже кислый лимон имеет высокий индекс, мандарины, хурма.
Чтобы не ошибиться, уберите все фрукты, каши перед сном – за 4-5 часов до сна. Оставьте все белковые продукты – рыба, морепродукты, мясо. И овощи можно оставить – те, которые растут над землей, а не корнеплоды.
Оставьте все белковые продукты – рыба, морепродукты, мясо. И овощи можно оставить – те, которые растут над землей, а не корнеплоды.
— Большинство круп, фруктов, молочные продукты имеют высокий инсулиновый индекс? Когда их можно есть без вреда для здоровья и для талии?
Алексей Ковальков: Их можно есть, но только не вечером. Возвращаясь домой вечером, вы делаете себе стейк, филе-миньон, немножко салата, добавляете бальзамический уксус, столовую ложку нерафинированного оливкового масла – и у вас прекрасный ужин. Пусть он будет в 8-9 вечера – ничего страшного. Мясо переваривается долго и всю ночь поддерживает вас по аминокислотам. Клетки, которые разрушаются ночью, снова восстанавливаются, делятся за счет аминокислот, не считая влияния на соматотропный гормон.
— Что эффективнее работает для похудения: правильный поздний ужин или интервальные голодания?
Алексей Ковальков: Интервальное голодание предусматривает просто еду по интервалу: вы можете есть в 7, 8, 9 вечера. Но это не совсем правильно. Самое лучшее – классическая формула поддержки гормонального фона. Худеем мы или полнеем не от того, что мы едим, а от того, как организм вырабатывает на это определенные гормоны. В данном случае – соматотропный гормон и инсулин.
Но это не совсем правильно. Самое лучшее – классическая формула поддержки гормонального фона. Худеем мы или полнеем не от того, что мы едим, а от того, как организм вырабатывает на это определенные гормоны. В данном случае – соматотропный гормон и инсулин.
СОМАТОТРОПИН — это… Что такое СОМАТОТРОПИН?
(гормон роста, соматотропный гормон), белковый гормон. Молекула С. представляет собой одну полипептидную цепь, состоящую из 190-191 аминокислотных остатков (мол. м. ок. 22 тыс.). По хим. структуре, физ.-хим. и биол. св-вам С. сходен с пролактином и плацентарным лактогеном и поэтому объединяется с ними в одно семейство. Считается, что эти три гормона произошли в процессе эволюции из общего предшественника.
Установлена первичная структура С. человека и неск. видов животных. С. разной видовой принадлежности, обладая большими или меньшими различиями в аминокислотной последовательности, проявляют четкую структурную гомологию друг с другом.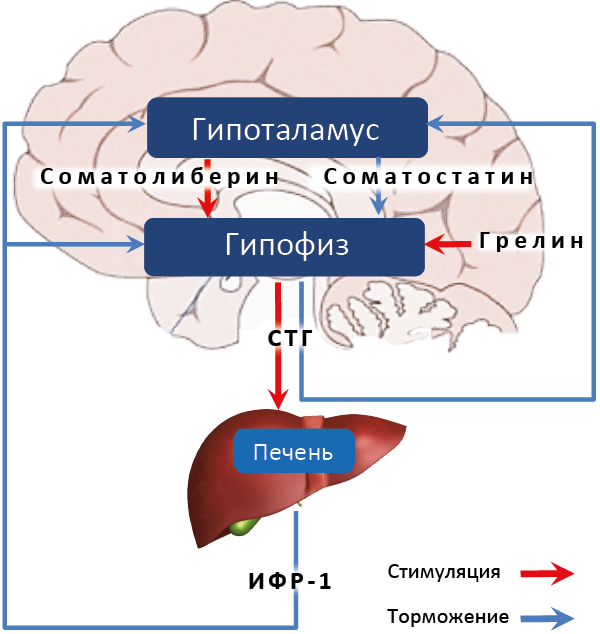 Все они содержат один остаток триптофана и 4 остатка цистеина. Последние образуют в молекуле два дисульфидных мостика, к-рые формируют две петли-большую, включающую центр. участок аминокислотной последовательности (в С. человека между цис-теином-54 и цистеином-165), и малую (на С-концевом участке между цистеином-182 и цистеином-189). Высокое содержание в молекуле С. остатков неполярных аминокислот обусловливает большую склонность к образованию в р-ре димеров и более крупных агрегатов.
Все они содержат один остаток триптофана и 4 остатка цистеина. Последние образуют в молекуле два дисульфидных мостика, к-рые формируют две петли-большую, включающую центр. участок аминокислотной последовательности (в С. человека между цис-теином-54 и цистеином-165), и малую (на С-концевом участке между цистеином-182 и цистеином-189). Высокое содержание в молекуле С. остатков неполярных аминокислот обусловливает большую склонность к образованию в р-ре димеров и более крупных агрегатов.
Пространств. структуру молекулы С. отличает высокая степень упорядоченности. В полипептидной цепи С. человека выявлено 4a-спирали и 3 нерегулярных участка.
С. человека отличается от изученных С. животных на 34-35% (С. животных неактивны при введении людям).
С. вырабатывается и секретируется в кровь специализир. клетками гл. обр. передней доли гипофиза-соматотрофами. Содержание С. в гипофизе человека более чем на порядок превышает содержание др. гормонов этой эндокринной железы. Для С. характерен мол. полиморфизм, к-рый обусловлен альтернативным сплайсингом пре-мРНК или посттрансляц. модификацией (специфич. ограниченный протеолиз, гликозилирование, фосфорилирование и др.). Продукт альтернативного сплайсинга пре-мРНК с мол. м. 20 тыс. выделен из гипофиза человека; у него отсутствует участок, занимающий положение 32-46 в молекуле С. У женщин при беременности в результате экспрессии вариантного гена С. продуцируется в плаценте мол. форма С, отличающаяся от обычного гормона в 15 положениях полипептидной цепи.
гормонов этой эндокринной железы. Для С. характерен мол. полиморфизм, к-рый обусловлен альтернативным сплайсингом пре-мРНК или посттрансляц. модификацией (специфич. ограниченный протеолиз, гликозилирование, фосфорилирование и др.). Продукт альтернативного сплайсинга пре-мРНК с мол. м. 20 тыс. выделен из гипофиза человека; у него отсутствует участок, занимающий положение 32-46 в молекуле С. У женщин при беременности в результате экспрессии вариантного гена С. продуцируется в плаценте мол. форма С, отличающаяся от обычного гормона в 15 положениях полипептидной цепи.
С.-полифункцион. гормон. Являясь специфич. стимулятором роста тела (скелета и мягких тканей), он участвует также в регуляции всех видов обмена в-в. Осн. дефект развития организма человека и животных в условиях недостаточности С.-задержка роста костей. Избыток С. в растущем организме может приводить к гигантизму, а у взрослых-к ненормальному увеличению отдельных органов и тканей. Действие С. на рост костей опосредовано через соматомедины — инсулиноподобные ростовые факторы полипептидной природы.
на рост костей опосредовано через соматомедины — инсулиноподобные ростовые факторы полипептидной природы.
Отдельные стороны биол. действия С. могут в той или иной мере воспроизводиться фрагментами его полипептидной цепи. Фрагмент 31-44 С. человека проявляет характерное для гормона жиромобилизующее действие. Фрагмент 44-77 воспроизводит диабетогенное действие С., вызывая при введении животным нарушение обмена глюкозы. Фрагменты С. разл. видовой принадлежности 77-107, 96-133, 87-124 способны вызывать биол. эффекты гормона, связанные со стимуляцией ростовых процессов в организме.
Биосинтез и секреция С. находятся под сложным контролем, включающим регуляцию гормонами гипоталамуса- соматостатином и соматолиберином, а также нек-рыми др. гормонами и продуктами обмена в-в.
Препараты С. получают выделением из гипофизов людей и животных, а также методами генетич. инженерии. С. человека применяют для лечения гипофизарных карликов, а также при др. состояниях, связанных с недостатком этого гормона в организме.
состояниях, связанных с недостатком этого гормона в организме.
Лит.: Гормон роста человека. Сборник научных трудов. Научный центр биологических исследований АН СССР, Пущино, 1988; Павловский А. Г. [и др.], «Докл. АН СССР», 1989, т. 305, №4, с. 861-64; Булатов А. А., «Проблемы эндокринологии», 1990, т. 36, № 4, с. 30-35; Lewis U. [а. о.], «Recent. Prog. Horm.Res.», 1980, v. 36, p. 477-508. А. А. Булатов.
Химическая энциклопедия. — М.: Советская энциклопедия.
Под ред. И. Л. Кнунянца.
1988.
Бычий соматотропин (bST) | FDA
Соматотропин крупного рогатого скота (bST), также известный как гормон роста крупного рогатого скота, является лекарственным средством для животных, одобренным FDA для увеличения производства молока у дойных коров. Этот препарат основан на соматотропине, который естественным образом вырабатывается у крупного рогатого скота. Соматотропин — это белковый гормон, вырабатываемый гипофизом животных, включая человека, и необходим для нормального роста, развития и поддержания здоровья.
Этот препарат основан на соматотропине, который естественным образом вырабатывается у крупного рогатого скота. Соматотропин — это белковый гормон, вырабатываемый гипофизом животных, включая человека, и необходим для нормального роста, развития и поддержания здоровья.
Ранние исследования, проведенные в 1930-х и 1940-х годах в России и Англии, показали, что надой молока у коров может быть увеличен путем инъекции экстрактов гипофиза крупного рогатого скота, в частности, bST. Английские ученые пытались увеличить производство молока у коров во время Второй мировой войны с помощью BST, полученного из гипофиза, чтобы облегчить нехватку пищи. Однако только в 1980-х годах стало технически возможным и экономически целесообразным производить большие коммерческие количества bST с помощью процесса с использованием биотехнологии.BST, полученный с помощью этого процесса, обычно называют «рекомбинантным» bST или «rbST». Этот процесс также полезен для получения более последовательного и очищенного источника bST.
FDA одобряет лекарство для животных только после того, как информация и / или исследования показали, что пища (в данном случае молоко и мясо) животных, подвергшихся лечению, безопасна для употребления в пищу людьми, и что препарат не причиняет вреда обработанным животным, или окружение. Препарат также должен быть эффективным, то есть работать по назначению.Маркировка лекарственных препаратов для животных содержит все инструкции по безопасному и эффективному использованию и одобрена FDA. FDA публикует на своем веб-сайте общедоступные документы (сводки о свободе информации), в которых резюмируется информация, которую FDA использовало для определения того, что препарат безопасен для обработанных животных, продукты животного происхождения (съедобные ткани, такие как мясо и молоко) безопасны для людей. ешьте, и что продукт эффективен.
FDA одобрило продукт bST в 1993 году под торговой маркой «Posilac ™» (суспензия цинка sometribove) после того, как определило, что его использование будет безопасным и эффективным. Posilac ™ одобрен для безрецептурного применения у дойных коров примерно через 2 месяца после того, как у коровы появится теленок, и до конца периода лактации. В это время коровам вводят Posilac ™ подкожно (под кожу) каждые 14 дней. Типичный период лактации у коровы составляет примерно 10 месяцев и начинается сразу после того, как у нее родится теленок. Таким образом, леченым молочным коровам обычно дают Posilac ™ в течение примерно 8 месяцев в году. После 10-месячного периода лактации производитель прекращает доение коровы, чтобы дать ее молочной железе 2-месячный период для отдыха и восстановления, прежде чем у нее появится теленок и начнется следующий период лактации.
Posilac ™ одобрен для безрецептурного применения у дойных коров примерно через 2 месяца после того, как у коровы появится теленок, и до конца периода лактации. В это время коровам вводят Posilac ™ подкожно (под кожу) каждые 14 дней. Типичный период лактации у коровы составляет примерно 10 месяцев и начинается сразу после того, как у нее родится теленок. Таким образом, леченым молочным коровам обычно дают Posilac ™ в течение примерно 8 месяцев в году. После 10-месячного периода лактации производитель прекращает доение коровы, чтобы дать ее молочной железе 2-месячный период для отдыха и восстановления, прежде чем у нее появится теленок и начнется следующий период лактации.
Ключевым фактором в определении FDA, что молоко и мясо коров, получавших Posilac ™, безопасны для употребления в пищу людьми, является то, что bST представляет собой большой белок. Как и большинство пищевых белков, bST расщепляется пищеварительными ферментами в желудочно-кишечном тракте и не всасывается в неизменном виде. Расщепленные протеолитические фрагменты не обладают биологической активностью. Более того, даже если он был введен инъекцией, bST не способствует биологической активности в организме человека, потому что соматотропины низших видов млекопитающих не проявляют активности в организме человека.Posilac ™ имеет нулевой день вывода. Это означает, что молоко и мясо коров безопасны для употребления людьми в любое время после того, как животное будет обработано Posilac ™. Многочисленные международные организации по охране здоровья и безопасности пищевых продуктов, а также многие национальные регулирующие органы подтвердили безопасность молока и мяса коров, получавших bST, для употребления в пищу людьми. Дополнительная информация о безопасности молока и мяса от обработанных коров представлена в ссылках ниже.
Расщепленные протеолитические фрагменты не обладают биологической активностью. Более того, даже если он был введен инъекцией, bST не способствует биологической активности в организме человека, потому что соматотропины низших видов млекопитающих не проявляют активности в организме человека.Posilac ™ имеет нулевой день вывода. Это означает, что молоко и мясо коров безопасны для употребления людьми в любое время после того, как животное будет обработано Posilac ™. Многочисленные международные организации по охране здоровья и безопасности пищевых продуктов, а также многие национальные регулирующие органы подтвердили безопасность молока и мяса коров, получавших bST, для употребления в пищу людьми. Дополнительная информация о безопасности молока и мяса от обработанных коров представлена в ссылках ниже.
FDA провело оценку результатов многочисленных исследований, прежде чем было одобрено, чтобы определить, безопасен ли Posilac ™ для обработанных молочных коров.Многие исследования проводились в типичных фермерских условиях во многих регионах США. Эффект лечения оценивался по всем аспектам здоровья коров, потребления корма, способности иметь теленка и здоровья их потомства. FDA пришло к выводу, что Posilac ™ безопасен для здоровых молочных коров. Некоторое усиление побочных эффектов наблюдалось у коров, получавших Posilac ™, но FDA определило, что эти эффекты можно контролировать в нормальных условиях сельского хозяйства в США. Маркировка продукта определяет потенциальные побочные эффекты для коров, подвергшихся лечению, так что фермеры могут принять информированное решение о том, использовать ли Posilac ™ в своем стаде.Мониторинговое исследование после одобрения, проведенное в 28 стадах в США, включая более 1000 дойных коров, подтвердило безопасность продукта для обработанных коров. Дополнительная информация о безопасности Posilac ™ для дойных коров представлена в ссылках ниже.
Эффект лечения оценивался по всем аспектам здоровья коров, потребления корма, способности иметь теленка и здоровья их потомства. FDA пришло к выводу, что Posilac ™ безопасен для здоровых молочных коров. Некоторое усиление побочных эффектов наблюдалось у коров, получавших Posilac ™, но FDA определило, что эти эффекты можно контролировать в нормальных условиях сельского хозяйства в США. Маркировка продукта определяет потенциальные побочные эффекты для коров, подвергшихся лечению, так что фермеры могут принять информированное решение о том, использовать ли Posilac ™ в своем стаде.Мониторинговое исследование после одобрения, проведенное в 28 стадах в США, включая более 1000 дойных коров, подтвердило безопасность продукта для обработанных коров. Дополнительная информация о безопасности Posilac ™ для дойных коров представлена в ссылках ниже.
Как и в случае со всеми лекарствами, одобренными FDA, Агентство продолжает контролировать безопасность и эффективность Posilac ™ посредством надзора после утверждения и анализа всех сообщений о побочных эффектах лекарств.
Для получения дополнительной информации о bST см. Следующие отчеты и документы утверждения.
Отчеты
Гражданская петиция
Обзоры свободы информации
Сводные данные о воздействии на окружающую среду
-
Текущее содержание по состоянию на:
Somatotropin — обзор | Темы ScienceDirect
II.C.3 Использование — рекомбинантная ДНК и генная инженерия
Многие важные с медицинской точки зрения белки, например человеческий инсулин и человеческий соматотропин (гормон роста), находятся в дефиците. Теперь, когда понятны механизмы синтеза белка, можно ввести сегмент ДНК, кодирующий, скажем, человеческий белок, в бактерии, культивировать бактерии, позволить им синтезировать белок, а затем собрать этот белок. Такой процесс включает технологию рекомбинантной ДНК.
Такой процесс включает технологию рекомбинантной ДНК.
Сначала должен быть подготовлен сегмент ДНК, который кодирует требуемый белок.Его можно очистить от клеток, в которых он происходит, путем частичной деградации всей клеточной ДНК и выделения соответствующего фрагмента. В качестве альтернативы, если доступна очищенная м-РНК для белка, соответствующую ДНК можно получить с использованием обратной транскриптазы. Если требуемый сегмент ДНК короткий, небольшое его количество может быть синтезировано химическим путем в лаборатории, а затем большее количество может быть получено путем ферментативной репликации в так называемой полимеразной цепной реакции (ПЦР).
Во-вторых, эта ДНК должна быть включена в «вектор», который будет переносить ДНК в бактериальные клетки.Вектор может быть ДНК вируса, который может проникать в используемый штамм бактерии. Чаще чужеродная ДНК вводится в плазмиду, небольшой кольцевой фрагмент ДНК, который может реплицироваться в бактериальных клетках.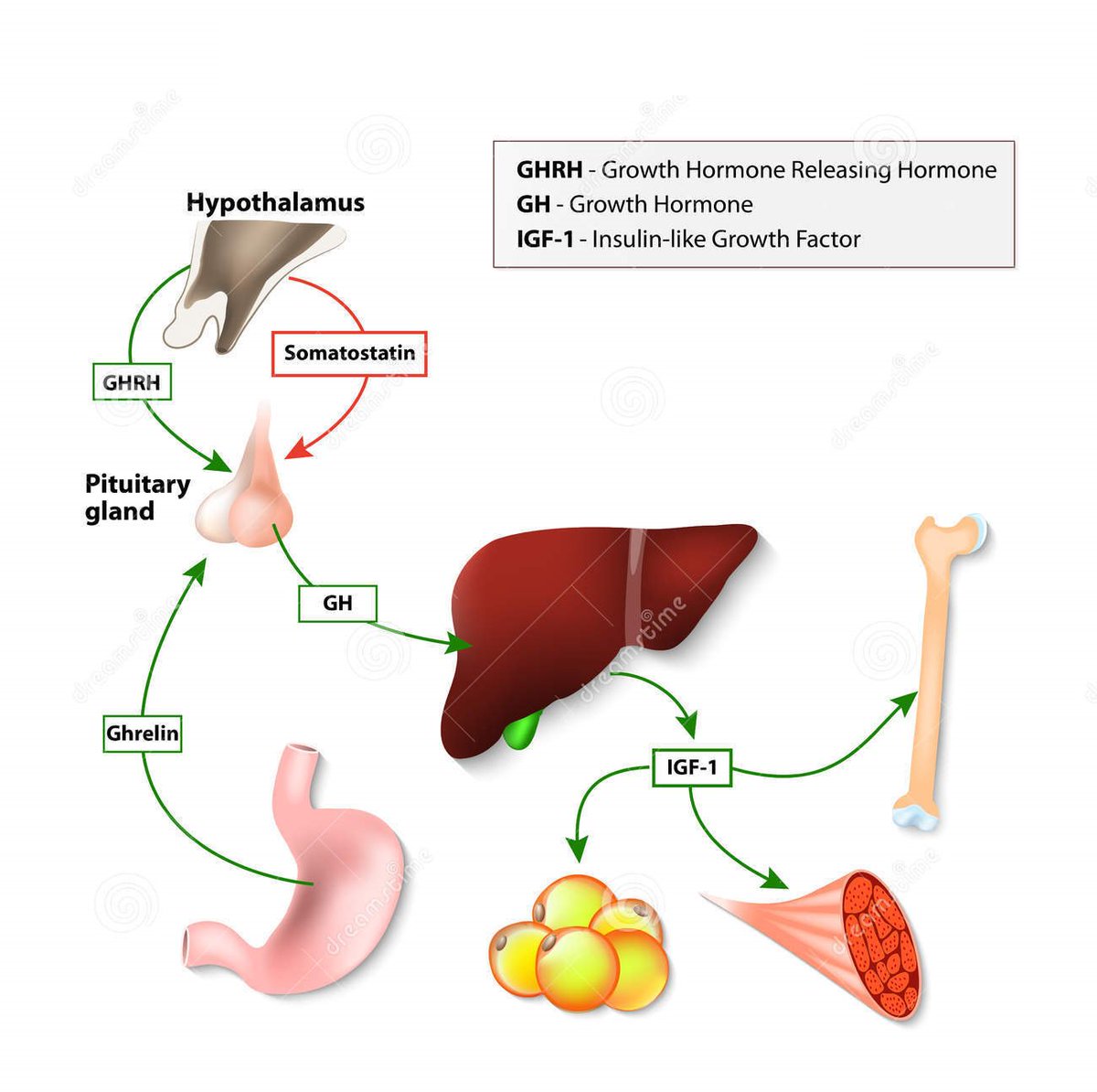 Кольцевая плазмидная ДНК обычно «разрывается» ферментом, а другой фермент используется для присоединения чужеродной ДНК. Если обрезанные концы плазмидной ДНК и чужеродной ДНК имеют комплементарные последовательности, то правильное сочетание этих двух проще. Эти так называемые «липкие» концы могут быть получены ферментами или химическим синтезом.Продукт — искусственная комбинация ДНК бактериальной плазмиды и, например, ДНК человека — называется рекомбинантной ДНК.
Кольцевая плазмидная ДНК обычно «разрывается» ферментом, а другой фермент используется для присоединения чужеродной ДНК. Если обрезанные концы плазмидной ДНК и чужеродной ДНК имеют комплементарные последовательности, то правильное сочетание этих двух проще. Эти так называемые «липкие» концы могут быть получены ферментами или химическим синтезом.Продукт — искусственная комбинация ДНК бактериальной плазмиды и, например, ДНК человека — называется рекомбинантной ДНК.
Затем плазмиду вводят в бактериальную клетку, и бактерию клонируют (т.е. клетке дают возможность делиться несколько раз), получая потомство бактерий с той же генетической структурой, что и исходная клетка. Каждая клетка несет ДНК, кодирующую требуемый белок, и если в ДНК вставлены правильные элементы управления, каждая клетка синтезирует белок.Позже белок можно очистить от бактериальной культуры.
Таким образом стало возможным производить человеческий инсулин, гормон роста и интерферон (противовирусный белок) из E. coli — распространенной бактерии в пищеварительном тракте человека.
coli — распространенной бактерии в пищеварительном тракте человека.
Опасения, что новые и опасные штаммы E. coli могут возникнуть в результате экспериментов с рекомбинантной ДНК, в основном развеялись строгим контролем над видами экспериментов, которые можно проводить, и более глубоким пониманием механизмов контроля, задействованных в бактериальной нуклеиновой кислоте. метаболизм.
Есть надежда, что эти методы позволят производить полезные с медицинской точки зрения белки дешево и в больших масштабах. Кроме того, могут быть «созданы» новые бактерии с полезными свойствами (например, бактерии, способные превращать целлюлозу в метан для производства энергии). (В настоящее время необходимо использовать два разных микроорганизма: один превращает целлюлозу в кислоты, второй — эти кислоты в метан.)
Встраивая ДНК со специфическими изменениями оснований в бактерии, можно получить белки всего с одной измененной аминокислотой.Этот процесс, известный как сайт-направленный мутагенез, позволил провести подробные исследования роли отдельных аминокислот, например, в активности и стабильности ферментов. Есть надежда, что в будущем таким способом можно будет получать промышленно важные ферменты с улучшенной термостабильностью.
Есть надежда, что в будущем таким способом можно будет получать промышленно важные ферменты с улучшенной термостабильностью.
Генная инженерия также может быть проведена на растениях и животных, хотя обычно возникают некоторые трудности с введением новой ДНК в растительную или животную клетку и обеспечением ее использования для кодирования нового белка.Отдельные растительные клетки можно трансформировать путем инфицирования бактерией Agrobacterium tumefaciens , несущей плазмиду, содержащую желаемую новую ДНК. Когда бактерия контактирует с растительной клеткой, часть плазмидной ДНК переносится в ядро растительной клетки и интегрируется в ДНК растительной клетки. Затем целые растения могут быть получены из отдельных растительных клеток в культуре путем введения гормонов. Таким образом, можно выращивать полноценные растения с измененной генетической структурой.Устойчивость к болезням можно повысить, например, путем включения в растение гена белка оболочки вируса. Похоже, что это останавливает репликацию вируса в растении. Первые коммерчески выращиваемые генетически модифицированные растения содержат ДНК, кодирующую фермент, придающий устойчивость к гербицидам, или белки, обладающие инсектицидным действием. В первом случае для уничтожения сорняков на посевах нужно использовать меньше гербицидов, так как опрыскивание можно проводить, когда и сорняки, и культурные растения хорошо разрастаются. Во втором случае применение внешних пестицидов может не потребоваться, поскольку сами культурные растения, содержащие новый инсектицидный белок, могут убить вторгшихся насекомых.В настоящее время хлопок, соя, кукуруза и рапс, содержащие эти модификации, выращиваются в коммерческих целях, но из-за опасений по поводу возможных экологических проблем, таких как потенциальный вред для полезных насекомых, внедрение новых генетически модифицированных сельскохозяйственных культур замедлилось.
Первые коммерчески выращиваемые генетически модифицированные растения содержат ДНК, кодирующую фермент, придающий устойчивость к гербицидам, или белки, обладающие инсектицидным действием. В первом случае для уничтожения сорняков на посевах нужно использовать меньше гербицидов, так как опрыскивание можно проводить, когда и сорняки, и культурные растения хорошо разрастаются. Во втором случае применение внешних пестицидов может не потребоваться, поскольку сами культурные растения, содержащие новый инсектицидный белок, могут убить вторгшихся насекомых.В настоящее время хлопок, соя, кукуруза и рапс, содержащие эти модификации, выращиваются в коммерческих целях, но из-за опасений по поводу возможных экологических проблем, таких как потенциальный вред для полезных насекомых, внедрение новых генетически модифицированных сельскохозяйственных культур замедлилось.
Расширение этой работы может привести к «генной инженерии» у людей, где генетические заболевания (т.е. болезни, вызванные дефектным или отсутствующим ферментом) могут быть излечены путем включения ДНК, кодирующей этот белок. Однако будет трудно гарантировать, что последующий биосинтез белка находится под правильным контролем, чтобы белок вырабатывался в нужных количествах в соответствующих тканях.
Однако будет трудно гарантировать, что последующий биосинтез белка находится под правильным контролем, чтобы белок вырабатывался в нужных количествах в соответствующих тканях.
Небольшие количества ДНК человека, обнаруженные на месте преступления, теперь можно амплифицировать с помощью технологии ПЦР, а ДНК можно гидролизовать ферментами, специфичными для определенных последовательностей оснований. Поскольку считается, что образ произведенных фрагментов характерен для одного человека, в настоящее время этот процесс используется для выявления лиц, совершивших серьезные преступления.
Анализ крови: Соматомедин C (IGF-1) (для родителей)
Что это такое
Тест на соматомедин C, также называемый тестом на инсулиноподобный фактор роста-1 (или IGF-1), помогает врачам оценить, вырабатывает ли человек нормальное количество гормона роста человека (hGH или соматотропин).
HGH вырабатывается гипофизом, железой размером с горошину в головном мозге, которая помогает контролировать рост и функцию других желез. Соматомедин C — это белок, вырабатываемый в печени и мышцах, известный как фактор роста — его производство стимулируется гормоном роста.
Соматомедин C — это белок, вырабатываемый в печени и мышцах, известный как фактор роста — его производство стимулируется гормоном роста.
В то время как уровни гормона роста меняются в течение дня в зависимости от диеты и уровня активности, уровни соматомедина С в крови более стабильны, что делает его измерение довольно надежным индикатором того, сколько гормона роста вырабатывает гипофиз в целом.
Почему это сделано
Тест на соматомедин С в первую очередь назначается для проверки нарушений работы гипофиза и аномалий выработки гормона роста. Такие симптомы, как низкий рост или чрезмерный рост (гигантизм), могут потребовать проведения теста на соматомедин С.
Тест также можно использовать для оценки состояния питания ребенка, поскольку недоедание может снизить уровень соматомедина С.
Препарат
Вашего ребенка могут попросить прекратить есть и пить за 10–12 часов до этого теста. Если в день обследования ребенок будет носить футболку или рубашку с короткими рукавами, это может облегчить жизнь вашему ребенку и специалисту, который будет брать кровь.
стр. 2
Процедура
Медицинский работник очистит поверхность кожи антисептиком и наложит эластичную ленту (жгут) вокруг плеча, чтобы оказать давление и вызвать набухание вены от крови.Иглу вводят в вену (обычно в руку с внутренней стороны локтя или на тыльной стороне кисти), отбирают кровь и собирают во флакон или шприц.
После процедуры резинка снимается. После того, как кровь собрана, игла удаляется, и область покрывается ватой или повязкой, чтобы остановить кровотечение. Сбор крови для этого теста займет всего несколько минут.
Чего ожидать
Забор крови доставляет только временный дискомфорт и может казаться быстрым уколом булавкой.После этого могут появиться легкие синяки, которые пройдут через несколько дней.
стр.3
Получение результатов
Проба крови будет обработана в лаборатории. Поскольку это не обычный тест, результаты могут быть доступны в лаборатории только через неделю или две после взятия образца.
Риски
Тест на соматомедин С считается безопасной процедурой. Однако, как и во многих медицинских тестах, при заборе крови могут возникнуть некоторые проблемы, например:
- обморок или головокружение
- гематома (скапливающаяся под кожей кровь, вызывающая образование шишки или синяка)
- Боль, связанная с множественными проколами для определения местоположения вены
Помощь вашему ребенку
Анализ крови относительно безболезнен.Тем не менее, многие дети боятся иголок. Объяснение теста языком, понятным вашему ребенку, может помочь немного ослабить страх.
Позвольте вашему ребенку задавать техническому специалисту любые вопросы, которые могут у него возникнуть. Посоветуйте своему ребенку расслабиться и оставаться неподвижным во время процедуры, так как напряжение и движение мышц могут затруднить и затруднить взятие крови. Также может помочь, если ваш ребенок смотрит в сторону, когда игла вводится в кожу.
Если у вас есть вопросы
Если у вас есть вопросы о тесте на соматомедин С, поговорите со своим врачом.
Отслеживание рекомбинантного бычьего соматотропина ab (использование) с помощью транскриптомики: потенциал соматических клеток крупного рогатого скота в многодозовом продольном исследовании
Влияние rbST на удой в качестве среднего и стандартного отклонения молочной продуктивности (кг в день) в каждом цикле обработки, а также разницы в продуктивности между обеими группами (% дополнительного молока, произведенного группой rbST по сравнению с контрольными животными).От цикла 0 до цикла 3 производство молока увеличивается в обеих группах, что, возможно, указывает на то, что животные еще не достигли пика лактации. Хотя первая доза rbST была введена примерно через 2 месяца после родов, как рекомендовано производителем, важно отметить, что эта рекомендация основана на математических моделях, которые определяют пик производства молока через 60–90 дней после родов.
 Однако эти модели представляют собой только теоретические подходы, и дни молочного пика (DIM) на пике молока сильно различаются между стадами и коровами, будучи обусловлены, среди прочего, благополучием и кормлением 37 .От цикла 4 до конца исследования можно было наблюдать снижение надоев молока у контрольных коров, в то время как животные, получавшие rbST, по-видимому, сохраняли свою продуктивность относительно постоянной при потреблении в среднем 30–35 кг молока в день, показывая очевидную тенденцию к снижению. только при прекращении гормонального лечения (циклы 14, 15 и 16). В этот момент различия в продуктивности, наблюдаемые между группами, вернулись к уровням, очень близким к уровням, наблюдаемым в цикле 0. Примечателен тот факт, что продуктивность в группе rbST была значительно выше, чем в контроле в течение всего исследования, за исключением цикла 6. когда эти животные производили только на 5% больше, чем контрольные субъекты (таблица 2).На основании схемы введения rbST каждые две недели, рекомендованной производителем, на 70-й день группа обработанных животных должна была получить новую дозу рекомбинантного гормона роста.
Однако эти модели представляют собой только теоретические подходы, и дни молочного пика (DIM) на пике молока сильно различаются между стадами и коровами, будучи обусловлены, среди прочего, благополучием и кормлением 37 .От цикла 4 до конца исследования можно было наблюдать снижение надоев молока у контрольных коров, в то время как животные, получавшие rbST, по-видимому, сохраняли свою продуктивность относительно постоянной при потреблении в среднем 30–35 кг молока в день, показывая очевидную тенденцию к снижению. только при прекращении гормонального лечения (циклы 14, 15 и 16). В этот момент различия в продуктивности, наблюдаемые между группами, вернулись к уровням, очень близким к уровням, наблюдаемым в цикле 0. Примечателен тот факт, что продуктивность в группе rbST была значительно выше, чем в контроле в течение всего исследования, за исключением цикла 6. когда эти животные производили только на 5% больше, чем контрольные субъекты (таблица 2).На основании схемы введения rbST каждые две недели, рекомендованной производителем, на 70-й день группа обработанных животных должна была получить новую дозу рекомбинантного гормона роста. Однако эта доза не применялась, чтобы можно было оценить, может ли группа rbST восстановить профиль транскрипции до введения дозы через 28 дней без гормонального введения (рис. 1). Возможно, из-за этого недостатка гормона статистически значимые различия, существующие в молочной продуктивности между двумя группами, исчезли, подчеркнув влияние rbST на показатели продуктивности молока (Таблица 2).На 84-й день снова вводили rbST, и снова появились значительные различия в молочной продуктивности между двумя группами (24%). Максимальная разница на 43% больше молока у обработанных животных по сравнению с контрольными коровами наблюдалась в цикле 12, что связано как с поддержанием продуктивности за счет rbST, так и с естественным снижением у контрольных самок. Любопытно, что эти значительные различия сохранялись до конца исследования, даже почти через два месяца после введения последней дозы (12 -я доза , день 168) (таблица 2).
Однако эта доза не применялась, чтобы можно было оценить, может ли группа rbST восстановить профиль транскрипции до введения дозы через 28 дней без гормонального введения (рис. 1). Возможно, из-за этого недостатка гормона статистически значимые различия, существующие в молочной продуктивности между двумя группами, исчезли, подчеркнув влияние rbST на показатели продуктивности молока (Таблица 2).На 84-й день снова вводили rbST, и снова появились значительные различия в молочной продуктивности между двумя группами (24%). Максимальная разница на 43% больше молока у обработанных животных по сравнению с контрольными коровами наблюдалась в цикле 12, что связано как с поддержанием продуктивности за счет rbST, так и с естественным снижением у контрольных самок. Любопытно, что эти значительные различия сохранялись до конца исследования, даже почти через два месяца после введения последней дозы (12 -я доза , день 168) (таблица 2).
Таблица 2 Надой молока в обработанной (N = 6) и контрольной группах (N = 3) на протяжении всего исследования.
Выделение РНК из соматических клеток крупного рогатого скота
МСК — это простой для сбора источник РНК для исследований экспрессии генов, поскольку эти клетки можно выделить из сырого молока по очень простому протоколу. Кроме того, сбор образцов является дешевым и неинвазивным, поскольку молоко можно собирать в доильном зале без прямого контакта с животным и, следовательно, не вызывая у него стресса, который может повлиять на полученные результаты.В этом исследовании лечение rbST не оказало значительного влияния ( P = 0,099) на количество РНК, выделенной из МСК, при средней концентрации 120,69 ± 68,31 мкг · мл -1 в образцах из группы rbST и 132,36 ± 68,86 мкг / мл -1 в пробах из контрольной группы. Среднее значение отношения A260 / 280 составило 1,766 ± 0,095. Возможно, что стадия очистки с помощью спин-колонок увеличила соотношение A260 / 280 и, следовательно, чистоту образцов РНК. Хотя включение этого шага увеличивает стоимость образца в рутинном анализе, он позволяет получать образцы с более высокой чистотой. Среднее значение RIN, наблюдаемое для проанализированных образцов, составляло 6,88 ± 0,82. Некоторые факторы могли повлиять на целостность образцов. Образцы, использованные в этом исследовании, представляли собой соматические клетки крупного рогатого скота, выделенные из молока. Молоко характеризуется сложной микробиотой, и РНКазы, полученные из этой микробиоты, могут нести ответственность за более низкую целостность РНК. Кроме того, некоторые соматические клетки, присутствующие в молоке, могут частично разрушаться. Эти факты также наблюдались в исследовании, в котором для транскриптомических исследований использовался вагинальный мазок крупного рогатого скота с целью поиска биомаркеров для отслеживания злоупотребления анаболическими средствами 38 .Кроме того, процесс доения, сбора и транспортировки молока в лабораторию может, несмотря на то, что он выполняется как можно быстрее, повлиять на целостность РНК.
Среднее значение RIN, наблюдаемое для проанализированных образцов, составляло 6,88 ± 0,82. Некоторые факторы могли повлиять на целостность образцов. Образцы, использованные в этом исследовании, представляли собой соматические клетки крупного рогатого скота, выделенные из молока. Молоко характеризуется сложной микробиотой, и РНКазы, полученные из этой микробиоты, могут нести ответственность за более низкую целостность РНК. Кроме того, некоторые соматические клетки, присутствующие в молоке, могут частично разрушаться. Эти факты также наблюдались в исследовании, в котором для транскриптомических исследований использовался вагинальный мазок крупного рогатого скота с целью поиска биомаркеров для отслеживания злоупотребления анаболическими средствами 38 .Кроме того, процесс доения, сбора и транспортировки молока в лабораторию может, несмотря на то, что он выполняется как можно быстрее, повлиять на целостность РНК.
Влияние rbST на гены соматотропной оси
Набор из 18 генов (таблица 1) был выбран для создания планшетов OpenArray ® , используемых в этом исследовании. Этот отбор был основан на способности этих генов получить характерную транскриптомную сигнатуру rbST, которую можно использовать в качестве стандарта для контроля ab (использования) rbST у молочного скота.Предыдущие исследования экспрессии генов с rbST были разработаны как исследования с однократной дозой и однократным отбором образцов в посмертной ткани молочной железы 27 или многодозовые (пять доз) исследования с отбором образцов крови и мышц in vivo 31 . Эти методы считаются инвазивными, относительно дорогими и, следовательно, непрактичными для контроля на молочных фермах. В случае соматотропина контроль должен осуществляться in vivo , поскольку конечной целью является предотвращение попадания rbST-молока на рынок молочных продуктов.
Этот отбор был основан на способности этих генов получить характерную транскриптомную сигнатуру rbST, которую можно использовать в качестве стандарта для контроля ab (использования) rbST у молочного скота.Предыдущие исследования экспрессии генов с rbST были разработаны как исследования с однократной дозой и однократным отбором образцов в посмертной ткани молочной железы 27 или многодозовые (пять доз) исследования с отбором образцов крови и мышц in vivo 31 . Эти методы считаются инвазивными, относительно дорогими и, следовательно, непрактичными для контроля на молочных фермах. В случае соматотропина контроль должен осуществляться in vivo , поскольку конечной целью является предотвращение попадания rbST-молока на рынок молочных продуктов.
В этом исследовании экспрессия IGF-1 была обнаружена только во всех точках выборки у одной коровы (корова 7), получавшей rbST, и не была обнаружена в MSC контрольной группы. Тот факт, что было возможно обнаружить мишень IGF-1 только во всех точках выборки у одной коровы, может указывать на существование различных локальных ответов молочных желез на экзогенный rbST у отдельных особей. Большинство молекул IGF-1, обнаруженных в кровотоке, связаны с высоким сродством с одним или несколькими из шести известных связывающих IGF-1 белков (IGFBP-1-6), которые модулируют биодоступность IGF-1 в тканях-мишенях 39 .Предыдущие исследования показали, что rbST сильно влияет на активацию IGFBP-5 в скелетных мышцах крупного рогатого скота 31 и подавляет IGFBP-3 в ткани молочной железы 32 . Однако в этом исследовании транскрипты ни IGFBP-3, ни IGFBP-5 не были обнаружены в любой момент времени. Этот результат может быть связан с тем, что МСК состоят в основном из лейкоцитов 40 , в которых репрессивный эффект IGFBP может быть не так важен, как в ткани молочной железы. Следовательно, и IGF-1, и IGF-1 связывающие белки отбрасываются в качестве потенциальных маркеров в соматических клетках в этом исследовании.
Другим ключевым компонентом соматотропной оси является рецептор IGF-1 (IGF-1R), который является первичным сигнальным рецептором для IGF-1, который опосредует большинство его биологических эффектов. В день 1 группа rbST (0,348 ± 0,131) имела значительно ( P <0,001) более высокое относительное содержание IGF-1R, чем контрольная группа (0,0898 ± 0,0486). В различных исследованиях, в которых оценивалась концентрация rbST в крови после введения, было обнаружено, что более высокие концентрации этого рекомбинантного гормона были обнаружены после введения rbST 14,15 .Следовательно, значительные различия, наблюдаемые в группе, получавшей лечение, могут быть связаны с ответом на IGF-1, синтезируемым как ответ, на более высокие концентрации rbST у обработанных коров после введения первой дозы. На фиг. 2 можно наблюдать, что относительное содержание IGF-1R для двух первых циклов введения rbST также было значительно выше в группе rbST, чем в контрольной группе во многих точках отбора проб. Любопытно, что на 84-й день исследования относительное содержание IGF-1R было аналогичным в группе rbST (0.070 ± 0,057) и в контрольной группе (0,110 ± 0,030). Этот день совпал с шестым введением rbST, и между этой дозой и пятой дозой был промежуток в 28 дней вместо 14 дней.
В день 1 группа rbST (0,348 ± 0,131) имела значительно ( P <0,001) более высокое относительное содержание IGF-1R, чем контрольная группа (0,0898 ± 0,0486). В различных исследованиях, в которых оценивалась концентрация rbST в крови после введения, было обнаружено, что более высокие концентрации этого рекомбинантного гормона были обнаружены после введения rbST 14,15 .Следовательно, значительные различия, наблюдаемые в группе, получавшей лечение, могут быть связаны с ответом на IGF-1, синтезируемым как ответ, на более высокие концентрации rbST у обработанных коров после введения первой дозы. На фиг. 2 можно наблюдать, что относительное содержание IGF-1R для двух первых циклов введения rbST также было значительно выше в группе rbST, чем в контрольной группе во многих точках отбора проб. Любопытно, что на 84-й день исследования относительное содержание IGF-1R было аналогичным в группе rbST (0.070 ± 0,057) и в контрольной группе (0,110 ± 0,030). Этот день совпал с шестым введением rbST, и между этой дозой и пятой дозой был промежуток в 28 дней вместо 14 дней. Следовательно, возможно, что группа rbST восстановила физиологический уровень IGF-1R после нескольких дней без rbST, демонстрируя даже отменяющие эффекты подавления транскрипции IGF-1R. Эти результаты показывают, что IGF-1R является возможным хорошим кандидатом для включения в панель генов для обнаружения использования rbST на молочных фермах.Хотя другие авторы не обнаружили значительного влияния rbST на уровни IGF-1R в скелетных мышцах 31 , в этом исследовании наблюдалась четкая реакция на уровни транскрипта этого рецептора в МСК. В этом смысле лейкоциты, нейтрофилы и моноциты могут продуцировать гормон роста и IGF-1 и экспрессировать свои рецепторы, что указывает на то, что сигнальные пути IGF-1 / IGF-1R могут выполнять регуляторные функции в иммунной системе, включая пролиферацию иммунных клеток 41,42 . Разница между двумя исследованиями может быть связана с использованием разных матриц.МСК, возможно, могли бы лучше реагировать на более высокие уровни циркулирующего IGF-1 и увеличивать количество рецепторов для этой молекулы в своей мембране
Следовательно, возможно, что группа rbST восстановила физиологический уровень IGF-1R после нескольких дней без rbST, демонстрируя даже отменяющие эффекты подавления транскрипции IGF-1R. Эти результаты показывают, что IGF-1R является возможным хорошим кандидатом для включения в панель генов для обнаружения использования rbST на молочных фермах.Хотя другие авторы не обнаружили значительного влияния rbST на уровни IGF-1R в скелетных мышцах 31 , в этом исследовании наблюдалась четкая реакция на уровни транскрипта этого рецептора в МСК. В этом смысле лейкоциты, нейтрофилы и моноциты могут продуцировать гормон роста и IGF-1 и экспрессировать свои рецепторы, что указывает на то, что сигнальные пути IGF-1 / IGF-1R могут выполнять регуляторные функции в иммунной системе, включая пролиферацию иммунных клеток 41,42 . Разница между двумя исследованиями может быть связана с использованием разных матриц.МСК, возможно, могли бы лучше реагировать на более высокие уровни циркулирующего IGF-1 и увеличивать количество рецепторов для этой молекулы в своей мембране
Рисунок 2
Относительное содержание IGF-1R и CCND-1 в первом и втором циклах rbST введение в контрольной группе (N = 3) и группе лечения (N = 6). Непараметрический U-критерий Манна-Уитни использовался для сравнения надоев молока в каждом цикле между обработанной и контрольной группами. Звездочки представляют собой статистически значимые различия между обработанной группой и обеими контрольными группами.* ( p < 0,05), ** ( p <0,01), *** ( p <0,001).
Непараметрический U-критерий Манна-Уитни использовался для сравнения надоев молока в каждом цикле между обработанной и контрольной группами. Звездочки представляют собой статистически значимые различия между обработанной группой и обеими контрольными группами.* ( p < 0,05), ** ( p <0,01), *** ( p <0,001).
Влияние rbST на гены, связанные с иммунной системой
Фактор некроза опухоли (TNF) и интерлейкин-1β (IL-1β) — два цитокина, тесно связанных с иммунной системой 43 . Предположительно из-за их взаимосвязи, на протяжении всего исследования можно было выявить аналогичные тенденции в относительной численности транскриптов TNF и IL-1β. Введение rbST вызывало значительное увеличение относительного количества транскриптов TNF и IL-1β.Стоит отметить, что на 9, 23 и 35 дни относительные содержания TNF и IL-1β были значительно выше в группе rbST по сравнению с контрольной группой (рис. 3). Эти дни соответствуют второй неделе циклов rbST, примерно через 7–9 дней после инъекции Lactotropina®. Следовательно, возможно, что транскриптомные изменения, вызванные rbST в этих двух цитокинах, более очевидны на второй неделе цикла rbST. Любопытно, что на 84-й день (28 дней после введения 5 th rbST) не было значительных различий между группами (рис.3). В этом контексте в других предыдущих исследованиях использовались мощные транскриптомные технологии для обнаружения использования анаболических агентов у крупного рогатого скота 26,38 . В этих исследованиях также наблюдалась повышенная транскрипция IL-1β, один из них значительно 26 , и это очень интересно, потому что в указанном исследовании использовались клетки крови, состав которых очень похож на состав МСК, поскольку в них высока доля белого кровяные клетки. Однако ранее упомянутые исследования не обнаружили влияния анаболических агентов на TNF, в то время как настоящее исследование обнаружило сильное влияние введения rbST на относительное содержание TNF.В связи с этим сообщалось, что экзогенное введение rbST во время лактации может усиливать иммунный ответ у коров 44 .
Следовательно, возможно, что транскриптомные изменения, вызванные rbST в этих двух цитокинах, более очевидны на второй неделе цикла rbST. Любопытно, что на 84-й день (28 дней после введения 5 th rbST) не было значительных различий между группами (рис.3). В этом контексте в других предыдущих исследованиях использовались мощные транскриптомные технологии для обнаружения использования анаболических агентов у крупного рогатого скота 26,38 . В этих исследованиях также наблюдалась повышенная транскрипция IL-1β, один из них значительно 26 , и это очень интересно, потому что в указанном исследовании использовались клетки крови, состав которых очень похож на состав МСК, поскольку в них высока доля белого кровяные клетки. Однако ранее упомянутые исследования не обнаружили влияния анаболических агентов на TNF, в то время как настоящее исследование обнаружило сильное влияние введения rbST на относительное содержание TNF.В связи с этим сообщалось, что экзогенное введение rbST во время лактации может усиливать иммунный ответ у коров 44 . Фактически, количество соматических клеток молока увеличивалось раньше и быстрее у коров, страдающих колиформным маститом, при введении rbST 45 . Гормон роста и его рекомбинантная версия демонстрируют способность модулировать воспалительную реакцию и нейтрофильную защиту лактирующей молочной железы крупного рогатого скота у здоровых и больных коров 45 .Это может объяснить повышенную регуляцию TNF и IL-1β у коров, получавших rbST.
Фактически, количество соматических клеток молока увеличивалось раньше и быстрее у коров, страдающих колиформным маститом, при введении rbST 45 . Гормон роста и его рекомбинантная версия демонстрируют способность модулировать воспалительную реакцию и нейтрофильную защиту лактирующей молочной железы крупного рогатого скота у здоровых и больных коров 45 .Это может объяснить повышенную регуляцию TNF и IL-1β у коров, получавших rbST.
Рисунок 3
Относительное содержание транскрипции CCND1, IGF-1R, IL1β и TNF в группе, обработанной rbST (N = 6), и контрольной группе (N = 3) в дни -10, 1, 9, 23, 35, 84 Были добавлены пробы за один день коров внешнего контроля (N = 3). Односторонний подход ANOVA применялся для сравнения более двух групп. Звездочки представляют собой статистически значимые различия между обработанной группой и обеими контрольными группами.* ( p < 0,05), ** ( p <0,01), *** ( p <0,001).
В скрининговых исследованиях с использованием транскриптомики очень трудно найти конкретный ген, который можно было бы использовать в качестве очень надежного гена. Следует отметить, что как IL-1β, так и TNF могут активироваться в других процессах, таких как субклинический мастит 46,47 . Различные исследования, проведенные в США, показали, что крупные фермы с большей вероятностью примут rbST, что предполагает не только потенциальный компонент размера фермы в использовании и прибыльности rbST, но и компонент оператора (возраст и образование) 48,49 .Рекомбинантный соматотропин часто упоминается как технология, требующая интенсивного управления, связанная с использованием других ориентированных на продуктивность технологий и методов управления, характерных для крупных хозяйств, и реже встречается у пастбищных животных 49,50 . В этом смысле субклинический мастит вызывает снижение надоев у пораженных коров 51 . Следовательно, было бы интересно объединить данные транскриптомных анализов с данными по молочной продуктивности. Кроме того, он может сопровождаться микробиологическим анализом молока у коров с подозрением на выявление основных патогенов, связанных с субклиническим маститом.Но что действительно увеличивает вероятность дискриминации, так это включение в панель большего количества генов.
Кроме того, он может сопровождаться микробиологическим анализом молока у коров с подозрением на выявление основных патогенов, связанных с субклиническим маститом.Но что действительно увеличивает вероятность дискриминации, так это включение в панель большего количества генов.
Влияние rbST на клеточный цикл, пролиферацию, дифференцировку и адгезию
Известно, что rbST увеличивает синтез молока за счет увеличения оборота (пролиферация / апоптоз) и активности эпителиальных клеток молочной железы, что указывает на то, что rbST влияет на метаболические пути, регулирующие обмен клеток / цикл и обмен веществ 52 . Клеточный цикл контролируется циклинами и циклин-зависимыми киназами.Из них циклин D (кодируемый геном CCND1) координирует развитие клеточного цикла посредством внеклеточной стимуляции (например, фактора роста, доступности питательных веществ) и управляет переходом G1 в фазу S, что приводит к митозу клеток. Однако большинство взрослых клеток поддерживается в состоянии покоя, известном как фаза G0, состоянии покоя, и они могут повторно войти в клеточный цикл в фазе G1 при соответствующих митогенных стимулах 53 . В этом исследовании было замечено, что лечение rbST сильно влияет на транскрипцию CCND1.До введения первой дозы rbST достоверных различий между контрольной и rbST-группами не было (рис. 3). Однако после первой дозы можно было наблюдать значительные различия между двумя группами в разных точках отбора проб. Относительное содержание CCND1 было значительно выше в группе rbST, чем в контрольной группе в двух первых циклах лечения rbST (рис. 2). Этот эффект, по-видимому, особенно очевиден через 9 дней после введения rbST, подобно транскриптам TNF и IL-1β.Таким образом, на 9, 23 и 35 дни исследования относительное содержание CCND1 было значительно выше в группе rbST, чем в контрольной группе (рис. 3). Наконец, на 84 день (28 дней после введения 5 th rbST) не было значительных различий между группами (фиг. 3), как в случае цитокинов. Кроме того, в последний день (219) отбора проб (51 день после последних доз rbST) не было значимых различий ( P > 0,05) между группой rbST (0,433 ± 0.
В этом исследовании было замечено, что лечение rbST сильно влияет на транскрипцию CCND1.До введения первой дозы rbST достоверных различий между контрольной и rbST-группами не было (рис. 3). Однако после первой дозы можно было наблюдать значительные различия между двумя группами в разных точках отбора проб. Относительное содержание CCND1 было значительно выше в группе rbST, чем в контрольной группе в двух первых циклах лечения rbST (рис. 2). Этот эффект, по-видимому, особенно очевиден через 9 дней после введения rbST, подобно транскриптам TNF и IL-1β.Таким образом, на 9, 23 и 35 дни исследования относительное содержание CCND1 было значительно выше в группе rbST, чем в контрольной группе (рис. 3). Наконец, на 84 день (28 дней после введения 5 th rbST) не было значительных различий между группами (фиг. 3), как в случае цитокинов. Кроме того, в последний день (219) отбора проб (51 день после последних доз rbST) не было значимых различий ( P > 0,05) между группой rbST (0,433 ± 0. 141) и контрольной группы (0,430 ± 0,178). Следовательно, экзогенное введение rbST вызывает сверхэкспрессию CCND1. Это может привести к активации клетки в фазе G0 и, в конкретном случае ткани молочной железы, увеличению выработки молока за счет увеличения количества альвеолярных клеток молочной железы 54 .
141) и контрольной группы (0,430 ± 0,178). Следовательно, экзогенное введение rbST вызывает сверхэкспрессию CCND1. Это может привести к активации клетки в фазе G0 и, в конкретном случае ткани молочной железы, увеличению выработки молока за счет увеличения количества альвеолярных клеток молочной железы 54 .
Другими генами, связанными с клеточным циклом, являются опухолевый белок D52-подобный 2 (TPD52L2) и сиртуин 2 (SIRT2). Подобно тому, как это наблюдалось для CCND1, TNF и IL-1β, можно было найти значительно более высокое значение ( P <0.001) относительное количество транскриптов SIRT2 в группе rbST (1,517 ± 0,199), чем в контрольной группе (0,506 ± 0,250) на 23 день исследования, но в этом случае только во время второго цикла введения rbST (рис. 4) . Повышенные уровни транскриптов CCND1 и SIRT2 после второго введения Lactotropina® в обработанной группе могли быть результатом воздействия экзогенного rbST на клеточный цикл. Циркуляция этого пептидного гормона в организме приведет к активации клеточного цикла в клетках-мишенях. Однако в других циклах rbST взаимосвязь между введением дозы и изменениями относительного количества транскриптов SIRT2 не была столь очевидной, как во второй дозе. В дополнение к вышесказанному, примечательно, что в обработанной группе наблюдалось значительно более высокое относительное количество транскриптов TPD52L2 ( P <0,05) в течение 4 дней после первого введения rbST. Другой компонент, участвующий в метаболизме клеток за счет его соответствующей роли в трансляции, - это фактор элонгации эукариот 1 гамма (EEF1G).
Однако в других циклах rbST взаимосвязь между введением дозы и изменениями относительного количества транскриптов SIRT2 не была столь очевидной, как во второй дозе. В дополнение к вышесказанному, примечательно, что в обработанной группе наблюдалось значительно более высокое относительное количество транскриптов TPD52L2 ( P <0,05) в течение 4 дней после первого введения rbST. Другой компонент, участвующий в метаболизме клеток за счет его соответствующей роли в трансляции, - это фактор элонгации эукариот 1 гамма (EEF1G).
Рисунок 4
Эволюция относительной численности некоторых генов-мишеней во всех точках выборки исследования в группе, получавшей rbST (N = 6), и в контрольной группе (N = 3).
В этом исследовании относительное количество транскриптов EEF1G не следовало очевидной тенденции, связанной с введением rbST. Однако на 17 и 30 дни (3 и 2 дня после второй и третьей доз rbST, соответственно) относительное количество транскриптов EEF1G было значительно выше в группе rbST. Предыдущее исследование 27 пришло к выводу, что лечение rbST увеличивает уровни транскриптов EEF1G в ткани молочной железы, но оно использовало только одну точку отбора проб через 6 дней после введения соматотропина. Следовательно, невозможно напрямую сравнить эти результаты с результатами, полученными в этом исследовании, в котором 36 точек выборки использовались для транскриптомных анализов в течение 8 месяцев. Другой ген, включенный в это исследование, — белок фактора 8 EGF глобула молочного жира (MFGE8). На рис. 4 можно наблюдать, что относительная численность MFGE8 в группе rbST сильно варьировалась между днями отбора проб.В частности, McCoard et al . 27 наблюдали, что через 6 дней после введения rbST относительное содержание MFGE8 в ткани молочной железы крупного рогатого скота было выше. Однако, как упоминалось ранее, это исследование включало только одну точку данных после однократной дозы rbST. Настоящий долгосрочный эксперимент с множественными дозами продемонстрировал, что паттерны транскрипции у крупного рогатого скота, получавших rbST, имеют большую изменчивость с течением времени.
Предыдущее исследование 27 пришло к выводу, что лечение rbST увеличивает уровни транскриптов EEF1G в ткани молочной железы, но оно использовало только одну точку отбора проб через 6 дней после введения соматотропина. Следовательно, невозможно напрямую сравнить эти результаты с результатами, полученными в этом исследовании, в котором 36 точек выборки использовались для транскриптомных анализов в течение 8 месяцев. Другой ген, включенный в это исследование, — белок фактора 8 EGF глобула молочного жира (MFGE8). На рис. 4 можно наблюдать, что относительная численность MFGE8 в группе rbST сильно варьировалась между днями отбора проб.В частности, McCoard et al . 27 наблюдали, что через 6 дней после введения rbST относительное содержание MFGE8 в ткани молочной железы крупного рогатого скота было выше. Однако, как упоминалось ранее, это исследование включало только одну точку данных после однократной дозы rbST. Настоящий долгосрочный эксперимент с множественными дозами продемонстрировал, что паттерны транскрипции у крупного рогатого скота, получавших rbST, имеют большую изменчивость с течением времени. Например, данные, полученные для CCND1, показали, что влияние rbST на транскрипцию некоторых генов увеличивается с увеличением количества доз.Хотя возможно, что rbST влияет на транскрипцию гена MFGE8, полученные результаты показали как повышающую, так и понижающую регуляцию. Следовательно, MFGE8 не может быть предложен в качестве идеального кандидата для отслеживания использования rbST (ab) у крупного рогатого скота, поскольку не было возможности наблюдать четкую тенденцию в его транскрипции. Другой ген, связанный с адгезией клеток, оцениваемый в этом исследовании, — это катенин альфа-подобный 1 (CTNNAL1). Однако не удалось обнаружить существенных различий в его транскрипции в результате введения rbST.
Например, данные, полученные для CCND1, показали, что влияние rbST на транскрипцию некоторых генов увеличивается с увеличением количества доз.Хотя возможно, что rbST влияет на транскрипцию гена MFGE8, полученные результаты показали как повышающую, так и понижающую регуляцию. Следовательно, MFGE8 не может быть предложен в качестве идеального кандидата для отслеживания использования rbST (ab) у крупного рогатого скота, поскольку не было возможности наблюдать четкую тенденцию в его транскрипции. Другой ген, связанный с адгезией клеток, оцениваемый в этом исследовании, — это катенин альфа-подобный 1 (CTNNAL1). Однако не удалось обнаружить существенных различий в его транскрипции в результате введения rbST.
Другие гены
Лактоферрин (LTF) представляет собой железосвязывающий гликопротеин, принадлежащий к семейству трансферринов 55 . На рисунке 4 показана эволюция относительной численности гена LTF во всех точках выборки, оцененных в этом исследовании. Хотя повышенная регуляция LTF наблюдалась в предыдущих исследованиях с анаболическими веществами у крупного рогатого скота 38 , не удалось установить четкую тенденцию LTF в отношении лечения rbST. Например, на 9 и 53 дни относительная численность LTF значительно ниже у животных, получавших rbST.Однако на 91-й день относительная численность в этой группе была значительно выше. Необходимо обсудить результаты, полученные для гена коллагена III типа α 1 (COL3A1). Предыдущее исследование показало, что лечение rbST у молочного скота вызывает активацию гена COL3A1 в ткани молочной железы через 6 дней после введения rbST 27 . Однако в настоящей работе обнаружить транскрипты гена COL3A1 не удалось. Также в этом исследовании не была обнаружена транскрипция ESR2.
Панель генов для мониторинга использования rbST (ab) у молочного скота
Конечной целью этой работы было предложить стандартную панель генов, комбинированный образец транскрипции которых позволил бы разработать метод скрининга для контроля неправильного использования rbST на молочных фермах через МСК.В отличие от других предыдущих исследований 27,31,32 , эта работа проанализировала образцы транскрипции генов, связанных с rbST, в 8-месячном эксперименте в реальных условиях, включая 12 циклов введения rbST и контрольных животных. Этот подход позволил получить более точные данные, чтобы различать коров, получавших rbST, и коров контрольной группы.
Был проведен многомерный статистический анализ для выяснения модификаций паттернов транскрипции МСК как следствие введения rbST.Для этой цели использовались только транскрипты девяти генов, которые были успешно измерены в течение всего эксперимента (IGF1R, CCND1, TNF, IL1β, SIRT2, EEFG1, MFEG8, LTF, TDP52L2), за исключением тех генов, которые экспрессировались только в очень небольшом количестве. кейсы / образцы. Основная цель анализа PCA — выявить глобальные закономерности в данных, обнаружив корреляцию между различными переменными, то есть в данном конкретном случае транскрипции разных генов. Проекция образцов в новое многомерное пространство основных компонентов (ПК) потенциально позволит дифференцировать rbST и контрольные группы, выделив также те гены, которые обладают большей способностью, как биомаркеры лечения.На графике оценок анализа PCA, показанном на рис. 5, можно было увидеть тенденцию к группированию в двух группах образцов MSC, при этом животные, обработанные rbST, обозначены красными кружками, а контрольные животные — черными прямоугольниками и помечены в соответствии с экспериментальными данными. день. Различные образцы группы rbST оказались смешанными с контролями в левой части графика, но, как ни странно, большинство из них соответствует дню введения соматотропина (дни 14, 28, 57 или 84) или первым 2-3 дням. после дозы (дни 2, 3, 17, 44 или 115), при которой не было обнаружено явного транскриптомного нарушения.Напротив, очень немногие контрольные животные могут быть классифицированы как коровы, получавшие лечение по PCA, и их ситуация объясняется экстремальными значениями, в частности, плохо различимыми генами, такими как LTF, MFGE8 или SIRT2.
Рисунок 5 График
PCA, построенный с использованием полных транскриптомных профилей соматических клеток молока (МСК), на котором можно различить коров, получавших rbST (N = 6, красные кружки), и контрольных животных (N = 3; черные прямоугольники). быть мельком. Образцы МСК маркируют в соответствии с днем эксперимента, т.е. днем 0 является день введения первой дозы rbST у обработанных животных.
Транскриптомные профили также были подвергнуты OPLS-DA, из которого также были указаны потенциальные дискриминационные гены. На рис. 6а показано визуальное представление многомерной модели, где образцы MSC от контрольных животных нанесены черными квадратами, а образцы из группы rbST — красными кружками. Подобно PCA, несколько образцов rbST проецируются среди контрольных образцов в левой части эллипса. Однако эти образцы были собраны, когда транскриптомное нарушение, вызванное rbST, исчезло (или еще не появилось), поэтому строго их можно было классифицировать как контрольные в тот конкретный момент.И наоборот, очень немногие контрольные образцы были ошибочно классифицированы как rbST. Когда набор тестов недоступен, как в данном случае, метод перекрестной проверки является основной стратегией для оценки качества модели. Результаты процедуры перекрестной проверки суммируются по значению различных параметров качества. В этом исследовании многомерная модель OPLS показала следующие характеристики: R 2 (X) = 0,6, R 2 (Y) = 0,4 и Q 2 = 0,3. Модель объясняет 60% вариации в x-пространстве и 40% вариации в y-пространстве, а точность предсказания составляет 30%.Эти значения указывают на относительно хорошее описание данных моделью и среднюю предсказуемость 34 . Значение p, рассчитанное с помощью CV-ANOVA, составило 3,01 × 10 -7 , что свидетельствует о существовании значительных различий между двумя классами модели. Тот факт, что эта модель была построена с панелью генов с разной дискриминирующей способностью, не следует игнорировать, поскольку это влияет на распознающую способность OPLS. Кроме того, те экспериментальные дни с очень небольшим или отсутствующим эффектом rbST на их транскрипты определенно искажают модель, поскольку на практике они принадлежат к одной группе, но действуют как другая.В будущих моделях многомерного скрининга должна использоваться панель выбранных высокоразличительных генов, и предпочтительно «известные» и «неизвестные» образцы, которые будут спроецированы в многомерной модели, будут принадлежать схожим популяциям (возраст, порода и т. Д.) И период лактации. моменты, в попытке преодолеть межиндивидуальную изменчивость животных 35 . В таких подходах также важно, чтобы прогнозируемая совокупность была больше, чем прогнозируемые выборки. Наконец, причины дискриминации на OPLS-DA были исследованы на соответствующем S-графике (рис.6b), который выявил вклад каждой переменной (транскрипции гена) в разделение двух классов выборки. Как отмечалось в предыдущих разделах, наиболее дискриминантная транскрипция в MSC была обнаружена в генах CCND1, IGF-1R, TNF и IL-1β. Очевидно, что лечение rbST вызывает активацию этих генов, и их использование в будущих панелях мониторинга является многообещающим вариантом для рутинного контроля на молочном животноводстве.
Рисунок 6 Диаграмма рассеяния
OPLS-DA ( a ), построенная с использованием транскриптомных профилей соматических клеток молока, демонстрирующая различие между контрольными (N = 3; черные кружки) и rbST (N = 6; красные точки) животными, обозначены в соответствии с экспериментальным днем (день 0 — день 1-й дозы в группе rbST).S-график ( b ), связанный с дискриминантным анализом OPLS, выделяющий гены, более подверженные влиянию rbST, в верхнем правом углу графика и, следовательно, с более высокой дискриминационной способностью.
Как и при обычном контроле для выявления незаконного использования rbST с этой панелью генов, не будет никакой информации о том, когда коров лечили (другими словами, это слепой анализ), в идеале следует брать пробы каждый день во время лактации / контролируется. Однако с практической точки зрения это предложение звучит немного нереалистично.Предлагается случайный сбор молока один раз в неделю с чередованием рабочих дней. Поскольку соматотропин вводится регулярно в течение всей лактации (начиная с 80–100 дней после родов, раз в две недели), у всех лактирующих коров на ферме, при хорошем плане отбора проб, в какой-то момент на ферме должен быть обнаружен rbST. Транскриптомные данные, полученные из собранных образцов, необходимо сравнить с набором транскриптомных данных из контрольной популяции. Те образцы, которые представили более высокие значения генов, предложенные в этой статье, следует рассматривать как подозрительные.Вторым шагом должно быть исследование конкретной ситуации каждой «положительной» коровы (мастит, беременность и т. Д.) И, при необходимости, продолжение подтверждающего анализа. Важно также подчеркнуть высокую пропускную способность этого подхода ПЦР в реальном времени, что делает план отбора проб осуществимым.
Гормон роста человека производится в лаборатории
Вне лабораторий инженеров-генных, которые работают над одним из самых захватывающих направлений науки, появилась копия молекулы гормона роста человека.Это последний человеческий гормон, который был произведен в лаборатории в последние месяцы в результате широко распространенных и иногда противоречивых исследований, направленных на превращение некоторых бактерий в крошечные фабрики гормонов.
Гормон роста человека производится в лаборатории
Биохимики Калифорнийского университета в Сан-Франциско объявили на прошлой неделе, что они изменили гены штамма бактерий, чтобы бактерии производили гормон роста человека. Это вещество — единственное средство от гипофизарного карликовизма, гормонального дефицита, которым страдают по крайней мере 20 000 американцев.
Доктор Джон Д. Бакстер, член исследовательской группы, сказал в телефонном интервью, что для совершенствования и очистки гормона, вырабатываемого бактериями, потребуется дальнейшая работа. Он сказал, что через год должно быть достаточно вещества, доступного для широкомасштабных испытаний, чтобы продемонстрировать, что гормон, химически идентичный гормону, вырабатываемому в организме человека, работает в живых существах. Он сказал, что примерно через два года он может быть готов к общему использованию.
Кроме того, по словам доктора Бакстера, команда из Сан-Франциско экспериментировала с использованием гормона, продуцируемого бактериями, для остановки кровотечения из определенных типов язв и ускорения заживления переломов.По его словам, предварительные результаты исследований язв обнадеживают, но результаты заживления перелома неубедительны.
«Этот гормон, безусловно, будет испробован при многих условиях», — сказал д-р Бакстер. «Насколько широко его использование ожидает результатов многих тестов».
С доктором Бакстером работали доктора. Джозеф А. Марсьяль, Роберт А. Холлуэлл и Ховард М. Гудман. Их исследование проводилось в Медицинском институте Говарда Хьюза Калифорнийского университета в Сан-Франциско.Полный отчет об их работе планируется опубликовать в следующем месяце в журнале Science.
Их достижение было еще одним примером того, что иногда называют сплайсингом генов или, более формально, технологией рекомбинантной ДНК. Это включает объединение частей ДНК генетического материала или дезоксирибонуклеиновой кислоты, новых способов и трансплантации сегментов или отдельных генов от одного вида к другому через средние бактериальные плазмиды, вещество, которое играет ключевую роль в наследственных аспектах бактериальной клетки.ДНК является активным веществом генов всех живых существ и, следовательно, основным химическим веществом наследственности.
Хотя сплайсинг генов был признан за его потенциал в диагностике и лечении заболеваний, он также вызвал опасения. Что, если бы это привело к созданию новых и опасных бактерий или продуцированных веществ, вызывающих рак или другие нежелательные побочные эффекты? Следовательно, текущие исследования контролируются строгими руководящими принципами, установленными Национальными институтами здравоохранения.
Ученые из Сан-Франциско использовали опухоли гипофиза, удаленные у пациентов, для создания последовательности ДНК, которая направляет клетки на выработку гормона роста человека. Затем эти последовательности ДНК были вставлены в штамм бактерий, родственных тем, которые населяют кишечник человека. Быстрый рост бактериальных клеток привел к появлению множества копий ДНК. Затем этой ДНК манипулировали таким образом, чтобы бактерии могли синтезировать гормон роста.
По мнению ученых, гормон роста может быть одним из важнейших веществ, синтезируемых с помощью генной инженерии.. На данный момент единственным источником гормона роста являются гипофиз, удаленный из трупов. Чтобы сделать одного ребенка на год, нужно 50 трупов.
Недостаток гормона роста вызван нарушением функции гипофиза, который производит гормоны. Дети с этим заболеванием никогда не растут. «Это гормон, который нам действительно нужен, в отличие от инсулина», — сказал доктор Бакстер. Запасов инсулина, полученного в основном от крупного рогатого скота и свиней, достаточно для лечения диабетиков.
Исследования по производству гормона инсулина путем сплайсинга генов «находятся примерно на той же стадии, что и гормон роста.Синтетический инсулин был недавно произведен учеными Калифорнийского университета в Сан-Франциско и Медицинского центра «Город надежды» в Дуарте, Калифорния. Решающий шаг в исследованиях на животных был сделан учеными Гарвардского университета.
Его эффективность была проверена в Институте Солка в Ла-Хойя, Калифорния. Частная компания Genentech Inc. в Пало-Альто, Калифорния, экспериментирует с способами синтеза инсулина в коммерческих количествах.
Другой гормон, соматостатин, который вырабатывается мозгом, также был произведен путем сплайсинга генов в Калифорнийском университете.Маловероятно, что соматостатин, продуцируемый бактериями, будет производиться на коммерческой основе; так как уже есть химическая версия. Этот гормон используется в основном в лабораторных исследованиях механизмов мозга для управления многими гормональными функциями во всем теле.
Гормон роста | Encyclopedia.com
Определение
Тесты на гормон роста измеряют уровни определенных гормонов, которые регулируют рост человека. Эти уровни гормонов измеряются в образцах сыворотки крови, полученных при венепункции.Чтобы изучить функцию гормона роста в определенных условиях, некоторые лекарства можно вводить до взятия крови и измерения уровня гормонов. Гормон роста человека (чГР) (соматотропин) вырабатывается соматотропами в передней доле гипофиза. Его роль в нормальном росте и развитии организма состоит в том, чтобы стимулировать производство белка в мышечных клетках и запускать высвобождение энергии при расщеплении жиров. Диагностические тесты на гормоны роста включают тест на гормон соматотропина, тест на соматомедин C, тест на стимуляцию гормона роста (также известный как тест на аргинин или тест на толерантность к инсулину) и тест на подавление гормона роста (тест на нагрузку глюкозы).
Цель
Тесты на гормон роста назначаются врачами для определения нормального, повышенного или пониженного уровня гормона роста и других родственных гормонов в крови, а также для диагностики состояний, которые могут быть результатом аномального уровня гормонов или дисфункции гипофиза. Некоторые из распространенных причин для тестирования:
- для выявления аномалий роста, которые могут вызвать задержку полового созревания и маленький рост у подростков
- для помощи в диагностике гиперпитуитаризма, который может вызвать гигантизм или акромегалию
- для скрининга на дисфункцию гипофиза
- для помощи в диагностике опухолей гипофиза или опухолей, связанных с гипоталамусом, областью мозга
- для мониторинга эффектов терапии гормона роста, назначаемой при определенных состояниях
Описание
Гормоны роста человека играют важную роль в нормальном росте и развитии человека.Главный гормон роста человека — это белок, состоящий из 191 аминокислоты, строительных блоков белков. Производство этого белка контролируется двумя другими гормонами, секретируемыми гипоталамусом: гормоном высвобождения гормона роста (GHRH), который контролирует секрецию hGH; и гормон, ингибирующий гормон роста (GHIH), который подавляет секрецию hGH. Все здоровые люди имеют измеримые уровни гормона роста на протяжении всей жизни, но есть два заметных всплеска роста, один при рождении, а другой в период полового созревания, и каждый раз гормон роста играет жизненно важную роль.Наиболее очевидный эффект гормона роста — это линейный рост скелета (высота), но метаболические эффекты гормона роста (результат активности гормона роста в организме) на мышцы, печень и жировые клетки являются важной частью его функции. Когда возникает какой-либо вопрос о росте или развитии, педиатры могут исследовать уровни основного гормона роста hGH, его рецепторов и стимуляторов, железы, вырабатывающие гормоны, и сложные взаимодействия гормонов, которые контролируют нормальное развитие.
Соматотропин (чГР) секретируется соматотропами передней доли гипофиза.Обычно он секретируется во время сна с пиковым высвобождением около 22:00, полуночи и 2 часов ночи. Большинство эффектов hGH опосредуются другими гормонами, включая соматомедины, IGH-I (соматомедин C) и IGH-II, которые представляют собой инсулиноподобные гормоны роста, которые также влияют на линейный рост, и два гипоталамических гормона (GHRH и GHIH), которые регулируют hGH, реагируя на изменения уровня сахара в крови (глюкозы) и белка. Когда уровень глюкозы в крови падает, GHRH запускает секрецию сохраненного hGH.Когда уровень глюкозы в крови повышается, секреция hGH отключается из-за активности GHIH. Повышение уровня белка в крови вызывает аналогичную реакцию. Эта петля обратной связи, наряду с эффектами приема пищи и упражнений , отвечает за колебания уровня гормона роста в течение дня. Кроме того, доступность глюкозы и аминокислот в крови для роста также регулируется гормонами адреналином, глюкагоном и инсулином. Все эти факторы роста могут быть оценены, чтобы понять дефицит гормонов или дисфункцию желез при подозрении на дефицит роста.
Ряд гормональных состояний может привести к чрезмерному или замедленному росту. Из-за своей критической роли в производстве гормона роста и других гормонов дисфункциональный гипофиз часто приводит к нарушению роста. Карликовость (очень маленький рост) может быть следствием недостаточной продукции hGH, недостатка IGH-I или недостатка реакции ткани-мишени на любой из этих гормонов роста. Избыточная выработка hGH или IGH-I или чрезмерная реакция на эти гормоны могут привести к гигантизму или акромегалии, оба из которых характеризуются очень большим ростом.
Гигантизм является результатом чрезмерной выработки гормона роста в раннем детстве, что приводит к росту скелета до 8 футов (2,5 м) или более. Акромегалия возникает, когда повышается выработка гормона роста после начала полового созревания. В этом состоянии эпифизарные пластинки длинных костей тела не закрываются, и они остаются чувствительными к дополнительному стимулированному росту гормона роста. Это заболевание характеризуется увеличением черепа, кистей и стоп, носа, шеи и языка.
Соматротропин
Соматротропин (hGH) измеряется в клинической лаборатории для выявления дефицита hGH у подростков с низким ростом, задержкой половой зрелости и другими аномалиями роста или развития.Тест на соматотропин также помогает документировать избыточное производство hGH, ответственного за гигантизм или акромегалию, и подтверждает недостаточную активность или избыточную продукцию гипофиза (гипопитуитаризм или гиперпитуитаризм, соответственно). Однако из-за различной секреции hGH, а также продукции hGH в ответ на стресс, физические упражнения или другие факторы, случайные анализы не являются адекватным определением дефицита hGH. Чтобы получить более точные показания, образец крови можно взять через один-полтора часа после сна (уровень гормона роста увеличивается во время сна), или можно выполнять физические упражнения в течение 30 минут перед забором крови.(Уровень гормона роста человека увеличивается после тренировки.) Ожидается, что уровень гормона роста в конце периода физической нагрузки будет максимальным.
Somatomedin C
Тест на соматомедин C обычно назначается для выявления аномалий гипофиза, дефицита гормона роста и акромегалии. Также называемый инсулиноподобным фактором роста (IGF-1), соматомедин C считается более точным отражением концентрации hGH в крови, поскольку такие переменные, как время дня, уровень активности или диета, не влияют на результаты тестов.Соматомедин C является частью группы пептидов, называемых соматомединами, через которые hGH оказывает свое действие. Поскольку он циркулирует в кровотоке в связке с белками длительного действия, он более стабилен, чем чГР. Однако уровни соматомедина C действительно зависят от уровней hGH, и, как правило, уровни соматомедина C будут низкими, когда уровни hGH недостаточны. Аномально низкие уровни соматомедина С потребуют дальнейшего исследования, поэтому врачи могут провести тест на стимуляцию гормона роста для диагностики дефицита гормона роста. Негипофизарные причины пониженного содержания соматомедина C включают недоедание , тяжелые хронические заболевания, тяжелые заболевания печени, гипотиреоз и карликовость Ларона.
Тест на стимуляцию гормона роста
Тест на стимуляцию гормона роста, также называемый провокационным тестом на гормон роста, толерантностью к инсулину или тестом на аргинин, проводится для проверки способности организма вырабатывать гормон роста человека и подтверждения подозреваемого дефицита гормона роста. У нормального пациента может быть низкий уровень гормона роста, но если уровень гормона роста все еще остается низким после стимуляции, можно поставить более точный диагноз. Тест включает создание состояния инсулино-индуцированной гипогликемии (посредством внутривенной инъекции инсулина) для стимуляции выработки гормона роста и секреции кортикотропина.Если такая стимуляция безуспешна, вероятен сбой в работе передней доли гипофиза. Может потребоваться получить образцы крови после сеанса энергичной тренировки продолжительностью 20 минут.
Вещество, называемое фактором высвобождения гормона роста, также использовалось для стимуляции гормона роста. Этот подход считается более точным и специфичным для дефицита гормона роста, вызванного гипофизом. Дефицит гормона роста также подозревается, когда определение возраста костей с помощью рентгеновских лучей указывает на задержку роста по сравнению с хронологическим возрастом.По состоянию на 2004 год лучшим методом выявления пациентов с дефицитом гормона роста был положительный тест на стимуляцию с последующим положительным ответом на терапевтическое испытание гормона роста.
Тест на подавление гормона роста
Эта процедура, также называемая нагрузочным тестом глюкозы, выполняется для оценки избыточных исходных уровней hGH и подтверждения диагноза гигантизма у детей (и акромегалии у взрослых). Процедура требует взятия двух разных образцов крови: один до того, как ребенок проглотит 100 граммов глюкозы, а второй — через два часа после приема глюкозы.Обычно такая нагрузка глюкозой подавляет секрецию гормона роста. У ребенка с чрезмерным уровнем hGH отсутствие подавления указывает на дисфункцию передней доли гипофиза и подтверждает диагноз гигантизма (или акромегалии).
Меры предосторожности
Прием некоторых лекарств, таких как амфетамины, дофамин, кортикостероиды и фенотиазины, может увеличивать или уменьшать секрецию гормона роста. Педиатр может прекратить прием некоторых лекарств до проведения тестов на гормон роста.Другие факторы, которые могут влиять на секрецию гормона роста, включают стресс, упражнения, диету и аномальный уровень глюкозы. Педиатр может дать рекомендации относительно активности ребенка перед обследованием. Тесты на гормон роста не следует проводить в течение недели после любого радиоактивного сканирования, такого как рентген, МРТ или компьютерная томография.
Подготовка
Тест на чГР или соматотропин требует, чтобы образец крови натощак был взят из вены, обычно в руке. Ребенку не следует ничего есть и пить с полуночи накануне анализа до момента взятия пробы крови.Поскольку стресс и физические нагрузки повышают уровень гормона роста, ребенок должен находиться в полном покое в течение 30 минут перед забором крови. Если врач запросил два образца, их следует брать в последовательные дни примерно в одно и то же время, предпочтительно между 6 и 8 часами утра.
Для теста на соматомедин С также требуется образец крови натощак. Пациенту не следует ничего есть или пить с полуночи накануне до момента взятия пробы крови.
Тест на стимуляцию гормона роста требует внутривенного введения аргинина и / или инсулина.Образцы венозной крови будут взяты через 0, 60 и 90 минут после инъекции.
Для тестирования на подавление гормона роста требуется два образца крови натощак, один перед тестом и еще один через два часа после того, как ребенку будет дан раствор глюкозы перорально. Ребенку не следует есть и пить с полуночи накануне до момента взятия проб крови, а физическая активность должна быть ограничена по крайней мере за 10–12 часов до анализа.
Последующий уход
Обычно гормональные анализы не оказывают никакого эффекта, и можно возобновить нормальную деятельность.Можно наложить повязку, чтобы сохранить чистоту места венепункции или внутривенного введения лекарств и остановить кровотечение, которое может произойти. Об необычном кровотечении или появлении синяка на этом участке следует сообщить педиатру. За ребенком следует внимательно наблюдать после более обширного теста на стимуляцию гормона роста и теста на подавление гормона роста. Педиатр может ограничить деятельность непосредственно в предтестовый период.
Риски
Тесты на гормон роста не имеют значительных рисков.Небольшой дискомфорт может возникнуть во время и после теста на стимуляцию гормона роста из-за внутривенного введения инсулина. Низкий уровень сахара в крови (гипогликемия) является результатом введения инсулина в организм ребенка, что может вызвать у некоторых детей головокружение или вялость. Некоторые дети могут испытывать сонливость, потоотделение и / или нервозность, и все это можно исправить после теста путем приема сока или вливания глюкозы в соответствии с рекомендациями педиатра. В тяжелых случаях гипогликемия может вызвать кетоз (чрезмерное количество побочных продуктов жирных кислот в организме), ацидоз (нарушение кислотно-щелочного баланса организма) или шок.Во время теста медицинский персонал внимательно наблюдает, чтобы предотвратить эти маловероятные реакции или отреагировать на них. Тесты на подавление гормона роста могут вызвать у некоторых детей тошноту после приема глюкозы. Ледяные крошки могут помочь облегчить этот симптом.
Нормальные результаты
Результаты представлены в нанограммах на миллилитр (нг / мл). Нормальные результаты могут отличаться от лаборатории к лаборатории в зависимости от метода, используемого для измерения, но результаты обычно находятся в следующих диапазонах.
Соматотропин (чГР):
- мужчины: 5 нг / мл
- женщины: менее 10 нг / мл
- дети: 0–10 нг / мл
- новорожденные: 10-40 нг / мл
Соматомедин C:
- взрослый: 42–110 нг / мл
- ребенок: 0–8 лет; девочки 7–110 нг / мл; мальчики 4–87 нг / мл
- 9–10 лет: девочки 39–186 нг / мл; мальчики 26–98 нг / мл
- 11–13 лет: девочки 66–215 нг / мл; мальчики 44–207 нг / мл
- 14–16 лет: девочки 96–256 нг / мл; мальчики 48–255 нг / мл
Стимуляция гормона роста: более 10 нг / мл
КЛЮЧЕВЫЕ ТЕРМИНЫ
Акромегалия — Редкое заболевание, возникающее в результате избыточного гормона роста, вызванного доброкачественной опухолью.Если такая опухоль развивается в течение первых десяти лет жизни, результатом является гигантизм (при котором рост ускоряется), а не акромегалия. Симптомы включают огрубление черт лица, увеличение кистей, стоп, ушей и носа, выступание челюсти и удлиненное лицо.
Карликовость гипофиза — Низкий рост. Когда это вызвано дефицитом гормона роста, в отличие от всплеска позднего роста или генетики, могут наблюдаться аномально медленный рост и низкий рост с нормальными пропорциями.
Гигантизм — Чрезмерный рост, особенно в высоту, в результате гиперпродукции гормона роста в детстве или подростковом возрасте опухолью гипофиза.Без лечения опухоль в конечном итоге разрушает гипофиз, что приводит к смерти в раннем взрослом возрасте. Если опухоль развивается после остановки роста, результатом является акромегалия, а не гигантизм.
Гипофиз — Самая важная из эндокринных желез (железы, которые выделяют гормоны непосредственно в кровоток), гипофиз расположен в основании головного мозга. Иногда ее называют «главной железой», она регулирует и контролирует деятельность других эндокринных желез и многие процессы в организме, включая рост и репродуктивную функцию.Также называется гипофизом.
Что касается подавления гормона роста, обычно глюкоза подавляет уровень гормона роста до уровня от неопределяемого до 3 нг / мл в течение от 30 минут до двух часов. У детей стимуляция отскока может произойти через два-пять часов.
Проблемы родителей
Родители могут быть обеспокоены реакцией ребенка на венепункцию или реакцией на внутривенное введение лекарств до тестирования. Родители могут успокоить ребенка, заранее успокоив ребенка и объяснив процедуру.Медицинский персонал и педиатр могут дать инструкции до, во время и после тестов, а также внимательно наблюдать, чтобы минимизировать любые риски. Родители могут быть готовы к сонливости или головокружению после тестирования, имея под рукой сок и кусочки льда, которые помогут облегчить любые чувства, связанные с тошнотой .
Ресурсы
КНИГИ
Czernichow, P., et al. Расстройства роста и обмена веществ при хронических детских заболеваниях: Кембридж, декабрь 2001 г. Гормональные исследования. Базель, Швейцария: S. Karger AG, 2002.
DeGroot, Leslie, et al. Действие гормонов, рост и созревание гипофиза, иммунология, питание, сахарный диабет. Кент, Великобритания: Elsevier — Health Science Division, 2001.
ВЕБ-САЙТЫ
«Гормон роста». Лабораторные тесты онлайн: Американская ассоциация клинической химии, 2001–2004 гг. Доступно в Интернете по адресу
Л. Ли Калверт
Дженис О. Флорес
Гейл Энциклопедия здоровья детей: от младенчества до подросткового возраста Culvert, L .; Флорес, Янис
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie. - Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.