|
Генотропин® |
Лиофилизат д/пригот. р-ра д/п/к введения 5.3 мг/1 мл: картридж двухсекционный с растворителем 1 или 5 шт. рег. №: ЛС-000066 Лиофилизат д/пригот. р-ра д/п/к введения 12 мг/1 мл: картридж двухсекционный с растворителем 1 или 5 шт. рег. №: ЛС-000066 |
|||
|
Джинтропин® |
Лиофилизат д/пригот. р-ра д/п/к введения 4 МЕ: фл. 5 шт. в компл. с растворителем и шприцами одноразовыми; фл.20 шт.; фл.10 или 50 шт. в компл. с растворителем рег. №: ЛСР-003523/09 Дата перерегистрации: 26. Лиофилизат д/пригот. р-ра д/п/к введения 10 МЕ: фл. 5 шт. в компл. с растворителем и шприцами одноразовыми; фл. 20 шт.; фл.10 или 50 шт. в компл. с растворителем рег. №: ЛСР-003523/09 Дата перерегистрации: 26.12.18 |
|||
|
Динатроп® |
Лиофилизат д/пригот. рег. №: ЛП-000517 Дата перерегистрации: 26.04.17 Лиофилизат д/пригот. р-ра д/п/к введения 10 МЕ: фл. 1 шт. в компл. с растворителем и шприцем рег. №: ЛП-000517 Дата перерегистрации: 26.04.17 Лиофилизат д/пригот. р-ра д/п/к введения 16 МЕ: фл. 1 шт. в компл. с растворителем и шприцем рег. №: ЛП-000517 Дата перерегистрации: 26.04.17 Лиофилизат д/пригот. р-ра д/п/к введения 20 МЕ: фл. 1 шт. в компл. с растворителем и шприцем рег. №: ЛП-000517 Дата перерегистрации: 26.04.17 |
|||
|
Нордитропин® НордиЛет® |
Р-р д/п/к введения 10 мг/1. рег. №: П N015447/01 |
|||
|
Нордитропин® НордиЛет® |
Р-р д/п/к введения 15 мг/1.5 мл: картридж в шприц-ручке 1.5 мл 1 шт. рег. №: П N015447/01 |
|||
|
Нордитропин® НордиЛет® |
Р-р д/п/к введения 5 мг/1. рег. №: П N015447/01 |
|||
|
Омнитроп® |
Раствор д/п/к введения 3.3 мг/1 мл: картридж 1.5 мл 1 шт. рег. №: ЛП-001262 |
|||
|
Омнитроп® |
Раствор д/п/к введения 6. рег. №: ЛП-001262 |
|||
|
Растан® |
Лиофилизат д/пригот. р-ра д/п/к введения 4 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛС-001603 Лиофилизат д/пригот. р-ра д/п/к введения 16 МЕ: фл. 1 шт. рег. №: ЛСР-006157/09 Дата перерегистрации: 24.02.10 Лиофилизат д/пригот. р-ра д/п/к введения 20 МЕ: фл. 1 шт. в компл. с растворителем рег. №: ЛСР-006157/09 Дата перерегистрации: 24.02.10 |
|||
|
Растан® |
Р-р д/п/к введения 5 мг/1 мл (15 МЕ/1 мл): картридж 3 мл, вмонтированный в шприц-ручку БиоматикПен®2 рег. Дата перерегистрации: 18.09.18 |
|||
|
Нордитропин® Симплекс® |
Р-р д/п/к введен. 10 мг/1.5 мл: картриджи 1 шт. рег. №: П N013373/01 |
|||
|
Нордитропин® Симплекс® |
Р-р д/п/к введен. рег. №: П N013373/01 |
|||
|
Нордитропин® Симплекс® |
Р-р д/п/к введен. 5 мг/1.5 мл: картриджи 1 шт. рег. №: П N013373/01 |
|||
|
Сайзен® |
Лиофилизат д/пригот. рег. №: П N016125/01 Дата перерегистрации: 24.02.10 |
|||
|
Хуматроп® |
Лиофилизат д/пригот. р-ра д/инъекц. 6 мг: картриджи 3 мл 1 шт. в компл. с растворителем в шприце рег. №: П N015141/01-2003 Лиофилизат д/пригот. р-ра д/инъекц. 12 мг: картриджи 3 мл 1 шт. в компл. с растворителем в шприце рег. №: П N015141/01-2003 |
Сдать анализ: Соматотропный гормон (HGH)
Описание анализа:
Соматотропный гормон (СТГ) – гормон, выделяемый гипофизом, и отвечающий за контроль процессов роста в человеческом организме. Без участия соматотропного гормона невозможно нормальное развитие детей – под его контролем происходит рост костей от рождения до завершения полового созревания.
При недостаточной концентрации соматотропного гормона в крови ребенок начинает отставать в росте от сверстников. При избыточной – растет слишком быстро, причем в некоторых случая это приводит к гигантизму, который влечет за собой множество проблем со здоровьем. Пациенты с гигантизмом часто страдают от головных болей, ухудшения зрения, постоянной слабости, болей в суставах и онемения конечностей.
Пациенты с гигантизмом часто страдают от головных болей, ухудшения зрения, постоянной слабости, болей в суставах и онемения конечностей.
После завершения полового созревания и закрытия зон роста, избыточное количество соматотропного гормона может проявляться акромегалией. Для неё характерно увеличение кистей и стоп в размерах, утолщение костей (в том числе, надбровных дуг и скул), разрастание мягких тканей и огрубление черт лица. Пациенты с акромегалией часто страдают от повышенного давления, диабета, артрозов и головных болей.
Без адекватного лечения акромегалия, как и гигантизм, является заболеванием, ощутимо сокращающим длительность жизни.
Хотя нормальный уровень соматотропного гормона в крови критически важен для детей и подростков, организму взрослых он также необходим. С его участием осуществляется обмен жирных кислот, регулируется плотность костной ткани и поддерживается нормальная мышечная масса.
Секреция соматотропного гормона гипофизом осуществляется неравномерно – максимальная концентрация гормона в крови наблюдается, как правило, в ночное время. Потому тест на СТГ часто дополняется измерением уровня инсулиноподобного фактора роста. Последний анализ позволяет лишь косвенно оценить уровень соматотропного гормона в крови, зато его уровень остается стабильным на протяжении суток.
Потому тест на СТГ часто дополняется измерением уровня инсулиноподобного фактора роста. Последний анализ позволяет лишь косвенно оценить уровень соматотропного гормона в крови, зато его уровень остается стабильным на протяжении суток.
Показания к назначению анализа
Исследование может быть назначено терапевтом, педиатром или эндокринологом. Показаниями могут являться:
- гигантизм у детей и подростков;
- акромегалия у взрослых;
- отставание ребенка в росте;
- симптомы дефицита СТГ у взрослых (снижение плотности костей, снижение выносливости, проблемы с обменом липидов) – назначается редко и только после исключения других возможных причин наблюдаемых симптомов;
- подозрение на опухоли гипофиза.
Значение результатов
Концентрация соматотропного гормона в крови измеряется в нанограммах на миллилитр (нг/мл, ng/ml). Его референтные значения (норма, для большинства здоровых людей) сильно изменяются, в зависимости от возраста пациента.
Если для детей до года нормальной является концентрация от 7,7 до 30,8 нг/мл, то для детей возрастом от 1 до 14 лет – 0,8-7,7 нг/мл. У взрослых женщин нормальным считается уровень СТГ менее 8 нг/мл, а у мужчин – менее 3 нг/мл.
Наиболее частой причиной превышения указанных значений являются опухоли гипофиза, хотя в некоторых случаях они могут быть и причиной дефицита соматотропного гормона. Перед интерпретацией результатов важно знать, не принимает ли пациент препараты, влияющие на концентрацию СТГ. Так инсулин, допамин, амфетамины, эстрогены и никотиновая кислота повышают концентрацию соматотропного гормона, тогда как кортикоиды – снижают.
Подготовка к исследованию
За сутки до забора крови нужно отказаться от жирной пищи, а за 12 часов – от пищи вообще. По предварительному согласованию с врачом, за сутки отменяется прием медикаментов, способных исказить результат.
Материал для исследования: венозная кровь.
Метод исследования: ХРИ.
Срок проведения: 2 рабочих дня.
Запись на анализы
Исследование уровня соматотропного гормона в крови
АНМО «Ставропольский краевой клинический консультативно-диагностический центр»:
355017, г. Ставрополь, ул. Ленина 304
(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнее
Обособленное подразделение «Диагностический центр на Западном обходе»:
355029 г. Ставрополь, ул. Западный обход, 64
(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-68-89 (факс)
Посмотреть подробнее
Клиника семейного врача:
355017 г. Ставрополь, пр. К. Маркса, 110 (за ЦУМом)
Ставрополь, пр. К. Маркса, 110 (за ЦУМом)
(8652) 951-951, (8652) 31-51-51 (контактный телефон)
(8652) 31-50-60 (регистратура)
Посмотреть подробнее
Невинномысский филиал:
357107, г. Невинномысск, ул. Низяева 1
(86554) 95-777, 8-962-400-57-10 (регистратура)
Посмотреть подробнее
Обособленное структурное подразделение в г. Черкесске :
369000, г. Черкесск, ул. Умара Алиева 31
8(8782) 26-48-02, +7-988-700-81-06 (контактные телефоны)
Посмотреть подробнее
Обособленное структурное подразделение в г. Элисте :
358000, г. Элиста, ул. Республиканская, 47
8(989) 735-42-07 (контактные телефоны)
Посмотреть подробнее
ЗАО «Краевой клинический диагностический центр»:
355017 г. Ставрополь, ул. Ленина 304
Ставрополь, ул. Ленина 304
(8652) 951-951, (8652) 35-61-49 (факс)
(8652) 951-951, (8652) 31-51-51 (справочная служба)
Посмотреть подробнее
Обособленное структурное подразделение на ул. Савченко, 38 корп. 9:
355021, г. Ставрополь, ул. Савченко, 38, корп. 9
8 (8652) 316-847 (контактный телефон)
Посмотреть подробнее
Обособленное структурное подразделение на ул. Чехова, 77 :
355000, г. Ставрополь, ул. Чехова, 77
8(8652) 951-943 (контактный телефон)
Посмотреть подробнее
Обособленное структурное подразделение в г. Михайловске:
358000, г. Михайловск, ул. Ленина, 201 (в новом жилом районе «Акварель»).
8(988) 099-15-55 (контактный телефон)
Посмотреть подробнее
Соматотропная недостаточность: возможности современной педиатрии
Низкий рост – отличительный признак ряда наследственных болезней и синдромов, встречающихся в детском возрасте. Нарушения роста и развития у детей являются чрезвычайно актуальными проблемами педиатрии. Нормальный рост и развитие детей, как и состояние их здоровья, имеют огромное социальное и медицинское значение, поскольку служат серьезными индикаторами благополучия и здоровья населения в целом. Особую значимость в педиатрической практике приобретают вопросы генетически обусловленных форм задержки роста
и физического развития у детей.
Нарушения роста и развития у детей являются чрезвычайно актуальными проблемами педиатрии. Нормальный рост и развитие детей, как и состояние их здоровья, имеют огромное социальное и медицинское значение, поскольку служат серьезными индикаторами благополучия и здоровья населения в целом. Особую значимость в педиатрической практике приобретают вопросы генетически обусловленных форм задержки роста
и физического развития у детей.
Влияние гормонов на рост
Задержки роста у детей – состояние гетерогенное. Многие эндокринные, соматические, генетические и хромосомные заболевания сопровождаются задержкой роста. Наиболее часто отставание в росте обусловлено конституциональными особенностями роста и развития ребенка. Важнейшей клинической проблемой задержек роста у детей является дифференциальная диагностика различных вариантов гипофизарного нанизма с целью определения точного варианта низкорослости, прогноза заболеваний и, следовательно, выбора методов терапии. Долгое время эти больные были абсолютно бесперспективными в плане лечения. Сегодня же дети с дефицитом гормона роста (ГР) на фоне заместительной гормональной терапии рекомбинантным соматотропином прекрасно растут и при длительной терапии могут достичь вполне удовлетворительных параметров физического развития взрослого человека. В связи с этим выявление среди низкорослых детей больных с соматотропной недостаточностью, то есть отбор больных для заместительной терапии ГР, является очень важной клинической задачей. Однако решение этой проблемы сопряжено с большими сложностями, которые обусловлены многообразием форм нанизма, а также трудной переносимостью детьми и высокой стоимостью гормональных методов исследования соматотропной недостаточности.
Сегодня же дети с дефицитом гормона роста (ГР) на фоне заместительной гормональной терапии рекомбинантным соматотропином прекрасно растут и при длительной терапии могут достичь вполне удовлетворительных параметров физического развития взрослого человека. В связи с этим выявление среди низкорослых детей больных с соматотропной недостаточностью, то есть отбор больных для заместительной терапии ГР, является очень важной клинической задачей. Однако решение этой проблемы сопряжено с большими сложностями, которые обусловлены многообразием форм нанизма, а также трудной переносимостью детьми и высокой стоимостью гормональных методов исследования соматотропной недостаточности.
Чтобы понять физиологию процесса роста, необходимо ознакомиться со всеми факторами, влияющими на него. Наиболее тяжелые нарушения процессов роста наблюдаются при патологии эндокринной системы. Известно, что практически все гормоны непосредственно или пермиссивно участвуют в процессах роста. Самым выраженным ростовым эффектом обладает соматотропный гормон. Синтез и секреция ГР осуществляются высокоспециализированными клетками гипофиза – соматотрофами. Регулируется секреция ГР гипоталамическими структурами через рилизинг-гормоны, оказывающие стимулирующий (соматолиберин) или подавляющий (соматостатин) эффект. Недавно была открыта новая физиологическая система, контролирующая пульсовую секрецию ГР, – рилизинг-пептиды. В настоящее время синтезирован целый спектр рилизинг-пептидов, способных усиливать секрецию ГР. Исследуется возможность использовать эти препараты при лечении детей с задержкой роста, обусловленной соматотропной недостаточностью гипоталамического происхождения, то есть при сохранной функции соматотрофов. Секреция гипоталамических гормонов, в свою очередь, контролируется несколькими нейротрансмиттерными системами (катехоламинэргической, серотонинэргической, дофаминэргической), оказывающими стимулирующий или ингибирующий эффект.
Синтез и секреция ГР осуществляются высокоспециализированными клетками гипофиза – соматотрофами. Регулируется секреция ГР гипоталамическими структурами через рилизинг-гормоны, оказывающие стимулирующий (соматолиберин) или подавляющий (соматостатин) эффект. Недавно была открыта новая физиологическая система, контролирующая пульсовую секрецию ГР, – рилизинг-пептиды. В настоящее время синтезирован целый спектр рилизинг-пептидов, способных усиливать секрецию ГР. Исследуется возможность использовать эти препараты при лечении детей с задержкой роста, обусловленной соматотропной недостаточностью гипоталамического происхождения, то есть при сохранной функции соматотрофов. Секреция гипоталамических гормонов, в свою очередь, контролируется несколькими нейротрансмиттерными системами (катехоламинэргической, серотонинэргической, дофаминэргической), оказывающими стимулирующий или ингибирующий эффект.
На уровне тканей ростовой эффект ГР осуществляется специфическими пептидами – инсулиноподобными факторами роста (ИФР – соматомединами). Основным местом синтеза этих пептидов является печень. Контролирует синтез соматомединов ГР. Основной точкой приложения ИФР являются эпифизы трубчатых костей, где при участии этих пептидов происходит пролиферация хондроцитов и, следовательно, линейный рост ребенка.
Основным местом синтеза этих пептидов является печень. Контролирует синтез соматомединов ГР. Основной точкой приложения ИФР являются эпифизы трубчатых костей, где при участии этих пептидов происходит пролиферация хондроцитов и, следовательно, линейный рост ребенка.
Секреция ГР подвержена суточным колебаниям и имеет пульсирующий характер. Максимально высокие пики ГР наблюдаются в ночные часы: до 70% суточного количества гормона выделяется ночью. Кроме того, ГР принимает активное участие в адаптационных реакциях организма, поэтому его уровень в течение суток может изменяться и по этой причине. Так, повышение уровня ГР наблюдается при гипогликемии и физической нагрузке. Аминокислоты, глюкагон, вазопрессин, тиреоидные и половые гормоны активно влияют на синтез и выделение ГР и во многом определяют его уровень в крови. Основной эффект ГР – активация анаболических процессов, которые реализуются в ростовом эффекте, увеличение мышечной массы и усиление физической активности. Однако известно, что ГР активно влияет и на другие процессы, которые, безусловно, способствуют реализации ростового эффекта. Так, например, ГР повышает абсорбцию кальция и тем самым улучшает минерализацию костной ткани, активизирует процессы гликогенолиза, липолиза и транспорт глюкозы в ткани и, следовательно, усиливает энергетический обмен. Липолитический эффект ГР также способствует снижению массы тела за счет уменьшения количества подкожного и висцерального жира. Гипохолестеринемический эффект гормона наряду с непосредственным влиянием ГР на сократимость миокарда оказывает существенное влияние на состояние сердечно-сосудистой системы. Хорошо известно влияние ГР на интеллектуальные возможности и психический статус человека: усиливается интеллектуальная активность, улучшаются память и настроение.
Так, например, ГР повышает абсорбцию кальция и тем самым улучшает минерализацию костной ткани, активизирует процессы гликогенолиза, липолиза и транспорт глюкозы в ткани и, следовательно, усиливает энергетический обмен. Липолитический эффект ГР также способствует снижению массы тела за счет уменьшения количества подкожного и висцерального жира. Гипохолестеринемический эффект гормона наряду с непосредственным влиянием ГР на сократимость миокарда оказывает существенное влияние на состояние сердечно-сосудистой системы. Хорошо известно влияние ГР на интеллектуальные возможности и психический статус человека: усиливается интеллектуальная активность, улучшаются память и настроение.
Тиреоидные гормоны (ТГ) в физиологических количествах производят значительный анаболический эффект. В отличие от эффекта ГР, ТГ в большей степени влияют на дифференцирование, созревание тканей (прежде всего костной), чем на линейный рост ребенка. В связи с этим задержки роста при дефиците ТГ характеризуются диспропорциональным развитием ребенка. В то же время ТГ, активно влияя на синтез и секрецию ГР, ускоряют и линейный рост.
В то же время ТГ, активно влияя на синтез и секрецию ГР, ускоряют и линейный рост.
Половые гормоны (ПГ) обладают мощным анаболическим эффектом, ускоряя как линейный рост (пубертатный скачок в росте), так и дифференцирование костной ткани.
Ростовой эффект ПГ осуществляется лишь при наличии ГР, уровень которого в этот период жизни под влиянием ПГ значительно повышается.
Инсулин играет важную роль в регуляции процессов роста, поскольку обеспечивает анаболические процессы энергией и непосредственно усиливает синтез белка.
Глюкокортикоиды, активизируя процессы глюконеогенеза, оказывают выраженное катаболическое действие. Кортизол оказывает отрицательное влияние на процессы роста еще и по той причине, что активно тормозит секрецию ГР.
Минералокортикоиды и тиреокальцитонин непосредственно не участвуют в процессах роста, однако, усиливая процессы концентрации калия в клетке (минералокортикоиды) и оссификацию костной ткани (тиреокальцитонин), безусловно, улучшают ростовой эффект анаболических гормонов.
В период внутриутробной жизни значительный ростовой эффект наряду с ГР и ТГ оказывает хорионический соматомаммотропин (плацентарный лактоген). Именно этот гормон во время внутриутробной жизни, в отсутствие основных анаболических гормонов, обеспечивает нормальный рост плода.
Совместное действие вышеперечисленных гормонов обеспечивает нормальные процессы роста и развития. В то же время на каждом этапе жизни ребенка какой-либо из анаболических гормонов проявляет особенно высокую активность. Так, в первые годы жизни высок уровень ТГ. Именно на этом этапе ТГ обусловливают окончательное созревание органов и систем, прежде всего ЦНС. К тому же высокий уровень ТГ активно стимулирует секрецию ГР, то есть оказывает выраженный ростовой эффект.
После 3-4 лет жизни и до наступления пубертата превалируют процессы линейного роста. Подобный эффект в основном обеспечивается анаболическим действием ГР. На этом этапе жизни темпы роста составляют 5-6 см в год.
На фоне пубертатного периода повышается уровень ПГ и в ответ на это – уровень ГР, что способствует ускоренному росту подростка (до 10-15 см в год).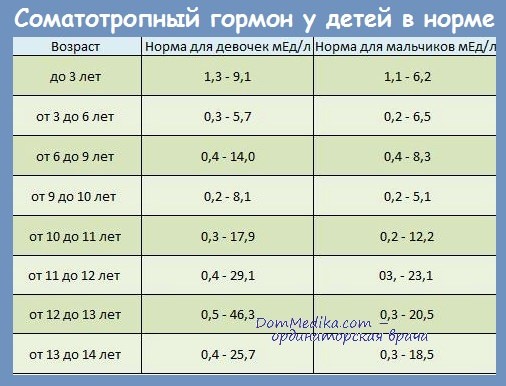 В то же время половые гормоны ускоряют процессы дифференцирования костей скелета, в результате чего происходит слияние эпифизарных щелей и прекращение роста человека. Во многом окончательный рост взрослого человека определяется генетически детерминированными сроками начала, продолжительностью и течением пубертатного периода.
В то же время половые гормоны ускоряют процессы дифференцирования костей скелета, в результате чего происходит слияние эпифизарных щелей и прекращение роста человека. Во многом окончательный рост взрослого человека определяется генетически детерминированными сроками начала, продолжительностью и течением пубертатного периода.
Задержка роста и отставание «костного» возраста являются симптомами многих эндокринных заболеваний, для которых характерен дефицит анаболических или избыток катаболических гормонов.
Причины соматотропной недостаточности
Актуальность проблемы соматотропной недостаточности у детей заключается в наиболее выраженной задержке роста по сравнению с другими заболеваниями, приводящими к низкорослости. Частота этого варианта нанизма, по данным разных авторов, составляет от 1:10000 до 1:15000. Дефицит ГР может быть результатом повреждения гипоталамических или гипофизарных структур. У некоторых пациентов клиника соматотропной недостаточности при нормальном уровне ГР в крови может быть обусловлена нарушением периферической чувствительности к действию гормона в результате патологии рецепторов или, возможно, синтеза биологически не активного ГР. Соматотропная недостаточность довольно часто сочетается с выпадением функции других гормонов гипофиза – пангипопитуитаризмом. Различают идиопатический и органический варианты заболевания. Идиопатический вариант встречается значительно чаще, однако в последние годы в связи с совершенствованием диагностической техники все чаще появляется возможность выявить истинную природу заболевания. Так, использование методов компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) позволяет обнаружить опухоли и дефекты развития гипоталамо-гипофизарной системы и установить у таких больных органический вариант заболевания. Совершенствование генетических методов исследования позволяет выявить патологию гена ГР и таким образом уточнить причину соматотропной недостаточности.
Соматотропная недостаточность довольно часто сочетается с выпадением функции других гормонов гипофиза – пангипопитуитаризмом. Различают идиопатический и органический варианты заболевания. Идиопатический вариант встречается значительно чаще, однако в последние годы в связи с совершенствованием диагностической техники все чаще появляется возможность выявить истинную природу заболевания. Так, использование методов компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) позволяет обнаружить опухоли и дефекты развития гипоталамо-гипофизарной системы и установить у таких больных органический вариант заболевания. Совершенствование генетических методов исследования позволяет выявить патологию гена ГР и таким образом уточнить причину соматотропной недостаточности.
Итак, при идиопатическом варианте пангипопитуитаризма признаков органического повреждения ЦНС нет, патологический процесс, как правило, формируется на уровне гипоталамических структур. У мальчиков заболевание встречается в 2-4 раза чаще, чем у девочек.
Клиническая картина заболевания обусловлена дефицитом гипоталамических гормонов и, следовательно, нарушением функции эндокринных желез. При этом доминируют симптомы дефицита ГР, то есть имеет место выраженная пропорциональная задержка роста. При отсутствии лечения рост взрослых больных не превышает 120 см у женщин и 130 см у мужчин. При рождении и в первые месяцы жизни дети с соматотропной недостаточностью по данным физического развития практически не отличаются от здоровых детей. Задержка роста становится заметной на втором году жизни. Постепенно темпы роста ухудшаются, и после 4 лет жизни дети прибавляют в год не более 2-3 см. Костный возраст значительно отстает от хронологического (более чем на 2 года).
Помимо задержки роста, у детей с дефицитом ГР наблюдается склонность к гипогликемическим состояниям (снижены процессы гликогенолиза). Гипогликемия у некоторых детей может быть первым признаком заболевания и нередко выявляется уже в период новорожденности.
Дефицит тиреотропного гормона (ТТГ) у больных с пангипопитуитаризмом является причиной вторичного врожденного гипотиреоза, что определяет целый комплекс характерных симптомов: психическую вялость, сухость кожных покровов, брадикардию, гипотонию, запоры, поздние появление и смена зубов. Интеллект страдает в меньшей степени, чем при первичном врожденном гипотиреозе. Это обусловлено тем, что щитовидная железа при вторичном гипотиреозе не повреждена и способна нормально функционировать. Роль стимулятора функции щитовидной железы в период внутриутробной жизни берет на себя хориогонин. В этих условиях щитовидная железа плода внутриутробно синтезирует достаточное количество тиреотропного гормона для созревания ЦНС. В постнатальном периоде жизни выраженный дефицит тиреотропного гормона у больных с соматотропной недостаточностью ухудшает процессы роста и дифференцирования костей скелета.
Интеллект страдает в меньшей степени, чем при первичном врожденном гипотиреозе. Это обусловлено тем, что щитовидная железа при вторичном гипотиреозе не повреждена и способна нормально функционировать. Роль стимулятора функции щитовидной железы в период внутриутробной жизни берет на себя хориогонин. В этих условиях щитовидная железа плода внутриутробно синтезирует достаточное количество тиреотропного гормона для созревания ЦНС. В постнатальном периоде жизни выраженный дефицит тиреотропного гормона у больных с соматотропной недостаточностью ухудшает процессы роста и дифференцирования костей скелета.
Дефицит гонадотропных гормонов (ГТГ) является причиной развития гипогонадизма. У части мальчиков с пангипопитуитаризмом уже при рождении имеются признаки внутриутробного дефицита ГТГ (крипторхизм и микрофаллос). В дальнейшем у всех больных выявляются симптомы тяжелого гипогонадизма: вторичные половые признаки отсутствуют, зоны роста остаются открытыми. Выраженный дефицит ПГ, а следовательно, и отсутствие пубертатного скачка в росте еще более усугубляют задержку роста.
У большинства больных с пангипопитуитаризмом имеют место дефицит адренокортикотропного гормона (АКТГ) и гипокортицизм, симптомы которого, как правило, не выявляются. Лишь на фоне терапии тиреоидными и анаболическими препаратами, повышающими активность метаболических процессов, потребность в глюкокортикоидах возрастает и могут выявляться симптомы надпочечниковой недостаточности, чаще в ответ на стрессовую ситуацию.
В дальнейшем уже у взрослых пациентов с врожденной соматотропной недостаточностью, помимо задержки роста, наблюдаются ожирение с абдоминальным типом распределения жира, снижение мышечной массы, остеопороз, гиперхолестеринемия и ранний атеросклероз, низкий уровень физической и интеллектуальной активности. Все это в значительной степени ухудшает качество жизни больных.
При органическом варианте может иметь место повреждение гипоталамо-гипофизарной системы вследствие врожденных дефектов (аплазия или гипоплазия, септо-оптическая дисплазия, синдром пустого турецкого седла, аневризма) или деструктивных повреждений. Наиболее часто у таких больных выявляется врожденная опухоль – краниофарингеома. Помимо задержки роста, у больных с органическим вариантом соматотропной недостаточности может быть выраженная неврологическая симптоматика, признаки повышения внутричерепного давления, ограничение полей зрения. По мере прогрессирования процесса и выпадения других тройных гормонов появляются симптомы гипотиреоза, гипокортицизма, гипогонадизма. Для этого заболевания характерен несахарный, иногда транзиторный, диабет.
Наиболее часто у таких больных выявляется врожденная опухоль – краниофарингеома. Помимо задержки роста, у больных с органическим вариантом соматотропной недостаточности может быть выраженная неврологическая симптоматика, признаки повышения внутричерепного давления, ограничение полей зрения. По мере прогрессирования процесса и выпадения других тройных гормонов появляются симптомы гипотиреоза, гипокортицизма, гипогонадизма. Для этого заболевания характерен несахарный, иногда транзиторный, диабет.
При изолированном дефиците ГР другие соматотропные гормоны выделяются в нормальных количествах, в связи с чем наблюдается более благоприятное течение заболевания: рост взрослых больных несколько выше (у женщин – 125 см, у мужчин – 145 см), симптомов гипотиреоза нет, половое созревание наступает обычно на 2-4 года позже, но протекает нормально, больные, как правило, фертильны. Костный возраст отстает от хронологического, но дифференцирование костей скелета нарушается в меньшей степени, чем при пангипопитуитаризме. По окончании пубертатного периода зоны роста у больных закрываются.
По окончании пубертатного периода зоны роста у больных закрываются.
В настоящее время известны еще три варианта изолированного дефицита соматотропного гормона. Частичный дефицит ГР встречается примерно у 10% больных с изолированным дефицитом ГР. Этот вариант заболевания характеризуется неполным выпадением ГР и более легким течением заболевания. Селективный вариант заболевания характеризуется нарушением регуляции синтеза ГР вследствие нейросекреторной дисфункции. При этом чаще нарушается лишь спонтанная секреция ГР. Однако возможны и другие варианты: снижение спонтанной и стимулированной (на одной из проб) секреции ГР или при нормальном уровне спонтанной секреции уменьшение (на одной из проб) стимулированной секреции ГР. Селективный вариант изолированного дефицита ГР чаще всего имеет место у большинства детей с семейной низкорослостью. Психосоциальный нанизм может встречаться у детей из неблагополучных семей. У подобных детей развивается выраженная задержка роста, костного возраста, психического развития, доказано наличие дефицита ГР. При изменении условий жизни детей уровень ГР самостоятельно восстанавливается, дети начинают расти, однако отставание интеллектуального развития, как правило, сохраняется в течение всей жизни.
При изменении условий жизни детей уровень ГР самостоятельно восстанавливается, дети начинают расти, однако отставание интеллектуального развития, как правило, сохраняется в течение всей жизни.
Синдром Ларона обусловлен нарушением чувствительности рецепторов к ГР. Клиническая картина у больных с подобным синдромом идентична клинической картине изолированного дефицита ГР. Взрослые больные с этим синдромом редко достигают роста 130 см. В то же время уровень ГР (базальный и стимулированный) у больных обычно превышает нормальные показатели, достигая в отдельных случаях 50-100 нг/мл. Отсутствие эффекта ГР объясняют снижением уровня соматомединов (прежде всего ИФР-1), синтез которых не повышается при введении экзогенного ГР. Описаны семейные случаи заболевания, часто в таких семьях регистрируются кровные браки.
Чрезвычайно актуальным является вопрос дифференциальной диагностики вариантов нанизма с целью выявления пациентов с соматотропной недостаточностью. Напомним, что, помимо дефицита ГР (или нарушения механизма его действия), выраженная задержка роста может быть обусловлена дефицитом других анаболических гормонов.
Для большинства больных с врожденным гипотиреозом характерна выраженная задержка роста и костного возраста. Однако, в отличие от пациентов с соматотропной недостаточностью, у данной группы больных наблюдаются диспропорциональная задержка роста и другие характерные клинические симптомы основного заболевания, позволяющие без труда установить причину задержки роста. Сложность дифференциальной диагностики этих состояний может возникнуть лишь в том случае, когда у больного с легким вариантом первичного врожденного гипотиреоза имеет место пропорциональная задержка роста и костного возраста (моносимптомный вариант заболевания) и нет других симптомов врожденного гипотиреоза. Особенности гормонального профиля этих заболеваний позволяют легко установить правильный диагноз: повышение уровня ТТГ и нормальный на фоне стимуляции уровень ГР (после насыщения ТГ) позволяет исключить у больного дефицит соматотропного гормона как причину задержки роста и установить диагноз первичного гипотиреоза (моносимптомный вариант).
Для больных с гипогонадизмом и задержкой полового созревания также характерна задержка роста и костного возраста. Однако эти симптомы начинают обращать на себя внимание лишь в подростковом возрасте. В детстве темпы роста и костный возраст, как правило, соответствуют хронологическому. Выраженная задержка роста как результат преждевременного слияния эпифизарных щелей всегда имеет место у больных с преждевременным половым развитием любой этиологии.
Высокий уровень глюкокортикоидов (синдром Иценко-Кушинга, длительный прием глюкокортикоидных препаратов), обладающих катаболическим эффектом, также может быть причиной задержки роста у детей. Диагностика подобных вариантов задержки роста не трудна, так как на первый план в клинической картине выступают характерные симптомы основного заболевания.
Этапы дифференциальной диагностики
Таким образом, задержка роста у детей и подростков может фиксироваться при многих эндокринных и неэндокринных заболеваниях. Высокая стоимость гормонального обследования, сложность проведения и плохая переносимость детьми диагностических тестов при исследовании соматотропной функции гипофиза диктуют необходимость проведения дифференциальной диагностики вариантов нанизма поэтапно.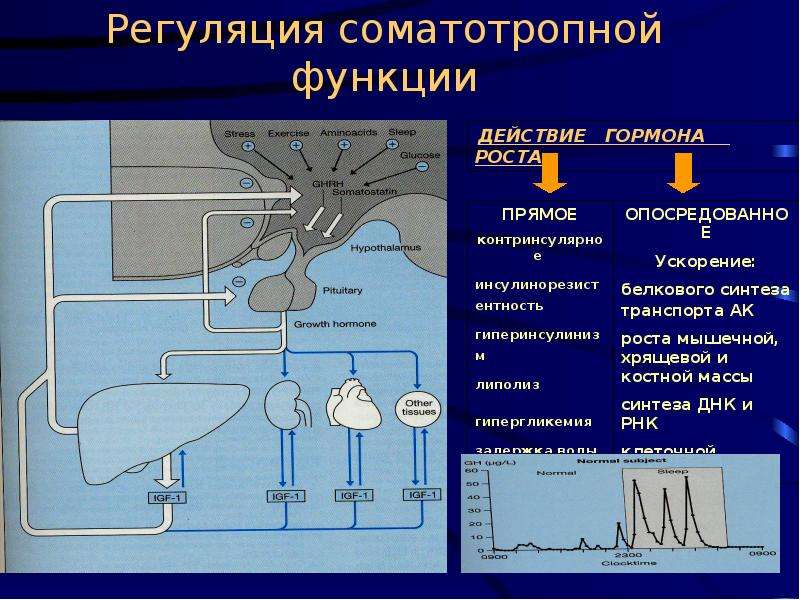 Цель такого подхода к методике проведения дифференциальной диагностики заключается в том, чтобы установить у части пациентов вариант нанизма (по возможности без проведения сложных гормональных исследований), тем самым ограничивая круг пациентов, которым необходимо провести исследование соматотропной функции гипофиза.
Цель такого подхода к методике проведения дифференциальной диагностики заключается в том, чтобы установить у части пациентов вариант нанизма (по возможности без проведения сложных гормональных исследований), тем самым ограничивая круг пациентов, которым необходимо провести исследование соматотропной функции гипофиза.
Первый этап дифференциальной диагностики предполагает выделение пациентов с задержкой роста без клинических признаков соматотропной недостаточности и основного заболевания, которое и явилось причиной задержки роста. По этим признакам без гормонального обследования устанавливается вариант нанизма. Второй этап предполагает выделение больных с клиническими признаками, указывающими на соматотропную недостаточность. Ключевыми признаками дефицита ГР являются значительное отставание в росте, низкие темпы роста (менее 4 см в год), выраженное отставание костного возраста (величина отношения костного возраста к хронологическому составляет менее 0,9). Такие больные нуждаются в проведении гормонального обследования. Однако в связи с тем, что в данной группе пациентов могут оказаться больные, задержка роста у которых обусловлена гипотиреозом или гипогонадизмом, гормональные обследования целесообразно начинать с исследования тиреоидной и половой функций. Методы исследования этих функций более просты и безопасны. Третий этап предполагает исследование и оценку уровня ТТГ, ТГ и ПГ. Выявление гормональных признаков первичного гипотиреоза (моносимптомный вариант) или первичного гипогонадизма позволяет исключить соматотропную недостаточность как причину задержки роста у обследуемого пациента. Следует помнить, что наличие у девочки с задержкой роста первичного гипогонадизма требует дальнейшего обследования для исключения мозаичного варианта синдрома Шерешевского-Тернера (дисгенезии яичников). Нормальная тиреоидная и половая функции или вторичный характер патологии этих желез не исключает наличия соматотропной недостаточности и требует продолжения гормонального обследования. Таким образом, формируется группа пациентов, которым необходимо провести исследование соматотропной функции гипофиза – четвертый этап.
Однако в связи с тем, что в данной группе пациентов могут оказаться больные, задержка роста у которых обусловлена гипотиреозом или гипогонадизмом, гормональные обследования целесообразно начинать с исследования тиреоидной и половой функций. Методы исследования этих функций более просты и безопасны. Третий этап предполагает исследование и оценку уровня ТТГ, ТГ и ПГ. Выявление гормональных признаков первичного гипотиреоза (моносимптомный вариант) или первичного гипогонадизма позволяет исключить соматотропную недостаточность как причину задержки роста у обследуемого пациента. Следует помнить, что наличие у девочки с задержкой роста первичного гипогонадизма требует дальнейшего обследования для исключения мозаичного варианта синдрома Шерешевского-Тернера (дисгенезии яичников). Нормальная тиреоидная и половая функции или вторичный характер патологии этих желез не исключает наличия соматотропной недостаточности и требует продолжения гормонального обследования. Таким образом, формируется группа пациентов, которым необходимо провести исследование соматотропной функции гипофиза – четвертый этап.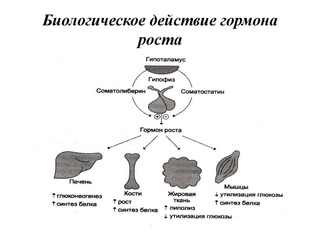 На этом этапе проводится исследование уровня базальной, спонтанной и стимулированной секреции ГР. Хорошим скрининговым тестом, позволяющим заподозрить соматотропную недостаточность, является исследование уровня ИФР-1 в крови. Уменьшение уровня соматомедина свидетельствует о снижении секреции ГР или его действия на периферии.
На этом этапе проводится исследование уровня базальной, спонтанной и стимулированной секреции ГР. Хорошим скрининговым тестом, позволяющим заподозрить соматотропную недостаточность, является исследование уровня ИФР-1 в крови. Уменьшение уровня соматомедина свидетельствует о снижении секреции ГР или его действия на периферии.
Исследование базального уровня ГР малоинформативно, так как в течение дня и у здорового ребенка могут наблюдаться значительные колебания уровня гормона в крови. Лишь исходно высокий уровень ГР (>10 нг/мл) позволяет без дополнительного обследования исключить заболевание, обусловленное дефицитом ГР. Низкий базальный уровень гормона не является доказательством его дефицита. Исследование спонтанной секреции ГР – очень информативный тест. Доказано, что рост ребенка в большей степени коррелирует именно со спонтанной секрецией ГР. Оценивается спонтанная секреция ГР по максимальному ночному пику. Уровень ГР >10 нг/мл позволяет исключить соматотропную недостаточность. К сожалению, на практике этот тест используют очень редко, поскольку для проведения теста требуется специальная система, позволяющая производить забор крови у ребенка во время сна.
К сожалению, на практике этот тест используют очень редко, поскольку для проведения теста требуется специальная система, позволяющая производить забор крови у ребенка во время сна.
В настоящее время наиболее часто соматотропная функция гипофиза оценивается по уровню стимулированной секреции ГР. Во избежание ошибок и для выявления вариантов нейросекреторной дисфункции существует правило, диктующее необходимость проведения у каждого больного не менее 2 стимуляционных проб. Повышение уровня ГР >10 нг/мл (в обеих пробах) исключает дефицит ГР. Уровень ГР на фоне проб <7 нг/мл позволяет установить диагноз соматотропной недостаточности. Уровень ГР в пределах 7-10 нг/мл свидетельствует о частичном дефиците ГР. Отсутствие повышения уровня ГР в одной из проб дает основание говорить о селективном дефиците ГР, то есть о нейросекреторной дисфункции.
При выявлении у больного с задержкой роста симптомов, указывающих на гипотиреоз, исследование уровня ГР следует проводить на фоне насыщения ТГ, у подростков с задержкой роста и отсутствием признаков полового развития – после насыщения ПГ.
Дифференцирование вариантов соматотропной недостаточности (пангипопитуитаризм или изолированный дефицит ГР) проводят на основании клинических и лабораторных данных об уровне других соматотропных гормонов (ТТГ, ГТГ, АКТГ).
Уточнение уровня поражения гипоталамо-гипофизарной системы (гипоталамус или гипофиз) у больных с соматотропной недостаточностью проводят на основании данных пробы с рилизинг-ГР – соматолиберином. Повышение уровня ГР в ответ на введение соматолиберина свидетельствует о гипоталамическом уровне патологии, а отсутствие реакции – о поражении гипофиза (возможно, опухолевого характера). Наличие выраженной задержки роста в сочетании с высоким уровнем ГР дает основание заподозрить синдром Ларона. Снижение в крови уровня соматомедина (ИФР-1) подтверждает диагноз синдрома Ларона.
Лечебная тактика
Для лечения больных с соматотропной недостаточностью с 1985 г. во всем мире используют генно-инженерный ГР человека. Эффективность этого препарата у больных с соматотропной недостаточностью очень высока.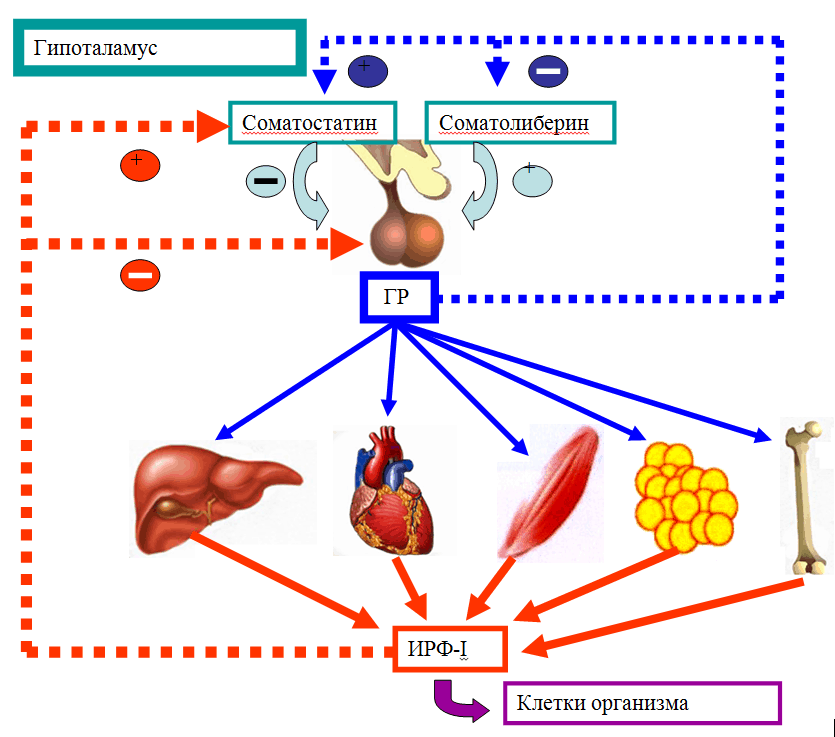 В первый год лечения дети вырастают в среднем на 10-12 см. В последующие годы темпы роста несколько снижаются, но обычно превышают среднегодовую скорость роста и составляют, как правило, более 5-6 см в год. При длительном и систематическом лечении пациенты достигают нормальных параметров роста взрослого человека. У лиц более молодого возраста со значительным отставанием дифференцирования костей скелета эффективность препарата выше. Так, дети первых лет жизни (до 2 лет) достигают нормального для хронологического возраста роста в течение 5 лет систематического лечения.
В первый год лечения дети вырастают в среднем на 10-12 см. В последующие годы темпы роста несколько снижаются, но обычно превышают среднегодовую скорость роста и составляют, как правило, более 5-6 см в год. При длительном и систематическом лечении пациенты достигают нормальных параметров роста взрослого человека. У лиц более молодого возраста со значительным отставанием дифференцирования костей скелета эффективность препарата выше. Так, дети первых лет жизни (до 2 лет) достигают нормального для хронологического возраста роста в течение 5 лет систематического лечения.
Очень сложным вопросом у больных с изолированным дефицитом ГР являются сроки начала спонтанного пубертата. В случае ускорения костного возраста при лечении больных ГР дети быстрее вступают в пубертат и, следовательно, не могут достичь удовлетворительного роста. В связи с этим возникает вопрос о целесообразности назначения подобным пациентам с целью остановки пубертатного развития синтетических люлиберинов. При достижении приемлемого роста препарат отменяют, и половое развитие у больного восстанавливается.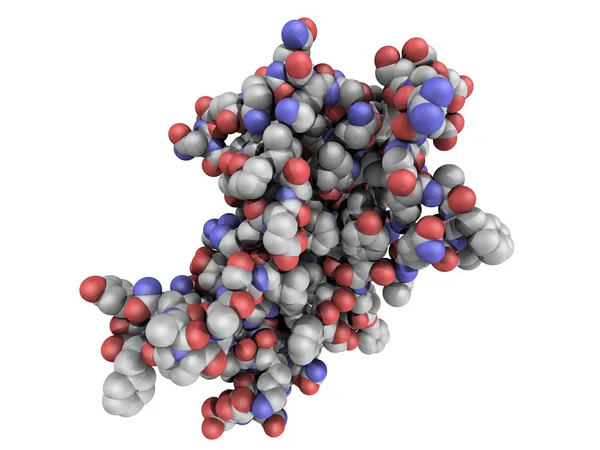 Целесообразность подобного вмешательства широко обсуждается в литературе.
Целесообразность подобного вмешательства широко обсуждается в литературе.
До последнего времени в большинстве руководств по лечению ГР рекомендовалось проводить терапию до полного слияния эпифизарных щелей или достижения приемлемого роста. В то же время хорошо известно, что ГР, помимо усиления линейного роста, обладает и другими очень важными эффектами, значительно повышающими качество жизни человека: нормализует липидный обмен, кардиальную функцию, массу тела, мышечную массу, минерализацию костной ткани, интеллектуальную активность. В связи с этим в настоящее время доминирует точка зрения о необходимости пожизненной заместительной терапии ГР у больных с соматотропной недостаточностью. Следовательно, при достижении приемлемого роста и окончательного слияния эпифизарных щелей необходимо продолжать лечение ГР. Рекомендуемые дозы составляют 0,1-0,2 ЕД/кг массы тела в неделю. Исследования по определению оптимальной дозы препарата у взрослых пациентов с соматотропной недостаточностью продолжаются. Лечение вторичного гипотиреоза, гипогонадизма и гипокортицизма (при необходимости) проводится в течение всей жизни.
Лечение вторичного гипотиреоза, гипогонадизма и гипокортицизма (при необходимости) проводится в течение всей жизни.
Больные с органической формой соматотропной недостаточности (чаще краниофарингеомой), помимо эндокринологического, нуждаются в нейрохирургическом наблюдении и лечении. Вопрос о лечении ГР решается эндокринологом и нейрохирургом совместно. Противопоказано назначение препарата при прогрессирующем росте опухоли. При удалении краниофарингеомы лечение ГР проводится по обычной схеме. Рецидивы опухоли встречаются крайне редко. Опасность развития рецидива опухоли на фоне заместительной терапии ГР не превышает таковую у лиц, не получающих гормональную терапию.
Пациенты с соматотропной недостаточностью по типу нейросекреторной дисфункции также нуждаются в заместительной терапии ГР. Этот вариант дефицита ГР имеет место у большинства пациентов с семейной низкорослостью. Следовательно, при выявлении у детей с семейной низкорослостью данного варианта соматотропной недостаточности необходимо решать вопрос о заместительной терапии ГР. По данным литературы, на фоне короткого курса лечения (6 месяцев) в обычном режиме у детей с семейной низкорослостью был отмечен значительный ростовой эффект. За 6 месяцев лечения дети в среднем выросли на 6 см, опережения костного возраста по отношению к хронологическому не наблюдалось. По окончании курса лечения коэффициент отношения костного возраста к хронологическому не превышал 0,9, что дает основание надеяться на нормальные сроки вступления детей в пубертат. Однако на основании данных короткого курса лечения нельзя быть уверенным, что при длительном лечении не произойдет более быстрого вступления в пубертат и, как следствие, ухудшения прогноза относительно окончательного роста пациента. В связи с этим в настоящее время можно рекомендовать лишь короткие, возможно, повторные (2-3) курсы лечения (не более 6 месяцев) под контролем «костного» возраста.
По данным литературы, на фоне короткого курса лечения (6 месяцев) в обычном режиме у детей с семейной низкорослостью был отмечен значительный ростовой эффект. За 6 месяцев лечения дети в среднем выросли на 6 см, опережения костного возраста по отношению к хронологическому не наблюдалось. По окончании курса лечения коэффициент отношения костного возраста к хронологическому не превышал 0,9, что дает основание надеяться на нормальные сроки вступления детей в пубертат. Однако на основании данных короткого курса лечения нельзя быть уверенным, что при длительном лечении не произойдет более быстрого вступления в пубертат и, как следствие, ухудшения прогноза относительно окончательного роста пациента. В связи с этим в настоящее время можно рекомендовать лишь короткие, возможно, повторные (2-3) курсы лечения (не более 6 месяцев) под контролем «костного» возраста.
Таким образом, для своевременного проведения необходимых терапевтических мероприятий соматотропную недостаточность очень важно выявить в раннем возрасте. Клинические данные свидетельствуют о том, что в целом эффективность лечения выше у детей младшего возраста с меньшей скоростью роста до лечения, с большей задержкой роста и костного созревания, с большим дефицитом соматотропного гормона. При рано начатом и регулярно проводимом лечении удается достичь прогнозируемого роста (Consensus guidelines for the diagnosis and treatment of Growth Hormone Deficiency in childhood and adolescence: summary statement of the GH Research Society, 2000). В большинстве случаев больные достигают ожидаемого клинического эффекта и адаптируются к условиям окружающей жизни.
Клинические данные свидетельствуют о том, что в целом эффективность лечения выше у детей младшего возраста с меньшей скоростью роста до лечения, с большей задержкой роста и костного созревания, с большим дефицитом соматотропного гормона. При рано начатом и регулярно проводимом лечении удается достичь прогнозируемого роста (Consensus guidelines for the diagnosis and treatment of Growth Hormone Deficiency in childhood and adolescence: summary statement of the GH Research Society, 2000). В большинстве случаев больные достигают ожидаемого клинического эффекта и адаптируются к условиям окружающей жизни.
Благодаря возможностям получения соматотропина с помощью генно-инженерных технологий показания к его применению значительно расширились и в настоящее время не ограничиваются только лечением при гипофизарной карликовости. Имеются данные об эффективности соматотропина в лечении детей с внутриутробной задержкой роста, хондродисплазией, состоянием после облучения по поводу лейкозов и опухолей мозга, после трансплантации почки, с хронической почечной недостаточностью и другими заболеваниями.
Подготовил Андрей Ковтун
СТАТТІ ЗА ТЕМОЮ
24.11.2021
Інфекційні захворювання
Нові стратегії лікування COVID‑19
Пандемія коронавірусної хвороби (COVID‑19) є загрозою для громадського здоров’я в усьому світі. Високі показники госпіталізації пов’язані з відсутністю специфічної противірусної терапії на ранніх етапах захворювання. Цьому й іншим питанням була присвячена науково-практична конференція з міжнародною участю «Нові стратегії лікування COVID‑19», яка відбулася 29 жовтня під егідою АТ «Фармак». …
…
23.11.2021
Акушерство/гінекологія
Акушерська кровотеча та ризик виникнення серцево- судинного захворювання через три десятиліття: популяційне когортне дослідження
Представляємо вашій увазі результати дослідження U.V. Ukah, R.W. Platt et al. (2020), у якому встановлено, що наявність
в анамнезі у жінки акушерської кровотечі є фактором ризику виникнення у неї в подальшому серцево-судинного захворювання.
Особливо високий ризик виникнення серцево-судинного ускладнення виявлено у пацієнток із кровотечею, яким було проведено
переливання крові. На підставі отриманих даних важливо дослідити можливості кардіопрофілактики в осіб із акушерськими
На підставі отриманих даних важливо дослідити можливості кардіопрофілактики в осіб із акушерськими
кровотечами…
Глава 15.10. Доклинические и клинические исследования биоаналогичного (биоподобного) лекарственного препарата соматотропного гормона
Содержимое (Table of Contents)
1. Введение
Настоящая глава является дополнением к главе 15.2 настоящих Правил и устанавливает требования проведения доклинических и клинических исследований для демонстрации подобия (сходства) лекарственных препаратов, содержащих соматотропин и заявленных как биоаналогичные (биоподобные) уже представленному на рынке оригинальному (референтному) препарату.
В разделе, посвященном проведению доклинических исследований, представлены рекомендации для оценки фармако-токсикологических свойств препаратов. В разделе, посвященном клиническим исследованиям, содержатся указания для демонстрации подобия (сходства) фармакодинамических, фармакокинетических свойств, эффективности и безопасности 2 препаратов и план управления рисками. Также представлены критерии для экстраполяции клинических данных на другие показания, утвержденные для оригинального (референтного) препарата.
Регистрационное досье нового рекомбинантного гормона роста человека (соматотропина), заявленного в качестве подобного уже представленному на рынке лекарственному препарату, должно содержать доказательства сопоставимости рассматриваемого нового препарата оригинальному (референтному) лекарственному препарату, уже зарегистрированному в Союзе.
Соматотропин продуцируется клетками передней доли гипофиза и представляет собой аминокислотную негликозилированную цепочку, состоящую из 191 аминокислоты, с молекулярной массой 22 кДа. В клинической практике применяется рекомбинантный гормон роста человека (рчГР), который имеет аналогичную с эндогенным аминокислотную последовательность и производится с использованием технологии рекомбинантной ДНК в системе экспрессирующей клеток E. coli, дрожжей или клеток млекопитающих. Для характеристики структуры и биологической активности соматотропина доступны соответствующие физико-химические и биологические методы. Ряд методик и биологических тестов необходимо использовать для характеристики активной фармацевтической субстанции и таких родственных примесей, как дезамидированные и окисленные формы и агрегаты.
Ряд методик и биологических тестов необходимо использовать для характеристики активной фармацевтической субстанции и таких родственных примесей, как дезамидированные и окисленные формы и агрегаты.
Соматотропин обладает мощным анаболическим, липолитическим и контринсулярным (острая инсулиноподобная активность) эффектами. Данные эффекты обусловлены как непосредственным взаимодействием с рецепторами (например, на адипоцитах и гепатоцитах), так и косвенно в результате стимуляции инсулиноподобных факторов роста (преимущественно ИФР-1). Препараты, содержащие в качестве действующего вещества соматотропины, используются в клинической практике для стимуляции нормального роста и (или) формирования тела у больных с дефицитом соматотропина и при некоторых состояниях без дефицита соматотропина. Считается, что при применении рекомбинантного гормона роста человека при всех одобренных в настоящее время показаниях он взаимодействует с одними и теми же рецепторами.
Препараты рчГР используются в широком диапазоне доз для лечения детей в период их роста, в то же время взрослые больные являются более чувствительными к побочным эффектам препарата.
Описаны случаи выработки антител в ответ на введение рчГР, в том числе очень редко — нейтрализующих антител. Это в основном было связано с чистотой и стабильностью применяемых препаратов. Препараты рчГР вводят подкожно, возможные факторы риска развития иммунного ответа, связанные с особенностями состояния больных, не известны.
2. Сфера применения
Настоящая препарат специфичная глава содержит доклинические и клинические требования к подтверждению биоаналогичности (биоподобия) 2 лекарственных препаратов, содержащих рчГР.
3. Связь с другими главами
В главах 15 — 15.2 настоящих Правил содержатся общие указания по разработке биоаналогичных (биоподобных) лекарственных препаратов.
4. Основной текст документа
4.1. Доклинические исследования
До проведения клинических исследований необходимо провести сравнительные доклинические исследования. Основной целью доклинических исследований является выявление возможных различий фармакотоксикологических характеристик биоаналогичного (биоподобного) и оригинального (референтного) препаратов гормона роста, а не изучение результатов как таковых. Выбор подхода к методу исследования должен быть полностью обоснован в доклиническом обзоре (модуль 2.4 регистрационного досье).
Выбор подхода к методу исследования должен быть полностью обоснован в доклиническом обзоре (модуль 2.4 регистрационного досье).
Исследование фармакодинамики
Исследование in vitro
Для оценки любых возможных различий биологической активности между биоаналогичным (биоподобным) и оригинальным (референтным) препаратами необходимо представить данные, полученные при проведении ряда сравнительных биотестов (например, исследований связывания с рецепторами, оценки пролиферации клеток), многие из которых могут быть получены в процессе изучения качества препаратов.
Исследование in vivo
Сравнительные исследования in vivo фармакодинамических свойств биоаналогичного (биоподобного) и оригинального (референтного) препаратов проводятся с использованием экспериментальных моделей (на грызунах). Например, анализируется динамика увеличения массы тела и (или) роста большеберцовой кости у неполовозрелых гипофизэктомированных крыс. Такие данные могут быть получены в процессе выполнения тестов, связанных с оценкой качества препаратов.
Такие данные могут быть получены в процессе выполнения тестов, связанных с оценкой качества препаратов.
Токсикологические исследования
Токсикологические исследования должны включать в себя по крайней мере 1 сравнительное исследование 1 дозы при многократном введении с использованием релевантных видов животных (например, крыс) при длительности исследования не менее 4 недель. В процессе проведения исследований выполняются соответствующие измерения токсикокинетики препарата, особое внимание необходимо уделить изучению иммунного ответа на препарат.
Необходимо представить данные изучения местной переносимости по крайней мере у 1 вида животных. Если это возможно, данные исследования могут быть проведены в процессе оценки токсичности при многократном введении препарата.
Изучение фармакологической безопасности, репродуктивной токсичности, мутагенности и канцерогенности не входит в перечень стандартных требований к доклиническим исследованиям подобных биологических лекарственных препаратов, содержащих в качестве активной фармацевтической субстанции рчГР.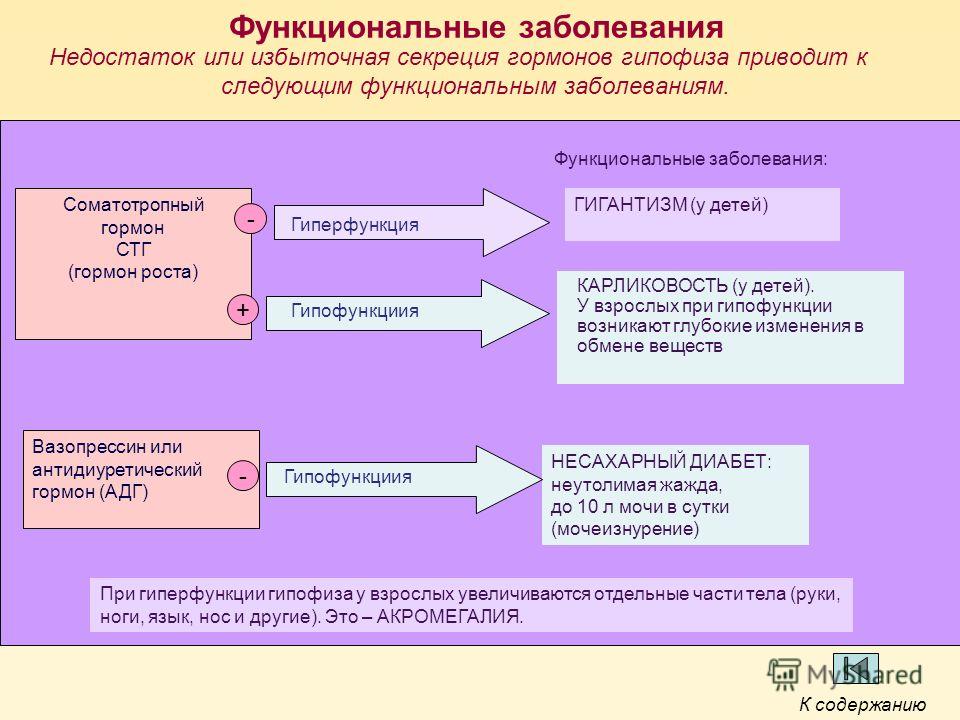
4.2. Клинические исследования
Исследование фармакокинетики
Сравнительная оценка фармакокинетических свойств рчГР проводится в одном перекрестном исследовании биоаналогичного (биоподобного) и оригинального (референтного) препаратов при подкожном введении. В исследование можно привлекать здоровых добровольцев, однако при этом следует рассмотреть необходимость подавления продукции эндогенного гормона роста такими препаратами, как аналоги соматостатина.
К первичным показателям, на основании которых проводится характеристика фармакокинетических свойств препаратов, относится AUC, вторичными показателями фармакокинетики являются Cmax и T1/2. Пределы сопоставимости также должны быть определены заранее и должным образом обоснованы.
Исследование фармакодинамики
Изучение фармакодинамических свойств препарата предпочтительно проводить в рамках исследования фармакокинетики. Для этого необходимо подобрать дозу таким образом, чтобы она соответствовала линейной восходящей части кривой «доза — эффект».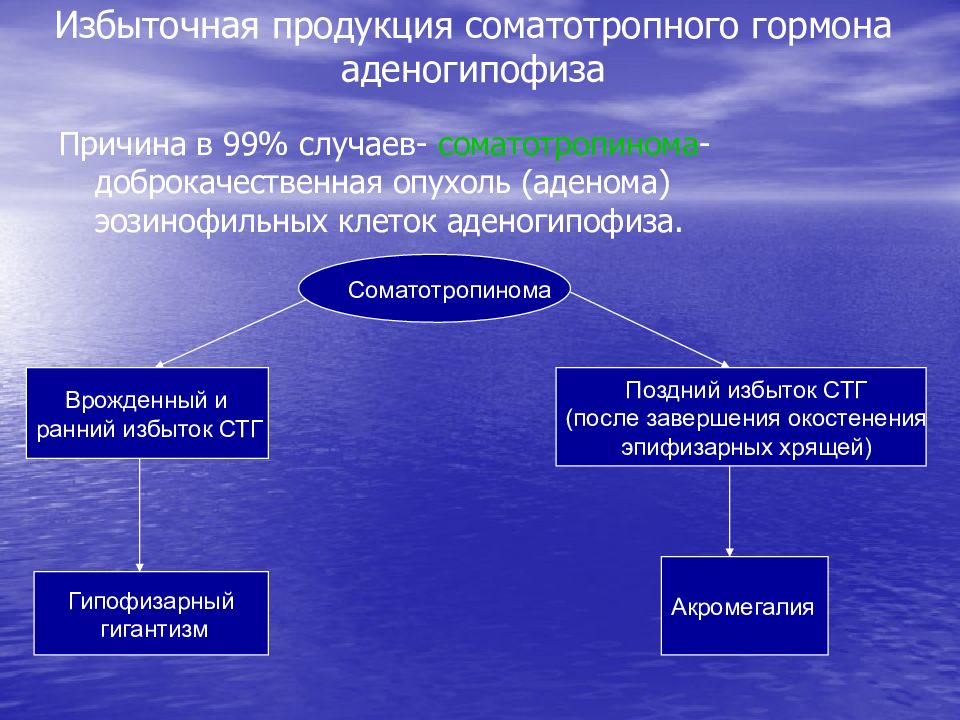 Наиболее подходящим маркером для сравнительной оценки фармакодинамических свойств биоаналогичного (биоподобного) и оригинального (референтного) препаратов является ИФР-1. Кроме того, для оценки фармакодинамики могут быть использованы и другие маркеры, например, белок, связывающий инсулиноподобный фактор роста (ИФРВР-3). Следует учитывать, что вследствие отсутствия четкой связи между уровнем ИФР-1 в сыворотке и индуцируемым им ростом тела ИФР-1 не может использоваться как суррогатный маркер эффективности соматотропина в клинических исследованиях.
Наиболее подходящим маркером для сравнительной оценки фармакодинамических свойств биоаналогичного (биоподобного) и оригинального (референтного) препаратов является ИФР-1. Кроме того, для оценки фармакодинамики могут быть использованы и другие маркеры, например, белок, связывающий инсулиноподобный фактор роста (ИФРВР-3). Следует учитывать, что вследствие отсутствия четкой связи между уровнем ИФР-1 в сыворотке и индуцируемым им ростом тела ИФР-1 не может использоваться как суррогатный маркер эффективности соматотропина в клинических исследованиях.
Исследование эффективности
Сравнительное изучение эффективности биоаналогичного (биоподобного) и оригинального (референтного) препаратов должно быть продемонстрировано как минимум в 1 рандомизированном параллельном исследовании достаточной статистической мощности. Для исключения системной ошибки исследование эффективности должно быть двойным слепым. Если это невозможно, необходимо закрыть доступ лицу, отвечающему за измерение параметров клинической эффективности, к данным о распределении испытуемых по группам.
Чувствительность к лечению рчГР выше среди больных с дефицитом гормона роста, чем среди больных, у которых отсутствует дефицит гормона роста. Оптимальной и хорошо изученной моделью оценки эффективности является популяция детей с дефицитом гормона роста, которые ранее не получали подобное лечение, поскольку такой подход обеспечит использование чувствительной и хорошо изученной модели. В исследование необходимо включать детей препубертатного периода для исключения трудности в интерпретации данных, связанной с активным ростом в пубертатный период и ростом, обусловленным эффектом препарата. Это достигается лимитированием возраста (по календарному или костному возрасту) при включении в исследование. Важно, чтобы группы исследования были однородными по исходным характеристикам, поскольку это будет влиять на чувствительность исследования и точность конечных точек.
Первичной конечной точкой исследований эффективности является динамика (изменение) скорости роста или отклонения от динамики стандартной скорости роста по сравнению с исходным уровнем за определенный период времени. В качестве вторичной конечной точки рекомендуется показатель отставания от стандартного роста. Следует делать поправку на факторы, влияние которых на рост при лечении соматотропином уже известно.
При проведении сравнительных исследований необходимо не менее 3 раз проводить измерение роста в каждой временной точке исследования и рассчитывать усредненные данные. При проведении измерений роста рекомендуется применение поверенных измерительных приборов, использование стандартных методик, проведение измерений в одно и то же время суток, предпочтительно одним и тем же исследователем. Это позволяет снизить число ошибок измерения и вариабельность.
Для получения достоверных результатов важно проводить измерение роста до исследования и в процессе исследования с помощью одной и той же стандартизованной методики и с использованием одних и тех же валидированных измерительных приборов.
При кратковременных измерениях роста велика вероятность появления ошибок, связанных со значительной вариабельностью кратковременных периодов роста и сезонными колебаниями, поэтому рекомендованная продолжительность фазы сравнения составляет от 6 до 12 месяцев. Вычисление темпов роста при предварительной обработке данных должно осуществляться с учетом данных, полученные в течение не менее чем 6 месяцев и не более чем 18 месяцев. Диапазон параметров сопоставимости должен быть определен и полностью обоснован заранее, главным образом на основе клинических показателей, обеспечивающих достоверность исследования.
4.3. Исследование безопасности
Данных, полученных при наблюдении за пациентами в ходе исследований эффективности, обычно достаточно для создания адекватной предмаркетинговой базы данных по безопасности. Заявитель должен представить сравнительные показатели по иммуногенности, полученные от пациентов, участвовавших в исследовании эффективности, за 12-месячный период с интервалом забора образцов в 3 месяца. Тестирование нужно проводить с использованием валидированных методов, обладающих достаточной специфичностью и чувствительностью.
Кроме того, клиническое изучение безопасности включает в себя контроль содержания ИФР-1, ИФРВР-3, определение инсулина и глюкозы в крови натощак.
4.4. План фармаконадзора
При регистрации препарата необходимо представить в модуль 1 регистрационного досье план управления рисками в соответствии с Правилами регистрации и экспертизы лекарственных средств для медицинского применения и надлежащей практикой фармаконадзора. При этом необходимо учитывать риски, установленные в процессе разработки препарата, потенциальные риски, связанные с иммуногенностью, а также указать, как эти вопросы будут исследованы при наблюдении в пострегистрационный период.
4.5. Экстраполяция результатов исследований
Результаты исследований эффективности и безопасности, полученные в исследованиях, проведенных в популяции детей с дефицитом гормона роста, могут быть экстраполированы на другие показания, указанные для оригинального (референтного) препарата при условии должного обоснования со стороны заявителя.
Поделиться ссылкой:
История терапии гормоном роста
Indian J Endocrinol Metab. 2011 сен; 15 (Дополнение 3): S162 – S165.
Вагиш С. Айяр
Отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия
Отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия
Автор для корреспонденции: Д-р Вагиш С. Айяр, отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия. Электронная почта: moc.liamg@rayyagav Авторские права: © Индийский журнал эндокринологии и метаболизма
Это статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.
Abstract
Хотя важность гипофиза для роста была признана в конце 19 века, терапия гормоном роста (GH) стала доступной для детей и подростков с тяжелым дефицитом GH только в конце 1950-х годов. Использование GH для других состояний было ограничено из-за ограниченного количества человеческого гормона, производного от гипофиза.С неограниченной доступностью рекомбинантного человеческого GH (rhGH) сценарий лечения GH сильно изменился. В настоящее время постоянно увеличивается список показаний к лечению гормона роста у детей, подростков и взрослых.
Ключевые слова: Гормон роста, история, гипофиз
ВВЕДЕНИЕ
Борьба за открытие гормона роста (GH) была длительной и упорной. Этот увлекательный обходной путь к открытиям потребовал участия множества клиницистов, химиков, физиологов и патологов.Сказка наполнена удивительными прозрениями, а также поразительными ошибками, интуитивной прозорливостью и неудачными трудами, победами и поражениями.
ИСТОРИЯ ГОРМОНА РОСТА
Усилия по приобретению гипофизарного гормона роста для лечения детей с дефицитом гормона роста начались в середине 1940-х годов. Первоначальная работа над субприматами длилась почти десять лет. Эти усилия привели к очистке бычьего GH Ли и Эвансом в Калифорнийском университете в Беркли и Фишманом в Йельском университете. А свиной GH был очищен Рабеном и Вестермейером в Тафтсе.Но ни один из этих препаратов не показал значительной биохимической или метаболической активности, потому что действие GH зависит от вида [1].
Гормон роста (GH) впервые был выделен из гипофиза человека в 1956 году Ли и Папкофф в Калифорнии и Рабеном в Массачусетсе, но его биохимическая структура не была выяснена до 1972 года. В 1958 году Рабен сообщил о результатах. первого испытания, демонстрирующего влияние человеческого гормона роста на рост. К 1960 году стало ясно, что дети с дефицитом гормона роста выиграют от гипофизарного гормона роста.В 1960 году было сформировано Национальное агентство по гипофизу (NPA) для достижения целей координации сбора и извлечения гипофиза для поддержки как фундаментальных, так и клинических исследований. [1,2] В период с 1963 по 1985 год NPA контролировало почти все лечение GH в Соединенных Штатах. Состояния. И за этот период около 7700 детей в Соединенных Штатах и 27000 детей во всем мире получали GH, выделенный из гипофиза человека, для лечения тяжелого дефицита гормона роста (GHD). [3,4]
К 1985 году гипофизарный GH использовался почти для всех. 30 лет в США и Канаде в исследовательских или терапевтических целях.В 1985 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (US FDA) получило сообщения о четырех молодых взрослых в Соединенных Штатах с смертельной, медленной вирусной (прионной) болезнью Крейцфельдта-Якоба (CJD), которые лечились GH от NPA в 1960-е годы. Связь была признана при просмотре данных в течение нескольких месяцев FDA и NIH. 19 апреля 1985 г. распространение ГР гипофиза было приостановлено, а использование ГР гипофиза быстро прекратилось. И вот захватывающая и важная эпоха в детской эндокринологии внезапно подошла к концу.[5]
Идентификация биохимической структуры GH в 1972 году стала катализатором развития человеческого GH на основе рекомбинантной ДНК, ген которого был впервые клонирован в 1979 году. Компания Genentech (Сан-Франциско, Калифорния) разработала в 1981 году был получен первый рекомбинантный человеческий GH (rhGH) путем биосинтетического процесса. Позже был разработан усовершенствованный процесс выработки rhGH, названный технологией секреции белка. При этом векторная плазмида выделяется из штамма E.coli , а цепь ДНК, которую необходимо клонировать, происходит из соответствующего источника.И плазмида, и необходимая цепь ДНК расщепляются рестрикционными ферментами, соединяются вместе и затем преобразуются в кольцевую структуру. Рекомбинантная плазмида вставляется в E.coli , который затем трансформируется для синтеза желаемого белка. В настоящее время это наиболее распространенный метод, используемый для синтеза rhGH, известного как соматотропин. Прекращение приема человеческого трупного GH привело к быстрому утверждению Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) синтетического метионилового GH компании Genentech, который был представлен в США в 1985 году для лечения тяжелого детского GHD.[6,7]
До открытия rhGH лечение GH применялось только в самых тяжелых случаях GHD и из-за нехватки материалов. С развитием rhGH стал доступен неограниченный коммерческий источник, что позволило получить постоянно растущий список одобренных FDA показаний для использования GH у детей без дефицита GH и дополнительных показаний для взрослых. [8,9]
HISTORY ПОКАЗАНИЯ К ГОРМОННОЙ ТЕРАПИИ У ДЕТЕЙ
Дефицит гормона роста (1985)
GHD может быть результатом нарушения оси GH в гипоталамусе или гипофизе.Эта этиология дисфункции может быть врожденной или приобретенной. Классическое проявление тяжелой формы GHD характеризуется низким ростом, медленным ростом и замедленным созреванием скелета с пониженной секрецией GH в ответ на провокационную стимуляцию. Несмотря на этот обширный список этиологий, причина GHD у большинства детей — идиопатическая. Лечение GH GHD у детей в определенной степени стандартизировано во всем мире. rhGH вводится один раз в день подкожно, обычно вечером, чтобы имитировать нормальную физиологию.[3,9]
Хроническая почечная недостаточность (1993)
Дети, страдающие хронической болезнью почек (ХБП), склонны к развитию тяжелой недостаточности роста. Этиология нарушения уремического роста многофакторна. Терапия гормона роста — это общепринятая мера для увеличения конечного роста. В различных исследованиях лечение GH при ХБП улучшило конечный рост. У пациентов с ХЗП препубертатного возраста реакция роста положительно связана с продолжительностью терапии гормоном роста и начальной степенью нарушения роста. Это отрицательно было связано с продолжительностью диализа.Дозы, рекомендуемые для детей с ХБП, выше, чем для пациентов с ГР. У детей, получавших GH, лечение обычно прекращается после трансплантации, но иногда его возобновляют, если скорость роста остается низкой. Лучшие результаты наблюдаются у детей, которые раньше начинают лечение, которые моложе и у которых наблюдается более легкое ухудшение функции почек. [10,11]
Синдром Тернера (1997)
Синдром Тернера (TS) поражает примерно одного из 1500–2500 живорожденные самки.Один из наиболее распространенных и заметных признаков синдрома — чрезвычайно низкий рост. Женщины, не получающие лечения, примерно на 20–21 см ниже нормальных женщин в своей популяции. rhGH использовался для увеличения роста и окончательного роста у девочек с TS. Хотя органический дефицит GH не является признаком TS, эффективность rhGH в увеличении линейного роста и конечного роста у пациентов с TS хорошо документирована. [12,13]
Синдром Прадера-Вилли (2000)
Синдром Прадера-Вилли ( PWS) является первым заболеванием человека, приписываемым геномному импринтингу, при котором гены экспрессируются по-разному в зависимости от родителя происхождения.Дети с СПВ демонстрируют глубоко ненормальный состав тела с фенотипом, подобным тому, что наблюдается при классическом GHD. Назначение GH детям с GHD не только восстанавливает линейный рост, но также способствует росту безжировой массы тела, снижает жировую массу за счет увеличения окисления жиров и общего расхода энергии тела, увеличивает минеральную плотность костей и снижает факторы риска сердечно-сосудистых заболеваний. Хотя терапия GH в настоящее время одобрена для лечения недостаточности роста, вторичной по отношению к PWS, сами по себе эти другие преимущества могут оправдать испытание терапии GH.[14,15]
Маленький для гестационного возраста (2001)
Маленький для гестационного возраста (SGA) определяется как масса тела при рождении или длина тела, по крайней мере, на 2 SD балла (SDS) ниже среднего гестационного возраста. Независимо от того, рождаются ли эти дети преждевременно или доношенными, большинство младенцев с SGA переживают постнатальный рост, достаточный для нормализации своего роста к 2 годам. Это называется догоняющим ростом. Несколько исследований показали, что большинство детей с SGA получают пользу от терапии GH и достигают нормального взрослого роста.[16,17]
Идиопатический низкий рост (2003)
Идиопатический низкий рост (ISS) определяется как состояние, при котором рост человека более чем на 2 SDS ниже соответствующего среднего роста для данного возраста, пола, и группа населения без признаков системных, эндокринных, пищевых или хромосомных аномалий. В частности, дети с ISS имеют нормальный вес при рождении и имеют достаточный уровень GH. Показано, что терапия GH увеличивает средний рост взрослого, связанный с терапией GH (средняя продолжительность 4–7 лет) у детей с ISS на 3.5–7,5 см по сравнению с историческим контролем, с прогнозируемым ростом взрослых пациентов до лечения или с контрольными группами, не получавшими лечения, или с контрольными группами плацебо. Не было никаких необычных проблем безопасности GH у пациентов с ISS. [18,19]
Недостаток гена, содержащего гомеобокс низкого роста (2006)
В 2006 году FDA США одобрило использование rhGH у пациентов с гомеобоксом низкого роста. -содержащий ген (SHOX) дефицит. Гаплонедостаточность гена SHOX связана с низким ростом, деформацией Маделунга и высоким сводчатым небом и считается основной причиной низкого роста у девочек с TS.Ген SHOX является довольно частой причиной низкого роста, и лечение гормона роста эффективно улучшает линейный рост пациентов с различными формами SHOX-D. [19,20]
Синдром Нунан (2007)
Синдром Нунан это клинически неоднородное заболевание, характеризующееся пропорциональным послеродовым низким ростом, дисморфическими чертами лица, деформациями грудной клетки и врожденным пороком сердца. Помимо черт лица и сердечных заболеваний, одним из основных признаков НС является низкий рост.Причина нарушения роста неясна, и были проведены испытания с применением rhGH. Несколько исследований показывают, что краткосрочная терапия гормона роста (1–4 года) способна увеличить скорость роста и улучшить показатель SD по росту (SDS). [19,21]
Дефицит гормона роста у взрослых
Лечение гормона роста у взрослых с дефицитом гормона роста. был одобрен FDA в 1996 году. Впоследствии был оценен большой клинический опыт лечения взрослых с GHD. Хотя в целом лечение кажется безопасным, некоторые области требуют длительного наблюдения, например, риски непереносимости глюкозы, рецидива опухоли гипофиза / гипоталамуса и рака.Преимущества лечения гормоном роста взрослых с дефицитом гормона роста были обнаружены в отношении состава тела, здоровья костей, факторов риска сердечно-сосудистых заболеваний и показателей качества жизни. Однако снижение сердечно-сосудистых событий и смертности еще предстоит продемонстрировать, а затраты на лечение остаются высокими [] [22].
Таблица 1
История терапии гормоном роста
ВЫВОДЫ
GH является важным фактором, способствующим росту. До 1985 года GH получали путем экстракции из трупного гипофиза.В связи с доступностью неограниченного количества rhGH список показаний для детей и взрослых без дефицита GH постоянно растет. Помимо состояний, упомянутых выше, рчГР также одобрен для лечения истощения, связанного с ВИЧ, и синдрома короткой кишки. В настоящее время имеются сообщения об использовании GH при муковисцидозе, воспалительном заболевании кишечника, ювенильном ревматоидном артрите, остеопорозе и у пациентов, которым требуется хроническое введение глюкокортикоидов. Лечение rhGH действительно увеличивает рост взрослого человека в некоторых случаях и кажется безопасным лечением.Однако недавно FDA [23] предупредило общественность о результатах французского обсервационного исследования (SAGhE), описывающего небольшой повышенный риск смерти у взрослых, получавших rhGH в детстве, от некоторых типов низкого роста. В настоящее время FDA считает, что преимущества rhGH по-прежнему перевешивают его потенциальные риски. По мере того, как мы узнаем больше о GH, неизбежно, что его использование будет расширяться.
Сноски
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПРАВОЧНАЯ ИНФОРМАЦИЯ
1. Frasier SD. Не очень хорошие старые времена: работа с гормоном роста гипофиза в Северной Америке, 1956–1985 гг. J Pediatr. 1997; 131: S1–4. [PubMed] [Google Scholar] 2. Самнер Дж. Гормон роста человека: текущий статус доступности и полезности. Педиатрия. 1969; 44: 766–7. [Google Scholar] 3. Франклин С.Л., Геффнер МЭ. Гормон роста: расширение доступных продуктов и показаний. Endocrinol Metab Clin North Am. 2009. 38: 587–611. [PubMed] [Google Scholar] 4. Escamilla RF, Hutchings JJ, Deamer WC, Li CH, Forsham PH.Долгосрочные эффекты гормона роста человека (Li) на гипофизарный карлик. J Clin Endocrinol Metab. 1961; 21: 721–6. [PubMed] [Google Scholar] 5. Отчет Комитета по использованию гормона роста Детского эндокринного общества им. Лоусона Уилкинса, май 1985 г. Дегенеративное неврологическое заболевание у пациентов, ранее лечившихся гормоном роста человека. J Pediatr. 1985; 107: 10–2. [PubMed] [Google Scholar] 6. Кронин MJ. Новаторское производство рекомбинантного гормона роста: количество фунтов на милю роста. J Pediatr. 1997; 131: S5–7.[PubMed] [Google Scholar] 7. Флод Х. Гормон роста человека, полученный с помощью технологии рекомбинантной ДНК: Разработка и производство. Acta Paediatr Scand Suppl. 1986; 325: 1–9. [PubMed] [Google Scholar] 8. Такеда А., Купер К., Берд А., Бакстер Л., Фрэмптон Г. К., Господаревская Е. и др. Рекомбинантный гормон роста человека для лечения нарушений роста у детей: систематический обзор и экономическая оценка. Оценка медицинских технологий. 2010; 14: 1. [PubMed] [Google Scholar] 9. Hindmarsh PC, редактор. Эндокринное развитие.2-е изд. Vol. 18. Базель: Karger Publishers; 2010. Текущие показания к терапии гормоном роста; С. 92–108. [PubMed] [Google Scholar] 10. Ниссель Р., Линдберг А., Мельс О., Хаффнер Д. Международный совет Pfizer International Growth Database (KIGS). Факторы, позволяющие прогнозировать околокональный рост у детей и подростков с хроническим заболеванием почек, принимающих гормон роста. J Clin Endocrinol Metab. 2008; 93: 1359–65. [PubMed] [Google Scholar] 11. Franke D, Zivicnjak M, Ehrich JH. Лечение гормоном роста почечной недостаточности в младенчестве и раннем детстве.Педиатр Нефрол. 2009; 24: 1093–6. [PubMed] [Google Scholar] 12. Бакстер Л., Брайант Дж., Кейв С.Б., Милн Р. Рекомбинантный гормон роста для детей и подростков с синдромом Тернера. Кокрановская база данных Syst Rev.2007: CD003887. [PubMed] [Google Scholar] 13. Болар К., Хоффман А.Р., Манитис Т., Липпе Б. Долгосрочная безопасность рекомбинантного гормона роста человека при синдроме Тернера. J Clin Endocrinol Metab. 2008; 93: 344–51. [PubMed] [Google Scholar] 14. Каррел А.Л., Майерс С.Е., Уитмен Б.А., Аллен Д.Б. Преимущества долгосрочной терапии GH при синдроме Прадера-Вилли: 4-летнее исследование.J Clin Endocrinol Metab. 2002; 87: 1581–5. [PubMed] [Google Scholar] 15. Whitman BY, Myers S, Carrel A, Allen D. Поведенческое влияние лечения гормоном роста детей и подростков с синдромом Прадера-Вилли: 2-летнее контролируемое исследование. Педиатрия. 2002; 109: E35. [PubMed] [Google Scholar] 16. Майорана А., Чианфарани С. Влияние терапии гормоном роста на рост взрослых детей, рожденных маленькими для гестационного возраста. Педиатрия. 2009; 124: e519–31. [PubMed] [Google Scholar] 17. Ли П.А., Чернаусек С.Д., Хоккен-Колега А.С., Чернихов П.Заявление Международной конференции по развитию консенсуса Консультативного совета по малому возрасту гестационного возраста: Ведение маленьких детей, рожденных с малым для гестационного возраста, 24 апреля — 1 октября 2001 г. Педиатрия. 2003; 111: 1253–61. [PubMed] [Google Scholar] 18. Коэн П., Рогол А.Д., Дил С.Л., Сенгер П., Рейтер Е.О., Росс Дж. Л. и др. Участники семинара по консенсусу ISS 2007. Заявление о консенсусе по диагностике и лечению детей с идиопатическим низким ростом: резюме Общества по исследованию гормона роста, Педиатрического эндокринного общества им. Лоусона Уилкинса и семинара Европейского общества детской эндокринологии.J Clin Endocrinol Metab. 2008; 93: 4210–7. [PubMed] [Google Scholar] 19. Коллетт-Сольберг П.Ф. Обновление гормональной терапии детей. J Clin Endocrinol Metab. 2011; 96: 573–9. [PubMed] [Google Scholar] 20. Блюм В.Ф., Кроу Б.Дж., Куигли К.А., Юнг Х., Цао Д., Росс Дж. Л. и др. SHOX Study Group. Гормон роста эффективен при лечении низкого роста, связанного с дефицитом гомеобокса низкого роста: результаты двухлетнего рандомизированного контролируемого многоцентрового исследования. J Clin Endocrinol Metab.2007. 92: 219–28. [PubMed] [Google Scholar] 21. Феррейра Л.В., Соуза С.А., Арнхольд И.Дж., Мендонка Б.Б., Хорхе А.А. Мутации PTPN11 (протеин-тирозинфосфатаза, нерецепторный тип 11) и ответ на терапию гормоном роста у детей с синдромом Нунана. J Clin Endocrinol Metab. 2005; 90: 5156–60. [PubMed] [Google Scholar] 22. Молич М.Э., Клеммонс Д.Р., Малозовски С., Мерриам Г.Р., Шале С.М., Вэнс М.Л. Подкомитет по клиническим рекомендациям эндокринного общества, Stephens PA. Оценка и лечение дефицита гормона роста у взрослых: Руководство по клинической практике эндокринного общества.J Clin Endocrinol Metab. 2006; 91: 1621–34. [PubMed] [Google Scholar] 23. Сообщение о безопасности лекарств, 22 декабря 2010 г. [Последний доступ 1 мая 2011 г.]. Доступна с:
http://www.fda.gov.
Лечение гормоном роста — обзор
Семейство генов гормона роста
У людей семейство генов гормона роста (GH) расположено на хромосоме 5 и состоит из следующих пяти генов (GH, плацентарный гормон роста (GH-V) , хорионический соматомаммотропиновый гормон 1 (CSh2), хорионический соматомаммотропиновый гормон 2 (CSh3), и псевдоген, называемый хорионический соматомаммотропин-подобный гормон, хромосом, который расположен на длинном плече 17 хромосом. генный локус, который охватывает ∼46.8 килобаз (кб). Кроме того, родственный белок, пролактин человека (PRL), включен в семейство генов GH и находится на хромосоме 6. Все эти гены имеют сходную структуру и, как полагают, произошли от общего предка. 5 В отличие от GH, который экспрессируется главным образом, хотя и не исключительно, в гипофизе, GH-V представляет собой гликозилированный белок, который продуцируется в синцитиотрофобластных клетках плаценты, в основном замещая GH гипофиза во время беременности. Он отличается от гормона роста гипофиза 13 из 191 аминокислотных остатков 5 и, как было показано, способствует росту и опосредует материнскую инсулинорезистентность.У человека гены CSH также экспрессируются в плаценте и кодируют белок, известный как плацентарный лактоген . Каждый член семейства белков GH содержит ∼200 аминокислот с двумя (GH) или тремя (PRL) дисульфидными связями и молекулярной массой ∼22000 с аналогичными коэффициентами седиментации и диффузии. Аминокислотный состав и последовательность молекул сопоставимы, идентичность аминокислотной последовательности варьируется от ~ 60% до 90%. 6 Члены семейства GH синтезируются как белки-предшественники, то есть они содержат аминоконцевые секреторные сигнальные пептиды. 5
Первичные транскрипты мРНК каждого соответствующего гена содержат пять экзонов и четыре промежуточных последовательности с кодонами начала и остановки трансляции, расположенными в экзонах 1 и 5, соответственно. 5 Несколько экспрессируемых генов, связанных с GH, также подвергаются альтернативному сплайсингу мРНК-предшественника. Один хорошо задокументированный транскрипт мРНК с альтернативным сплайсингом — это транскрипт GH гипофиза. Альтернативный сплайсинг мРНК предшественника GH приводит к новой мРНК, кодирующей изоформу GH размером 20 кДа. Эта мРНК содержит делецию, кодирующую аминокислоты с 32 по 46 (рис.20-1) в экзоне 3 мРНК предшественника GH. 20kDA GH можно легко обнаружить в гипофизе и крови. 7
Было идентифицировано семейство генов, которое кодирует несколько факторов транскрипции, включая POU1F1 (домен POU, класс 1, фактор транскрипции 1, ранее назывался PIT1 ) и PROP1 (пророк PIT1 ) и клонированы, и было обнаружено, что они оказывают большое влияние на развитие клеток, продуцирующих GH. Экспрессия этих генов важна для дифференциации клеточных линий гипофиза до соматотрофов, которые в конечном итоге синтезируют и высвобождают GH. 8 Экспрессия и секреция GH соматотрофами контролируются питанием, сном, физическими упражнениями и некоторыми гормонами, а также гипоталамическими пептидами, такими как GH-высвобождающий гормон (GHRH) и соматостатин, и стимуляторами секреции GH, включая грелин. Эта тема подробно рассматривается далее в этой главе.
С момента первого открытия принципа стимуляции роста гипофиза в 1921 году, 1 гормон роста человека (GH) был идентифицирован, очищен и охарактеризован.В 1979 году была клонирована и экспрессирована комплементарная ДНК (кДНК) GH. 2 Впоследствии (в 1985 г.) рекомбинантный (r) hGH был получен и одобрен для клинического использования у пациентов с дефицитом GH (GHD). С тех пор было одобрено несколько других клинических показаний для использования GH, которые обсуждаются позже.
Основные научные открытия, сделанные за последние несколько десятилетий, установили механизм, с помощью которого GH взаимодействует со своим рецептором (GHR), идентифицировали нижестоящие внутриклеточные сигнальные пути, создали несколько линий мышей с измененным действием GH и сообщили о взаимосвязи GH со старением и долголетие.Другой важной серией открытий стало открытие молекул, регулирующих секрецию гормона роста гипофизом. В этой главе резюмируются недавние и важные открытия в области GH, а также приводится соответствующая справочная информация и ссылки на более подробные обзоры более ранней работы.
Дефицит гормона роста у детей — педиатрия
-
Клиническая оценка, включая критерии роста и другой анамнез
-
Уровни инсулиноподобного фактора роста 1 (IGF-1) и IGF-связывающего белка типа 3 (IGFBP- 3) уровни
-
Обычно подтверждение провокационным тестированием
-
Оценка других гормонов гипофиза и других причин плохого роста
Текущие согласованные рекомендации по диагностике дефицита гормона роста требуют интеграции критериев роста, истории болезни и т. Д. лабораторные исследования и результаты визуализации.
Измерение уровней IGF-1 и IGFBP-3 начинает оценку оси GH / IGF-1. IGF-1 отражает активность GH, а IGFBP-3 является основным носителем пептидов IGF. Уровни IGF-1 и IGFBP-3 измеряются, потому что уровни GH непостоянны, сильно изменчивы и их трудно интерпретировать.
Визуализирующие исследования выполняются при аномальном росте; костный возраст следует определять по рентгенограмме левой руки (условно). При дефиците GH созревание скелета обычно задерживается в той же степени, что и рост.При дефиците GH показано обследование гипофиза и гипоталамуса с помощью МРТ, чтобы исключить кальцификаты, опухоли и структурные аномалии.
Скрининговые лабораторные тесты проводятся для поиска других возможных причин плохого роста, в том числе
-
Гипотиреоз (например, тиреотропный гормон, тироксин)
-
Нарушения со стороны почек (например, электролиты, уровень креатинина)
-
Воспалительные и иммунные состояния (например, антитела к тканевой трансглутаминазе, С-реактивный белок)
-
Гематологические расстройства (например, общий анализ крови с дифференциалом)
Потому что ответы гормона роста обычно аномальны у пациентов с пониженной щитовидной железой или Функция надпочечников, провокационное тестирование у этих пациентов следует проводить только после проведения адекватной заместительной гормональной терапии.
Тест на толерантность к инсулину — лучший провокационный тест для стимуляции выработки гормона роста, но его делают редко, потому что это рискованно. Другие провокационные тесты менее опасны, но и менее надежны. К ним относятся тесты с использованием инфузии аргинина (500 мг / кг внутривенно в течение 30 минут), клонидина (0,15 мг / м 2 перорально [максимум 0,25 мг]), леводопы (10 мг / кг перорально для детей; 500 мг перорально для взрослых. ) и глюкагон (0,03 мг / кг внутривенно [максимум 1 мг]). Уровни GH измеряются в разное время после приема лекарства в зависимости от лекарства.
Поскольку ни один тест не дает 100% эффективности в выявлении высвобождения GH, проводятся два провокационных теста GH (обычно в один и тот же день). Уровни GH обычно достигают пика через 30–90 минут после введения инсулина или начала инфузии аргинина, от 30 до 120 минут после леводопы, от 60 до 90 минут после клонидина и от 120 до 180 минут после глюкагона. Реакция GH, которая считается нормальной, несколько произвольна. Как правило, любого стимулированного уровня GH> 10 нг / мл (> 10 мкг / л) достаточно, чтобы исключить дефицит GH.Дефицит GH может быть рассмотрен для ответов.
Провокационное тестирование может не выявить незначительных дефектов в регулировании высвобождения GH. Например, у детей с низким ростом, вторичным по отношению к секреторной дисфункции GH, результаты провокационных тестов на высвобождение GH обычно нормальны. Однако серийные измерения уровней GH в течение 12–24 часов указывают на аномально низкую 12- или 24-часовую интегральную секрецию GH. Однако этот тест дорогостоящий и неудобный и, следовательно, не является предпочтительным тестом при дефиците GH.
Если подтверждено снижение высвобождения GH, необходимо провести тесты на секрецию других гормонов гипофиза и (в случае отклонения от нормы) гормонов их целевых периферических эндокринных желез, а также исследования гипофиза с помощью визуализации, если это не было сделано ранее.
Тест на гормон роста
Определение
Тест на гормон роста измеряет количество гормона роста в крови.
Гипофиз вырабатывает гормон роста, который заставляет ребенка расти. Эта железа расположена у основания мозга.
Альтернативные названия
Тест GH
Как проводится тест
Требуется образец крови.
Как подготовиться к тесту
Ваш лечащий врач может дать вам особые инструкции о том, что вы можете или не можете есть перед тестом.
Как будет выглядеть тест
Когда игла вводится для забора крови, некоторые люди чувствуют умеренную боль. Другие чувствуют только укол или покалывание. После этого может появиться небольшая пульсация или небольшой синяк.Это скоро уйдет.
Почему проводится тест
Этот гормон можно проверить, если характер роста человека отклоняется от нормы или есть подозрение на другое заболевание.
- Слишком большое количество гормона роста (GH) может вызвать аномальное усиление модели роста. У взрослых это называется акромегалией. У детей это называется гигантизмом.
- Слишком мало гормона роста может вызвать замедление или стабилизацию роста у детей. У взрослых он иногда может вызывать изменения в энергии, мышечной массе, уровне холестерина и прочности костей.
Тест GH также может использоваться для контроля реакции на лечение акромегалии.
Нормальные результаты
Нормальный диапазон уровня GH обычно составляет:
- Для взрослых мужчин — от 0,4 до 10 нанограммов на миллилитр (нг / мл) или от 18 до 44 пикомолей на литр (пмоль / л)
- Для взрослые женщины — от 1 до 14 нг / мл или от 44 до 616 пмоль / л
- Для детей — от 10 до 50 нг / мл или от 440 до 2200 пмоль / л
GH высвобождается импульсами. Размер и продолжительность импульсов зависят от времени суток, возраста и пола.Вот почему случайные измерения GH редко бывают полезными. Более высокий уровень может быть нормальным, если кровь была взята во время пульса. Более низкий уровень может быть нормальным, если кровь была взята в конце пульса. GH наиболее полезен при измерении как часть теста на стимуляцию или подавление.
Нормальные диапазоны значений могут незначительно отличаться в разных лабораториях. Некоторые лаборатории используют разные измерения или тестируют разные образцы. Поговорите со своим врачом о значении ваших конкретных результатов теста.
Что означают аномальные результаты
Высокий уровень гормона роста может указывать на:
- Слишком много гормона роста у взрослых, называемое акромегалией.(Для подтверждения этого диагноза проводится специальный тест.)
- Аномальный рост из-за избытка гормона роста в детстве, называемый гигантизмом. (Для подтверждения этого диагноза проводится специальный тест.) Сопротивление
- GH.
- Опухоль гипофиза.
Низкий уровень GH может указывать на:
- Замедление роста в младенчестве или детстве, вызванное низким уровнем GH. (Для подтверждения этого диагноза проводится специальный тест.)
- Гипопитуитаризм (снижение функции гипофиза).
Риски
Сдача крови сопряжена с небольшим риском. Вены и артерии различаются по размеру от одного человека к другому и от одной стороны тела к другой. Получить образец крови у одних людей может быть сложнее, чем у других.
Другие риски, связанные с забором крови, незначительны, но могут включать:
- Обильное кровотечение
- Обморок или головокружение
- Множественные проколы для поиска вен
- Гематома (скопление крови под кожей)
- Инфекция (незначительное рисковать, если кожа порвалась)
Список литературы
Ali O.Гиперпитуитаризм, высокий рост и синдромы чрезмерного роста. В: Kliegman RM, Stanton BF, St. Geme JW, Schor NF, ред. Учебник педиатрии Нельсона . 20-е изд. Филадельфия, Пенсильвания: Эльзевьер; 2016: глава 560.
Chernecky CC, Berger BJ. Гормон роста (соматотропин, GH) и гормон-рилизинг-гормон роста (GHRH) — кровь. В: Chernecky CC, Berger BJ, ред. Лабораторные исследования и диагностические процедуры . 6-е изд. Филадельфия, Пенсильвания: Эльзевьер; 2013: 599-600.
Cooke DW, Divall SA, Radovick S.Нормальный и аномальный рост у детей. В: Мелмед С., Полонский К.С., Ларсен П.Р., Кроненберг Х.М., ред. Учебник эндокринологии Вильямса . 13-е изд. Филадельфия, Пенсильвания: Эльзевьер; 2016: глава 24.
Чего нельзя делать с гормонами роста: Центр гормонов баланса: Альтернативная медицина
Гормоны роста (GH) естественным образом присутствуют в организме человека и стимулируют рост, размножение клеток и регенерацию клеток. Хотя без них человек не может увеличить мышечную массу или плотность костей, они также важны для поддержания здоровья всех тканей человека, включая мозг и другие жизненно важные органы.
GH уменьшает возрастные заболевания, повышает либидо и помогает поддерживать умственную активность. Если у человека низкий уровень гормона роста, у него могут проявляться такие симптомы, как потеря мышечной массы, увеличение веса, снижение полового влечения и снижение уровня энергии.
Для большинства из нас единственное упоминание гормонов роста могло быть связано с новостями о спортсмене или бодибилдере, который использовал их для наращивания мышечной массы или повышения производительности. Это незаконно и очень опасно, если человек не испытывает дефицита гормона роста.
Признаки и симптомы дефицита гормона роста
Если у вас, как у взрослого, есть дефицит гормона роста, у вас могут быть следующие симптомы:
- Беспокойство
- Депрессия
- Мужское облысение
- Снижение полового влечения
- Снижение мышечной массы
- Снижение силы
- Проблемы с концентрацией и памятью
- Сухая, тонкая кожа
- Повышенный уровень триглицеридов
- Усталость
- Проблемы с сердцем
- Высокий уровень ЛПНП
- Инсулинорезистентность
- Низкая
- толерантность к упражнениям плотность костей
- Чувствительность к горячему / холодному воздуху
- Низкая энергия
- Увеличение веса, особенно в области талии
Взрослым, испытывающим эти симптомы, важно поговорить с медицинским работником для тестирования, диагностики и надлежащего лечения.
Что делают гормоны роста?
Для тех, кто страдает дефицитом GH, лечение GH может оказаться очень полезным. Преимущества включают:
- Повышенный метаболизм
- Регулирование иммунной системы
- Улучшение работы сердца
- Улучшенная регенерация тканей
- Устойчивость к остеопорозу
- Уменьшение жировых отложений
- Увеличение мышечной массы и силы
- Пониженный уровень холестерина
- Пониженный
- фертильность
Таким образом, пациенты, проходящие курс лечения GH, могут испытывать:
- более гладкую и упругую кожу
- более густые волосы
- более крепкие ногти
- уменьшение целлюлита
- улучшение настроения
- более глубокий сон
?
Для тех, кто страдает дефицитом гормона роста, лечение гормоном роста может дать потрясающие результаты.Но для тех, у кого нет дефицита GH, использование GH для повышения работоспособности или наращивания мышечной массы опасно, потому что это влияет на способность организма вырабатывать гормоны естественным образом.
Кроме того, хотя лечение гормон роста увеличивает мышечную массу, исследования показывают, что это не приводит к повышению производительности. В конце концов, спортсмены или бодибилдеры, которые ошибочно полагают, что GH улучшит их на футбольном поле или в тренажерном зале, фактически рискуют своим здоровьем напрасно.
Более того, те, кто думает, что GH может быть своего рода «фонтаном молодости» антивозрастного лечения (больше энергии, больше мышц, меньше жира!), Будут разочарованы, узнав, что FDA не одобрило его для этого конкретного приложение тоже.
Безопасны ли гормоны роста?
При назначении медицинским работником лечение GH безопасно и эффективно для тех, кто страдает дефицитом GH. Однако, как и при любой другой медицинской процедуре, лечение GH сопряжено как с риском, так и с побочными эффектами, хотя многие из них случаются редко.Некоторые из них могут включать:
- Акромегалия, состояние, характеризующееся толстой, грубой и жирной кожей
- Прогрессирование рака, поскольку GH вызывает пролиферацию клеток
- Боль в мышцах и суставах
- Отек
- Затуманенное зрение
- Головокружение и головные боли
- Апноэ во сне
- Диабет
Кроме того, есть пациенты, которым лечение гормона роста не рекомендуется. К ним относятся люди, которые:
- Имеют опухоли или рак
- Серьезно больны
- Получили травмы в результате травмы
- Имеют серьезные проблемы с дыханием
Как диагностируется дефицит гормона роста?
Если у вас проявляются симптомы дефицита гормона роста, вам следует обратиться за диагнозом к медицинскому работнику, который проведет анализы крови для определения уровней химической продукции в организме.Кроме того, они осмотрят вас:
- Размер мышц
- Цвет кожи
- Качество волос
- Уровни энергии
- Выносливость
- Функция мозга
- Настроение
После постановки диагноза ваш медицинский работник, скорее всего, пропишет вам курс инъекционного лечения гормона роста.
Как я могу получить гормоны роста?
Самый безопасный способ получить GH — по рецепту лицензированного медицинского специалиста. У вас может возникнуть соблазн приобрести GH у одной из многих компаний в Интернете или на телевидении, которые рекламируют продукты GH в форме таблеток или спреев.Их заявления об антивозрастных средствах, уменьшении жира, наращивании мышц, восстановлении роста волос, укреплении иммунной системы, повышении энергии, улучшении полового влечения и многом другом могут показаться чудодейственным средством, которое вы так долго искали!
Однако, не имея доказательств, подтверждающих эти утверждения, Федеральная торговая комиссия не одобрила эти продукты и не подтвердила их обещанные результаты. Более того, когда вы покупаете GH из ненадежного источника, вы можете получить нечистый или поддельный препарат, который потенциально может нанести вам вред.
Узнайте, может ли GH помочь вам
После того, как медицинский работник поставит вам диагноз дефицита GH, он может назначить инъекции GH в качестве лечения. Обычно это включает ежедневные дозы гормона роста и посещения врача каждые четыре-восемь недель на протяжении всего курса лечения. Во время этих посещений ваш врач будет контролировать ваш уровень холестерина, уровень глюкозы в крови и плотность костей, чтобы убедиться, что все ваши уровни находятся на должном уровне.
Если вы обеспокоены тем, что у вас может быть дефицит GH или проявляются симптомы дефицита GH, важно, чтобы медицинский работник оценил и диагностировал ваше состояние.Медицинская бригада Центра гормонов баланса готова встретиться с вами и провести тесты, необходимые для постановки профессионального диагноза.
Гормон роста: изоформы, клинические аспекты и анализы интерференция | Клинический диабет и эндокринология
Clemmons DR. Заявление о консенсусе по стандартизации и оценке анализов гормона роста и инсулиноподобного фактора роста. Clin Chem. 2011; 57: 555–9.
Артикул
PubMed
CAS
Google ученый
Wieringa GE, Sturgeon CM, Trainer PJ. Гармонизация измерений гормона роста: что делать дальше. Clin Chim Acta. 2014; 432: 68–71.
Артикул
PubMed
CAS
Google ученый
Bidlingmaier M, Freda PU. Измерение гормона роста человека иммуноанализами: текущее состояние, нерешенные проблемы и клинические последствия. Гормон роста IGF Res. 2010; 20: 19–25.
Артикул
CAS
Google ученый
Попий В., Бауманн Г. Лабораторные измерения гормона роста. Clin Chim Acta. 2004; 350: 1–16.
Артикул
PubMed
CAS
Google ученый
Chen EY, Liao YC, Smith DH, Barrera-Saldana HA, Gelinas RE, Seeburg PH. Локус гормона роста человека: нуклеотидная последовательность, биология и эволюция. Геномика. 1989; 4: 479–97.
Артикул
PubMed
CAS
Google ученый
Ho Y, Liebhaber SA, Cooke NE. Активация кластера генов человеческого GH: роли в целевой модификации хроматина. Trends Endocrinol Metab. 2004; 15: 40–5.
Артикул
PubMed
CAS
Google ученый
Lecomte CM, Renard A, Martial JA. Новый вариант природного чГР — 17,5 кДа, полученный методом альтернативного сплайсинга. Дополнительная согласованная последовательность, которая может играть роль в выборе точки ветвления. Nucleic Acids Res. 1987; 15: 6331–48.
Артикул
PubMed
PubMed Central
CAS
Google ученый
Льюис У. Дж., Сингх Р. Н., Боневальд Л. Ф., Сиви Б. К.. Измененное протеолитическое расщепление гормона роста человека в результате дезамидирования. J Biol Chem. 1981; 256: 11645–50.
PubMed
CAS
Google ученый
Bustamante JJ, Gonzalez L, Carroll CA, Weintraub ST, Aguilar RM, Munoz J, Martinez AO, Haro LS.О-гликозилированный гормон роста человека с массой 24 кДа имеет муцин-подобный двухантенарный дисиалилированный тетрасахарид, присоединенный к Thr-60. Протеомика. 2009; 9: 3474–88.
Артикул
PubMed
PubMed Central
CAS
Google ученый
Baumann GP. Изоформы гормона роста. Гормон роста IGF Res. 2009; 19: 333–40.
Артикул
CAS
Google ученый
Вада М., Икеда М., Такахаши Ю., Асада Н., Чанг К. Т., Такахаши М., Хондзё М.Полный агонистический эффект рекомбинантного гормона роста человека 20 кДа (hGH) на клетки CHO, стабильно трансфицированные кДНК рецептора hGH. Mol Cell Endocrinol. 1997. 133: 99–107.
Артикул
PubMed
CAS
Google ученый
Цунекава Б., Вада М., Икеда М., Учида Н., Наито Н., Хондзё М. Гормон роста человека мощностью 20 килодальтон (кДа) отличается от гормона роста человека массой 22 кДа воздействием на человека. рецептор пролактина. Эндокринология. 1999; 140: 3909–18.
Артикул
PubMed
CAS
Google ученый
Solomon G, Reicher S, Gussakovsky EE, Jomain JB, Gertler A. Крупномасштабное приготовление и определение in vitro биологически активных плацентарных (20 и 22K) и гипофизарных (20K) гормонов роста человека: гормоны роста плаценты не обладают лактогенной активностью в организме человека. Гормон роста IGF Res. 2006. 16: 297–307.
Артикул
CAS
Google ученый
Wada M, Uchida H, Ikeda M, Tsunekawa B, Naito N, Banba S, Tanaka E, Hashimoto Y, Honjo M. 20-килодальтонный (кДа) гормон роста человека (hGH) отличается от 22-kDa hGH в образование комплекса с рецептором hGH на поверхности клетки и hGH-связывающим белком, циркулирующим в плазме крови человека. Мол Эндокринол. 1998. 12: 146–56.
Артикул
PubMed
CAS
Google ученый
Исикава М., Татибана Т., Камиока Т., Хорикава Р., Кацумата Н., Танака Т.Сравнение соматогенного действия гормонов роста человека 20 кДа и 22 кДа на спонтанных карликовых крысах. Гормон роста IGF Res. 2000. 10: 199–206.
Артикул
CAS
Google ученый
Сатодзава Н., Такедзава К., Мива Т., Такахаши С., Хаякава М., Оока Х. Различия во влиянии 20 K- и 22 K-hGH на задержку воды у крыс. Гормон роста IGF Res. 2000; 10: 187–92.
Артикул
CAS
Google ученый
Ishikawa M, Yokoya S, Tachibana K, Hasegawa Y, Yasuda T., Tokuhiro E, Hashimoto Y, Tanaka T. Сывороточные уровни 20-килодальтонного человеческого гормона роста (GH) параллельны уровням 22-килодальтонного человеческого GH в нормальном и коротком дети. J Clin Endocrinol Metab. 1999; 84: 98–104.
Артикул
PubMed
CAS
Google ученый
Yao-Xia L, Jing-Yan C, Xia-Lian T, Ping C, Min Z. Формы гормона роста человека (hGH) 20 кДа и 22 кДа проявляют различные профили внутриклеточной передачи сигналов и свойства.Gen Comp Endocrinol. 2017; 248: 49–54.
Артикул
PubMed
CAS
Google ученый
Де Пало Е.Ф., Де Филиппис В., Гатти Р., Спинелла П. Изоформы и сегменты / фрагменты гормона роста: молекулярная структура и лабораторные измерения. Clin Chim Acta. 2006; 364: 67–76.
Артикул
PubMed
CAS
Google ученый
Суч-Санмартин Дж., Бош Дж., Сегура Дж., Ву М., Ду Х, Чен Дж., Ван С., Вила-Перелло М., Андреу Д., Гутьеррес-Гальего Р.Характеристика изоформы гормона роста 5 кДа. Факторы роста. 2008. 26: 152–62.
Артикул
PubMed
CAS
Google ученый
Miletta MC, Lochmatter D, Pektovic V, Mullis PE. Изолированный дефицит гормона роста 2 типа: от гена к терапии. Endocr Dev. 2012; 23: 109–20.
Артикул
PubMed
CAS
Google ученый
Hettiarachchi M, Watkinson A, Leung KC, Sinha YN, Ho KK, Kraegen EW.Фрагмент гормона роста человека (hGh54-91) вызывает инсулинорезистентность и гиперинсулинемию, но менее эффективен, чем 22 кДа hGH у крыс. Эндокринная. 1997; 6: 47–52.
Артикул
PubMed
CAS
Google ученый
Синха Ю.Н., Якобсен Б.П. Гормон роста человека (hGH) — (44-191), предположительно диабетогенный фрагмент hGH, циркулирует в крови человека: измерение с помощью радиоиммуноанализа. J Clin Endocrinol Metab. 1994; 78: 1411–8.
PubMed
CAS
Google ученый
Sinha YN, Jacobsen BP, Lewis UJ. Антитела к недавно обнаруженным мышиным пептидам гипофиза 13-18 кДа перекрестно реагируют с гормоном роста и пролактином нескольких видов, включая человека. Biochem Biophys Res Commun. 1989; 163: 386–93.
Артикул
PubMed
CAS
Google ученый
Прадхананга С., Уилкинсон И., Росс Р.Дж. Пегвисомант: строение и функции. J Mol Endocrinol. 2002; 29: 11–4.
Артикул
PubMed
CAS
Google ученый
Kopchick JJ. Открытие и механизм действия пегвисоманта. Eur J Endocrinol. 2003; 148 (Дополнение 2): S21–5.
Артикул
PubMed
CAS
Google ученый
Копчик Дж. Дж., Паркинсон К., Стивенс Е. К., тренер П. Джей. Антагонисты рецепторов гормона роста: открытие, разработка и использование у пациентов с акромегалией. Endocr Rev.2002; 23: 623–46.
Артикул
PubMed
CAS
Google ученый
Ng FM, Jiang WJ, Gianello R, Pitt S, Roupas P. Молекулярные и клеточные действия структурного домена гормона роста человека (AOD9401) на метаболизм липидов у крыс с ожирением Zucker. J Mol Endocrinol. 2000; 25: 287–98.
Артикул
PubMed
CAS
Google ученый
Хеффернан Массачусетс, Цзян В.Дж., Торберн А.В., Нг FM. Влияние перорального введения синтетического фрагмента гормона роста человека на метаболизм липидов. Am J Physiol Endocrinol Metab.2000; 279: E501–7.
Артикул
PubMed
CAS
Google ученый
Бустаманте Дж., Григорян А.Л., Муньос Дж., Агилар Р.М., Тревино Л.Р., Мартинес А.О., Аро Л.С. Гормон роста человека: изоформа массой 45 кДа с чрезвычайно стабильными межцепочечными дисульфидными связями имеет ослабленную активность связывания с рецептором и пролиферацию клеток. Гормон роста IGF Res. 2010. 20: 298–304.
Артикул
CAS
Google ученый
Богушевски К.Л., Свенссон П.А., Янссон Т., Кларк Р., Карлссон Л.М., Карлссон Б. Клонирование двух новых транскриптов гормона роста, экспрессируемых в плаценте человека. J Clin Endocrinol Metab. 1998. 83: 2878–85.
PubMed
CAS
Google ученый
Викерс М. Х., Гилмор С., Гертлер А., Брейер Б. Х., Танни К., Уотерс М. Дж., Глюкман П. Д.. 20-кДа плацентарный hGH-V имеет пониженную диабетогенную и лактогенную активность по сравнению с 22-кДа hGH-N, сохраняя при этом антилипогенную активность.Am J Physiol Endocrinol Metab. 2009; 297: E629–37.
Артикул
PubMed
CAS
Google ученый
Сурья С., Саймонс К., Ротман Э., Баркан А.Л. Сложная ритмичность секреции гормона роста у человека. Гипофиз. 2006; 9: 121–5.
Артикул
PubMed
CAS
Google ученый
Ribeiro-Oliveira A Jr, Abrantes MM, Barkan AL. Сложная ритмичность и возрастная зависимость секреции гормона роста сохраняются у пациентов с акромегалией: еще одно доказательство нынешнего гипоталамического контроля соматотропином гипофиза.J Clin Endocrinol Metab. 2013; 98: 2959–66.
Артикул
PubMed
PubMed Central
CAS
Google ученый
Цусима Т., Като Ю., Миячи Ю., Чихара К., Терамото А., Ирие М., Хашимото Ю. Концентрации 20K гормона роста человека в сыворотке крови у здоровых взрослых и пациентов с различными эндокринными расстройствами. Исследовательская группа 20K hGH. Endocr J. 2000; 47 (Suppl): S17–21.
Артикул
PubMed
CAS
Google ученый
Леунг К.С., Хоу С., Гуй Л.Й., Форель Г., Вельдхейс Д.Д., Хо К.К. Физиологическая и фармакологическая регуляция гормона роста 20 кДа. Am J Physiol Endocrinol Metab. 2002; 283: E836–43.
Артикул
PubMed
CAS
Google ученый
Бауманн Г., Столар М.В., Бьюкенен Т.А. Медленная скорость метаболического клиренса варианта гормона роста человека с концентрацией 20 000 дальтон: последствия для биологической активности. Эндокринология. 1985; 117: 1309–13.
Артикул
PubMed
CAS
Google ученый
Nindl BC, Kraemer WJ, Marx JO, Tuckow AP, Hymer WC. Молекулярная гетерогенность гормона роста и упражнения. Exerc Sport Sci Rev.2003; 31: 161–6.
Артикул
PubMed
Google ученый
Tuckow AP, Rarick KR, Kraemer WJ, Marx JO, Hymer WC, Nindl BC. Ночная секреторная динамика гормона роста изменяется после упражнений с отягощениями: анализ деконволюции 12-часовых иммунофункциональных и иммунореактивных изоформ.Am J Physiol Regul Integr Comp Physiol. 2006; 291: R1749–55.
Артикул
PubMed
CAS
Google ученый
Уоллес Дж. Д., Кунео Р. К., Бидлингмайер М., Лундберг П.А., Карлссон Л., Богушевски К.Л., Хей Дж., Хили М.Л., Наполи Р., Далл Р., Розен Т., Страсбургер С.Дж. Ответ молекулярных изоформ гормона роста на интенсивную физическую нагрузку у тренированных взрослых мужчин. J Clin Endocrinol Metab. 2001. 86: 200–6.
PubMed
CAS
Google ученый
Pagani S, Cappa M, Meazza C, Ubertini G, Travaglino P, Bozzola E, Bozzola M. Изоформы гормона роста высвобождаются в ответ на физиологические и фармакологические стимулы. J Endocrinol Investig. 2008; 31: 520–4.
Артикул
CAS
Google ученый
Kraemer WJ, Nindl BC, Marx JO, Gotshalk LA, Bush JA, Welsch JR, Volek JS, Spiering BA, Maresh CM, Mastro AM, Hymer WC. Хронические тренировки с отягощениями у женщин потенцируют биоактивность гормона роста in vivo: характеристика вариантов молекулярной массы.Am J Physiol Endocrinol Metab. 2006; 291: E1177–87.
Артикул
PubMed
CAS
Google ученый
Пирс JR, Tuckow AP, Alemany JA, Rarick KR, Staab JS, Harman EA, Nindl BC. Влияние острых и хронических упражнений на варианты гормона роста с дисульфидной связью. Медико-спортивные упражнения. 2009; 41: 581–7.
Артикул
PubMed
CAS
Google ученый
Hymer WC, Kraemer WJ, Nindl BC, Marx JO, Benson DE, Welsch JR, Mazzetti SA, Volek JS, Deaver DR. Характеристики циркулирующего гормона роста у женщин после острых тяжелых упражнений с отягощениями. Am J Physiol Endocrinol Metab. 2001; 281: E878–87.
Артикул
PubMed
CAS
Google ученый
Kraemer WJ, Rubin MR, Hakkinen K, Nindl BC, Marx JO, Volek JS, French DN, Gomez AL, Sharman MJ, Scheett T., Ratamess NA, Miles MP, Mastro A, VanHeest J, Maresh CM , Уэлш-младший, Хаймер WC.Влияние мышечной силы и общей работы на изоформы гормона роста плазмы, вызванные физической нагрузкой, у женщин. J Sci Med Sport. 2003. 6: 295–306.
Артикул
PubMed
CAS
Google ученый
Kraemer WJ, Nindl BC, Volek JS, Marx JO, Gotshalk LA, Bush JA, Welsch JR, Vingren JL, Spiering BA, Fragala MS, Hatfield DL, Ho JY, Maresh CM, Mastro AM, Hymer WC . Влияние использования оральных контрацептивов на биоактивность гормона роста in vivo после упражнений с отягощениями: ответы вариантов молекулярной массы.Гормон роста IGF Res. 2008; 18: 238–44.
Артикул
CAS
Google ученый
Нельсон А.Е., Хо К.К. Злоупотребление гормоном роста спортсменами. Nat Clin Pract Endocrinol Metab. 2007; 3: 198–9.
Артикул
PubMed
Google ученый
Хашимото Ю., Камиока Т., Хосака М., Мабучи К., Мидзути А., Симадзаки И., Цуну М., Танака Т. Экзогенный гормон роста 20К (GH) подавляет эндогенную секрецию 22K GH у нормальных мужчин.J Clin Endocrinol Metab. 2000; 85: 601–6.
Артикул
PubMed
CAS
Google ученый
Wallace JD, Cuneo RC, Bidlingmaier M, Lundberg PA, Carlsson L, Boguszewski CL, Hay J, Boroujerdi M, Cittadini A, Dall R, Rosen T, Strasburger CJ. Изменения не-22-килодальтонных (кДа) изоформ гормона роста (GH) после введения 22-кДа рекомбинантного человеческого GH обученным взрослым мужчинам. J Clin Endocrinol Metab. 2001; 86: 1731–7.
PubMed
CAS
Google ученый
Keller A, Wu Z, Kratzsch J, Keller E, Blum WF, Kniess A, Preiss R, Teichert J, Strasburger CJ, Bidlingmaier M. Фармакокинетика и фармакодинамика GH: зависимость от пути и дозировки введения. Eur J Endocrinol. 2007; 156: 647–53.
Артикул
PubMed
CAS
Google ученый
Baumann GP.Допинг гормона роста в спорте: критический обзор стратегий использования и выявления. Endocr Rev.2012; 33: 155–86.
Артикул
PubMed
CAS
Google ученый
Бидлингмайер М., Зур Дж., Эрнст А., Ву З., Келлер А., Страсбургер С.Дж., Бергманн А. Высокочувствительные хемилюминесцентные иммуноанализы для определения допинга гормона роста в спорте. Clin Chem. 2009; 55: 445–53.
Артикул
PubMed
CAS
Google ученый
Богушевски К.Л., Йоханнссон Г., Бенгтссон Б.А., Йоханссон А., Карлссон Б., Карлссон Л.М. Циркулирующие изоформы гормона роста, не содержащие 22 килодальтона, у мужчин с акромегалией до и после транссфеноидальной хирургии. J Clin Endocrinol Metab. 1997; 82: 1516–21.
PubMed
CAS
Google ученый
Tsushima T, Katoh Y, Miyachi Y, Chihara K, Teramoto A, Irie M., Hashimoto Y. Концентрация 20K гормона роста человека (20K hGH) в сыворотке крови, измеренная с помощью специфического иммуноферментного анализа.Исследовательская группа 20K hGH. J Clin Endocrinol Metab. 1999; 84: 317–22.
PubMed
CAS
Google ученый
Мураками Ю., Симидзу Т., Ямамото М., Като Ю. Уровни 20 килодальтон человеческого гормона роста (20K-hGH) в сыворотке крови у пациентов с акромегалией до и после лечения октреотидом и транссфеноидальной хирургии. Эндокр Дж. 2004; 51: 343–8.
Артикул
PubMed
CAS
Google ученый
Lima GA, Wu Z, Silva CM, Barbosa FR, Dias JS, Schrank Y, Strasburger CJ, Gadelha MR. Изоформы гормона роста у пациентов с акромегалией до и после лечения октреотидом LAR. Гормон роста IGF Res. 2010; 20: 87–92.
Артикул
CAS
Google ученый
Coya R, Algorta J, Boguszewski CL, Vela A, Carlsson LM, Aniel-Quiroga A, Busturia MA, Martul P. Циркулирующие изоформы гормона роста без 22 кДа после повторной стимуляции GHRH у нормальных субъектов.Гормон роста IGF Res. 2005; 15: 123–9.
Артикул
CAS
Google ученый
Rigamonti AE, Grugni G, Marazzi N, Bini S, Bidlingmaier M, Sartorio A. Неизмененное соотношение циркулирующих уровней гормона роста / изоформ GH у взрослых с синдромом Прадера-Вилли после введения GHRH плюс аргинин. Гормон роста IGF Res. 2015; 25: 168–73.
Артикул
CAS
Google ученый
Rigamonti AE, Crino A, Bocchini S, Convertino A, Bidlingmaier M, Haenelt M, Tamini S, Cella SG, Grugni G, Sartorio A. Введение GHRH плюс аргинин и аргинин вызывает такое же соотношение уровней изоформ GH у молодых пациентов с Prader -Синдром Вилли. Гормона роста IGF Res. 2017;
Katsumata N, Shimatsu A, Tachibana K, Hizuka N, Horikawa R, Yokoya S, Tatsumi KI, Mochizuki T, Anzo M, Tanaka T. Продолжение усилий по стандартизации измеренных значений гормона роста в сыворотке крови в Японии.Эндокр Дж. 2016; 63: 933–6.
Артикул
PubMed
Google ученый
Канакис Г.А., Крисулиду А., Баргиота А., Эфстатиаду З.А., Папанастасиу Л., Теодоропулу А., Тигас С.К., Вассилиади Д.А., Цагаракис С., Алевизаки М. Постоянная проблема несовпадающего фактора роста I и инсулиноподобного фактора роста. результаты оценки пролеченных пациентов с акромегалией: систематический обзор и метаанализ. Clin Endocrinol. 2016; 85: 681–8.
Артикул
CAS
Google ученый
Casagrande A, Bronstein MD, Jallad RS, Moraes AB, Elias PC, Castro M, Czepielewski MA, Boschi A, Ribeiro-Oliveira A Jr, Schweizer JR, Vilar L, Nazato DM, Gadelha MR, Abucham J Все остальные следователи с. Длительная ремиссия акромегалии после отмены октреотида — редкое и часто неустойчивое событие. Нейроэндокринология. 2017; 104: 273–9.
Артикул
PubMed
CAS
Google ученый
Рибейро-Оливейра-младший, Баркан А. Меняющееся лицо акромегалии — достижения в диагностике и лечении. Nat Rev Endocrinol. 2012; 8: 605–11.
Артикул
PubMed
CAS
Google ученый
Ribeiro-Oliveira A Jr, Faje A, Barkan A. Надир постглюкозного гормона роста и инсулиноподобный фактор роста-1 у наивно активных пациентов с акромегалией: всегда ли эти параметры коррелируют? Arq Bras Endocrinol Metabol. 2011; 55: 494–7.
Артикул
PubMed
Google ученый
Ribeiro-Oliveira A Jr, Faje AT, Barkan AL. Ограниченная полезность перорального теста на толерантность к глюкозе при биохимически активной акромегалии. Eur J Endocrinol. 2011; 164: 17–22.
Артикул
PubMed
CAS
Google ученый
Abreu A, Tovar AP, Castellanos R, Valenzuela A, Giraldo CM, Pinedo AC, Guerrero DP, Barrera CA, Franco HI, Ribeiro-Oliveira A Jr, Vilar L, Jallad RS, Duarte FG, Gadelha M , Богушевский К.Л., Абухам Дж., Навес Л.А., Мусолино Н.Р., де Фариа М.Э., Россато К., Бронштейн М.Д.Проблемы диагностики и лечения акромегалии: акцент на сопутствующие заболевания. Гипофиз. 2016; 19: 448–57.
Артикул
PubMed
PubMed Central
CAS
Google ученый
Джустина А., Баркан А., Казануева Ф.Ф., Каваньини Ф., Фроман Л., Хо К., Вельдхейс Дж., Васс Дж., Фон Вердер К., Мелмед С. Критерии лечения акромегалии: согласованное заявление. J Clin Endocrinol Metab. 2000; 85: 526–9.
PubMed
CAS
Google ученый
Кацнельсон Л., Лоус Э. Р. мл., Мелмед С., Молитч М. Е., Мурад М. Х., Утц А., Васс Дж. А., Эндокрин С. Акромегалия: руководство по клинической практике эндокринного общества. J Clin Endocrinol Metab. 2014; 99: 3933–51.
Артикул
PubMed
CAS
Google ученый
Yuen KC, Tritos NA, Samson SL, Hoffman AR, Katznelson L. Клинический обзор состояния болезни Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологии: обновленная информация о тестировании на стимуляцию гормона роста и предложенная пересмотренная точка отсечения для Тест на стимуляцию глюкагоном в диагностике дефицита гормона роста у взрослых.Endocr Pract. 2016; 22: 1235–44.
Артикул
PubMed
Google ученый
Freda PU, Nuruzzaman AT, Reyes CM, Sundeen RE, Post KD. Значимость «аномальных» уровней гормона роста надира после перорального приема глюкозы у послеоперационных пациентов с акромегалией в стадии ремиссии с нормальным уровнем инсулиноподобного фактора роста-I. J Clin Endocrinol Metab. 2004. 89: 495–500.
Артикул
PubMed
CAS
Google ученый
Pokrajac A, Wark G, Ellis AR, Wear J, Wieringa GE, Trainer PJ. Различия в анализах GH и IGF-I ограничивают применимость критериев международного консенсуса к местной практике. Clin Endocrinol. 2007; 67: 65–70.
Артикул
CAS
Google ученый
Эндерт Э., ван Роден М., Флиерс Э, Пруммель М.Ф., Вирзинга В.М. Установление исходных значений для эндокринных тестов — часть V: акромегалия. Neth J Med. 2006; 64: 230–5.
PubMed
CAS
Google ученый
Schilbach K, Strasburger CJ, Bidlingmaier M. Биохимические исследования в диагностике и наблюдении за акромегалией. Гипофиз. 2017; 20: 33–45.
Артикул
PubMed
CAS
Google ученый
Пена-Порта Ю.М., Бургасе-Эсталло I, Николас-Санчес Ф., Висенте-де-Вера Флористан С. Хроническая болезнь почек и акромегалия: когда внешность обманчива. Нефрология. 2014; 34: 800–2.
PubMed
Google ученый
Фельдт-Расмуссен У., Клозе М. Клиническое лечение дефицита гормона роста у взрослых. В: De Groot LJ, Chrousos G, Dungan K, Feingold KR, Grossman A, Hershman JM, Koch C, Korbonits M, Mc Lachlan R, New M, Purnell J, Rebar R, Singer F, Vinik A, редакторы. Эндотекст. Южный Дартмут; 2000.
Wagner IV, Paetzold C, Gausche R, Vogel M, Koerner A, Thiery J, Arsene CG, Henrion A, Guettler B, Keller E, Kiess W, Pfaeffle R, Kratzsch J. Клинические доказательства — основанные на пороговых значениях для тестов стимуляции GH у детей с резервным копированием результатов со ссылкой на масс-спектрометрию.Eur J Endocrinol. 2014; 171: 389–97.
Артикул
PubMed
CAS
Google ученый
Чиной А., Мюррей П.Г. Диагностика дефицита гормона роста в детском и переходном возрасте. Лучшая практика Res Clin Endocrinol Metab. 2016; 30: 737–47.
Артикул
PubMed
CAS
Google ученый
Chaler EA, Ballerini G, Lazzati JM, Maceiras M, Frusti M, Bergada I, Rivarola MA, Belgorosky A, Ropelato G.Пороговые значения сывороточного гормона роста (GH) в тестах на фармакологическую стимуляцию (PhT), оцениваемых у низкорослых детей, с использованием хемилюминесцентного иммунометрического анализа (ICMA), калиброванного по международному стандарту рекомбинантного GH человека 98/574. Clin Chem Lab Med. 2013; 51: e95–7.
Артикул
PubMed
CAS
Google ученый
Метаболические эффекты прекращения лечения гормоном роста
Дефицит гормона роста (GHD) у взрослых связан с повышенным ожирением, 1 неблагоприятным профилем липидов в сыворотке 2 и снижением переносимости физической нагрузки.Сообщалось также о 3 летаргии, плохом настроении и социальной изоляции, 4 снижении минеральной плотности костей 5 и повышенной смертности, что отчасти является результатом увеличения смертности от сердечно-сосудистых заболеваний 6. Известно, что лечение гормон роста оказывает анаболический эффект как у детей, так и у взрослых, увеличивая задержку азота в течение нескольких дней после начала лечения.7 Повышенное удержание азота отражает увеличение синтеза белка и массы без жира, что, в свою очередь, связано с повышенным расходом энергии. Вследствие этих ранних метаболических изменений лечение гормоном роста (GH) у взрослых с тяжелым дефицитом GH (GHD) приводит к улучшению переносимости упражнений, 9 состав тела, 10
11 и психологическое благополучие, 12 и в настоящее время используется для лечения взрослых с тяжелой формой GHD.
В настоящее время неясно, какие люди, у которых в детстве был диагностирован GHD, выиграют от продолжения лечения GH во взрослой жизни. В настоящее время лечение GH прекращается, когда пациенты завершают период полового созревания. Сорок процентов людей, у которых в детстве был диагностирован GHD, больше не демонстрируют GHD при повторном тестировании в молодом возрасте.13 Таким образом, вероятно, что не все дети, получавшие GH от ранее диагностированного GHD в детстве, получат пользу от лечения во взрослой жизни.Важные ранние метаболические изменения были продемонстрированы после начала лечения гормоном роста у детей.8 Они включают увеличение скорости метаболизма в покое (RMR) и безжировой массы, а также уменьшение жировой массы. Эти ранние метаболические изменения коррелируют с более долгосрочными изменениями в росте14. Мы предположили, что обращение этих метаболических эффектов произойдет при прекращении лечения GH, и что величина этих ранних метаболических изменений может быть предиктором более поздних изменений в составе тела.Таким образом, эти изменения могут быть использованы для выявления тех людей, которые с наибольшей вероятностью столкнутся с побочными эффектами от прекращения лечения гормоном роста в раннем взрослом возрасте и, следовательно, тех, кто с наибольшей вероятностью получит пользу от продолжения лечения.
Объекты и методы
ПРЕДМЕТОВ
Были изучены одиннадцать пациентов подросткового возраста (семь мальчиков), которые прекратили лечение ГР. Средний возраст составлял 17,0 (диапазон от 14,5 до 18,5) лет, и 10 лет были постпубертатными. Секреторный статус GH до лечения GH был оценен у этих пациентов путем измерения их реакции на инсулино-индуцированную гипогликемию (девять пациентов) и глюкагон (два пациента).GHD был диагностирован, когда максимальная концентрация GH в сыворотке была <20 мЕд / мл. Средняя максимальная концентрация GH перед лечением составляла 6,2 (диапазон от 0,2 до 16,9) мЕд / мл. У семи человек был изолированный GHD, а у четырех - множественный дефицит гормонов гипофиза. Дефицит GH был идиопатическим в трех случаях, в одном случае связан с краниофарингиомой и в семи случаях был результатом лечения злокачественных новообразований (астроцитома, острый лимфобластный лейкоз (два пациента), неходжкинская лимфома, глиома, рабдомиосаркома и медуллобластома).Не было различий в максимальных концентрациях GH между людьми с изолированным GHD и людьми с недостаточностью нескольких гормонов гипофиза . Средняя продолжительность лечения GH составляла 7,5 (от 1,7 до 11,8) лет.
Эффекты прекращения лечения GH у пациентов с GHD сравнивались с эффектами, полученными в двух других группах подростков: 10 здоровых постпубертатных контролей (три мальчика), набранные из местной школы, средний возраст 16,8 (диапазон от 16,5 до 17 лет.1) лет и пять человек (один мужчина), которые лечились GH, но у которых не было GHD, средний возраст 16,2 (диапазон от 14,4 до 17,4) лет. У трех из них был синдром Тернера, один синдром Лери-Вейля и один вариант с нормальным ростом (максимальная концентрация гормона роста в сыворотке, 53,2 мЕд / мл при серийных измерениях, проводимых каждые 20 минут в течение ночи). Пациенты с синдромом Тернера и синдромом Лери-Вейля не проходили предварительное тестирование на GH, но не было никаких клинических признаков, указывающих на GHD, и причина их низкого роста была очевидна.Средняя продолжительность лечения гормоном роста составила 3,2 (диапазон от 2,0 до 7,0) года. Четыре пациента были постпубертатными. У всех трех девочек с синдромом Тернера была яичниковая недостаточность, и их лечили комбинацией этинилэстрадиола и норэтистерона (Loestrin 20). Эти пациенты без GHD были включены для оценки эффекта прекращения GH как такового, чтобы определить, являются ли какие-либо метаболические изменения, наблюдаемые у пациентов с GHD, показателями продолжающейся эндокринопатии, а не просто результатом прекращения лечения GH.
МЕТОДЫ
У пациентов, получавших GH, измерения RMR и состава тела проводились в среднем за 9,4 (диапазон от 4 до 20) месяцев до прекращения GH, при прекращении GH и через две недели, шесть месяцев и один год спустя. Аналогичные измерения проводились дважды в год у здоровых контрольных групп. Рост измеряли с помощью настенного ростометра Harpenden (Holtain Ltd, Crymych, Dyfed, UK), а вес — с помощью балансира (Avery Ltd, Бирмингем, Великобритания). Индекс массы тела рассчитывался исходя из веса (кг) / роста (м) 2 .Измерения были выражены в виде баллов стандартного отклонения (SDS) с использованием стандартов роста для британских детей 1990 года15.
16 Период полового созревания оценивался по методу Таннера.
Скорость метаболизма в покое
При каждом посещении измерения RMR проводились в стандартных условиях, рано утром натощак, при этом испытуемые отдыхали на спине в термонейтральной среде. В каждом случае первые 10 минут измерений RMR отбрасывались, чтобы гарантировать получение значений в установившемся состоянии покоя.Потребление кислорода и производство углекислого газа измеряли с помощью непрямой калориметрии с вентилируемым колпаком (метаболический монитор Deltatrac II MBM-200; Datex, Хельсинки, Финляндия), и RMR рассчитывали с использованием уравнения Weir.18 Поскольку RMR зависит от размера тела и доли метаболически активная ткань, RMR (кДж / день) также была выражена с поправкой на размер тела (кДж / кг веса тела / день) и на массу без жира (кДж / кг безжировой массы / день).
Состав тела
Состав тела измеряли с помощью толщины кожной складки и двухэнергетической абсорбции лучей x (DXA).Измерения толщины кожной складки проводились с помощью штангенциркуля Holtain на трехглавой, двуглавой, подлопаточной и надподвзной областях. Плотность тела рассчитывалась на основе суммы измерений кожной складки с использованием уравнений Дурнина и Рахамана для конкретных полов.19 Доля веса тела, приходящаяся на жир, рассчитывалась с использованием уравнения Siri, 20 из которого определялась масса безжировой массы и жира. масса может быть получена для каждого человека.
DXA-измерения массы без жира, жировой массы и процентного содержания жира проводили с использованием сканера QDR 1000 / W (Hologic Inc, Уолтем, Массачусетс, США).21 DXA-измерение состава тела у здоровых контрольных лиц было выполнено только при первоначальной оценке, хотя измерения толщины кожной складки и RMR были повторены через год.
Минерализация костей
Содержание минералов в костях всего тела (BMC) и площадь кости (BA) были измерены с помощью DXA-сканирования с использованием сканера QDR 1000 / W. Обычно данные о минералах костной ткани, полученные с помощью DXA, представляются как поверхностная плотность, но при этом не учитываются изменения BMC, возникающие в результате изменений возраста и размера тела.Поэтому для BMC использовались прогностические формулы, которые обеспечивают метод интерпретации измеренного BMC, который не зависит от этих переменных.22 Измеренный BMC был выражен как процент от прогнозируемого значения (% BMC), что позволяет сравнивать значения у субъектов. с широким диапазоном размеров тела и возраста.
Наше исследование было одобрено местными комитетами по этике исследований Южного Гламоргана и Ньюкасла, и от каждого пациента было получено информированное согласие.
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Средние значения
сравнивались с использованием независимых тестов t .Изменения внутри субъектов сравнивались с использованием парных тестов t . Различные диагностические группы сравнивали с использованием однофакторного дисперсионного анализа (ANOVA). Если соотношение F было значимым (р <0,05), применяли апостериорный тест множественного сравнения Тьюки. Согласие между двумя методами измерения состава тела оценивалось методом, описанным Бландом и Альтманом23.
Результаты
Пациенты с GHD и без него, а также здоровые люди из контрольной группы были примерно одного возраста (таблица 1).Пациенты с GHD и без GHD были короче и легче, чем в контрольной группе, при этом пациенты без GHD были значительно короче, чем пациенты с GHD (таблица 1). Различий в показателях массы тела между группами не было. Группа без GHD получала GH в течение более короткого среднего времени, чем группа с GHD, но разница была незначительной.
СТАВКА МЕТАБОЛИЧЕСКОГО НАДЕЖНОСТИ
Во время лечения GH не было значительных различий между значениями RMR для пациентов с GHD по сравнению со здоровыми контрольными субъектами, тогда как группа без GHD имела значительно более высокий RMR при прекращении лечения GH.Не было значительных изменений в RMR в группе GHD или группе без GHD в течение года до прекращения GH. Значительное снижение RMR / кг массы без жира в день наблюдалось только через две недели, шесть месяцев и один год после прекращения лечения GH (11,3, 12,6 и 11,8 кДж / кг массы без жира в день, соответственно; p <0,01). у тех, у кого есть GHD. В группе без GHD RMR / кг безжировой массы в день оставался значительно выше, чем в группе GHD в каждом случае, и не было отмечено значительного снижения в течение года исследования.Через год у здоровых контрольных субъектов был значительно увеличен RMR, выраженный в кДж / день, но не с поправкой на размер и состав тела (таблица 2). RMR / кг массы без жира в день был значительно ниже у пациентов с GHD по сравнению с контрольной группой и людьми без GHD через год после прекращения лечения. Хотя RMR / кг безжировой массы в день был выше в группе без GHD при приеме GH, чем в контрольной, не было различий между двумя группами через год после прекращения приема GH (рис. 1).
Таблица 2
Показатели скорости метаболизма в покое (RMR)
Рисунок 1
Средняя (SD) скорость метаболизма в покое до прекращения (Pre-dis) лечения GH, при прекращении (при прекращении) лечения и через две недели, шесть месяцев и один год после прекращения лечения. * p <0,01 по сравнению со значениями при прекращении лечения гормоном роста; † p <0,005 по сравнению с группой GHD; ‡ p <0,05 по сравнению с группой GHD и контролем.
СОСТАВ КУЗОВА
Значения процентного содержания жира были стабильно выше при измерении толщины кожной складки, чем при ДРА.При сравнении толщины кожных складок с измерениями DXA было обнаружено среднее смещение 4,4% (пределы согласия от 11,5% до -2,7%) (рис. 2).
фигура 2
Согласование между толщиной кожной складки и измерениями процентного содержания жира методом DXA. Разница между методами заключается в измерении кожной складки за вычетом измерения процентного содержания жира DXA.
При измерении толщины кожной складки у пациентов с GHD наблюдалось увеличение жировой массы и процентного содержания жира в организме через шесть месяцев (2,3 кг и 3,0% соответственно; p <0.05) и через год (3,9 кг и 4,3% соответственно; p <0,05) после прекращения приема ГР (таблица 3; рис 3). Измерения DXA выявили еще большие изменения (6,4 кг и 5,9% соответственно через шесть месяцев и 6,5 кг и 7,8% соответственно через один год; все значения p <0,05) у пациентов с GHD (таблица 4). В течение года здоровые контрольные субъекты также продемонстрировали небольшое среднее увеличение жировой массы (1,8 кг), измеренное по толщине кожной складки (p <0,05), хотя это изменение не было значимым, если выразить в процентах жира в организме.Никаких значительных изменений жировой массы у пациентов без GHD не наблюдалось. Процентное содержание жира в организме увеличилось в группе без GHD через шесть месяцев при измерении по толщине кожной складки (4,1%; p <0,05), но не при измерении с помощью DXA, и через год больше не отличался значительно от времени, когда был GH. снято с производства. Никаких значительных изменений в безжировой массе не наблюдалось ни в здоровой контрольной группе, ни в одной из групп пациентов.
Таблица 3
Измерения состава тела на кожной складке
Рисунок 3
Среднее (SD) процентное содержание жира по толщине кожной складки до прекращения лечения GH (Pre-dis), при прекращении (при прекращении) и через две недели, шесть месяцев и один год после прекращения лечения.* p <0,05 по сравнению со значениями при прекращении лечения гормоном роста; † p <0,05 по сравнению с контролем через один год.
Таблица 4
Двухэнергетические рентгеновские абсорбтометрические измерения состава тела
Существовали значительные ассоциации между изменениями RMR / кг безжировой массы / день и последующими изменениями в составе тела в группе GHD, при этом у тех людей, у которых было наибольшее снижение RMR / кг безжировой массы / день в течение шести месяцев, было наибольшее увеличение. в жировой массе (рис.4) и процентном содержании жира (рис.5) в год (p <0.05). В группе без GHD такой ассоциации не наблюдалось. Изменения в RMR / кг безжировой массы и последующие изменения в составе тела были одинаковыми, независимо от того, имели ли пациенты с GHD изолированный GHD или множественный дефицит гормонов гипофиза.
Рисунок 4
Изменение скорости метаболизма в покое (RMR) / кг массы без жира через шесть месяцев после прекращения лечения и последующее изменение жировой массы через год у пациентов с дефицитом гормона роста.
Рисунок 5.
Изменение скорости метаболизма в покое (RMR) / кг массы без жира через шесть месяцев после прекращения лечения и последующее изменение процентного содержания жира через один год у пациентов с дефицитом гормона роста.
Не было значимой связи между концентрациями GH перед лечением при тестировании на стимуляцию и метаболическими изменениями, которые последовали за прекращением лечения GH.
МИНЕРАЛИЗАЦИЯ КОСТИ
Не было значительных различий в% BMC при сравнении пациентов с GHD с контрольной группой (среднее (SD), 97,5% (3,9%) и 101,0% (5,8%) соответственно) на момент прекращения лечения. Однако группа без GHD имела более низкий% BMC (среднее (SD) 94,7% (3,4%)), чем контрольная группа (p <0.05). Никаких значительных изменений BMC не было отмечено за год исследования ни в группе GHD, ни в группе без GHD.
Обсуждение
Наше исследование показало, что RMR снижается через две недели после прекращения лечения GH в конце пубертатного всплеска роста и остается подавленным до одного года у лиц, ранее идентифицированных как имеющие начало GHD, по сравнению со здоровыми людьми из контрольной группы. Увеличение жировой массы и процентного содержания жира в организме становится очевидным через шесть месяцев после прекращения приема ГР, и эти изменения в составе тела сохраняются через год после прекращения лечения, хотя в дальнейшем значительного увеличения не происходит в период от шести месяцев до года.Это отражает эффекты, наблюдаемые после начала лечения GH у детей, когда максимальные изменения в безжировой массе произошли в первые шесть недель с небольшим увеличением впоследствии14. пролеченные пациенты после шести недель лечения GH вернулись к уровням до лечения к 12 неделям 14, тогда как в нашем исследовании значения RMR оставались подавленными через год после прекращения лечения.
Интересно отметить, что при лечении GH пациенты без GHD имели более высокий RMR / кг безжировой массы в день, чем здоровый контроль, но через год после прекращения терапии значения были аналогичными.Это может указывать на то, что пациенты без GHD испытали аномально повышенный RMR во время лечения GH, возможно, как следствие аномально повышенных концентраций GH в сыворотке. Неизвестно, может ли это иметь потенциально неблагоприятные последствия для здоровья в будущем.
Мы показали важные ранние метаболические изменения при прекращении лечения GH и последующие изменения в составе тела. Изменения жировой массы наблюдались только у пациентов с GHD. Хотя процентное содержание жира увеличивалось как в группах с GHD, так и без GHD, при измерении толщины кожной складки через шесть месяцев это было устойчивым только у пациентов с GHD через один год.Контрольная группа также продемонстрировала увеличение жировой массы через один год, хотя это увеличение было не таким большим, как в группе GHD, и не было отмечено никаких изменений процентного содержания жира. В контрольной группе доля девочек была выше, чем в группах пациентов с GHD и без GHD. Мы набрали контрольную группу из местной школы и были ограничены меньшим количеством мальчиков, которые согласились принять участие. Можно было ожидать, что у здоровых девочек контрольной группы в подростковом возрасте будет наблюдаться большее увеличение жировых отложений, чем у мальчиков, и, таким образом, наблюдаемая разница между пациентами и контрольной группой в течение года после лечения GH имеет еще большее клиническое значение . Изменения в составе тела, наблюдаемые у пациентов с GHD, ранее получавших GH, не могут быть полностью отнесены к метаболическим последствиям прекращения лечения GH, но могут частично отражать нормальные изменения, наблюдаемые в конце полового созревания. Очевидно, что на композицию тела у этих людей влияют другие факторы, кроме GH. В нашем исследовании не предпринималась попытка оценить изменения в физической активности или рационе питания, которые могут повлиять на состав тела. Однако интересно отметить, что никаких значительных изменений в составе тела не наблюдалось в период исследования, в течение которого пациенты продолжали лечение GH (медиана, 9.4 месяца). У четырех пациентов был множественный дефицит гормонов гипофиза, и они получали заместительную терапию другими гормонами (такими как тироксин, половые стероиды или гидрокортизон), что могло повлиять на состав тела. Концентрации этих гормонов в сыворотке крови контролировались до и во время нашего исследования и оставались в соответствующих терапевтических диапазонах, что позволяет предположить, что одновременное лечение вряд ли повлияло на результаты.
BMC всего тела не был значительно снижен у пациентов с GHD, и не было отмечено значительного снижения через год после прекращения лечения GH.Это согласуется с данными некоторых исследований с участием молодых людей, 24 хотя другие продемонстрировали значительное снижение минеральной плотности костей у пожилых людей с длительным GHD.5 Наши результаты показывают, что адекватное лечение GH у детей предотвращает развитие относительной остеопении, которая может наблюдаться. у взрослых, перенесших длительный GHD. Для выявления снижения минерализации костей после прекращения лечения гормоном роста может потребоваться более длительное наблюдение. Снижение BMC было продемонстрировано у пяти пациентов без GHD.У трех из них был синдром Тернера, и снижение ККМ может отражать неоптимальное лечение эстрогенами. Еще у одного был синдром Лери-Вейля, и можно ожидать, что аномальное развитие костей при этом синдроме повлияет на измерения BMC.
В настоящее время пациенты-подростки прекращают лечение GH, когда они завершают свой рост. Поскольку GH теперь доступен для лечения GHD во взрослой жизни, существует повышенный интерес к выявлению тех людей, у которых был диагностирован GHD в детстве, которые, скорее всего, выиграют от более длительного лечения во взрослой жизни, когда рост будет завершен.В настоящее время лицензия на лечение GH во взрослой жизни разрешает лечение взрослых с выраженным GH (<5 мЕд / мл), хотя предыдущие исследования метаболических эффектов лечения GH во взрослой жизни показали преимущества в популяциях с концентрацией GH до лечения, варьирующейся от 3 мЕд / мл и 10 мЕд / мл.25-27 Поэтому маловероятно, чтобы абсолютная концентрация GH могла быть использована для определения того, каким людям лечение GH будет полезно во взрослом возрасте. Учитывая ограниченную корреляцию между биохимическими показателями дефицита GH и некоторыми последующими физиологическими эффектами (такими как рост) лечения, а также слабую корреляцию между результатами тестирования GH в более раннем детстве с результатами, полученными в молодом возрасте 13, наши результаты предполагают, что решение о продолжении лечения GHD во взрослой жизни должно частично основываться на доказательствах физиологической пользы, а не только на результатах тестирования стимуляции GH, проведенного в раннем детстве.В настоящее время рекомендуется, чтобы переоценка ответа GH на тестирование стимуляции гипофиза также была включена в оценку потребности в более длительном лечении GH. К сожалению, такие данные недоступны для большинства наших пациентов, многие из которых отказались от дальнейшего тестирования секреторного статуса GH на этом этапе.
Другие исследования изучали эффект прекращения лечения гормоном роста. Увеличение жировой массы было продемонстрировано измерениями биоэлектрического импеданса у людей с продолжающимся тяжелым GHD через три месяца после прекращения GH, тогда как у пациентов без GHD изменений не было.28 Процентное содержание жира в организме, измеренное с помощью DXA-сканирования, также увеличивалось через шесть и 12 месяцев после прекращения приема гормона роста, но в этом конкретном исследовании контрольная группа не показала такого увеличения.29 Небольшие и переменные сокращения мышечной силы и размера были показаны для происходят через год после прекращения лечения гормоном роста в небольшой группе подростков, но изменения в нормальной популяции в этом возрасте недостаточно документированы, что затрудняет интерпретацию этого открытия30.
Однако, насколько нам известно, наше исследование является первым, демонстрирующим, что отклонения от нормы RMR можно измерить в течение короткого промежутка времени после прекращения лечения GH.Одна из целей нашего исследования состояла в том, чтобы оценить, могут ли ранние метаболические эффекты прекращения приема ГР предсказать долгосрочные неблагоприятные эффекты на композицию тела и можно ли использовать эти эффекты для выявления тех людей, которые, скорее всего, получат пользу от лечения ГР на ранней стадии. взрослая жизнь. Мы продемонстрировали, что у тех людей, у которых наблюдается наибольшее снижение RMR / кг безжировой массы, впоследствии наблюдается наибольшее увеличение жировых отложений, хотя снижение RMR не объясняет всех изменений в жировой ткани (R 2 = 0.49; рис. 4), учитывая, что у нормальных здоровых подростков этого возраста можно ожидать некоторого увеличения жировых отложений. Мы бы предположили, что измерение ранних изменений RMR после прекращения лечения GH может быть использовано для выявления тех людей, которым будет полезно продолжение лечения GH во взрослой жизни. В отделениях, где нет необходимого оборудования, измерение толщины кожной складки для определения изменений в составе тела в течение года после прекращения приема ГР может быть использовано для выявления тех людей со значительным увеличением жировых отложений, которым следует рекомендовать пройти повторную оценку секреторного резерва ГР. .Затем лечение GH может быть повторно назначено на ранней стадии пациентам с подтвержденным GHD, чтобы предотвратить дальнейшее неблагоприятное воздействие на состав тела.
Благодарности
Мы благодарны г-ну Дж. Х. Пирсу, г-ну Д. Коулману и г-же Р. Дж. Петтит за помощь с измерениями DXA; Профессору А. Эйнсли-Грину и доктору П. Дж. Смиту за советы по дизайну исследования и за то, что мы позволили нам изучить их пациентов; и Pharmacia-Upjohn за финансовую поддержку исследования.
.
 02.10
02.10 12.18
12.18 р-ра д/п/к введения 4 МЕ: фл. 1 шт. в компл. с растворителем и шприцем
р-ра д/п/к введения 4 МЕ: фл. 1 шт. в компл. с растворителем и шприцем 5 мл: картридж в шприц-ручке 1.5 мл 1 шт.
5 мл: картридж в шприц-ручке 1.5 мл 1 шт. 5 мл: картридж в шприц-ручке 1.5 мл 1 шт.
5 мл: картридж в шприц-ручке 1.5 мл 1 шт. 7 мг/1 мл: картридж 1.5 мл 1 шт.
7 мг/1 мл: картридж 1.5 мл 1 шт. в компл. с растворителем
в компл. с растворителем №: ЛСР-006944/10
№: ЛСР-006944/10 15 мг/1.5 мл: картриджи 1 шт.
15 мг/1.5 мл: картриджи 1 шт. р-ра д/п/к введения 8 мг: фл. 1 или 5 шт. в компл. с растворителем в картридже и устройством д/пригот. р-ра «Клик. изи»
р-ра д/п/к введения 8 мг: фл. 1 или 5 шт. в компл. с растворителем в картридже и устройством д/пригот. р-ра «Клик. изи» 08.09
08.09